Capítulo 1
Anuncio

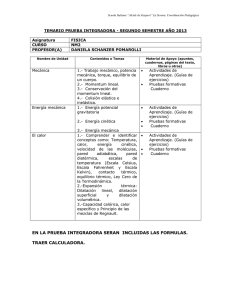
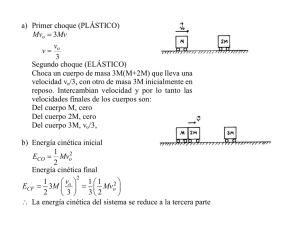
Capítulo 1.- Calor 1 Trabajo. El concepto físico de trabajo está relacionado con la fuerza y el desplazamiento de la misma, mediante la fórmula siguiente: T = f ∗ e ∗ cos Φ (1) T = trabajo. f = fuerza. e = espacio. Φ = ángulo entre la dirección de la fuerza y la del espacio. Es decir, el trabajo es el producto de la fuerza por el espacio recorrido por la misma en la dirección de la fuerza. En el sistema internacional de unidades (SI), la unidad de trabajo es el N ∗ m , que recibe el nombre de Julio y es el trabajo desarrollado por una fuerza de un Newton que recorre una longitud de un metro en la propia dirección y sentido de la fuerza. En el sistema técnico tradicional la unidad de trabajo es el kilopondímetro (Kpm), la relación entre ambas unidades es: Kpm = 9,8 Julios. Para facilitar el entendimiento de lo expuesto, diré que en el caso de que la dirección de la fuerza sea perpendicular al desplazamiento, desde el punto de vista físico no existe trabajo alguno (p.e. al cargar y desplazar una maleta, sólo realizamos trabajo cuando la alzamos, no cuando recorremos un camino con ella). El trabajo es una forma de energía y la cantidad de energía que se puede proporcionar en un tiempo determinado es un concepto importante que recibe el nombre de Potencia y viene dado por la ecuación: P= T t (2) Evidentemente, no es lo mismo efectuar un determinado trabajo en un tiempo de un segundo, un minuto o una hora. La unidad de potencia en el sistema SI es el Watio y nos indica que se tiene la capacidad de proporcionar un trabajo de un Julio por segundo. En el sistema técnico la unidad de potencia es el Kpm/s, si bien habitualmente se emplea un múltiplo que es conocido como CV (caballo de vapor) y que es igual a 75 Kpm/s. La relación existente entre las unidades de ambos sistemas es la siguiente: 1CV = 75Kpm / s = 75 ∗ 9,8 Julio / s = 735Watios = 0,735kW 2 Energía potencial. Es una forma de energía que se define como “energía de posición” y se entiende como la capacidad de realizar trabajo debida a la acumulación de energía disponible. Por ejemplo, si se eleva un objeto cuyo peso es de 98 N, hasta una altura de 10 m, la capacidad de trabajo posible será de 980 Julios. En este caso concreto, la formula que nos da el trabajo quedará como sigue: T = p∗h Siendo: p = El peso del cuerpo (la fuerza con que la tierra atrae al cuerpo de masa m) (3) h = altura a la cual está colocado el cuerpo. Como la dirección del desplazamiento es la misma que la de la fuerza, el cosΦ tomará el valor –1 o 1, según el objeto sea subido a la altura h, o descienda de la misma (en el primer caso se debe realizar un trabajo y en el segundo caso se recupera dicho trabajo) Nota aclaratoria.- El peso de 98 N (unidad de fuerza en el Sistema Internacional) equivale a 10 Kp (unidad de fuerza en el Sistema Técnico) que es la fuerza con que la tierra a trae un cuerpo con una masa de 10 Kg (unidad de masa en el Sistema M.K.S.). 3 Energía cinética. La energía cinética se define como “energía de movimiento” y se entiende como la capacidad de proporcionar trabajo como consecuencia de una disminución de velocidad: p.e cuando en una mesa de billar una bola choca con otra, disminuye su velocidad y el cambio de energía cinética se transforma en movimiento para la bola golpeada. Simplificando la complejidad del tema, puede procederse a la deducción siguiente: T = f ∗e = m∗a∗e Partiendo de (4) Dónde: m = masa. a = aceleración = (v f − vi ) (5) t Y admitiendo que se trata de un movimiento uniformemente acelerado, el espacio recorrido es: e= 1 a ∗t2 2 (6) Por lo que combinando las ecuaciones (4), (5) y (6) encontramos: T = m∗ (v − vi ) 2 f 2 (7) Lo que nos dice que la variación de velocidad por efecto de la aplicación de una fuerza externa supone siempre un cambio en la energía en el sistema, la cual recibe el nombre antes indicado de energía cinética. El ejemplo más común que interrelaciona ambas energías: la potencial y la cinética, es el del lanzamiento de una piedra desde un nivel de 0 m; al inicio existe sólo energía cinética la cual depende del impulso mecánico f ∗ t . Conforme va disminuyendo la velocidad desciende igualmente la energía cinética y sin embargo, puesto la piedra se está elevando, aumenta la energía potencial; cuando la piedra alcanza su altura máxima, la energía cinética es 0 y la energía potencial alcanza el mismo valor que tenía la energía cinética al principio. 4 Teoría cinético molecular. Aun a pesar de su antigüedad, esta teoría puede ayudarnos a comprender los fenómenos del intercambio térmico. Puesto que la materia esta formada por moléculas, el estado de agregación de estas nos puede permitir entender los distintos estados y sus cambios: • En primer lugar debemos decir que entre las moléculas existen unas fuerzas llamadas de cohesión que son las que contribuyen a mantenerlas próximas entre sí (debidas a las cargas eléctricas). Cuanto mayores son las fuerza de cohesión mayor también es el estado de agregación. • En segundo lugar hay que destacar que las moléculas no están en contacto unas con otras, sino que existen espacios intermoleculares (vacíos) que son mayores conforme se van debilitando las fuerzas de cohesión antes mencionadas. • Finalmente, para poder cerrar el panorama, debemos indicar que las moléculas están en movimiento permanente (movimiento vibratorio en el caso de sólidos y movimiento libre en el caso de gases), es decir se puede ver que dichas partículas poseen siempre una energía cinética determinada. En el caso del cero absoluto (-273,15 ºC aprox.), la energía cinética es cero, es el momento en el cual las moléculas están más próximas entre sí. A partir de ahí, conforme vayamos añadiendo energía, esta se utilizará en incrementar la energía cinética de las moléculas aumentando su movimiento vibratorio, incrementando los espacios intermoleculares y, en definitiva, aumentando el volumen ocupado por la materia (dilatación del sólido). Cuando se alcance un nivel de energía determinado, las fuerza de cohesión no podrán mantener las moléculas en posiciones fijas y se ganará lo que podríamos decir un grado de libertad, podrán desplazarse unas junto a otras y variar de forma para adaptarse al contenedor: habremos alcanzado el estado líquido. La cantidad de energía que debemos añadir para lograr este cambio de estado, en general, es bastante elevada. Si seguimos aumentando la cantidad de energía aportada al sistema llegaremos a ver, mediante un procedimiento de observación adecuado, el desplazamiento interno de masas de líquido, teniendo lugar también un aumento del volumen ocupado por el líquido. Llegará finalmente un momento en el cual alguna molécula alcance la energía cinética suficiente como para salir de la masa líquida, venciendo las fuerzas de cohesión y pasando al estado de vapor. Progresivamente el número de moléculas que va cambiando de estado irá aumentando, hasta que haya una gran masa de líquido que cambie de estado bruscamente ocasionando un violento movimiento. La fuente de energía usada para el aumento de la energía cinética es el calor, el paso de sólido a líquido recibe el nombre de fusión y el de líquido a vapor de evaporación (en la fase violenta que tiene lugar en toda la masa del líquido, se denominará ebullición). Los cambios de estado inversos reciben los nombres de solidificación y condensación respectivamente. Bajo ciertas circunstanciases posible el paso de la fase sólida a la fase vapor (sin pasar por el estado líquido), fenómeno que recibe el nombre de sublimación. En los gases perfectos se considera inexistente la acción entre moléculas. Existen fuerzas exteriores que pueden facilitar el tránsito de un estado a otro, por ejemplo: • • La presión exterior en caso de evaporación dificulta la salida de las moléculas de la masa líquida y por tanto será preciso añadir más energía. Por el contrario, en el caso de la solidificación de fluidos, una mayor presión significa una menor necesidad energética por cuanto el cambio de estado comporta una disminución de volumen que se ve favorecido por el aumento de presión. Naturalmente el caso del agua es una excepción, pues aumenta de volumen durante la solidificación y por tanto se requiere mayor energía para ayudar a efectuar el trabajo necesario para el aumento de volumen. 5 Energía interna. La ley de conservación de la energía establece que la energía cedida o transferida a un cuerpo, puede manifestarse o asimilarse de diversas formas. a) b) c) Incrementando la energía cinética. Incrementando la energía potencial. Produciendo un trabajo. La ecuación general de la energía es una concreción matemática de este concepto y se escribe como: ∆Q = ∆K + ∆P + ∆T (8) Donde: ∆Q = Energía térmica transferida. ∆K = Parte de la energía transferida que incrementa la energía cinética. ∆P = Parte de la energía transferida que incrementa la energía potencial. ∆T = Parte de la energía transferida que se utiliza para producir trabajo. Veamos ahora algunos ejemplos de aplicación: a) Si añadimos calor a un cuerpo en estado sólido o líquido, el aumento de volumen es generalmente imperceptible, en particular tratándose de cantidades razonablemente pequeñas, y por tanto el trabajo producido puede considerarse nulo. Nada queda tampoco en forma de energía potencial, por tanto toda la energía térmica se transforma en un aumento de la energía cinética de las moléculas, de forma que ∆Q = ∆K . El cambio producido puede apreciarse mediante un cambio de temperatura. b) Cuando un sólido pasa a fase líquida, podemos decir también que generalmente las variaciones de volumen son despreciables y además no se aprecia variación de temperatura que pueda indicarnos un aumento de la energía cinética de las moléculas. Tendremos aquí por tanto un incremento de la energía potencial y ∆Q = ∆P . c) Si se pasase del estado líquido a la fase vapor, habría un importante aumento de volumen y por tanto al aumento de energía potencial habría que añadir la energía necesaria para producir el trabajo correspondiente, quedando así: ∆Q = ∆P + ∆T . Los dos primeros sumandos de la ecuación (8) constituyen lo que podríamos llamar variación de su “energía interna” (∆U). 6 Calor. Entalpía. El calor es una forma de energía que se puede medir y cuantificar por los efectos que produce y solamente en los procesos de transferencia, así no se puede hablar de la cantidad de calor contenido en un cuerpo. El concepto apropiado sería hablar del “calor total” o “entalpía”, siendo esta última la palabra mas extendida. Es importante no confundir calor con entalpía. La absorción de calor por un sistema, conlleva un incremento de su entalpía; pero ésta, también puede aumentarse por la aplicación de un trabajo exterior, como ocurre en la compresión de un refrigerante. La entalpía de un cuerpo incluye su energía interna y el trabajo necesario para alcanzar el estado en el que se encuentra, así pues la entalpía viene determinada por: i = U + A ∗ p ∗ ∆v (9) Siendo: i = Entalpía. U = Energía interna. p = Presión. ∆v = variación de volumen. A = factor de conversión de la energía mecánica a energía térmica. Ello es así, porque el producto de la presión por el volumen es un trabajo: p∗v = 6.1 f ∗ (s ∗ l ) = f ∗ l = T s Cantidad de calor. Si ponemos en contacto térmico dos cuerpos a diferentes temperaturas, se produce un flujo de energía desde el cuerpo más caliente al cuerpo más frío, hasta que se alcanza una temperatura común en los dos cuerpos, llamada temperatura de equilibrio; en este momento cesa el flujo de energía. El cuerpo más caliente ha disminuido su temperatura y por lo tanto su energía interna, mientras que el cuerpo más frío aumenta su temperatura y por lo tanto su energía interna. En definitiva se ha se ha producido un paso de energía desde el cuerpo más caliente al cuerpo más frío, este tránsito de energía recibe el nombre de calor. Por lo tanto el calor "pasa, se absorbe, se cede, se pierde, etc. pero no se tiene". Una transferencia de calor puede provocar en general dos efectos: a) Un aumento de la temperatura. En éste caso se dice que se ha realizado una transferencia de calor sensible. b) Un cambio de estado. Sin variar la temperatura, en éste caso se dice que se ha realizado una transferencia de calor latente. Para poner un ejemplo, consideremos los vapores de refrigerante en la descarga de un compresor. Conducidos al condensador, sufrirán en primer lugar un enfriamiento, hasta alcanzar la temperatura de saturación, ocurriendo, en segunde lugar, la licuación a temperatura constante. Durante la primera fase se habrá llevado a cabo una transferencia de calor sensible, mientras que en la segunda fase habrá sido una transferencia de calor latente. 6.2 Unidades. Las unidades de medición del calor serán en el SI las mismas que para el trabajo: el Julio, aunque la más utilizada es el kilojulio (kJ). La unidad más utilizada hasta hoy es la caloría que corresponde a la cantidad de calor necesaria para elevar en un grado centígrado la temperatura de una masa de un gramo de agua, desde la temperatura de +14 a la de +15 ºC. El múltiplo utilizado en este caso es la kilocaloría (kcal). En la práctica existen otras unidades como el Btu (en los países de habla inglesa) y que expresa la cantidad de calor necesaria para elevar en un grado Fahrenheit la temperatura de una libra de agua, su uso tiende a desaparecer, pero se encuentran en la literatura muchos estudios que utilizan estas unidades. En realidad como concepto físico solo se puede hablar de cantidad de calor. El aporte del mismo es lo que coloquialmente denominamos “calor” y su sustracción recibe el nombre de “frío”, pero el frío no es sino la ausencia de calor y es por tanto incorrecto hablar de la frigoría como unidad de frío. 6.3 Calor específico. El calor específico, como la densidad o la viscosidad y la conductividad Térmica (que analizaremos más adelante), es una característica propia de un material y significa la cantidad de calor necesaria para elevar en una unidad la temperatura de una unidad de masa de la sustancia. En el SI la unidad es el Julio . Obviamente en cada sistema se definen las propias unidades, gr ∗º C en el sistema técnico (ST) es la caloría gr ∗º C También hay que tener en consideración los múltiplos: kJ kg ∗º C y la kcal kg ∗º C . El calor específico de los cuerpos puede medirse en laboratorio mediante un calorímetro y nos permite establecer la cantidad de calor que hay que añadir o extraer a un cuerpo para conseguir una variación de temperatura determinada, mediante el uso de la siguiente fórmula: Q = m ∗ ce ∗ (ti − tf ) (8) Dónde: Q = Cantidad calor transferido. m = Masa de la sustancia a calentar o enfriar. ce = Calor específico de la sustancia. ti = Temperatura inicial del producto. tf = Temperatura final. Si ti > tf la cantidad de calor será positiva y constituirá una carga térmica en el cálculo de una cámara frigorífica, será por tanto la cantidad de calor que debemos extraer del producto. Por el contrario, si ti < tf obtendremos una carga térmica negativa, significando que debemos extraer calor del entorno para cederlo al producto. Puesto que las distintas materias tienen porcentajes diferentes de agua en su constitución, la influencia de dichos porcentajes es notable en el calor específico de la sustancia y éste es el factor que hace que sean tan diferentes los calores específicos de una sustancia por encima o por debajo del punto de congelación (el hielo tiene un calor específico del orden de 1,88 kJ/kg mientras que el del agua es de 4,18 kJ/kg). 6.4 Calor sensible. Se denomina así la cantidad de calor que puede medirse de forma sensorial, es decir mediante apreciación de cambios mensurables, como la variación de temperatura. La aportación o sustracción de calor tiene una incidencia total y exclusiva en la variación de temperatura. Como se ha mencionado antes este calor se aplica en exclusiva al aumento o disminución de la energía cinética de las moléculas. 6.5 Calor latente. Es el calor que no tiene un efecto mensurable, se aplica al cambio de estado de la materia y no comporta ningún cambio de temperatura. Su valor depende del producto en cuestión. También en éste caso el porcentaje de constitución del agua en el producto determinante en la magnitud del calor latente. El calor latente se mide en el SI mediante Julio gr o su múltiplo kJ kg 7 Nivel térmico. El nivel de agitación molécular según se ha indicado anteriormente, tiene una influencia inmediata en la temperatura del producto. Quizá la mejor manera de entender los conceptos de calor y temperatura, sea la de establecer un símil hidráulico, como el que podemos apreciar en la fig. 1 R2 R1 H2 M2 H1 M1 V Fig. 1 En ella podemos ver que los niveles de líquido entre los recipientes nº 1 y nº 2 son diferentes. La masa de agua contenida en el recipiente 1 es mayor que la masa de agua contenida en el recipiente 2, sin embargo, el líquido alcaza una altura mayor en el recipiente 2 que en el 1, debido a las características físicas de cada uno de ellos. En forma similar, dos cuerpos de distintas substancias pueden mantener niveles energéticos diferentes, de forma que el que dispone de menor cantidad de energía acumulada alcance un nivel superior (tenga una temperatura superior). Si en el ejemplo anterior abriéramos la válvula V, el líquido pasaría del recipiente 2 al 1 por vasos comunicantes, a pesar de haber mayor cantidad de líquido en R1, hasta que los niveles se igualen. En forma análoga, el calor pasará del cuerpo con mayor temperatura al de menor temperatura, hasta que los dos tengan la misma temperatura y el calor cedido por un cuerpo será igual al calor ganado por el otro cuerpo. R1 R2 M4 H3 H3 M3 Fig.2 7.1 Temperatura. La temperatura de un cuerpo nos da la medida de su estado de calor o frío relativos. Podemos tener una idea de dicho estado en función del tacto, pero esta es una comprobación totalmente subjetiva y depende de muchos aspectos circunstanciales, por ello se ha desarrollado una tecnología que nos permita saber con precisión el nivel térmico de un cuerpo. Para ello se han definido unas unidades y unos instrumentos que nos permitan efectuar mediciones con suficiente precisión. La denominación de las unidades depende del origen o de su introductor: están los grados Celsius o Centígrados, Fahrenheit, Reamur y Kelvin. Las primeras son las más usadas hasta hoy y corresponden al Sistema Técnico, las segundas se usan solo en países de habla inglesa, la tercera se empleó durante cierta época en Francia y la cuarta corresponde al Sistema Intencional y los intervalos que corresponden a un grado son los mismos que con la escala Celsius. Para la medición se utilizan los instrumentos denominados termómetros que se describen seguidamente. 7.2 Termómetros. Su funcionamiento se basa en el efecto que produce la temperatura sobre ciertas sustancias, p.e. la dilatación de los cuerpos y la mejora de la conductividad eléctrica con la disminución de la temperatura, pudiendo además ser todos ellos para emplazamiento local (en campo) o a distancia (en panel local o en Sala de Control centralizada). De entre los distintos tipos de termómetros cabe destacar: a) Los que actúan en virtud de los fenómenos de dilatación o contracción, entre ellos se encuentran los de gases, líquidos y bimetálicos. • Los que utilizan gases aprovechan el aumento de presión a volumen constante (Ley de Gay Lusac que veremos más adelante) y tienen una construcción a base de una espiral o una hélice que varía la posición en función de la tensión a que la somete la presión. • Los de líquido son generalmente mercurio o alcohol y pueden ser del tipo de varilla (tipo termómetro clínico, también usado industrialmente), o también del tipo Bourdon, análogos a los mencionados antes para los gases (que son del tipo esfera). • Los bimetálicos aprovechan el hecho de que cada metal tiene una dilatación diferente, de forma que se colocan juntos dos metales con dilataciones muy distintas, de forma que al aumentar la temperatura se produzca una torsión que pueda transmitirse en un movimiento angular que se refleja en una escala adecuada, ver fig-5. Los termómetros están constituidos generalmente por tres partes básicas: Bulbo- Es la parte de mayor diámetro de los tipo varilla y su tamaño depende del tipo de líquido y la precisión deseada. Debe estar siempre totalmente sumergido en el fluido a medir; si por sus dimensiones no fuera posible, habría que aumentar el diámetro de la tubería en la que se tendría que insertar, mediante reducciones. . Capilar- Su longitud es variable, aunque el diámetro interno es muy reducido y debe estar protegido con tubo flexible, para evitar su rotura. Elemento de medición- Tratándose de los denominados “termómetros de esfera”, el elemento utilizado es el Tubo de Bourdon, pudiendo espiral o helicoidal. Los materiales mas utilizados para su fabricación son bronce fosforoso, cobre-berilio, acero inoxidable y acero al carbono. Fig. 3 Fig. 4 Fig. 5 Capilar- Su longitud es variable, aunque el diámetro interno es muy reducido y debe estar protegido con tubo flexible, para evitar su rotura. b) Los que actúan midiendo la variación de Resistencia Eléctrica: la variación de resistencia eléctrica con la temperatura se usa en termómetros en base a termistores y termómetros de resistencia eléctrica , se pueden utilizar distintos materiales: cobre, níquel o platino. Este último es el mas caro, pero de uso más extendido por el amplio margen de medición que admite, de –250 a 850 ºC, en la actualidad sólo se usan los otros materiales para sustituciones Las termorresistencias se fabrican con alambres finos soportados por un material aislante, encapsulándose seguidamente el conjunto. Se fabrican con una resistencia de 100 Ω a 0 ºC de temperatura (la de platino se conoce como Pt-100), en la fig. 6 se puede ver la relación existente entre la temperatura y la termoresistencia de níquel dentro de su rango de medición de –60 a +180 ºC . A continuación se montan dentro de una vaina o tubo metálico cerrado y el conjunto tiene un aspecto similar al de los termopares. Temperatura Resistencia en ºC en ohm -60 69,5 -50 74,2 -40 79,1 -30 84,1 -20 89,3 -10 94,6 0 100,0 10 105,6 20 111,3 30 117,1 40 123,0 50 129,1 60 135,3 70 141,7 80 146,2 90 154,9 100 161,7 110 168,7 120 175,9 130 183,3 140 190,9 150 198,7 160 206,7 170 214,9 180 223,1 Identificación componentes a) Cabezal b) Cuello c) Rosca a proceso d) Aislador cerámico e) metálica f) h) l) Vaina Termop ar o resist. Longitu d de la vaina Longitud del cuello Fig.6 Fig.7 c) Los que actúan midiendo la variación de Resistencia Eléctrica: la variación de resistencia eléctrica con la temperatura se usa en termómetros en base a termistores y termómetros de resistencia eléctrica, se pueden utilizar distintos materiales: cobre, níquel o platino. Este último es el mas caro, pero de uso más extendido por el amplio margen de medición que admite, de –250 a 850 ºC, en la actualidad sólo se usan los otros materiales para sustituciones Las termorresistencias se montan en varias configuraciones: • • • Configuración A se usa un circuito de dos hilos, con una conexión a cada extremo de la termorresistencia. Con este diseño la resistencia de los cables de conexión, así como las oscilaciones de temperatura ambiente falsean las lecturas, por lo que no se puede usar salvo con cables de conexión muy cortos y de baja resistencia. Con este procedimiento se usa una resistencia de calibración de 10 Ω para compensar la resistencia de los conductores de conexión Configuración B es el circuito más común con tres hilos. Los conductores deben tener la misma longitud, estar sometidos a idéntica temperatura ambiente y el sistema de puente de Wheatstone a la entrada del instrumento de medición está debidamente equilibrado. La configuración C consiste en cuatro cables de conexión y ofrece una mayor exactitud que las configuraciones anteriores. Naturalmente los cables deben tener la misma longitud y sección y en éste caso la resistencia de los cables no tiene ningún efecto sobre la medición. Se recomienda el uso de este sistema para longitudes superiores a 20 m. exactitud que las configuraciones A y B. Si los cuatro cables de conexión son de idéntica sección, longitud y material y se hallan sujetos a la misma temperatura ambiente, y si los dos pares de alambres se encuentran en partes opuestas del circuito puente, las resistencias de los alambres no tendrán efecto alguno en la medición de la resistencia de la termorresistencia. • d) Fig. 8 - Sistemas de conexión de termorresistencias a) Dos hilos , b) Tres hilos , c) Cuatro hilos Potencial termoeléctrico: Seebeck descubrió que si dos uniones de dos metales diferentes tienen temperaturas distintas, se genera en el circuito una fuerza electromotriz (f.e.m), y este fenómeno es el que ha dado lugar al desarrollo de los termopares. Son en todo similares a los medidores resistivos, solo que en lugar de medir una resistencia se mide una f.e.m Fig 9 Donde A y B son dos conductores de distinto material, T1 y T2 son las temperatura a que están sometidas cada una de las dos uniones e I es la corriente que se genera Fig.10 Esquema de un termopar y su sistema de medición 1. 2. 3. 4. Unión de medició n Unión de correcci ón Cable compen sado Unión de referenc ia. Tienen un rango de medición de –200 a +2.800 ºC. Y pueden estar hechos con distintas parejas de materiales, de ahí reciben su denominación: Tipo B ( PtRh 30% - PtRh 6%) Tipo R (PtRh 13% - Pt ) Tipo S (PtRh 10 % - Pt ) Tipo J (Fe - CuNi ) Tipo K (NiCr Ni) Tipo T (Cu - CuNi ) Tipo E ( NiCr - CuNi ) Cada tipo tiene unas condiciones de aplicación idóneas, sin embargo para la utilización en las instalaciones frigoríficas el más conveniente sería el tipo J (hasta –50 ºC),para temperaturas más bajas debería ser el tipo T e) Radiación electromagnética: tanto los termómetros de infrarrojos como los pirómetros ópticos se basan en los fenómenos de radiación para medir temperatura, ambos tienen la ventaja de que pueden medir a distancia. Los primeros pueden medir la temperatura de un objeto sin tocarlo. Hay muchos casos en los que la medida de temperatura sin contacto es crítica: cuando el objeto medido es pequeño, movible o inaccesible El rango de medición para los termómetros de infrarrojos es desde –50º a 3.000 ºC; los pirómetros ópticos se usan para temperaturas más elevadas. La tecnología aplicada está basada en la ley de Stefan, según la cual todos los cuerpos emiten una energía radiante en forma de ondas electromagnéticas, proporcional a su temperatura. Se trata de medir la energía emitida en el espectro infrarrojo para poder determinar así la temperatura del cuerpo a medir. 7.3 Escalas termométricas. Existen como se ha mencionado antes diversas escalas termométricas, sin embargo para la determinación de las mismas se debía partir de unos puntos fijos, los cuales fueron el punto de fusión del hielo y el de ebullición del agua. La escala Celsius o Centígrada dividió dicho intervalo en cien espacios iguales,asignando el valor 0 ºC al punto de fusión del hielo y +100 ºC al funto de ebullición. La escala Fahrenheit divide el intervalo en 180 partes iguales y asigna el valor +32 ºF al punto de fusión del hielo y, por tanto, +212 al de ebullición. La proporción entre ambas escalas nos permite hallar el valor en una escala, conociendo el valor de la otra: Fig.11 ºC = 100 5 ∗ (º F − 32) = ∗ (º F − 32) 180 9 (9) ºF = 180 9 ∗º C + 32) = ∗º C + 32) 100 5 (10) La escala Reamur establecía ochenta divisiones entre ambos puntos, pero esta escala está hoy en día en desuso. La escala absoluta de temperaturas parte del cero absoluto y existen dos denominaciones: Kelvin y Rankine. La primera mantiene los mismos intervalos que la escala centígrada, pero hay una diferencia entre ambas cifras de 273 º: ºK = 273 + ºC. La segunda mantiene los intervalos de los ºF, pero la determinación es la siguiente: ºR = 491 + ºF. 8 Dilatación lineal, superficial y cúbica. Con pocas excepciones el volumen de los cuerpos aumenta con la temperatura. Según la forma del cuerpo puede tener más importancia un tipo u otro de dilatación, por ejemplo en el caso de los raíles de un tren se hablará de la dilatación lineal pues predomina la dilatación longitudinal (de una sola dimensión) sobre las otras y será preciso cerciorarse de que no lleguen a tocarse las vías; en el supuesto de anillos, casquillos o camisas el factor predominante es la sección y en el caso de cubos, esferas o fluidos habrá que tener en consideración la dilatación cúbica. La formula que nos da el incremento de longitud, en el caso de la dilatación lineal, es la siguiente: ∆L = α ∗ Lo ∗ (tf − ti ) o bien L1 = Lo ∗ (1 + α ∗ (tf − ti )) (11) ∆L Lo ti tf Lf Fig. 12 ∆L = Variación de longitud Lo = Longitud inicial Lf = Longitud final to = Temperatura inicial tf = Temperatura final α = Coeficiente dilatación lineal en mm/(mm x ºC) En el caso de la dilatación superficial hay que tener en cuenta que se trata de una dilatación en dos dimensiones en lugar de una sola, por tanto (L )2 = (Lo )2 ∗ [(1 + α ∗ (tf − ti ))]2 y por tanto S 1 1 ( = S 0 ∗ 1 + 2 ∗α ∗ (tf − ti ) + α 2 ∗ (tf − ti ) 2 que si tenemos en cuenta que los valores al cuadrado son de orden muy pequeño, y por tanto despreciables, quedará: S 1 = S 0 ∗ (1 + 2 ∗ α ∗ (tf − ti )) = S 0 ∗ (1 + β ∗ (tf − ti )) Dónde β = 2α (12) ) Por razones análogas tendremos que: V 1 = V 0 ∗ (1 + 3 ∗ α ∗ (tf − ti )) = V 0 ∗ (1 + γ ∗ (tf − ti )) (13) Siendo γ = 3α 8.1 Fatiga térmica Cuando debido a las diferencias de temperatura con las cuales se trabaja (p.e entre la fase de montaje y la fase de funcionamiento) las estructuras, en particular las tuberías, pueden estar sometidas a lo que se llama fatiga térmica, será necesario comprobar que el sistema tiene un suficiente grado de libertad y resistencia como para asegurar que no se producirá una rotura del tubo. Para ello deberá hacerse un montaje que permita al tubo moverse sin llegar a superar el límite elástico o el de rotura. Cuando la barra de tubo no pueda contraerse o dilatarse de forma segura, será preciso recurrir a las liras o compensadores de dilatación. Para hacer la comprobación debemos partir del módulo de Young, el cual por definición es: Fn Fatiga tensora o fatiga de compresión A Y= = Deformación unitaria por tensión o compresión ∆L Lo (14) Aplicándolo en éste caso, tendremos al fórmula que nos dará la fatiga y que será la que debemos cotejar con el límite elástico. F = Y ∗ α ∗ (tf − ti ) A El cociente F A (15) nos dará el resultado en Kg/mm2, a pesar de que el límite elástico dependerá del material, deberemos además estimar un factor de seguridad de 1,5 aprox., con lo que el valor máximo recomendado estará alrededor de 1.200 Kg/mm2. La sección A corresponde a la de la corona circular del tubo: A = π ∗ (Re 2 − Ri 2 ) A continuación se indican los valores más usuales del módulo de Young (los límites elásticos dependerán de la calidad del material utilizado): Hierro forjado • Acero al carbono ............................................. 19421 x 103 Kg/mm2 • Cobre........................................................................ 10412 Kg/mm2 18420 Kg/mm2