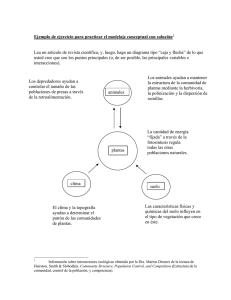
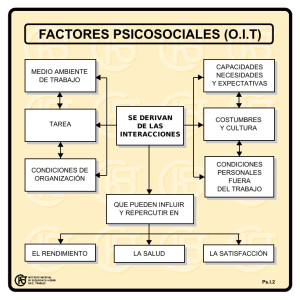
interacción
Anuncio

Interacciones entre los átomos, o… MODELOS DE ENLACE Las Sustancias Químicas (realidad) Y los enlaces... (el modelo ) ¿Cómo clasificamos a a las sustancias? ¿Por qué es importante clasificarlas? Por estado de agregación Estado de agregación sólidos líquidos gases Problemas... ¿A qué temperatura? ¿A qué presión? ¿ En qué tiempo? Problemas... “Semi” metales Metales de transición Cu+2, Cu+1 Gases “Nobles” ¿ Xe = He ? ¿Hidrógeno? ¿metal alcalino?... ¿halógeno? Inorgánicas vs. orgánicas Más problemas... Ca5(PO4)3(OH)... ¿Sería entonces éste un compuesto orgánico? ¿Orgánico o Inorgánico? ...Los compuestos orgánicos son los que contienen carbono... Sin embargo existen algunas excepciones, como: los óxidos de carbono, los carbonatos, los tiocianatos, los cianuros, los carbonilos metálicos, los carburos, el acero, etc. Más problemas Basura “inorgánica”... ...como el plástico... Verduras “orgánicas” ... A diferencia de...? Mejor volvamos a los estados de agregación... Empecemos por los sólidos Sólidos de “alta” temperatura de fusión Diamante... T.f. ≈ 4000°C (Cotton dice que es la más alta conocida...) Grafito... Temperatura de fusión ≈ 4000°C ... Ca5(PO4)3(OH) T.f. = 1600°C Hierro T.f. = 1528°C Sal común T.f. = 801 ¿Qué nos dice una alta temperatura de fusión? Es necesaria mucha energía para fundir al sólido, por lo tanto ¿cómo lo explicamos? Mediante el tipo de interacción que existe entre los átomos que forman a la sustancia. Si se requiere mucha energía se dice que la interacción es muy fuerte. Las interacciones tan fuertes hacen que se formen redes. Cada entidad está unida a varias entidades vecinas y así sucesivamente. Se forman redes tridimensionales. Pero, no nos dice nada acerca de la naturaleza de las interacciones. ¿qué sustancias forman redes? Los metales. Las sales iónicas como el NaCl. (Redes metálicas) (Redes iónicas) Diamante, grafito, óxido de silicio, etc. (redes covalentes reticulares) Hierro (Fen) (NaCl)n (GaAs)n Diamante (Cn) Sólidos de baja temperatura de fusión. Azufre, yodo, compuestos orgánicos ¿Qué nos dice una baja temperatura de fusión? Se requiere poca energía para que el sólido funda, pero no se descompone. ¿Cómo podemos explicarlo? Mediante una combinación de interacciones fuertes y débiles. Las interacciones fuertes forman a las unidades “discretas”, es decir a las moléculas. Al fundirse el sólido las moléculas mantienen su identidad, sólo se separan unas de las otras y se rompen las interacciones débiles. azufre Yodo (I2) Fenol (C6H7O) Sólidos covalentes moleculares En las moléculas, las interacciones fuertes se dan entre los átomos que forman a la molécula. La interacción que se da entre moléculas es relativamente débil. En este caso, para pasar al estado líquido lo que se requiere es romper las interacciones débiles entre moléculas, por lo que la temperatura de fusión es baja, ya que se requiere poca energía. Fósforo Blanco, T.f .= 44°C Rojo, T.f .= 590°C Negro T.f .= 610°C Gases, líquidos o sólidos de baja temperatura de fusión Suponer que una sustancia está formada por moléculas, nos permite explicar que existan los gases, los líquidos o los sólidos con baja temperatura de fusión. A este tipo de sustancias se les conoce como moleculares. En resumen Sólidos de alta temperatura de fusión: Interacciones muy fuertes: REDES Metálicas, iónicas y covalentes. Baja temperatura de fusión (sólidos, líquidos o gases) Interacciones fuertes y débiles: MOLÉCULAS ¿Cómo es la naturaleza de las interacciones que unen a los átomos? ¿Necesitamos otra propiedad observable? Podría ser… ¿...la cristalinidad...? Tipos de sustancias que forman cristales. Las sustancias que tienen interacciones tipo red. Las sustancias moleculares. O sea... casi cualquier tipo de sustancia puede formar cristales. ¿Y la solubilidad...? Problemas: Las sustancias no son “solubles o “insolubles”. Hay muchas sustancias iónicas insolubles en agua. Hay muchas sustancias covalentes moleculares solubles en agua. Algunos sólidos conducen la corriente Algunos sólidos se disuelven en agua y conducen la corriente Algunos sólidos fundidos conducen la corriente. (Fe)n (NaCl)n ¿Con esta propiedad podríamos proponer algún modelo para la naturaleza de las interacciones en las sustancias con distintas propiedades? ¿Qué me dice la conductividad? Existe una manifestación de cargas que se mueven al aplicar una diferencia de potencial y por tanto es razonable suponer que hay separación de cargas en el material. ¿Qué me dice la conductividad? Si las sustancias son sólidos que conducen la corriente, el modelo dice que pueden concebirse como un conjunto de iones positivos que se encuentran ordenadamente colocados dentro de un mar de electrones libres. Propiedad que corresponde a las Redes Metálicas. Lo que explica: 1. Que sean sólidos cristalinos, pero maleables. 2.- Que conduzcan la corriente en estado sólido. ¿Qué me dice la conductividad? Las sustancias que no conducen la corriente en sólido, pero que sí lo hacen al fundirse o disolverse en agua, pueden concebirse como un conjunto de entidades de carga opuesta (aniones y cationes). Propiedades que corresponden a las Redes Iónicas. Esto puede explicar: 1.- Que sean sólidos cristalinos y quebradizos. 2.- Que no conduzcan la corriente en estado sólido. 3.- Que sí conduzcan la corriente al estar fundidos. 4.- Que si se disuelvan en agua y conduzcan la corriente en disolución acuosa. ¿Qué me dice la conductividad? Las sustancias que nunca conducen la corriente pueden concebirse como aquellas en las que los electrones de valencia son compartidos entre átomos vecinos, por tanto los electrones NO tienen movilidad. Si son sólo unos cuantos átomos los que comparten electrones, se forma entre ellos una interacción covalente que da origen a una molécula. Ej. El azufre (S8) Si cada átomo comparte electrones con vecinos en distintas direcciones se forma una red covalente. Ej. El diamante (Cn) Conductividad Sí Conduce No conduce sólido fundido o disuelto sólido, fundido o disuelto Enlace metálico Enlace iónico Enlace covalente