Embarazo ectópico ESTERILIDAD FEMENINA
Anuncio

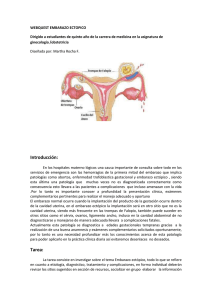
Embarazo ectópico Dr. Agustín Ballesteros Boluda IVI- Barcelona BLOQUE I ESTERILIDAD FEMENINA MÁSTER EN REPRODUCCIÓN HUMANA Contenido 1. Introducción.......................................................................................................................... 2 2. Consideraciones generales .................................................................................................... 2 2.1. Epidemiología................................................................................................................. 2 2.2. Actualidad ...................................................................................................................... 2 3. Diagnóstico ........................................................................................................................... 3 3.1. Clínica ............................................................................................................................ 3 3.2. Analítica ......................................................................................................................... 4 3.3. Ecografía ........................................................................................................................ 4 4. Tratamiento .......................................................................................................................... 5 4.1. Tratamiento no quirúrgico .............................................................................................. 5 4.1.1. Conducta expectante .............................................................................................. 5 4.1.2. Tratamiento farmacológico primario....................................................................... 6 4.1.3. Tratamiento farmacológico secundario: embarazo ectópico persistente ................. 9 4.2. Tratamiento quirúrgico................................................................................................. 10 4.2.1Tratamiento conservador ............................................................................................ 10 4.2.2. Tratamiento quirúrgico radical .................................................................................. 10 5. Lecturas recomendadas ...................................................................................................... 11 6. Tablas ................................................................................................................................. 12 Tabla nº 1............................................................................................................................ 12 TABLA Nº 2.......................................................................................................................... 13 7. Bibliografia.......................................................................................................................... 14 UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 1 de 15 MÁSTER EN REPRODUCCIÓN HUMANA 1. Introducción En condiciones normales la fecundación se produce en la fimbria y el óvulo fecundado permanece unos días en la trompa, donde inicia su desarrollo embrionario, y ya en la etapa de blastocisto llega a la cavidad uterina, donde se produce la implantación. El embarazo ectópico (EE), por lo tanto, es el producto de la implantación patológica del óvulo fecundado fuera de su lugar habitual, la cavidad uterina (1). En un 98% de los casos se localiza en la trompa y en el 2% en otros sitios como el ovario, el cuerno o el cuello uterino y en la cavidad abdominal. 2. Consideraciones generales 2.1. Epidemiología Hasta 1979, la incidencia de esta patología oscilaba entre un 0.30 y un 0.85 %, a partir de entonces se incrementó de un 0.90 a un 1.30 %. En España, Vanrell analizó el cambio aparecido en la frecuencia, de un 0.48 % en 1978, a un 1.11 % en 1991(2). Estas cifras son similares a las descritas por Washington (3), que también comprueba el incremento de un 0.45 % en 1970, a un 1.61 % en 1989. Recientemente, Coste publica una incidencia en la población francesa del 20.2 por 1000 nacidos vivos; del 15.8 por 1000 embarazos, y del 9.5 por 10000 mujeres con edades comprendidas entre 15 y 44 años, destacando un aumento de frecuencia con la edad, principalmente en mujeres mayores de 35 años (4). Actualmente se postula un incremento anual de 11 %(1). Este aumento en la frecuencia puede deberse por un lado, a un incremento de los factores etiológicos (enfermedad inflamatoria pélvica, DIU, técnicas de reproducción asistida, cirugía conservadora, etc.) (5) y por otro, a una mejoría en el diagnóstico, objetivando casos que antes habrían pasado desapercibidos (5,6). 2.2. Actualidad A pesar del aumento de frecuencia, se ha producido una disminución en la mortalidad debida a embarazo ectópico. Parry, en 1876, en la época previa a la salpingectomía de Lawson-Tait (1884), publicó 829 casos con un 69 % de mortalidad. Un siglo después, la mortalidad había disminuido hasta 0.35 % en 1970 y un 0.034% en 1987 (3). De todas maneras, el embarazo ectópico todavía supone un 13 % de la mortalidad en obstetricia (3). En relación a la morbilidad, para muchas parejas la consideración más importante es la disminución de la futura fertilidad (1). En la población general, la tasa de gestación normal es de 85 %, y la tasa de embarazo ectópico es de 1.6 %. Tras un embarazo ectópico, las posibilidades de embarazo descienden hasta un 50-60 % (3), con tan sólo un 30 % de gestaciones a término. El riesgo de un nuevo embarazo ectópico aumenta hasta un 13 %. Washington, en 1993, valoró los costes directos de este proceso (consultas, ingresos hospitalarios, cirugía, etc.) en 838.2 millones de dólares al año; y los indirectos (bajas UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 2 de 15 MÁSTER EN REPRODUCCIÓN HUMANA laborables, secuelas, etc.) en 250.2 millones de dólares al año. El coste de cada caso es de alrededor de 9482 dólares. El embarazo ectópico inicial no roto puede evolucionar de distintas maneras, siendo posible tanto su reabsorción espontánea como el aborto tubárico, también su rotura o incluso, con menor frecuencia su reimplantación en la cavidad abdominal. Estas situaciones se traducen en modificaciones en la clínica del embarazo ectópico; donde el cuadro clásico de rotura tubárica y shock se presenta hoy en menos de un 30% de los casos. Hemos pasado a ver embarazos ectópicos iniciales no rotos o formas hemodinámicamente estables con cada vez mayor frecuencia, lo que permite a su vez la instauración de tratamientos más conservadores en procura de conservar la fertilidad posterior. En todos estos cambios han sido fundamentales los nuevos recursos para el diagnóstico, sobre todo las determinaciones analíticas como el radioinmunoanálisis de la B-hCG y de la progesterona, así como de la ecografía de alta resolución por vía transvaginal y el uso más liberal de la laparoscopia diagnóstica. Existen situaciones como el embarazo heterotópico, donde la frecuencia de EE e intrauterino concomitantes en una concepción espontánea es de 1 en 30000 o menos, en estos casos la ecografía transvaginal en tiempo real representa una herramienta fundamental para establecer el diagnóstico. 3. Diagnóstico El hecho de realizar precozmente un diagnóstico certero depende directamente de la combinación entre clínica, biología y ecografía. 3.1. Clínica Aunque el EE puede presentarse en cualquier mujer en edad reproductora, con dolor abdominal y alteraciones menstruales, ante todo hay que tener presente los factores de riesgo que modifiquen el transporte normal del óvulo fecundado (Tabla 1), relacionados principalmente con daño tisular como consecuencia de reacciones inflamatorias causadas por enfermedad inflamatoria pélvica, secuelas de cirugía y embarazos ectópicos previos. Aunque no hay síntomas patognomónicos de un EE, es importante estar atento ante la combinación de dolor, alteración menstrual tras una corta amenorrea y síntomas previos de embarazo; sin embargo, estos síntomas son comunes a otras complicaciones de embarazos iniciales como amenaza de aborto y pueden ser resultado de situaciones coincidentes como irritación cervical, infección o trauma. Los síntomas más frecuentes son: dolor abdominal (9599%), hemorragia vaginal (60-80%), retraso menstrual (70%), síntomas de gestación (23%), mal estado general (23%), omalgia (8-10%), diarrea y vómitos (25%), y expulsión del molde decidual (10%) (1). El estado general de la paciente dependerá del estado evolutivo del EE, siendo los signos típicos: dolor anexial con la exploración (98%), sensibilidad abdominal (97%), dolor con la UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 3 de 15 MÁSTER EN REPRODUCCIÓN HUMANA movilización cervical (97%), Douglas doloroso y ocupado (70%), signo de Blumberg (54%), útero aumentado con masa anexial (32%) y defensa abdominal (18%) (1). La mayoría de los EE son diagnosticados entre las 5 y 12 semanas de gestación. El diagnóstico antes de las cinco semanas no está al alcance de las técnicas actuales y cerca de las 12 semanas si no ha ocurrido la ruptura, la palpación de una masa anexial orienta hacia esta patología, así como una disparidad en el aumento esperado de tamaño del útero. 3.2. Analítica La bibliografía muestra un amplio abanico de posibilidades analíticas, pero la que ha prevalecido sobre las demás es la determinación seriada de la b-hCG, de especial utilidad para orientar al ecografista en el diagnóstico. Mientras que en el embarazo normal sus valores se duplican cada 2-3 días, en el EE no se suele producir este incremento (9). Un incremento anormal en las concentraciones de hCG es diagnostico de una gestación anormal, y el 35% de los EE son diagnosticados cuando la hCG está declinando (9) Ya que las mujeres pueden experimentar sangrado genital irregular tempranamente durante el embarazo, frecuentemente no se conoce exactamente la edad gestacional del mismo. En estos casos hay que tomar en cuenta el nivel de b-hCG por encima del cual puede ser visualizado un saco gestacional por ecografía transvaginal, y que está por el orden de los 1800mUI (III Preparación Internacional de Referencia). (9) La determinación de la progesterona sérica, marcador indirecto muy sensible de la actividad trofoblástica, está más raramente disponible en el momento del examen ecográfico, aunque tiene una gran utilidad pronóstica sobre la evolución de la gestación. 3.3. Ecografía La introducción de la ecografía transvaginal ha incrementado el número de EE diagnosticados precozmente. Semiológicamente se han de analizar cinco puntos sucesivos: 1) No visualización del saco gestacional intrauterino: con valores de b-hCG en sangre que oscilan entre 350 y 1000UI/L, puede verse saco intrauterino, aunque con valores bajos la sensibilidad para diagnosticar EE es menor (9). La sensibilidad del ultrasonido para diagnosticar embarazo cuando el valor de hCG está debajo del nivel discriminador es de 30 a 40% y el valor predictivo positivo en estos casos es del 60%.(9) 2) Presencia de molde decidual: si no se apreciara, visualizándose una línea endometrial fina (expulsión decidual), la ausencia de regresión de los niveles de b-hCG es casi patognomónica de EE. 3) Detección de cuerpo lúteo, en cuya vecindad suele visualizarse el saco ectópico. 4) Masa anexial anormal: la visualización del EE es variable, a veces como saco completo, otras como una masa heterogénea, secundaria a hematosálpinx, y más precozmente como una imagen ecogénica lacunar de 1 cm. de diámetro. 5) Hemoperitoneo, a veces difícil de valorar por la existencia de coágulos. En ocasiones, la utilización del Doppler a color nos orienta sobre la localización del saco extrauterino. UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 4 de 15 MÁSTER EN REPRODUCCIÓN HUMANA La sensibilidad y especificidad de la ecografía en tiempo real se aproxima al 100% en gestaciones mayores a 5.5 semanas. En casi todos los casos, ante un EE potencial, el diagnóstico se establece de entrada a partir de estas tres armas diagnósticas, o a veces puede ser diagnosticado en un segundo momento tras el seguimiento ecográfico y biológico de la paciente. La laparoscopia prácticamente se ha ido abandonando en este proceso, aunque los avances en cirugía laparoscópica han abierto una nueva puerta en el tratamiento quirúrgico. 4. Tratamiento En los últimos años ha habido un cambio importante en la apreciación sobre el tratamiento del embarazo ectópico debido a varios factores, como son el mejor conocimiento de la biología del EE, con la evidencia de la posibilidad de resolución espontánea en algunos casos; el perfeccionamiento de los métodos diagnósticos de esta patología, que han condicionado un diagnóstico más precoz y seguro de la misma (ectópico inicial no roto). Se ha producido una modificación en la presentación clínica del EE, con disminución de los casos agudos, con alteración hemodinámica, y se diagnostican cada vez más frecuentemente formas no rotas, iniciales y asintomáticas (1). En la actualidad se ha evolucionado hacia una cirugía más conservadora (bien sea laparotómica o laparoscópica) y hacia un tratamiento no quirúrgico (expectante o médico). El objetivo en el tratamiento del EE sería la evolución hacia métodos más sencillos, más conservadores, con menos complicaciones, de menor coste económico, con más fácil recuperación clínica y con menores secuelas sobre la futura fertilidad; la tendencia sería en definitiva, hacia tratamientos médicos o mínimamente intervencionistas. 4.1. Tratamiento no quirúrgico 4.1.1. Conducta expectante La conducta expectante es la forma extrema de tratamiento no quirúrgico y consiste en la simple observación y el control estricto de la analítica, clínica y ecografía de la paciente, con la esperanza de que se produzca una interrupción de la gestación ectópica, que termine por producir un aborto tubárico o por reabsorberse en el interior de la trompa, posibilidades éstas bien documentadas en los trabajos clásicos de arias-Stella en 1954 o Cox y Steimberg en 1942. El objetivo del tratamiento, en la mayoría de los casos, es conservar la trompa afectada sin intervención y causando el mínimo daño tubárico. No obstante, desconocemos si dejar tejido trofoblástico puede causar oclusión tubárica y adherencias peritubáricas, incluso se plantea que este no sea el método ideal en aquellas pacientes que deseen preservar su fertilidad (6). Tampoco existe un método efectivo para saber qué EE se reabsorberán y en cuáles se producirá la rotura, a pesar de los avances en los métodos diagnósticos. La determinación de la UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 5 de 15 MÁSTER EN REPRODUCCIÓN HUMANA b-hCG no es un marcador adecuado para predecir la evolución de cada caso, ya que se han comunicado roturas con valores muy bajos y en descenso. Uno de los mayores inconvenientes es el prolongado período de hospitalización a que obliga tomar esta actitud, en la mayoría de los casos, superior a un mes (6,7), además de exigir un control exhaustivo de la paciente mediante vigilancia clínica, ecográfica y de laboratorio. En cuanto a los métodos predictivos para saber cuál será la evolución del ectópico, en la actualidad se está trabajando en los marcadores analíticos y en el estudio de proteínas endometriales (7). Según los reportes de la literatura publicada al respecto, de 463 casos tratados de forma expectante, se contempló un 78% de éxitos, un 82.8% de permeabilidad tubárica, un 60.5% de gestaciones intrauterinas y un 15% de recidivas (7, 8, 11,12). El tratamiento expectante es, pues, una alternativa para algunos casos concretos muy bien seleccionados, con un saco menor de 2-3 cm., trompa no rota y sin sangrado activo, asintomáticos o poco sintomáticos (hemodinámicamente estables) y con títulos de b-hCG bajos (250-1000 UI/L) y en descenso; en pacientes con aborto tubárico confirmado; en EE persistente (tras cirugía conservadora) y procurando que se trate de mujeres disciplinadas con una buena relación médico-paciente (6-8). 4.1.2. Tratamiento farmacológico primario El objetivo del tratamiento médico del embarazo ectópico consiste en la utilización de un fármaco que permita una resolución más rápida del mismo que la conducta expectante, bien sea provocando un aborto tubárico o bien induciendo la reabsorción del embarazo ectópico (5, 8,9). Este podría ser el tratamiento ideal si consiguiera disminuir los costes, la lesión tubárica y aumentar el potencial de fertilidad, aplicándose una vez se tenga el diagnóstico por los métodos mencionados sin tener que llegar a la laparoscopia. Existen diversas sustancias capaces de actuar sobre las células trofoblásticas y detener su desarrollo, y que han sido utilizadas por distintas vías, aplicándose tanto a nivel sistémico como local. Este tratamiento puede aplicarse en forma primaria para resolver el embarazo ectópico, o bien puede aplicarse de modo complementario al tratamiento quirúrgico, para tratar el embarazo ectópico persistente (sería tratamiento médico secundario). Tratamiento médico sistémico Se han utilizado fundamentalmente tres sustancias por vía general: el metotrexato, la actinomicina-D y el RU-486. Metotrexato: Interfiere en la síntesis de DNA y la multiplicación celular mediante la inhibición de la dihidrofolatorreductasa, que participa en la reducción del ácido dihidrofólico a tetrahidrofólico, esencial en la síntesis de las bases purina y timidita, que forman parte del DNA. Dado que el metotrexato interfiere con la síntesis del DNA, su acción es más efectiva si UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 6 de 15 MÁSTER EN REPRODUCCIÓN HUMANA las células son expuestas durante la fase S del ciclo de replicación celular, por lo cual se encuentra particularmente efectivo en tejidos con rápida división celular como las células en transformación tumoral y las células trofoblásticas derivadas del trofoectodermo (9). El tejido trofoblástico es especialmente sensible a esta acción del fármaco, lo cual lo hace útil para el tratamiento del ectópico y para mejorar su pronóstico, de la misma forma que lo ha hecho en el caso de la enfermedad trofoblástica gestacional. En pacientes con fallo renal, la dosis necesita ser ajustada para prevenir toxicidad derivada de una disminución de su aclaramiento. Una pequeña fracción de metotrexato puede excretarse por las vías biliares, pero la mayor parte lo hace por la acción de filtración glomerular y secreción tubular activa. Aproximadamente el 35% de la droga se une a proteínas del plasma, y otras dogas como las sulfonamidas, salicilatos, tetraciclina, cloramfenicol y fenitoína, pueden desplazarlo de sus sitios de unión a proteínas plasmáticas, aumentando sus niveles libres y potenciando su toxicidad (9). Se han publicado cientos de casos tratados por vía general, que incluye tanto la vía intravenosa como la intramuscular, así como la administración oral. Puede utilizarse como tratamiento primario, para tratar y prevenir embarazos ectópicos persistentes y en el caso de embarazos de ubicaciones inusuales. La eficacia es muy alta, rondando un 95%, con 80% de trompas repermeabilizadas y tasa de gestación del 40%. La incidencia de EE posterior es de aproximadamente 10%. Las dosis y pautas de administración han sido muy diversas, en algunos casos acompañados del uso de ácido folínico para atenuar los efectos secundarios; estos aparecen en un 20-50% de los casos, siendo los más frecuentes las alteraciones gastrointestinales (estomatitis, náuseas, malestar abdominal, alteración de enzimas hepáticas), efectos depletores sobre médula ósea (leucopenia, trombocitopenia), dermatitis, neumonitis intersticial y nefrotoxicidad. Afortunadamente la experiencia con el uso de metotrexato ha sido excelente, todos estos efectos son generalmente reversibles y pueden controlarse disminuyendo la dosis o interrumpiendo el tratamiento (17). Básicamente se han descrito protocolos de administración de dosis única y múltiple, los cuales son señalados en la Tabla Nº 2. La indicación de este tratamiento incluye casos de pacientes clínicamente estables, sin sangrado activo, con masas menores a 3.5 cm. y títulos bajos de hCG. Existen reportes muy dispares en cuanto a estos criterios, señalando algunos autores valores máximos de hCG para aplicar el tratamiento tan dispares como 1500 y 25000UI/L. También se ha considerado la presencia de latido cardíaco como de mal pronóstico, ya que implicaría un estado avanzado del desarrollo y con mayor riesgo de hemorragia al desprenderse de su lugar de implantación, sin embargo hay reportes de resultados satisfactorios con esta condición. Actinomicina-D: Es un quimioterápico más potente que el metotrexato que actúa interfiriendo en la síntesis de DNA y RNA. UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 7 de 15 MÁSTER EN REPRODUCCIÓN HUMANA Fue utilizado por primera vez en un caso de embarazo ectópico intersticial, en dosis de 0.5 mg IV/día en ciclos de 5 días con una semana de intervalo (66). Tiene menor toxicidad hepática y renal y parece no tener efecto nocivo sobre gestaciones posteriores, por lo cual podría ser una buena alternativa al metotrexato, sobre todo en gestaciones avanzadas en las que éste podría tener algún fallo. No obstante la experiencia es escasa. RU-486: Se han realizado algunas experiencias con éste fármaco, antagonista de la progesterona, el cual tiene 5 veces más afinidad por su receptor que la progesterona. Se ha empleado como abortivo precoz y existe una serie de 28 casos de pacientes con embarazos ectópicos en los cuales se utilizó una dosis de 200mg/día/4 días, con sólo 4 éxitos. En otro caso con un EE persistente tras salpingostomía, en dosis única de 650 mg VO, tampoco tuvo éxito y se solucionó mediante la administración de metotrexato (18). Tratamiento médico local La toxicidad del metotrexato y sus efectos secundarios llevaron a la utilización de pequeñas dosis del mismo, introducidas directamente en el saco gestacional con el propósito de disminuir la dosis total necesaria y, simultáneamente, reducir los efectos secundarios a nivel general. Fernández, en un estudio prospectivo aleatorizado, refiere que la inyección de 1mg/Kg. de metotexato en el saco gestacional es tan efectiva como su administración sistémica, y tiene la ventaja de disminuir los efectos secundarios (19). Parece que con esta pauta no es necesaria la utilización de ácido folínico. Aconseja la vía de administración local siempre que el saco sea fácilmente accesible (19). Los criterios de selección son similares a los del resto de los tratamientos no quirúrgicos; si bien se han intentado varias vías de acceso, la vía laparoscópica tiene la ventaja de ser ideal para el diagnóstico y permite una mejor valoración de las condiciones del ectópico, del estado de la trompa y de la pelvis. Tratamiento local con acceso laparoscopio: Metotrexato: Ha sido el primer fármaco en ser administrado por esta vía y el más utilizado. Los resultados en la bibliografía son similares a los de la vía sistémica. Hay quienes piensan que su uso no está exento de efectos sistémicos, y existen dudas sobre efectos tóxicos locales derivados de reacciones titulares en el interior de la trompa o por proximidad sobre las células germinales del ovario, que puedan afectar la futura fertilidad (6). Prostaglandinas: La prostaglandina F2-alfa ha sido utilizada por diversos autores por los siguientes efectos: aumento del peristaltismo tubárico, vasoespasmo de las arterias del meso y disminución de la producción de progesterona por el cuerpo lúteo. Estos autores informan porcentajes de éxito superiores al 90% y una permeabilidad tubárica del 95% (13), si se aplica en gestaciones con baja actividad trofoblástica. Se ha asociado a severos efectos secundarios como molestias digestivas y complicaciones cardiovasculares, con algún caso de edema agudo de pulmón, hipertensión arterial y arritmias. UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 8 de 15 MÁSTER EN REPRODUCCIÓN HUMANA Glucosa hipertónica: Para evitar los efectos secundarios de todos estos agentes se ha intentado la inyección en el interior del saco de glucosa hipertónica (10ml de suero glucosado al 50%), la cual induce necrobiosis local, probablemente por deshidratación celular. El tratamiento es seguro, económico, desprovisto de efectos secundarios y efectivo en las gestaciones ectópicas no rotas con valores de hCG inferiores a 2500 mUI/L (14). Los estudios histológicos no han mostrado lesiones relevantes en la pared tubárica; lo que no parece estar claro es la ventaja respecto a la salpingostomía, en cuanto a la frecuencia de ectópico persistente. Tratamiento local con acceso por punción con control ecográfico El tratamiento farmacológico local también puede realizarse con control ecográfico, inyectando distintas sustancias en el interior del saco. Se ha utilizado tanto la vía transvaginal como la abdominal e incluso la transvesical. La ecografía presenta la ventaja de que puede realizarse ambulatoriamente, sin requerir anestesia, con el inconveniente de que no siempre el saco gestacional ectópico es visualizable. Al igual que en la vía laparoscópica se han utilizado distintas sustancias, tales como: Metotrexato: la primera experiencia se publicó en la revista Lancet en 1987, por Feichtinger, quien utilizó una dosis de 10 mg de metotrexato y obtuvo un éxito de 89% (15). Existe bastante disparidad en la dosis administrada por esta vía, así como en los resultados, que son aceptables. Prostaglandinas: se han utilizado en escaso número de pacientes y los resultados son malos excepto cuando se combinan con metotrexato. Cloruro potásico: ya que actúa fundamentalmente sobre el corazón fetal produciendo asistolia, se ha empleado más frecuentemente en reducciones embrionarias selectivas en gestaciones múltiples. También en gestaciones heterotópicas, para actuar selectivamente sobre la gestación ectópica, respetando la intrauterina, cosa que no puede hacerse con el metotrexato sistémico ni local (16). 4.1.3. Tratamiento farmacológico secundario: embarazo ectópico persistente No siempre es posible garantizar la extirpación completa del tejido trofoblástico tras la cirugía conservadora; éste puede persistir parcialmente, crecer y proliferar, seguir produciendo hCG, pudiendo hacer sangrar la trompa y causando síntomas clínicos. Todo ello hace necesario el control de hCG en la cirugía conservadora del embarazo ectópico, que debe realizarse cada 3-6 días. Lo normal es que en 72 horas la b-hCG prácticamente se negativice o sea inferior al 20% de los valores previos a la cirugía. Si son superiores a 1000 UI/L en el séptimo día y sobre todo si permanecen estables o aumentan, se establece el diagnóstico de embarazo ectópico persistente. Su incidencia es mucho mayor en la cirugía conservadora que en la radical, y varía entre un 3.5 y 8.4% de los casos. Ante esta eventualidad se pueden tomar las siguientes actitudes: Si la b-hCG va en descenso y la paciente se encuentra asintomática, cabe la posibilidad de realizar una conducta expectante. UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 9 de 15 MÁSTER EN REPRODUCCIÓN HUMANA Si los valores de la b-hCG se mantienen iguales o aumentan puede intervenirse de nuevo, realizando generalmente una salpingectomía. La otra opción en este caso es realizar tratamiento médico sistémico (siendo el protocolo de dosis única el más utilizado), que quizá sea la opción más adecuada en virtud de la dificultad de localizar un pequeño foco de actividad en una trompa ya tratada, con el consiguiente riesgo de infección pélvica tras una segunda laparoscopia. El metotrexate también ha sido utilizado en el manejo de gestaciones extratubáricas, como el caso de implantaciones cervicales, intersticiales, ováricas o abdominales, donde la alternativa quirúrgica puede conllevar a una mayor morbilidad o compromiso reproductivo. 4.2. Tratamiento quirúrgico El primer tratamiento utilizado fue el radical, justificado por la alta mortalidad que presentaba esta patología. La introducción de la cirugía laparoscópica se ha podido realizar un diagnóstico previo a su rotura y un intento por salvar la trompa. Por otro lado la cirugía endoscópica ha permitido reducir el uso de la vía laparotómica en un interés por preservar la fertilidad, así como una reducción en los costos (17). 4.2.1Tratamiento conservador Consiste en realizar una salpingostomía con posterior aspiración del material trofoblástico. No se recomienda realizar la sutura posterior de la trompa. El primer factor a considerar para realizar este tratamiento es la posibilidad de intervención del EE. Para esto debe asentarse en una trompa sin alteraciones, ya que la presencia de un ectópico cornual o de una trompa alterada corre el riesgo de una hemorragia incoercible que obligue a practicar una salpingectomía. También es necesario realizar una buena limpieza del material trofoblástico, así como considerar la salpinguectomía si se observa un tamaño del saco mayor de 4 cm., mala accesibilidad a la trompa, hCG >20000 UI/L o rotura tubárica. Por último debemos considerar el deseo de fertilidad posterior de la pareja con el pronóstico real de fertilidad de la mujer, para intentar ofrecer la máxima posibilidad de embarazo intrauterino y limitando el riesgo de recidiva. En este sentido la tasa de recidiva no ofrece diferencias entre la cirugía conservadora y la radical (alrededor del 11%). La opción de cirugía conservadora de la trompa por vía laparoscópica es la opción quirúrgica principal, junto con el tratamiento médico sistémico con metotrexato. 4.2.2. Tratamiento quirúrgico radical La salpingectomía se realizará en casos en que no sea posible la cirugía conservadora con el acceso laparoscópico. Recurriremos a la laparotomía en caso de inestabilidad hemodinámica de la paciente, así como cuando existan adherencias importantes que contraindiquen la técnica laparoscópica. La indicación de cirugía radical va a depender en gran medida de los deseos de fertilidad posterior así como del estado de la trompa. UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 10 de 15 MÁSTER EN REPRODUCCIÓN HUMANA 5. Lecturas recomendadas Barnhart K, Esposito M, Coutifaris Ch. Reproductive endocrinology. An update on the medical treatment of ectopic pregnancy, in Obstetrics and Gynecology Clinics 2000. W.B. Saunders Company. Vol 27. Nº 3. Pouly JL. Estrategias del tratamiento del embarazo ectópico, en Cuadernos de medicina reproductiva 1996. Ed. Panamericana. Vol 2. Nº 1. Pp 157-171. UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 11 de 15 MÁSTER EN REPRODUCCIÓN HUMANA 6. Tablas Tabla nº 1 FACTORES QUE PUEDEN MODIFICAR EL TRANSPORTE DEL EMBRION Desarrollo anormal del huevo FACTORES OVULARES Alteraciones en la migración Alteraciones congénitas Tumoraciones tubáricas o uterinas Enfermedad inflamatoria pélvica Cirugía pélvica previa Endometriosis Alteraciones de fase lútea Uso de DIU Anticoncepción hormonal postcoital Inducción de la ovulación Técnicas de reproducción asistida. FACTORES TUBARICOS OTROS FACTORES UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 12 de 15 MÁSTER EN REPRODUCCIÓN HUMANA TABLA Nº 2 Componente Dosis única Dosis múltiple Metotrexate 50mg/M2 1mg/Kg. Leucovorin NO 0.1 mg/Kg. Frecuencia de dosis Una dosis, repetir a la semana si es necesario Más de 4 dosis de cada una de las drogas Días alternos de las drogas hasta caída de hCG del 15% Monitorizar nivel de hCG Basal, día 4, día 7 Basal, días 1,3,5,7 hasta caída de hCG del 15% Administrar dosis adicional Segunda dosis el día 7 si hCG no ha caído en 15% Sucesivas dosis si hCG no ha caído en 15% del valor anterior. Máximo 4 dosis Monitorizar hCG Semanal hasta no ser detectable Semanal hasta no ser detectable UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 13 de 15 MÁSTER EN REPRODUCCIÓN HUMANA 7. Bibliografia Parrilla JJ, González E, Abad L. Embarazo ectópico, en: Reproducción Humana, Interamericana, 2002, pp.227. McGraw-Hill Parrilla JJ, Server J, Delgado JL et al Tratamiento no quirúrgico del embarazo ectópico, en Libro del año de Obstetricia y Ginecología. Saned Ed. 1994. Washington AE, Katz P. Ectopic pregnancy in the United Status: Economics Consecuentes and Payment Source Trends. Obstet and Gynecol 1993; Vol 81, Nº 2 pp.287-292. Coste J, Job-Spira N, Aublet-Cuvelier B et al. Incidence of ectopic pregnancy. First results of a population-based register in France. Hum Repr 1994; Vol 9 Nº 4 pp. 742-745. Pansky M, Golan A, Bukovsky I, Nonsurgical magnagement of tubal pregnancy. Necessity in view of the changing clinical appearance. Am J Obstet Gynecol 1991; Vol 164. Nº 3. pp 888895. Balasch J, Barri P. Treatment of ectopic pregnancy: the new gynaecological dilemma. Hum Repr 1994; Vol 9. Nº 3, pp 547-558. Ylostalo P, Cacciatore B et al. Expectant management of ectopic pregnancy. Obstet Gynecol 1992; Vol 80. Nº 3. Part 1. pp 345-348. Fernández H, Lelaidier C, Baton C et al. Return of reproductive performance after expectant management and local treatment for ectopic pregnancy. Hum Repr; Vol 6. Nº10. pp 14741477. Barnhart K, Esposito M, Coutifaris Ch. Reproductive endocrinology. An update on the medical treatment of ectopic pregnancy, in Obstetrics and Gynecology Clinics 2000. W.B. Saunders Company. Vol 27. Nº 3. Parrilla JJ, Abad L, Server J et al. Non-surgical treatment of ectopic pregnancy in the sole remaining tube. Hum Repr 1995; Vol 10 Nº 7. pp 1966-1888. Korhonen J, Stenman U-H, Ylostalo P. Serum human chorionic gonadotropin dynamics during spontaneus resolution of ectopic pregnancy. Fertil Steril 1994; Vol 61. pp 632-636. Shalev E, Peleg D, Tsabari A et al. Spontaneus resolution of ectopic tubal pregnancy: natural history. 1993. Vol 63. pp15-19. Egarter C, Hussleim P. Treatment of tubal pregnancy by prostaglandins. Lancet 1988; May. 14. pp 1104-1105. Lang P, Tamussino K, Honigl W. Treatment of unruptured tubal pregnancy by laparoscopic instillation of hyperosmolar glucose solution. Am J Obstet Gynecol 1992; Vol 166. Nº 5. pp1378-1381. UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 14 de 15 MÁSTER EN REPRODUCCIÓN HUMANA Feichtinger W, Kemeter P. Letters to the editor: Conservative tratment of ectopic pregnancy by transvaginal aspiration under sonographic control and metotrexate injection. Lancet 1987. Feb 14. pp381-382. Robertson DE, Moye M, Hansen JN. Reduction of ectopic pregnancy by injection under ultrasound control. Lancet 1987. Apr 25. pp974-975. Pouly JL. Estrategias del tratamiento del embarazo ectópico, en Cuadernos de medicina reproductiva 1996. Ed. Panamericana. Vol 2. Nº 1. Pp 157-171. Kenigsberg D, Porte J. Medical treatment of residual ectopic pregnancy: RU 386 and metotrexate. Fert Steril1987; Vol 47. Nº 4. pp 702-703. Fernández H, Baton C, Benifla JL. Metotrexate tratment of ectopic pregnancy: 100 cases trated by primary transvaginal injection under sonographic control. Obstetrical and Gynecological survey 1993. Vol 161. pp 393-396. © 2012 – IVI Reservados todos los derechos UNIDAD 13: Embarazo ectópico BLOQUE I: ESTERILIDAD FEMENINA Página 15 de 15