Guia de quimica I
Anuncio

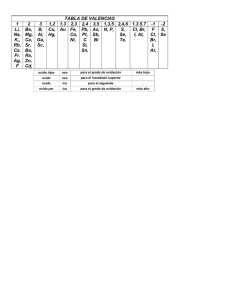
Competencia NOMENCLATURA DE COMPUETOS INORGANICOS 1. Óxidos básicos 2.- Óxidos ácidos 3.- Hidruros 4.-Hidracidos 5.- Sales sencillas 6.-Oxiacidos 7.-Hidroxidos 8.-Oxisales 1.- Aplicando reglas 1.- ¿como se llama? Obtención de un Compuesto 1 NOMENCLATURA DE COMPUESTOS INORGANICOS Cada momento de nuestra vida estamos en contacto con sustancias Químicas. El simple hecho de estar lavando tus manos con jabón, de colocarle limón a los churritos, incluso al lavarte los dientes implica estar en contacto con las sustancias químicas. Muchas de éstas sustancias no son naturales es decir no provienen de sustancias de organismos vivos, por lo que se llaman sustancias inorgánicas, generalmente éstas sustancias no contienen carbono, aunque se puede dar el caso como son el Ácido Carbónico que lo encontramos en la lluvia ácida, Óxido de Carbono IV, en la contaminación de los autos al quemar gasolina cundo no están afinados, Carbonato Ácido de Sodio, que lo usamos en casa al elaborar pasteles, y muchas más sustancias que puedes encontrar en el uso diario de productos químicos. Hoy en día se conocen casi cinco millones de compuestos químicos por lo que se creo un sistema, (un conjunto de reglas) que nos permite nombrar de igual manera en todo el mundo a todas las sustancias químicas, me refiero al lenguaje químico conocido como nomenclatura química, que proviene del latín nomen (nombre) y calare (a llamar). La nomenclatura es una parte muy importante del lenguaje de la química ya que el universo esta constituido por elementos y compuestos que son necesarios identificar y nombrar de manera que todos podamos entender. Esta nomenclatura, se rige por los dos criterios: el Ginebra o tradicional y el sistemático según la Internacional unión of pure and Applied Chemistry (I.U.P.A.C) con el único propósito de conseguir un lenguaje químico lo mas sencillo posible de las sustancias químicas. 2 ÓXIDOS Las aplicaciones de estos compuestos son de manera muy cotidiana, tal es el caso del la cal viva (CaO) utilizada en la construcción y como pasta de curación en dientes al mezclarse con liquido dental. La Gel de sílice (SiO2) son bolsitas blancas que suelen venir en aparatos electrónicos, calzado, ropa y otros objetos. Se presenta de forma granular en el interior de unas bolsitas, y tiene la función de absorber la humedad del espacio donde se encuentra. El (N2O) gas hilarante, el cual fue 74 usado durante mucho tiempo por los dentistas para que sus pacientes toleraran algunos procedimientos dentales dolorosos y por último el Cr2 O3 se utiliza para recubrir muchos metales y para protegerlos de la corrosión, como defensas, molduras y rines automotrices. Los óxidos son compuestos binarios, es decir están formados por dos elementos y se dividen en dos grupos. El oxigeno se puede combinar directamente con todos los elementos, excepto con los gases nobles (He, Ne, Ar, Kr, Xe, Rn), los halógenos (F, Cl, Br, I,) y algunos de los metales menos activos, como el cobre y el mercurio, que reaccionan lentamente para formar óxidos. Los Óxidos básicos o metálicos, son aquellos compuestos que se forman cuando se combina un elemento metálico con el oxigeno Fe 2 O3 Metal + Oxigeno o Oxido Metalico 3 Para formar los compuestos, las valencias con que trabaja cada elemento se intercambian, una vez formado el compuesto, el elemento metálico contiene la valencia del oxigeno y el oxigeno la valencia del elemento metálico. Cuando se combinan los elementos y sus valencias son numero pares, se realiza una operación matemática X 4 Y 2 o X 2Y4 X 2 Y4 XY2 Elementovalencia O 2 o Elemento2 Ovalencia Cuando el elemento a combinar con el oxigeno contiene una sola valencia, tal es el caso del grupo IA (Li+1, Na+!, K+!, Rb+!, Cs+!, Fr+!) y IIA (Be+2, Mg+2 Ca+2, Sr+2, Ba+2, Ra+2) de la tabla periódica, el método para nombrarlos consiste en poner la palabra oxido seguido el nombre del elemento metálico. Na 1 O 2 o Na 2 O Elementos con sus Compuesto respectivas valencias Na 2 O Na 1O 2 K 2O K 1O 2 2 2 Ca2 O2 = CaO Ca O 2 2 Ba 2 O2 = BaO Ba O Nombre tradicional Oxido de sodio Oxido de Potasio Oxido de Calcio Oxido de bario Ahora bien, si el metal presenta dos valencias podemos seguir utilizando el método tradicional para nombrarlos, el cual consiste en el nombre con la terminación “OSO” para el menor y la terminación “ICO” pera el de valencia mayor. Elementos con dos valencias Compuesto Fe2,3 Fe2 O2 = FeO Fe 2 O3 Oxido ferroso Oxido férrico Co2,3 Co2 O2 = CoO Co2 O3 Oxido cobaltoso Oxido cobaltico Nombre Tradicional 4 Otra forma de denominar a los óxidos es nombrar el metal con el número de oxidación representado con números romanos entre paréntesis. Ésta manera es la recomendad por la unión internacional de química pura y aplicada (IUPAC) por sus siglas en Ingles. Elementos con sus respectivas valencias Fe3O 2 Compuesto Fe 2 O3 Nombre IUPAC Oxido de de Hierro(III) Oxido de Titanio (IV) Ti 4 O 2 Ti 2 O4 = TiO2 3 3 Mg 2 O3 Oxido de Manganeso (III) Cu 3O 2 Cu 2 O3 Oxido de Cobre (III) Mg O Es necesario precisar que este sistema de números romanos solo se emplea para señalar a cationes que pueden tomar más de una carga. En ningún caso debe emplearse con metales que forman solo un tipo de catión. 1. Escribe el nombre de los siguientes óxidos metálicos: CaO _______________________________________ _______________________________________ b) MgO _______________________________________ c) Cs 2 O _______________________________________ d) Cs 2 O _______________________________________ e) Al 2 O3 A) 2.- Dar el nombre, a los siguientes compuestos. Compuesto Rb2 O Sr2 O2 Cu 2 O2 Cu 2 O Co 2 O Nombre tradicional IUPAC 5 3.- Obtener la formula de los siguientes compuestos Nombre tradicional Formula Oxido de bario Oxido de magnesio Oxido de estroncio Oxido Férrico Oxido cobaltico Oxido de calcio Oxido ferroso Oxido de níquel (III) Y los Óxidos no metálicos o anhídridos se forman cuando se combina un elemento no metálico con el oxigeno. No Metal + Oxigeno o Oxido no Metalico SO2 Debido a su composición exclusiva de no metales, sus reglas de nomenclatura tienen algunas diferencias respecto a los óxidos anteriores. Estos compuestos se pueden nombrar de dos formas. De acuerdo a la cantidad de oxigeno que tenga. Se le antepone a la palabra oxido el prefijo que nos indique la cantidad de oxigeno que presenta el compuesto, seguida de la preposición “de” y al último, el nombre del elemento no metálico. Para indicar el numero de átomos que conforman al compuesto, se utilizaran prefijos numerales como; mono, di, tri, tetra, penta, hexa hepta, octa, nona y deca. Compuesto CO CO2 N 2 O5 SO2 Nombre Monóxido de carbono Dióxido de Carbono Pentoxido de dinitrogeno Dióxido de azufre 6 Con la palabra anhídrido, mas la raíz del nombre del no metal, agregando la terminación según el grado de oxidación del no metal. Prefijos Hipo Oso Oso ico Per ico Con 4 valencias con 3 valencias con 2 valencias Compuesto Nombre Compuesto Nombre Compuesto Nombre Br2 O Anhídrido Hipobromoso SO2 Anhídrido Hiposulfuroso CO Anhídrido Carbonoso Br2 O3 Anhídrido bromoso S 2 O4 Anhídrido Sulfuroso CO2 Anhídrido Carbónico Br2 O5 Anhídrido brómico S 2 O6 Anhídrido Sulfúrico Br2 O7 Anhídrido Perbromico El elemento carbono contiene dos valencias(+2,+4) El azufre tienen tres valencias(2,4,6) 1. Escribe correctamente el nombre de los siguientes compuestos: C N 2 O3 ____________________________________ G MnO ____________________________________ ____________________________________ ____________________________________ ____________________________________ I 2 O5 ____________________________________ D SiO2 E Cl 2 O F CO2 f) 2. Escribe correctamente la formula de los siguientes compuestos a) monóxido de azufre ___________________________________ b) Monóxido de carbono __________________________________ c) Oxido de cloro (III) ____________________________________ d) anhídrido hipocloroso __________________________________ e) Pentóxido de difósforo _________________________________ f) Anhídrido fosforoso ____________________________________ 7 HIDRUROS Los Hidruros son compuestos binarios, al unirse un Metal con un Hidrógeno, forman Hidruros Metálicos y al unirse con el No Metal forman los Hidruros No metálicos. Para formar a los hidruros metálicos, se necesitan los metales del grupo I y II de la tabla periódica. Para nombrarlos se inicia con la palabra Hidruro enseguida el nombre del metal. Cuando el hidrogeno reacciona para formar hidruros presenta valencia -1 ya que tiene mayor electronegatividad que estos metales Li 1 H 1 o LiH Tradicional NaH Hidruro de Sodio criterio Ginebra Criterio U.I.P.A = Hidruro de cobre I CuH FeH 2 = Hidruro Ferroso FeH 3 = Hidruro Férrico CuH 2 = Hidruro de cobre II De los Hidruros no metálicos más importantes se encuentran el Amoniaco (Trihidruro de Nitrógeno y el Amonio (Tetrahidruro de nitrógeno). Evaluación formativa 1.- Compuestos binarios formados por un metal con el hidrogeno a) Óxidos b) Hidróxidos c) Sales d) Hidruros d) Oxácidos 2.- Son compuestos binarios que resultan de la combinación de un metal con el oxigeno. a) Óxidos b) Hidróxidos c) Sales d) Hidruros d) Oxácidos 3.- Compuestos que resultan de la combinación de un no metal con el oxigeno se les conoce como: a) Óxidos b) Hidróxidos c) óxidos ácidos d) Hidruros d) Oxácidos : 8 Dar el nombre y obtener su formula de los siguientes compuestos Formula LiH Nombre Nombre Hidruro de sodio Formula Hidruro de estroncio Hidruro de Magnesio KH CaH 2 Para tu reflexión Pirotecnia La pólvora es una mezcla de carbono, azufre, una sal formada por perclorato de potasio y otros componentes. Esta sustancia es un poderoso oxidante que al reaccionar con los demás componentes de la mezcla produce diversos óxidos todos ellos gaseosos. Si la reacción iniciada por la mecha se lleva a cabo debido a la rápida en un espacio cerrado, se produce una explosión debido a la rápida formación de los gases. Sin embargo, si existe un pequeño orificio, los productos gaseosos escapan por el e impulsan al conjunto, formando un cohete pirotécnico. El trasbordador espacial estadunidense utiliza el mismo principio para ponerse en orbita, aunque es este caso cada despegue requiere 750 kg de oxidante. Si a la pólvora se le añade determinados metales o compuestos de dichos metales, se producen explosiones de varios colores. 75 Efecto Luz roja Luz verde Luz azul Luz amarilla Luz blanca Humo blanco Humo de colores Chispas blancas Silbato Nitrato, cloruro o carbonato de estroncio Nitrato, clorato o cloruro de bario Carbonato, sulfato y oxido de cobre (II)cloruro de cobre (II). Sodio, oxalato de sodio o criolita Magnesio Mezcla de nitrato de potasio y azufre Mezcla de clorato de potasio, azufre y colorantes Aluminio, magnesio. Benzoato de potasio o salicilato de sodio. 9 HIDRACIDOS Cuando vamos al supermercado encontramos una gran variedad de productos químicos, de los cuales los que más se usan está por ejemplo el ácido muriático, sin embargo, la mayoría de la gente no lo nombra como Ácido Clorhídrico, el cual es un Hidrácido, lo conoce más como ácido muriático, veamos entonces cuál es su nombre según los diferentes criterios 76 Combinaciones binaria del hidrógeno con los elementos F, Cl, Br, I, S, Se, Te, reciben el nombre especial de hidrácidos, pues tales compuestos, en solución acuosa, se comportan como ácidos. Por esta razón, cuando se hallan disueltos en agua, se nombran anteponiendo la palabra ácido al nombre abreviado del elemento (que junto con el hidrógeno forma la combinación), al que se le añade la terminación hídrico. Los referidos elementos actúan en tal caso con su número de oxidación más bajo: -1 para los cuatro primeros y -2 para los tres últimos. Aplicando las reglas ya mecionadas, de acido seguida del nombre del no metal con la terminacion hidrico Formula HCl HF H2S HBr Nombre Criterio Ginebra Ácido clorhídrico Ácido fluorhídrico Ácido sulfhídrico Ácido bromhídrico Criterio U.I.Q.P.A. Cloruro de Hidrógeno. Fluoruro de Hidrogeno Sulfuro de Hidrogeno Bromuro de Hidrogeno a. Escribe correctamente el nombre de los siguientes compuestos a) HBr _______________________________________ b) H 2 Se ______________________________________ c) HCl _______________________________________ d) LiH ________________________________________ e) CaH 2 _______________________________________ f) H 2 S ________________________________________ g) NaH _______________________________________ h) H 2Te _______________________________________ i) HI _________________________________________ 10 SALES SENCILLAS Este tipo de compuestos se forman al reaccionar un metal con un no metal, es decir, son compuestos binarios. Se obtienen al reaccionar un hidrácido con un metal o un hidróxido. Son combinaciones iónicas de los no metales F, Cl, Br,I, S, Se, Te, con elementos metálicos, para nombrarlos debemos sustituir la terminación hídrico del ácido de donde proviene, por la terminación “uro”, después se nombra el metal. Estas Sales Binarias, son el resultado de unir ácido con una base, fenómeno que se da en las reacciones de neutralización: Ácido + Base Sal + Agua HCl + NaOH o NaCl + H 2 O SALES BINARIAS: Metal + No Metal Grupo: VIA y VIIA (principalmente) Formula PbCl 4 Al 2 S 3 KCl KCl LiBr Nombre cloruro de plomo sulfuro de aluminio (III) cloruro de potasio ioduro de cobre (I) bromuro de litio y si este presenta valencias variables, se tendrá que agregar la terminación “oso” o “ico” según corresponda. Algunos ejemplos de este tipo de sales son: Formula MgCl 2 FeCl 3 CuBr CuBr2 Nombre cloruro de magnesio cloruro férrico Bromuro Cuproso bromuro cúprico 11 1. Escribe correctamente el nombre de los siguientes compuestos: a) Fe 2 S 3 _____________________________ b) NaCl _____________________________ c) FeCl 3 _____________________________ d) AlI 3 _____________________________ e) MgCl 2 _____________________________ f) FeCl 2 ____________________________ g) Cr2 S 3 _____________________________ h) Ni 2 S 3 ______________________________ i) PbF4 ______________________________ 2. Escribe correctamente la formula de los siguientes compuestos: Nombre Formula Cloruro ferroso Bromuro de hierro (II) Bromuro de cobalto (II) Seleniuro de aluminio Fluoruro de calcio Yoduro de cesio Fluoruro de aluminio 12 OXIACIDOS Otra forma de nombrar a los compuestos son los Oxiácidos, función química que tiene los elementos Hidrógeno + No Metal + Oxígeno. Encontramos ejemplos de estas sustancias como parte complementaria de algunos compuestos como el que usamos para desengrasar hornillas de estufa, destapar caños o tuberías (H2SO4), o como conservador de alimentos como el ácido fosfórico. Los oxiácidos se encuentran formados por tres elementos, por lo que se clasifican como compuestos ternarios. Su fórmula típica es, H a X b Oc . En los oxiácidos, el oxígeno actúa con índice de oxidación -2, el hidrógeno con índice de oxidación +1, por lo que conocida la fórmula y teniendo en cuenta que el índice de oxidación resultante para una molécula ha de ser nulo, resulta sencillo determinar el número de oxidación correspondiente al elemento central X, que será siempre positivo. Los oxiácidos como su nombre lo indica son ácidos que contienen oxigeno y se obtienen a partir de un hidrácido más agua. Para nombrarlos existen tres maneras, las cuales son: Evaluación formativa 1.- Compuestos binarios formados por un No metal en combinación con el hidrogeno. a) Hidrácido b) Hidróxido c) Sales d) oxido 2.- Compuestos ternarios formados al combinarse un elemento metálico con el radical OH a) Óxidos b) Hidróxidos c) Sales d) Hidruros 3.- Compuesto ternario que resulta al combinarse el hidrogeno, con un no metal y el oxigeno. a) Óxidos b) Hidróxidos c) óxidos ácidos d) oxácido 4.- Este tipo de compuestos se forman al reaccionar un metal con un no metal (F, Cl, Br, I, S, Te, Se). a) Sales b) Hidróxidos c) óxidos ácidos d) Sales sencillas 13 1. Cuando el compuesto forma un solo oxácido. Formula Raíz del elemento Terminación Carbon ico H 2 CO2 Acido Bar ico H 3 BO3 2. Cuando en la reacción, el compuesto puede formar dos oxiácidos, utilizamos la terminación “oso”, para el que presenta menos oxigeno, y la terminación “ico” para el que presenta más oxigeno. Formula HNO 2 HNO 3 Acido Raíz del elemento Nitr Nitr Terminación oso ico H 2 SO3 sulfur oso H 2 SO4 Sulfur ico 3. Si del compuesto se producen más de dos oxiácidos, utilizaremos el prefijo “hipo” para el que contenga la menor cantidad de oxigeno; y el prefijo “per” para el oxiácido que tenga la mayor cantidad de oxigeno, con la terminación “oso” o “ico”, según corresponda. Formula HClO HClO 2 HClO 3 HClO 4 Acido Prefijo Hipo ----per Raíz del elemento clor clor clor Terminación oso oso ico clor ico 1. Escribe correctamente el nombre de los siguientes compuestos a. H 2 CO 2 ___________________________________________ b. H 2 CO3 ___________________________________________ c. H 2 SO4 ___________________________________________ d. H 3 PO4 ___________________________________________ e. HNO 3 ___________________________________________ f. H 2 SeO4 __________________________________________ 14 2. Escribe correctamente la formula de los siguientes compuestos Nombre Formula Acido sulfuroso Acido carbónico Acido fosforoso Acido telúrico Acido carbónico Acido nítrico Fluoruro de aluminio Para tu reflexión Electrolitos El cuerpo humano contiene sales en forma de iones a las que se les llama electrolitos, los cuales son indispensables para la vida. Ion t1 Na -1 Cl t2 Ca -2 HCO3 t1 K Función Catión primario extracelular, mantiene la presión osmótica en la sangre y tejidos; es necesario para la actividad nerviosa y muscular Anión extracelular; es necesario para la secreción del jugo gástrico; participa en el transporte de O2 y CO2 en la sangre. Es necesario pata huesos y dientes y para la actividad muscular. Es necesario como amortiguador para mantener el equilibrio acidobase de la sangre. Catión primario intracelular, mantiene la presión osmótica en la célula; es necesario para la actividad nerviosa y muscular. 15 HIDROXIDOS Los hidróxidos se clasifican como compuestos ternarios ya que están formados por tres elementos; hidrogeno, oxigeno y un metal. Un hidróxido está formado por la combinación del grupo hidróxido o hidroxilo (OH)-, con un ión positivo por lo general metálico. El grupo OH- es un caso típico de ión poliatómico negativo, y a efectos de nomenclatura se trata como si fuera un solo elemento con grado de oxidación (-1); de ahí que los hidróxidos sean considerados como compuestos seudobinarios. Los hidróxidos se comportan químicamente como bases; es más, constituyen las bases típicas. Como ya se menciono, en los hidróxidos el hidrogeno y el oxigeno se encuentran unidos formando el radical hidróxido (OH-) el cual otorga origen a su nombre, aunque también se les llama bases. Los hidróxidos o bases, se obtienen por la reacción de un óxido básico con agua. 1.- Cuando el elemento tenga una sola valencia Formula NaOH Ca OH 2 Nombre Tradicional Hidróxido de sodio Hidróxido de calcio 2.- Si se da el caso de que el elemento metálico presente más de una valencia, para nombrarlo se utilizará de forma genérica la palabra hidróxido, seguida del nombre del metal, indicando entre paréntesis en números romanos la valencia del elemento metálico o la terminación “oso” o “ico” según el grado de oxidación que corresponda. Formula Nombre Tradicional Criterio U.I.Q.P.A FeOH 2 Hidróxido ferroso Hidróxido de hierro (II) Hidróxido férrico Hidróxido de hierro (III) FeOH 3 16 1. Escribe correctamente los nombres de los siguientes compuestos: a) AgNO3 ________________________________ b) Cu OH 2 _______________________________ c) Al OH 3 _______________________________ d) Al 2 SO4 3 ______________________________ e) FeOH 2 ________________________________ f) FeOH 3 _______________________________ g) Mg OH 2 ______________________________ 17 OXISALES Las Sales Ternarias son compuestos llamados también Oxisales, provienen de los oxiácidos (ejemplo HNO3) con una base (ejemplo KOH), si las juntamos tendremos el nitrato de potasio (KNO3) + Agua. HNO3 + KOH KNO3 + H2O Es interesante conocer diferentes usos de las sales como el Sulfato de Cobre II, la metalurgia del cobre varía con la composición del mineral. Los minerales que contienen cobre nativo, se trituran, se lavan y se separa el cobre para fundirlo y prepararlo en barras. Si la mina consiste en óxido o carbonato de cobre, se tritura y se trata con ácido sulfúrico diluido para producir sulfato de cobre disuelto del que se obtiene el metal por electrólisis o, utilizando chatarra, por desplazamiento con el hierro. Para nombrar a las oxisales se utiliza el nombre del anión, que indica el ácido de donde proviene, pero no debemos de olvidar cambiar la terminación; si el ácido termina en “oso”, la sal deberá de terminar en “ito”; si el ácido termina en “ico”, la sal deberá de terminar en “ato”, y enseguida el nombre del elemento metálico. Ion NO2 Nombre Nitrito NO3 Nitrato 2 3 SO Sulfito SO42 Sulfato ClO3 Clorato CO 32 Carbonato PO 3 4 2 4 2 4 Fosfato ClO Clorito ClO Perclorato CrO Cromato 18 Acido HNO 2 HNO 3 Nombre del acido Ácido nitroso Ácido nítrico Oxisal NaNO2 NaNO3 Nombre de la sal Nitrito de sodio Nitrato de sodio H 2 SO3 Ácido sulfuroso K 2 SO3 Sulfito de potasio H 2 SO4 Ácido sulfúrico K 2 SO4 Sulfato de potasio Evaluación formativa Escribe el nombre de los siguientes compuestos, investiga para que se utilizan cada uno de ellos y en que productos de uso domestico, fábrica, talleres, etc, las puedes encontrar: 1.- CuCl _____________________________ 2.-FeCl2 _____________________________ 3.-CuNO2____________________________ 4.-NaOH_____________________________ 5.-MnO2_____________________________ 19 Para saber más Un enfoque químico El colesterol: lo bueno y lo malo accidentes cardiovasculares como el El publico esta enterado de que tener infarto del miocardio. alto el coleterol es malo para su salud y El aunque hay personas que saben que el colesterol se relaciona con las grasas, que obstruye las arterias y pede provocar infartos, la mayoria desconoce que se trata de un indispensable compuesto para el quimico fucionamiento normal de nuestro organismo y en ocasiones piensa incluso que es una enfermedad. ¿Qué esv el colesterol? de las membranas de muchas celulas animales; cuando una celula se divideo rompe tiene que formar una membrana nuva y para ello necesita colesterol. Este compuesto se encuentra tambien en las lipoproteinas del plasma sanguineo. Ademas de servir como elemento estructural de muchas membranas, el colesterol es importante precursor de muchos otros esteoides biologicameteactivos, como los acidos biliares, numrosas hormonas y la vitamina D3. El colesterol s tambien un nutrimento. ni es un en si una veneno, los animaes lo producen en su organismo y es esencial para el buen funcionmiento de este. Ahora bien, se ha demostrado que concentaciones elevadas de colesterol en la sangre conducen al riesgo de enfermar de arterioesclerosis y sufrir accidentes paises personas como han Estados Unidos modificado su las dieta disminuyendo el consumo de grasas animales para reducir la concentracion de colesterol en su sangre. En terminos gnerales, la dita del mexicano no propicia el desarrollo de la aterioesclerosis, ya que trdicionalmente no incluye cantidades excesias de productos de origen animal, como los lacteos y la carne y contiene abundntes alimentos ricos en fibra, como el frijol, el maiz, el chile, frutas y verduras variadas, disponibles en Mexico en cualquier epoca del año. Por esto es importante Sin embargo, el colesterol tiene tambin un efecto biologico ofensivo. Junto con otros lipidos puede depositarse en las paredes enfermedad no cardiovasculares, y es por eso que en El colesterol es componente fundamental se colesterol internas bloqueandolas y de las llegar a arterias ocasionar seguir nuestras costumbres alimentarias y no modificarlas, por mas atractivas que resulten las de otras culturas. Tudela, Víctor” El colesterol: lo bueno y lo malo”(La ciencia desde México) SEP, CONACYT núm., 140, 1996, pp 11-13, 68- 20 RESUMEN Los compuestos binarios se nombran de manera sistemática siguiendo un conjunto de reglas simple o fácil. En compuestos que contienen un metal y un no metal., siempre se nombra la raíz del no metal con la terminación –uro. En compuestos que contienen un metal que forma más de un catión (tipo II), se emplea un número romano para identificar la carga del catión. En compuestos binarios que solo contienen no metales (tipo III), se utilizan prefijos para especificar el numero de átomos. Los iones poli atómicos son entidades con carga formada de varios átomos unidos entre si. Además, estos tienen nombres especiales que es necesario memorizar. La nomenclatura de los compuestos iónicos que contienen iones poli atómicos es muy similar a la de compuestos iónicos binarios. Los nombres de los ácidos (moléculas que tienen uno o mas iones H+) dependen de que el anión contenga oxígeno. Los óxidos metálicos también llamados óxidos básicos, resultan de la unión de un metal con el oxigeno. El numero de oxidación del oxigeno es -2. Para nombrar a estos compuestos se antepone la palabra oxido, seguida de nombre del metal correspondiente. Los óxidos no metálicos, llamados también óxidos ácidos o anhídridos, resultan de la combinación de un no metal (numero de oxidación positivo) con el oxigeno. Para darles nombre se utilizan los prefijos griegos: mono (1), di (2), tri (3), tetra (4), penta (5), para indicar el numero respectivo de átomos en el compuesto correspondiente. Los hidruros resultan de la combinación del hidrogeno con cualquier metal. En los hidruros, el hidrogeno tiene numero de oxidación -1. Para nombrar estos compuestos, se antepone la palabra hidruro, seguida del nombre del metal correspondiente. Los hidrácidos resultan de la combinación de los aniones de la serie de los hidruros con el hidrogeno; es decir, de la combinación de un no metal con el hidrogeno. En los hidrácidos, el hidrogeno siempre tiene el numero de oxidación mas 1. Para el nombre de estos compuestos se antepone la palabra acido, seguida siempre del nombre del no metal correspondiente, con la terminación hídrico. Los hidróxidos o bases, que resultan de la reacción entre un metal y el hidróxido, siempre llevan en su formula un metal unido al radical OH. Se nombran anteponiendo la palabra hidróxido, seguida del nombre del metal correspondiente. 21 Nombre Obtención de un Compuesto No . 5 Con la ayuda de su maestro reúnanse en equipo de 4 o 5 alumnos y realicen la siguiente actividad. Contesten las preguntas y elaboren un informe escrito de la actividad con sus conclusiones. Objetivo: obtener un compuesto en estado gaseoso a partir de un solido y un líquido. Material y Sustancias: Material Sustancias 1 vaso de precipitado Cascara de huevo Vinagre 100 ml Procedimiento: 1.- Coloquen vinagre hasta la mitad del vaso de precipitado 2.- Desmenucen una cascara de huevo y coloquen los trozos dentro del vinagre. Evaluación: ¿Qué ocurre?: __________________________________________________________________ __________________________________________________________________ __________________________________________________________________ ¿Qué compuesto se formo?: __________________________________________________________________ __________________________________________________________________ ¿Con que otra sustancia se puede sustituir las cascaras de huevo para realizar el experimento? __________________________________________________________________ __________________________________________________________________ Conclusiones:______________________________________________________ __________________________________________________________________ __________________________________________________________________ __________________________________________________________________ __________________________________________________________________ 22 P R A C T I C A D E L A B O R A T O R I O