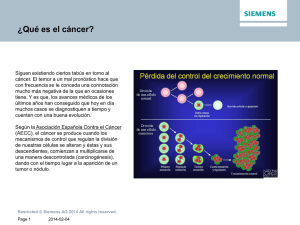
La imagen funcional en oncología
Anuncio

ACTUALIZACIONES SERAM La imagen funcional en oncología La imagen funcional en oncología Coordinadores: La imagen funcional en oncología (2012) Roser Ysamat Marfá y Javier Azpeitia Armán 0-0 Portada OK 2012.indd 1 23/11/12 14:21:56 ACTUALIZACIONES SERAM La imagen funcional en oncología 0-3 01-37.indd 1 23/11/12 11:48:53 © 2012 Sociedad Española de Radiología Médica © 2012 Elsevier España, S.L. Reservados todos los derechos. El contenido de esta publicación no puede ser reproducido, ni transmitido por ningún procedimiento electrónico o mecánico, incluyendo fotocopia o grabación magnética, ni registrado por ningún medio, sin la previa autorización por escrito del titular de los derechos de explotación. Elsevier y sus asociados no asumen responsabilidad alguna por cualquier lesión y/o daño sufridos por personas o bienes en cuestiones de responsabilidad de productos, negligencia o cualquier otra, ni por uso o aplicación de métodos, productos, instrucciones o ideas contenidos en el presente material. Dados los rápidos avances que se producen en las ciencias médicas, en particular, debe realizarse una verificación independiente de los diagnósticos y las posologías de los fármacos. Depósito legal: B-39457-2011 ISBN: 978-84-7592-755-8 Impreso en España 0-3 01-37.indd 2 23/11/12 11:48:54 ACTUALIZACIONES SERAM La imagen funcional en oncología Coordinadores: Roser Ysamat Marfá y Javier Azpeitia Armán 0-3 01-37.indd 3 23/11/12 11:48:54 0-3 01-37.indd 4 23/11/12 11:48:54 La imagen funcional en oncología Índice de autores J. Álvarez-Linera Prado E. Navas Campos Sección de Neurorradiología, Hospital Ruber Internacional, Madrid, España Radiología, DADISA, Grupo Healthtime, Cádiz, España J.M. Artigas Martín E. Pérez Gómez Jefe de Sección, Radiología de Urgencias, Servicio de Radiodiagnóstico, Hospital Universitario Miguel Servet, Zaragoza, España Unidad de Patología Mamaria, Hospital Universitario Dr. Josep Trueta, Girona, España P. Caro Mateo Radiología, DADISA, Grupo Healthtime, Cádiz, España Servicio de Medicina Nuclear, Hospital Universitario Virgen de las Nieves, Granada, España A. Luna Alcalá R. Salem Servicio de Radiología, Clínica Las Nieves, SERCOSA (Grupo Health Time), Jaén, España Department of Radiology, Section of Interventional Radiology and Division of Interventional Oncology, Robert H. Lurie Comprehensive Cancer Center, Northwestern University, Chicago, IL, USA M. Martí de Gracia Jefa de Sección, Radiología de Urgencias, Servicio de Radiodiagnóstico, Hospital Universitario La Paz, Madrid, España M.I. Martínez León Radiología Pediátrica, Hospital Materno-Infantil, Complejo Hospitalario Universitario Carlos Haya, Málaga, España K. Memon Department of Radiology, Section of Interventional Radiology and Division of Interventional Oncology, Robert H. Lurie Comprehensive Cancer Center, Northwestern University, Chicago, IL, USA 0-3 01-37.indd 5 A. Rodríguez Fernández R. Sánchez Sánchez Servicio de Medicina Nuclear, Hospital Universitario Virgen de las Nieves, Granada, España J.C. Vilanova Unidad de Resonancia Magnética, Clínica Girona, Girona, España Servicio de Radiodiagnóstico, Hospital Sta. Caterina, Salt, Girona, España Departamento de Ciencias Médicas, Facultad de Medicina, Universidad de Girona, Girona, España 23/11/12 11:48:54 0-3 01-37.indd 6 23/11/12 11:48:54 La imagen funcional en oncología Prólogo En los últimos años, la radiología o, si se prefiere, el diagnóstico por la imagen (definición que probablemente esté más en consonancia con el tema que nos ocupa), ha experimentado un gran avance al adoptar como métodos diagnósticos y terapéuticos las nuevas técnicas de imagen funcional y molecular. Esto supone para los radiólogos un reto importante, ya que implica un cambio conceptual hacia nuevas áreas de conocimiento que trascienden de las propias del radiodiagnóstico y que son más afines a otras disciplinas más técnicas, como por ejemplo la física o la química. Por otra parte, también impone la necesaria incorporación del radiólogo a equipos multidisciplinares que trabajen de forma conjunta en el diagnóstico y tratamiento de patologías específicas, aunque un primer paso en este sentido ya ha sido dado en la mayoría de los servicios de radiología gracias a la adopción de la organización por órganos/sistemas. Este progreso, debido a las nuevas técnicas funcionales, tiene una especial relevancia en el campo de la oncología, donde ha supuesto un avance espectacular en el diagnóstico y en la monitorización del tratamiento de las neoplasias por parte del radiólogo. Actualmente, además de disponer de una imagen anatómica muy exacta del tumor y de su relación con las estructuras vecinas, nos es posible estudiar in vivo la composición tisular, el grado de angiogénesis, el mapa de perfusión, el grado de actividad metabólica, etc., de una neoplasia y de sus metástasis. Todo ello deriva en una mayor precisión en la estadificación y, por ende, una mayor eficacia de los tratamientos ofertados al paciente. Al mismo tiempo es posible establecer las características específicas de cada tumor y proporcionar un tratamiento 0-3 01-37.indd 7 “a la carta” a cada paciente, mejorando la respuesta tumoral y el pronóstico, minimizando los efectos adversos y evitando tratamientos agresivos infructuosos. La patología oncológica interesa a todos los radiólogos al abarcar todos los órganos de la economía; es por ello que todos nos vemos implicados en la necesidad de actualizar nuestros conocimientos. Muchos de nosotros también nos estamos enfrentando a la incorporación de estas nuevas técnicas en nuestra práctica clínica diaria. Esta última circunstancia queda reservada a los especialistas que trabajan en los centros que disponen de la tecnología adecuada, pero todos los radiólogos, tarde o temprano, tendremos que lidiar con las nuevas técnicas funcionales, por lo que el Comité Científico del XXXI Congreso Nacional de la SERAM, a instancias de su Presidenta, la Dra. Oleaga Zufiria, ha escogido como tema del curso central del congreso y de esta monografía “La imagen funcional en oncología”. Los temas han sido elegidos en función de su relevancia en la práctica clínica, intentando a la vez cubrir el mayor número de áreas de la especialidad. El propósito de esta monografía ha sido presentar al lector una puesta al día de las respectivas técnicas de imagen funcional, incluyendo los aspectos técnicos, indicaciones y valor de la técnica respecto a la estadificación, planificación y monitorización del tratamiento. Todos los autores tienen una amplia experiencia en los temas respectivos, que queda plasmada en cada uno de los capítulos. Queremos agradecer a todos ellos su esfuerzo y su valiosa colaboración. R. Ysamat Marfá y J. Azpeitia Armán 23/11/12 11:48:54 0-3 01-37.indd 8 23/11/12 11:48:54 La imagen funcional en oncología Sumario Capítulo 1. El paciente oncológico en urgencias Capítulo 2. Tratamiento intraarterial en las neoplasias hepáticas Capítulo 3. Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica P. Caro Mateo y E. Navas Campos Capítulo 4. Cáncer de próstata. Papel de las técnicas funcionales en el diagnóstico y estadificación del cáncer de próstata: espectroscopia, difusión, perfusión. Seguimiento activo J.C. Vilanova y A. Luna Alcalá Capítulo 5. Tomografía por emisión de positrones/tomografía computarizada en la estadificación del cáncer de pulmón A. Rodríguez Fernández y R. Sánchez Sánchez Capítulo 6. Resonancia de cuerpo completo con difusión: aplicaciones oncológicas y en la evaluación de las metástasis óseas A. Luna Alcalá y J.C. Vilanova Capítulo 7. Papel de la resonancia magnética en el seguimiento de los gliomas J. Álvarez-Linera Prado Capítulo 8. Modificaciones en la estadificación por imagen de los tumores malignos pediátricos del SNC M.I. Martínez León Capítulo 9. E. Pérez Gómez 0-3 01-37.indd 9 .................... 1 .................... 13 .................... 19 .................... 38 .................... 50 .................... 61 .................... 78 .................... 90 .................... 97 J.M. Artigas Martín y M. Martí de Gracia K. Memon y R. Salem Cáncer de mama: aportación de la imagen funcional 23/11/12 11:48:54 0-3 01-37.indd 10 23/11/12 11:48:54 La imagen funcional en oncología 1 El paciente oncológico en urgencias J.M. Artigas Martína,* y M. Martí de Graciab aJefe de Sección, Radiología de Urgencias, Servicio de Radiodiagnóstico, Hospital Universitario Miguel Servet, Zaragoza, España bJefa de Sección, Radiología de Urgencias, Servicio de Radiodiagnóstico, Hospital Universitario La Paz, Madrid, España Introducción Complicaciones neurológicas El efecto combinado de múltiples factores, como mayor expectativa de vida, aumento real en la incidencia de tumores o reducción de la mortalidad oncológica debida a los avances continuos en su diagnóstico y tratamiento, ha elevado la prevalencia del cáncer en nuestra sociedad que, con frecuencia, es hoy una patología “crónica” sujeta a complicaciones intercurrentes en relación con el tumor, sus metástasis y productos (hormonas, citocinas) o el tratamiento aplicado, lo que ha multiplicado el número de consultas e ingresos urgentes en pacientes oncológicos1,2. Amplia disponibilidad y carácter no invasivo hacen de la radiología un elemento indispensable en el manejo urgente de las complicaciones del cáncer, cuya complejidad puede oscilar de mínima a extrema, pero que sigue una serie de pautas que el radiólogo de guardia debe conocer. Con frecuencia, los hallazgos radiológicos permiten identificar un tumor que debuta con una complicación (p. ej., obstrucción intestinal, atelectasia), la progresión de un tumor conocido que condiciona una situación urgente de forma directa (compresión medular, síndrome de vena cava superior) o indirecta (hipercoagulabilidad, síndromes paraneoplásicos), o bien complicaciones derivadas del tratamiento empleado (toxicidad, hemorragia, infecciones por inmunosupresión). En las próximas páginas se revisarán algunas de las principales complicaciones que dan lugar a situaciones de urgencia en pacientes oncológicos, donde la radiología e imagen aportan valor al proceso diagnóstico. Se han clasificado en 4 bloques de complicaciones distribuidas por órganos/sistemas: neurológicas, torácicas, abdominales y osteomusculares. Las técnicas de intervención mínimamente invasiva guiada por imagen, de gran utilidad en muchas de estas complicaciones, no serán tratadas en el presente capítulo, ni tampoco las complicaciones directas derivadas de la cirugía oncológica. Parece obligado señalar también que una exploración radiológica redundante, innecesaria o, sencillamente, no indicada, sólo añade inquietud, molestias y costes, especialmente en los pacientes oncológicos terminales, únicamente subsidiarios de medidas paliativas. La afectación neurológica por un tumor maligno ocasiona una serie de complicaciones que requieren una respuesta rápida, habitualmente multidisciplinar, encaminada a preservar la vida del paciente y a reducir el dolor y las complicaciones, potencialmente devastadoras. Patología cerebral aguda La aparición de un accidente cerebrovascular agudo de tipo isquémico en el paciente oncológico viene favorecida por su estado de hipercoagulabilidad y por el edema y la compresión vascular debidos a un posible tumor intracraneal. Algunos tumores, en especial metástasis de riñón, tiroides, coriocarcinoma y melanoma, tienen propensión al sangrado cerebral. La metástasis cerebral es el tumor intracraneal más frecuente y una complicación habitual en los pacientes con cáncer. La mayor parte son de localización supratentorial, con preferencia en la unión de la sustancia blanca con la gris (fig. 1). Su incidencia varía con el tipo de tumor primario, proviniendo con mayor frecuencia de pulmón, mama y melanoma. Producen déficits neurológicos, convulsiones o hipertensión endocraneal, favorecida por el edema, vasogénico o tumoral, y por la hidrocefalia obstructiva. Aunque la resonancia magnética (RM) es la herramienta diagnóstica más sensible y específica, en situación de urgencia suele emplearse la tomografía computarizada (TC), menos sensible, especialmente en tumores pequeños o localizados en la fosa posterior, pero que identifica bien hidrocefalia y hemorragia2. En pacientes con tratamiento esteroideo o inmunosupresor pueden aparecer infecciones oportunistas por virus y hongos cuya identificación precoz es clave, siendo la RM la técnica de elección. La encefalitis límbica paraneoplásica simula trastornos psiquiátricos y se debe a la secreción de sustancias por el tumor intracerebral; su diagnóstico y tratamiento precoces evitan el daño neuronal irreversible3. *Autor para correspondencia. Correo electrónico: jmartigas@salud.aragon.es (J.M. Artigas Martín). 0-3 01-37.indd 1 23/11/12 11:48:55 La imagen funcional en oncología 2 A B tes portadores de un tumor avanzado, es devastadora, con secuelas irreversibles de dolor, parálisis e incontinencia. La columna vertebral es la localización más frecuente de metástasis óseas (40%), y de estos pacientes, un 20% desarrollará compresión medular4. Casi cualquier tumor puede causarla, siendo los de mama, pulmón y próstata responsables de dos tercios de los casos, siguiendo en frecuencia el linfoma, mieloma y sarcomas3. La columna dorsal es el segmento afectado con mayor frecuencia (70%), seguido por la columna lumbosacra (20%) y cervical (10%). El mecanismo habitual es la erosión ósea con compresión epidural y vascular directa, pero también por invasión del canal medular a través de los agujeros de conjunción en masas paraespinales o por fractura patológica del cuerpo vertebral con protrusión de un fragmento al espacio epidural. Cualquiera de ellos asocia al componente mecánico directo otro vascular por ectasia venosa, edema e isquemia, que progresivamente propician la lesión neuronal irreversible4. El 80% de los casos de SCM aparece en pacientes diagnosticados de cáncer, y el dolor de espalda progresivo es el síntoma más constante, de forma que su aparición en un paciente oncológico debe sugerir SCM hasta probar lo contrario. Puede aparecer también dolor radicular, alteraciones de la marcha o disfunción de esfínteres, y un tercio de pacientes presentará otras metástasis vertebrales. La probabilidad de recuperación neurológica disminuye drásticamente cuando la compresión medular no se soluciona antes de 24-48 h5, considerándose una emergencia oncológica subsidiaria de estudio por RM inmediata, técnica que asocia cifras de sensibilidad del 93%, con especificidad del 97% y precisión del 95%2. La RM confirma la compresión medular, delimita tridimensionalmente al tumor, identifica otras posibles metástasis y estadifica el grado de compresión, siendo una herramienta esencial para planificar el tratamiento1 (fig. 2). Complicaciones torácicas Obstrucción de la vena cava superior Figura 1. Metástasis cerebral de cáncer de mama. Paciente de 51 años, con antecedente de cáncer de mama en remisión hasta ese momento, que acude a urgencias por cefalea y bradipsiquia progresivas de varios días de evolución. Masa (m) frontotemporal izquierda con edema perilesional (A) e importante realce tras la administración del contraste intravenoso (B), que comprime el asta anterior del ventrículo lateral y desplaza la línea media. Síndrome de compresión medular El síndrome de compresión medular (SCM) es la segunda complicación neurológica en frecuencia tras las metástasis cerebrales y su aparición, habitualmente, en pacien- 0-3 01-37.indd 2 La delgada pared de la vena cava superior (VCS) la hace especialmente vulnerable a la compresión e invasión por tumores mediastínicos o pulmonares. De etiología maligna en más del 90% de los casos, tres cuartas partes se deben a cáncer de pulmón, con frecuencia microcítico, y el resto a adenopatías mediastínicas por linfoma, cáncer de mama o tumores germinales1,6. Entre las causas benignas cabe destacar la trombosis de catéteres venosos centrales. Su contexto clínico dependerá de la velocidad de instauración, del desarrollo de flujo colateral y de la presencia de válvulas competentes que limiten el reflujo venoso al sistema nervioso central7, siendo típico el edema de su región de drenaje, disnea, tos o cefalea. La TC multicorte con reformateos multiplanares y de proyección de máxima intensidad, es la técnica de elección para confirmar su diagnóstico e identificar el punto y causa de la obstrucción6. Cuando se sospecha su presencia, 23/11/12 11:48:55 El paciente oncológico en urgencias A 3 B Figura 2. Compresión medular. Varón de 30 años con paraparesia progresiva de 2 días de evolución. A) Estudio de resonancia magnética, secuencia FSE potenciada en T2, plano sagital de columna dorsal, que muestra fractura patológica en D9, con masa epidural y compresión medular (asterisco). Hay otros focos hiperintensos vertebrales correspondientes a metástasis. B) La tomografía computarizada abdominal realizada a continuación demuestra una masa de 8 cm, con calcificación sugestiva de matriz osteoide (flecha), dependiente del hueso pubiano derecho, correspondiendo con el tumor primario (osteosarcoma). y con el fin de evitar los artefactos lineales ocasionados en las venas braquiocefálicas por el medio de contraste intravenoso (MCI) sin diluir, se recomienda realizar una adquisición tardía, tras concluir la administración de un bolo de MCI seguido de suero fisiológico o emplear MCI diluido, e inyección en una o ambas venas antecubitales8,9. Las claves diagnósticas son la identificación de una masa/ adenopatías mediastínicas que ocluyen la luz de la VCS y la presencia de colaterales venosas: ácigos/hemiácigos, intercostales, mediastínicas, paravertebrales, toracoepigástricas, mamaria interna, toracoacromioclavicular, pared anterior del tórax e, incluso, transhepáticas, con derivación sistemicoportal. Las opciones terapéuticas incluyen anticoagulación, trombólisis, bypass quirúrgico, radioterapia (RT) y quimioterapia (QT). El empleo de prótesis intravasculares expansibles produce una rápida resolución de la sintomatología en pacientes seleccionados6,9 (fig. 3). Derrame pericárdico El acúmulo de líquido pericárdico es frecuente en pacientes con cáncer avanzado y es signo de mal pronóstico 10. Se puede deber a metástasis, invasión directa del tumor o complicación terapéutica, y suele ser de tipo hemorrágico. Casi cualquier tumor puede causarlo, pero es frecuente en el cáncer de pulmón, mama, linfoma y leucemia. Habitualmente asintomático, el acúmulo rápido o cuantioso puede comprimir las cavidades cardíacas y originar taponamiento cardíaco, con alteración 0-3 01-37.indd 3 hemodinámica grave. Ocasionalmente, el engrosamiento pericárdico condiciona una pericarditis constrictiva. El derrame o engrosamiento pericárdico “no tumoral” aparece como consecuencia del tratamiento radio o quimioterápico, o por bloqueo linfático condicionado por adenopatías mediastínicas. Se ha descrito también en el contexto de la enfermedad injerto contra huésped y como complicación infecciosa (bacterias, virus, hongos) de la inmunosupresión8. Radiológicamente muestra los signos habituales de: ensanchamiento mediastínico “en frasco de velador” y “del sándwich” o “galleta oreo” en proyección lateral, que indicarán ecografía o TC para confirmar el diagnóstico e identificar además nódulos o engrosamiento pericárdico sugestivos de malignidad, compresión de cámaras cardíacas, o signos de insuficiencia cardíaca derecha, como dilatación de vena cava inferior y suprahepáticas, o reflujo del contraste a estas estructuras por TC. Esofagitis El tratamiento con RT/QT destruye indiscriminadamente las células con alto índice mitótico, incluidas las de la mucosa digestiva normal, provocando mucositis, eventualmente potenciada por la inmunosupresión, que propicia la colonización de gérmenes (hongos, virus, bacterias)11. La presencia de esofagitis de cualquiera de las etiologías comentadas es típica de los pacientes con cáncer y suele presentarse con disfagia y odinofagia. 23/11/12 11:48:55 B A La imagen funcional en oncología 4 A B C D Figura 3. Síndrome de vena cava superior. A-C) Varón de 63 años, con carcinoma microcítico pulmonar que presenta edema de miembros superiores y abotargamiento progresivo. Tomografía computarizada de tórax con contraste intravenoso, plano axial a nivel del cayado (A) y oblicuo sagital (B). Masa mediastínica (m) que invade y ocluye la vena cava superior (asterisco), con vascularización colateral profusa (flechas), más evidente en el reformateo volumétrico con proyección de máxima intensidad (C). Derivación por plexos venosos axilares, intercostal derecha y ácigos y vena mamaria interna izquierda. D) Catéter venoso central tipo Hickman en otro paciente oncológico, con defecto de repleción intraluminal en su punta debido a un trombo parcialmente oclusivo (flecha). Nódulo tiroideo incidental (n). Puede aparecer fístula traqueoesofágica hasta en el 5% de carcinomas esofágicos, especialmente tras RT, y con menor frecuencia en tumores primarios de pulmón y tráquea12. Clínicamente suele aparecer disfagia y síntomas de aspiración, siendo el esofagograma de bario el estudio de elección, que diferencia fístula de aspiración. Los medios de contraste hidrosolubles están contraindicados por el riesgo de edema pulmonar grave12. La TC puede demostrar la comunicación, habitualmente en el interior de la masa tumoral que invade esófago y árbol traqueobronquial8. 0-3 01-37.indd 4 Enfermedad tromboembólica Cualquier paciente oncológico presenta un grado variable de activación de la cascada coagulativa, que junto con otros factores de tipo general, como la restricción de la movilidad o el empleo generalizado de catéteres intravenosos, propicia la aparición de trombosis venosa profunda (TVP). La TVP puede anunciar un cáncer oculto o ser una complicación de un tumor conocido, potenciada por la hospitalización, cirugía o QT13. La presencia de TVP disminuye la supervivencia en los pacientes con cáncer, siendo el riesgo de muerte tras tromboembolia pulmonar de 4 a 23/11/12 11:48:55 El paciente oncológico en urgencias 8 veces mayor14. Como hallazgo incidental en estudios TC de estadificación en pacientes tumorales, la prevalencia de TVP es del 6,8%, incrementándose en pacientes ingresados y con enfermedad avanzada14. La tromboembolia pulmonar es la segunda causa de muerte en pacientes oncológicos ingresados. Su aparición puede interrumpir la pauta quimioterápica prevista, por el riesgo de eventos hemorrágicos propiciados por el efecto sinérgico de determinados fármacos (p. ej., gemcitabina, bevacizumab) con el tratamiento anticoagulante13,15. Opacidades pulmonares. Fiebre El parénquima pulmonar es asiento frecuente de complicaciones en los pacientes afectados de tumores sólidos y, muy especialmente, hematológicos. Entre otros factores se incluyen la inmunodepresión, debida al tumor y a su tratamiento, que propicia la patología infecciosa; la función de filtro para metástasis y émbolos de la red capilar pulmonar, y la especial susceptibilidad del lecho alveolocapilar a los efectos tóxicos de QT y RT, a la hemorragia trombocitopénica y a algunas reacciones antígeno-anticuerpo que lo sitúan como órgano diana8,16,17. La aparición de fiebre y opacidades pulmonares nuevas constituye un problema clínico frecuente en pacientes inmunodeprimidos y hasta el 60% de casos con granulocitopenia desarrollará una opacidad/infiltrado pulmonar en algún momento de su enfermedad18. La supresión de la medula ósea es un efecto tóxico de gran parte de los tratamientos con QT, que suele afectar a todas las líneas celulares, pero esencialmente a la serie blanca y característicamente a los neutrófilos. La mayoría de las pautas de QT provoca neutropenia máxima tras 8 días, que comienza a recuperarse pasados 5 días. Algunas de ellas, particularmente las empleadas en tumores hematológicos, provocan una neutropenia más severa y prolongada, especialmente si se asoció irradiación de médula ósea o hay infiltración tumoral de ésta1. Los pacientes con neutropenia febril tienen una probabilidad del 50% de infección oculta y, en ausencia de otra orientación clínica, el pulmón es la primera localización a investigar, habitualmente por radiología. Una opacidad pulmonar en un paciente neutropénico anuncia una situación de riesgo, especialmente cuando asocia signos de insuficiencia respiratoria o es de tipo difuso en la radiografía, alcanzando la mortalidad cifras del 50%19,20. La infección es responsable del 75% de las complicaciones pulmonares en pacientes neutropénicos, cifra que se eleva al 90% si la neutropenia es grave o la opacidad pulmonar es de tipo focal19. El resto de complicaciones pulmonares se debe a toxicidad a fármacos, manifestación pulmonar del tumor subyacente o procesos no relacionados, como embolia o edema pulmonar. Esta última es una posibilidad a considerar sistemáticamente, incluso en pacientes jóvenes previamente sanos, relacionándose su aparición con el efecto sinérgico de la toxicidad cardíaca de algunos fármacos (antraciclinas), la necesidad de hiperhidratación previa a la QT en leucemias, hipoproteinemia o el aumento de la permeabilidad alveo- 0-3 01-37.indd 5 5 locapilar de tipo tóxico (interleucina 2, gemcitabina), por radioterapia o por sepsis15,18,21. La caracterización del agente causal se considera objetivo prioritario, aunque no mejora el resultado en más del 10-20% de casos y se consigue únicamente en el 15-20%, incluyendo series autópsicas19. No obstante, el retraso diagnóstico asocia mayor morbimortalidad en pacientes graves18,20,22. La radiología constituye una alternativa no invasiva y rápida, pero que ofrece un diagnóstico específico en una minoría de casos, debido a la diversidad de patologías implicadas y a la ausencia de patrones de imagen específicos que permitan afirmar o excluir una u otra opción. Con mayor frecuencia proporciona una orientación diagnóstico-diferencial que debe correlacionarse con la información clínica y de laboratorio. La radiografía de tórax suele ser el método de imagen inicial, aunque tiene poca utilidad en la detección o exclusión precoz de opacidades pulmonares en pacientes inmunodeprimidos, con sensibilidad inferior al 50%21, por lo que se recomienda realizar sistemáticamente TC pulmonar, que identifica infección en más de la mitad de pacientes neutropénicos con radiografía normal y adelanta el diagnóstico un promedio de 5 días, con sensibilidad del 87% y valor predictivo negativo del 88%23,24. El estudio se focaliza en el parénquima pulmonar con técnica de alta resolución (TCAR) “volumétrica”, sin necesidad de administrar contraste intravenoso, salvo ante sospecha de tromboembolia pulmonar o hemoptisis. Para su valoración resulta imprescindible la información clínica que oriente sobre el grado de inmunosupresión/recuperación hematopoyética, antecedente de injerto alogénico o autólogo de células madre, pauta de QT y RT, corticoides, positividad a virus y relación temporal entre la aparición de la opacidad y el evento terapéutico16,21,25,26. La profilaxis sistemática empírica tiende a modificar los patógenos habituales en algunos grupos de riesgo (p. ej., Pneumocystis jiroveci en trasplante de médula ósea y leucemia linfoide crónica), desviando la incidencia hacia otros grupos, inicialmente menos probables (linfomas no hodgkinianos). La broncoscopia con lavado alveolar viene siendo la piedra angular del diagnóstico etiológico de la neumonía en pacientes oncológicos, pero no siempre es factible ni está exenta de riesgos18. Un reciente estudio20 no encuentra mayor riesgo para la broncoscopia, pero similar rendimiento diagnóstico para los análisis no invasivos rutinarios de esputo, aspirado nasofaríngeo, sangre y orina. La neumonía bacteriana es la causa más frecuente de infección durante la fase temprana de la neutropenia. Se considera responsable de hasta el 90% de los episodios21, pero tanto su frecuencia como el germen causal y su apariencia radiológica guardan relación con el tipo de déficit inmunitario18. La neumonía de la comunidad asocia mayor mortalidad en el paciente oncológico que en la población general, aunque la presencia de neutropenia ha sido cuestionada como factor de riesgo independiente, cuyo efecto quedaría diluido en el de una profunda alteración inmunológica cualitativa global común a los pacientes con cáncer27. La radiografía de tórax puede ser normal hasta en un 30% de los casos, como consecuencia del tratamiento 23/11/12 11:48:55 La imagen funcional en oncología 6 A B Figura 4. Mujer de 25 años, en tratamiento por linfoma de Hodgkin, con disnea, sin fiebre ni neutropenia significativa. A) Tomografía computarizada (TC) pulmonar con nódulos múltiples, bilaterales, rodeados de opacidad en vidrio deslustrado (“signo del halo”) (flecha) sugestivos de infección fúngica. B) El control TC (alta resolución) tras 2 semanas de tratamiento antifúngico muestra marcada reducción de tamaño de los nódulos (flecha). antibiótico empírico, pero es habitual la aparición de consolidación parenquimatosa con broncograma aéreo, frecuentemente de patrón bronconeumónico. En los pacientes neutropénicos las opacidades pulmonares aparecen más tardíamente y tienden a ser más tenues, “en vidrio esmerilado” (OVE), hallazgo tan frecuente en estos pacientes como poco específico, con cierto paralelismo entre el grado de opacidad y el de recuperación hematopoyética28. Además de la neutropenia hay otros factores de riesgo para neumonía bacteriana en el paciente oncológico, como el tratamiento corticoide, el drenaje bronquial inadecuado por tumor estenosante o la depresión del reflejo de la tos16. La neumonía por Legionella es frecuente en pacientes con tratamiento corticoide y rápidamente progresiva, desde una consolidación focal hasta la afectación difusa de ambos pulmones. La mayor parte de neumonías bacterianas responde al tratamiento antibiótico empírico, pero la afectación pulmonar puede progresar rápidamente ensombreciendo el pronóstico, especialmente cuando la cifra de neutrófilos baja de 1.000 células/µl, o si el tratamiento administrado no cubre el germen causal22. En estos casos hay que pensar en etiologías alternativas como hongos (Aspergillus spp.), virus, bacterias multirresistentes (Staphylococcus aureus, 0-3 01-37.indd 6 bacilos gramnegativos), P. jiroveci, micobacterias o bien etiología no infecciosa. La TC puede orientar o excluir diagnósticos de forma rápida y no invasiva combinando los hallazgos radiológicos con el contexto clínico/terapéutico, analítico y evolutivo21,25,26. La neumonía fúngica se sospechará en un paciente con neutropenia febril persistente que no responde al tratamiento empírico. Suele ser debida al género Aspergillus y su forma invasiva es frecuentemente mortal, por lo que su identificación precoz es crítica, aunque su confirmación es difícil28. Inicialmente la radiografía puede ser normal, siendo el hallazgo más característico en TC la presencia de nódulos rodeados de opacidades en vidrio deslustrado (“signo del halo”) (fig. 4) o focos de consolidación triangulares de base pleural, correspondientes a infartos hemorrágicos28. De aparición precoz, estos signos asocian elevada especificidad (93%) pero baja sensibilidad (33%)21. Con la recuperación hematopoyética, las opacidades se hacen más densas, pudiendo aparecer cavitación y separación de fragmentos de pulmón necrótico (“signo del menisco aéreo”)28. Estos hallazgos típicos aparecen en el 75% de casos diagnosticados de aspergilosis pulmonar invasiva, pudiendo quedar la imagen reducida a opacidades/consolidación inespecíficas18. Hay otra presentación con tra- 23/11/12 11:48:56 El paciente oncológico en urgencias queobronquitis necrosante que produce bronconeumonía focal o difusa19,29. P. jiroveci (previamente Pneumocystis carinii) es un organismo unicelular actualmente clasificado como hongo, responsable de neumonía en pacientes con alteración de la inmunidad celular. Aunque su frecuencia es baja en los pacientes con cáncer, predominando en las neoplasias hematológicas y tumores cerebrales, entraña riesgo vital. Son factores predisponentes el empleo de QT intensiva, tratamiento corticoide y bajo valor de CD4. Ante sospecha clínica y con radiografía normal o inespecífica, la TC puede mostrar hallazgos típicos, como OVE perihiliar bilateral, a menudo de distribución parcheada o geográfica y que puede asociar engrosamiento de septos interlobulillares18,28. La neumonía viral en pacientes neutropénicos asocia una mortalidad en torno al 50% y es responsable de hasta la mitad de neumonías en receptores de trasplante de células madre26. El citomegalovirus es el patógeno más frecuente en los pacientes inmunodeprimidos y característico de las neoplasias hematológicas18. Su diagnóstico es difícil por su frecuencia en la población general y lo inespecífico de sus hallazgos radiológicos: opacidades parcheadas, heterogéneas uni o bilaterales, OVE y consolidación alveolar19,28. Hasta el 15% de neumonías en pacientes oncológicos son polimicrobianas, siendo particularmente típicas en situaciones con gran alteración inmunitaria como trasplante alogénico de médula ósea de células madre hematopoyéticas y casos graves de enfermedad injerto contra huésped, donde pueden coexistir bacterias, hongos y virus18. La neumonía viral predispone característicamente a la infección secuencial por otros gérmenes como bacterias o P. jiroveci18. La neumonía consecutiva a obstrucción de la vía aérea por cáncer pulmonar o metástasis es característicamente polimicrobiana y puede derivar en absceso pulmonar y empiema. Su tratamiento antibiótico aislado es difícil y requiere solucionar la obstrucción con QT, RT o stent para facilitar el drenaje18. La neumonía aspirativa suele combinar aerobios y anaerobios. Su aparición se ve facilitada por la alteración de la actividad ciliar consecutiva a RT y alteración del reflejo tusígeno. Es particularmente frecuente en tumores de cara/cuello18. La patología pulmonar no infecciosa supone 1 de cada 4 casos de infiltrado pulmonar en pacientes inmunodeprimidos y, con frecuencia, su tratamiento empírico (p. ej., inmunosupresión) entra en conflicto con el de la patología infecciosa. La TCAR puede ser útil en la detección y caracterización de estas lesiones. Aparecen manifestaciones pulmonares en forma de bronquiolitis obliterante en un 10% de pacientes con enfermedad injerto contra huésped unos 9 meses después de un trasplante alogénico. Su contexto clínico, apariencia radiológica y momento de aparición son superponibles a los de la neumonía viral: OVE, patrón en mosaico, atrapamiento aéreo o engrosamiento de la pared bronquial, en la fase precoz, que son sustituidos por engrosamiento de tabiques interlobulillares y “árbol en brote” en las fases tardías. La neumonitis por radiación aparece en pacientes tratados con esta técnica por tumores de pulmón, cara/cuello o esófago y en el 5-25% de pacien- 0-3 01-37.indd 7 7 tes sometidos a irradiación corporal total como terapia de acondicionamiento previa al trasplante de médula ósea o de células madre. Su momento de aparición es variable, siendo características las OVE que luego pasan a consolidación, limitadas al campo irradiado, habitualmente paramediastínico y apical. Neumonitis tóxica por fármacos. Como consecuencia de un mejor conocimiento de la biología tumoral, la QT ha evolucionado desde los fármacos citotóxicos clásicos que atacan a las células con rápida proliferación, hasta otros nuevos que bloquean moléculas específicas implicadas en el crecimiento, diferenciación celular o aporte de nutrientes. El desarrollo de opacidades pulmonares es la manifestación más frecuente de ambos, habitualmente de tipo intersticial y OVE que pueden ser bilaterales o hacerse alveolares y evolucionar tardíamente hacia engrosamiento septal y atrapamiento aéreo por fibrosis. Su aspecto radiológico tiende a solaparse entre sí y con el resto de causas, previamente comentadas. Entre los clásicos figuran bleomicina y metotrexato, y entre los nuevos, gemcitabina, paclitaxel, oxaliplatino o inhibidores de la tirosina cinasa15. La infiltración leucémica afecta fundamentalmente al intersticio pulmonar perilinfático y se manifiesta por TCAR como afectación broncovascular y de tabiques interlobulillares con OVE, similar a la congestión pulmonar. La hemorragia pulmonar aparece típicamente en pacientes pancitopénicos tras lavado alveolar broncoscópico, tras una neumonía fúngica durante la recuperación hematopoyética, o con algunos fármacos (bevacizumab). En radiología simple aparece afectación difusa rápidamente progresiva y la TC muestra típicamente OVE y engrosamiento septal, muy similares al edema pulmonar15,19,29. Invasión de la vía aérea El carcinoma broncogénico es la primera causa de obstrucción tumoral de la vía aérea, aunque cualquier tumor mediastínico puede producirla. El contexto clínico dependerá del nivel de la obstrucción, siendo frecuente la aparición de disnea, estridor, hemoptisis y tos, sintomatología inespecífica común con otras entidades más frecuentes (asma, neumonía, bronquitis)2. La presencia de atelectasia o neumonía obstructiva es una complicación habitual en los tumores hiliares, cuyo tratamiento requiere la repermeabilización. La radiografía de tórax aporta los signos clásicos de neumonitis obstructiva, atelectasia o masa hiliar, pero la TC es más sensible en la demostración de estenosis bronquial, aporta información de gran utilidad para planificar la broncoscopia, ayuda en la diferenciación de moco intraluminal de tumor, que realza tras el contraste intravenoso, y evalúa las estructuras mediastínicas orientando la diferenciación de tumoración primaria/metástasis. Derrame pleural Los pacientes oncológicos con frecuencia desarrollan derrames pleurales, en ocasiones a tensión, cuya naturaleza puede ser benigna o maligna. Los primeros pueden obe- 23/11/12 11:48:56 8 decer a un bloqueo linfático, ser reactivos a neumonía obstructiva o a hipoproteinemia. El derrame pleural maligno típico viene ocasionado por invasión tumoral de la pleura, siendo típicos los cánceres de pulmón, mama, ovario y linfoma, y el adenocarcinoma la variedad histológica más frecuente8. El mesotelioma maligno aparece típicamente como un derrame pleural asociado a nódulos pleurales. Habitualmente detectados por radiografía, es la TC la que orienta sobre la etiología tumoral, identificando engrosamiento pleural circunferencial y multinodular asociado al derrame. Cuando un tumor mediastínico, usualmente linfomas y carcinomas metastásicos, invade la pared del conducto torácico, la linfa puede fugar al espacio pleural originando un quilotórax. Complicaciones abdominales La presencia de sintomatología abdominal en un paciente oncológico puede responder a múltiples causas, unas comunes a la población general (p. ej., apendicitis) y otras específicas vinculadas al tumor primitivo (p. ej., obstrucción, perforación, hemorragia) o a su tratamiento (cirugía, QT, RT, nuevas terapias moleculares). Puede afectar a cualquier órgano y con frecuencia asocia riesgo vital30. La mucosa intestinal presenta celularidad con alto índice mitótico que puede verse afectada por la QT, causando inflamación y aumento de la permeabilidad, e incluso ulceración y perforación. Este efecto se ve complicado con la predisposición a la infección debida a la inmunosupresión, tratamiento corticoide o antibiótico, o la tendencia a la hemorragia por necrosis tumoral o trombocitopenia30,31. Cualquier tumor maligno asocia inmunosupresión, pero la presencia de neutropenia (> 1.500 células/µl) define un grupo de pacientes donde las complicaciones, especialmente infecciosas, son más frecuentes y características 32. De igual forma, los pacientes con antecedente de trasplante de médula ósea o de células madre presentan complicaciones concretas. La sintomatología clínica suele encontrarse “amortiguada” por la situación inmunitaria, las muestras biológicas (sangre, heces) pueden demorarse días y la endoscopia asocia mayor riesgo por la trombocitopenia asociada. La indicación quirúrgica urgente es siempre difícil en el paciente oncológico y sus implicaciones pronósticas graves, siendo en ocasiones consecuencia del retraso en el diagnóstico de una complicación médica (p. ej., tiflitis). En ese contexto, la TC de abdomen puede proporcionar información de gran utilidad para identificar las causas quirúrgicas de abdomen agudo (perforación, obstrucción) o bien orientar hacia la posible patología específica: progresión tumoral, complicación infecciosa, inmunitaria, etc.31-33. Diarrea Es una complicación frecuente de la QT (5-fluorouracilo, capecitabina, irinotecan, tratamientos moleculares) y RT, 0-3 01-37.indd 8 La imagen funcional en oncología presente hasta en la mitad de los pacientes11. La enterocolitis neutropénica se origina por alteración de la integridad mucosa con posterior invasión por bacterias u hongos. Puede aparecer con tumores sólidos, pero es más frecuente en la leucemia aguda34. Afecta a cualquier tramo intestinal, con especial predilección por el colon derecho y ciego (tiflitis), apareciendo engrosamiento mural, desflecamiento pericolónico, ascitis y neumatosis mural32 (fig. 5A). La colitis por C. difficile aparece por colonización de dicho germen cuando la flora intestinal normal es alterada por tratamientos antibióticos o de QT. Es la infección nosocomial más frecuente del tracto digestivo11 y su intensidad varía desde diarrea leve a una colitis seudomembranosa. Aunque puede tener un aspecto similar a la anterior, habitualmente es una pancolitis sin afectación del intestino delgado, con mayor engrosamiento mural y nodularidad. Con frecuencia es el radiólogo el primero en sugerirla33. La forma aguda de la enfermedad injerto contra huésped aparece en el 10-50% de pacientes sometidos a trasplante alogénico de médula ósea y afecta a piel, tracto digestivo e hígado11,30. Sus hallazgos más típicos son dilatación de la luz y realce mucoso, con discreto engrosamiento mural31-33. La forma aguda de la proctitis actínica aparece en las 6 semanas posteriores a la irradiación pelviana por tumores pelvianos; asocia tenesmo rectal y hemorragia ocasional, cediendo espontáneamente en 6 meses11. Úlcera/perforación Como se ha comentado, la ulceración mucosa es una complicación frecuente de la QT, cuyos efectos son potenciados por la inmunosupresión y el tratamiento corticoide o analgésico. Los tumores gastrointestinales tienden a ulcerarse, así como las enterocolitis infecciosas o necrosantes 31. La perforación gastrointestinal en un paciente oncológico puede tener diferentes causas: rotura espontánea de un tumor que procede o afecta al conducto digestivo, ulceración neoplásica, necrosis posterapéutica, inducida por fármacos o complicando un proceso inflamatorio intestinal. La perforación complica entre un 2,5 y un 10% de cánceres de colon, pudiendo ser abierta a cavidad peritoneal o localizada con formación de abscesos y fístulas a los órganos de vecindad 35 (fig. 5B). La perforación gástrica puede aparecer complicando el tratamiento corticoide o quimioterápico, y la perforación de un linfoma intestinal suele presentarse en tumores avanzados o durante la QT de inducción31,33. Son múltiples las pautas quimioterápicas que pueden verse complicadas con perforación; entre los de incorporación reciente figura el bevacizumab (Avastin®), que es un anticuerpo monoclonal que bloquea la neoangiogénesis y que se emplea en el cáncer colorrectal; se han señalado como factores de riesgo la persistencia del tumor primario, la irradiación previa, la diverticulitis, el absceso o la obstrucción11,31. En cualquier caso, la clave diagnóstica sigue siendo la demostración de aire ectópico, abscesos, fístulas, trabeculación de la grasa y, con frecuencia, el propio punto de perforación35. 23/11/12 11:48:56 El paciente oncológico en urgencias 9 B A C * Figura 5. Complicaciones abdominales. A) Tiflitis neutropénica. Paciente con leucemia aguda que presenta dolor abdominal, fiebre y diarrea. Tomografía computarizada multidetector del abdomen, reformateo coronal que muestra engrosamiento mural del ciego con desestructuración y desflecamiento perivisceral (*). Ascitis (flecha). B) Perforación por cáncer de colon (sigma) estenosante (puntas de flecha). Burbujas de gas con aspecto de heces en el espacio subhepático (flechas). Ascitis (*). C) Cáncer de sigma estenosante (flecha) con distensión retrógrada de la luz del colon por obstrucción (*). Hemorragia La hemorragia tumoral se ve favorecida por la coexistencia de trombocitopenia o algunos tratamientos de QT, pudiendo manifestarse de diferentes maneras: hemoperitoneo complicando un tumor hepático, hemorragia digestiva alta (úlcera de estrés y gastritis favorecidas por corticoides, RT o QT, linfoma gástrico) o baja (cáncer de colon, colitis) o sangrado retroperitoneal33. La TC permite confirmar la hemorragia activa e identificar la causa, con objeto de indicar el tratamiento hemostático y dirigir su realización endoscópica, endovascular o quirúrgica. La identificación de colecciones intra o extraluminales con valores de atenuación > 60 UH es diagnóstica, incluyendo el diagnóstico diferencial de gastritis, úlcera péptica o estrés, necrosis tumoral y colitis, necrosante o infecciosa. Determinados fármacos son factores de riesgo, entre otros: corticoides, analgésicos, bevacizumab, imatinib (Gleevec®); este último tiene un potente y rápido efecto antitumoral y se emplea en los tumores estromales gastrointestinales avanzados, asociando episodios hemorrágicos en el 5% de los pacientes31. conocido, la misión del radiólogo es confirmar la obstrucción e identificar su etiología: adherencias peritoneales, carcinomatosis peritoneal o recidiva local del tumor primario33. La semiología TC es la habitual, masa estenosante y dilatación retrógrada en relación con la competencia de la válvula ileocecal; ocasionalmente puede identificarse colitis isquémica previa a la obstrucción o la presencia de una invaginación provocada por un tumor pediculado35. La obstrucción tumoral de la luz apendicular provoca un cuadro de apendicitis aguda que en ancianos con cáncer de ciego puede aparecer hasta en el 10-25% de casos 35. La obstrucción intestinal es una complicación frecuente del cáncer ginecológico, especialmente de origen ovárico, que puede complicar el 35-50% de los casos avanzados36. Por otra parte, el estreñimiento es un problema frecuente entre los pacientes tumorales, favorecido por ingesta oral escasa, limitada actividad física, fármacos (analgésicos opiáceos, antieméticos), QT, disbalance electrolítico, etc., cuya presencia debe tenerse en cuenta a la hora de valorar un cuadro de obstrucción intestinal aguda11. Obstrucción Infarto mesentérico Es una forma frecuente de presentación de los tumores digestivos, típica del cáncer de colon, al que complica en el 8-29% de casos, especialmente los de localización izquierda35 (fig. 5C). Cuando el antecedente tumoral es Su origen no ha sido bien clarificado, habiéndose relacionado con QT, hipercoagulabilidad sanguínea o embolia tumoral. Puede afectar tanto segmentos intestinales sanos como enfermos (fig. 6). 0-3 01-37.indd 9 23/11/12 11:48:56 A 10 La imagen funcional en oncología caciones específicas que propician una alteración metabólica importante con impacto directo sobre la función renal. La hipercalcemia tumoral aparece hasta en el 10-30% de los tumores avanzados, característicamente de mama, pulmón o mieloma múltiple, y se produce por movilización masiva del calcio óseo. El síndrome de lisis tumoral puede complicar el tratamiento de cualquier tumor, pero es característico de las neoplasias hematológicas; se debe a la liberación masiva de componentes intracelulares tras su necrosis1,9,10,30. Complicaciones osteomusculares Figura 6. Mujer de 60 años, sin tumoración previa conocida que presenta mal estado general y signos de shock. Tomografía computarizada multidetector reformateo coronal. Gran tumoración submucosa gástrica (estromal) (T). Neumatosis mural gástrica (puntas de flecha) y gas en porta (flechas). Ascitis (*). Otras La aparición de insuficiencia hepática aguda en un paciente oncológico puede guardar relación con la administración de fármacos hepatotóxicos, progresión tumoral, infección o coexistencia de patología hepática de base. La pancreatitis aguda es rara pero muy grave en estos pacientes, habiéndose asociado a hipercalcemia, infección por citomegalovirus o fármacos. Se ha sugerido una mayor incidencia de colecistitis alitiásica en pacientes inmunodeprimidos30,33. Síndrome oligúrico-anúrico La insuficiencia renal aguda en un paciente tumoral puede ser de causa obstructiva o no obstructiva. La obstrucción ureteral suele ser debida a invasión/compresión por adenopatías o tumores retroperitoneales, ginecológicos o de vejiga. La ecografía confirma obstrucción de la vía urinaria, pero la TC es de elección para la valoración completa del tumor. En ausencia de ectasia significativa, se considerarán causas renales o prerrenales para la insuficiencia renal, frecuente en los pacientes oncológicos, y factor limitante para la administración de medio de contraste yodado intravenoso37. Guarda relación con la nefrotoxicidad de la QT, pero también con la edad avanzada, anorexia y deshidratación (vómitos, QT). Existen compli- 0-3 01-37.indd 10 El esqueleto es el órgano afectado con mayor frecuencia por el cáncer metastásico 38 y donde produce una mayor morbilidad: dolor, hipercalcemia, fractura patológica y compresión medular. Se estima que en pacientes con tumor avanzado uno de estos eventos aparece cada 3-6 meses39. Aparecen metástasis vertebrales en un 10% de pacientes con cáncer, pero hasta un tercio de fracturas vertebrales en este grupo puede ser de origen no tumoral38. Los tumores primarios con mayor afinidad por el hueso son los de mama, próstata, tiroides, pulmón y riñón, abarcando los 2 primeros el 80% de casos, mientras que las metástasis óseas de tumores gastrointestinales son infrecuentes5. Debido a su mayor riqueza de médula ósea, las metástasis asientan preferentemente en el esqueleto axial y la columna es la primera localización38. El dolor óseo metastásico es la principal causa de consulta urgente en el paciente oncológico y la hipercalcemia la complicación metabólica más frecuente de la enfermedad metastásica ósea, con efectos importantes sobre los sistemas digestivo, renal y nervioso, que pueden llevar a la muerte. Principalmente es consecuencia de la destrucción ósea, aunque puede tener un sustrato hormonal. Aparece con mayor frecuencia en tumores de pulmón, mama y riñón, y en neoplasias hematológicas, fundamentalmente mieloma y linfoma. La destrucción tumoral de hueso reduce también su capacidad funcional, ocasionando microfracturas que desembocan en fracturas patológicas, cuyo asiento más frecuente es costal (29%). No obstante, el impacto funcional es mayor cuando la fractura asienta en una vértebra u otro hueso de carga. La presencia de lesiones grandes, osteolíticas, con erosión cortical, son signos radiológicos asociados a una mayor probabilidad de fractura patológica5,39, habiéndose descrito 3 localizaciones características: fémur subtrocantéreo, húmero subcapital y columna40 (figs. 2A y 7). Las fracturas de estrés por insuficiencia son particularmente frecuentes en el anciano oncológico y su diferenciación con las anteriores puede ser problemática con radiografía simple40. La TC multicorte proporciona información relevante acerca de la presencia de masa de partes blandas, erosión endóstica y alteraciones corticales o periósticas, si bien estas últimas pueden ser inespecíficas40. La RM identifica mejor los cambios en la médula ósea y el edema muscular, siendo de utilidad las secuencias potenciadas en difusión38,40. 23/11/12 11:48:56 El paciente oncológico en urgencias 11 Conclusiones La patología oncológica es causa habitual de consulta urgente por diferentes razones: elevada prevalencia, tendencia de muchos tumores a debutar con complicaciones de evolución aguda, tratamientos agresivos o progresión de la enfermedad que, tarde o temprano, se ve complicada con un evento urgente. Ello da lugar a una gran diversidad de situaciones que afectan a cualquier órgano o sistema, a cualquier hora del día o de la noche, cuya gravedad y complejidad pueden ser variables. Amplia disponibilidad, rendimiento diagnóstico, carácter no invasivo y, en ocasiones, hábitos sociales, hacen de la radiología e imagen diagnóstica técnicas indispensables para el manejo urgente —incluida su exclusión— de las complicaciones del paciente con cáncer, cuyas pautas principales, en positivo o en negativo, el radiólogo de guardia debe conocer. Bibliografía 1. Walji N, Chan AK, Peake DR. Common acute oncological emergencies: diagnosis, investigation and management. Postgrad Med J. 2008;84:418-27. 2. Behl D, Hendrickson AW, Moynihan TJ. Oncolog ic emergencies. Crit Care Clin. 2010;26:181-205. 3. Law M. Complications and emergencies in oncologic patients. Neurological complications. Cancer Imaging. 2009;9:S71-4. 4. Rajer M, Kovac V. Malignant spinal cord compression. Radiol Oncol. 2008;42:23-31. 5. Coleman RE. Skeletal complications of malignancy. Cancer. 1997;80 8 Suppl:1588-94. 6. Eren S, Karaman A, Okur A. The superior vena cava syndrome caused by malignant disease. Imaging with multi-detector row CT. Eur J Radiol. 2006;59:93-103. 7. Barceló R, Muñoz A, Rodríguez P, Pérez T. Urgencias en oncología. Gac Med Bilbao. 2004;101:11-5. 8. Quint LE. Thoracic complications and emergencies in oncologic patients. Cancer Imaging. 2009;9:S75-82. 9. Samphao S, Eremin JM, Eremin O. Oncological emergencies: clinical importance and principles of management. Eur J Cancer Care. 2010;19:707-13. 10. Halfdanarson TR, Hogan WJ, Moynihan TJ. Oncologic emergencies: diagnosis and treatment. Mayo Clin Proc. 2006;81:835-48. 11. Shafi MA, Bresalier RS. The gastrointestinal complications of oncologic therapy. Gastroenterol Clin N Am. 2010;39:62947. 12. Pickhardt P, Bhalla S, Balfe DM. Acquired gastrointestinal fistulas: classification, etiologies, and imaging evaluation. Radiology. 2002;224:9-23. 13. Lyman GH, Khorana AA. Cancer, clots and consensus: new understanding of an old problem. J Clin Oncol. 2009;27:48216. 14. Cronin CG, Lhan DG, Keane M, Roche C, Murphy JM. Prevalence and significance of asymptomatic venous thromboembolic disease found on oncologic staging CT. AJR Am J Roentgenol. 2007;189:162-70. 15. Torrisi JM, Schwartz LH, Gollub MJ, Ginsberg MS, Bosl GJ, Hricak H. CT findings of chemotherapy-induced toxicity: what radiologists need to know about the clinical and radiological manifestations of chemotherapy toxicity. Radiology. 2011;258:41-56. 0-3 01-37.indd 11 Figura 7. Paciente de 86 años, con mieloma múltiple. Caída sobre el lado derecho. La radiografía simple muestra fractura diafisaria del húmero y una segunda lesión osteolítica en localización distal a la fractura (*). Fractura costal (flecha). 16. Stover DE, Kaner RJ. Pulmonary complications in cancer patients. Cancer J Clin. 1996;46:303-20. 17. Jung JI, Kim HH, Park SH, Son SW, Chung MH, Kim HS, et al. Thoracic manifestations of breast cancer and its theraphy. Radiographics. 2004;24:1269-85. 18. Vento S, Cainelli F, Temesgen Z. Lung infections after cancer chemotherapy. Lancet Oncol. 2008;9:982-92. 19. Hansell DM, Armstrong P, Lynch DA, McAdams HP. El paciente inmunodeprimido. En: Tórax. Diagnóstico radiológico. Madrid: Marban Libros S.L.; 2007. p. 271-94. 20. Azoulay E, Mokart D, Lambert J, Lemiale V, Rabbat A, Kouatchet A, et al. Diagnostic strategy for hematology and oncology patients with acute respiratory failure: randomized controlled trial. Am J Respir Crit Care Med. 2010;182:1038-46. 21. Heussel CP. Importance of pulmonary imaging diagnostics in the management of febrile neutropenic patients. Mycoses. 2011;54 Suppl 1:17-26. 22. Rañó A, Agustí C, Benito N, Rovira M, Angrill J, Pumarola T, et al. Prognostic factors of non-HIV immunocompromised patients with pulmonary infiltrates. Chest. 2002;122:25361. 23. Heussel CP, Kauczor HU, Heussel G, Fischer B, Mildenberger P, Thelen M. Early detection of pneumonia in febrile neutropenic patients: use of thin-section CT. AJR Am J Roentgenol. 1997;169:1347-53. 24. Heussel CP, Kauczor HU, Heussel GE, Fischer B, Begrich M, Mildenberger P, et al. Pneumonia in febrile neutropenic 23/11/12 11:48:57 12 patients and in bone marrow and blood stem-cell transplant recipients: use of high-resolution computed tomography. J Clin Oncol. 1999;17:796-805. 25. Shorr AF, Gregory MS, O’Grady NP. Pulmonary infiltrates in the non-HIV-infected immunocompromised patient. Etiologies, diagnostic strategies and outcomes. Chest. 2004;125:260-71. 26. Heussel CP, Kauczor HU, Ullmann AJ. Pneumonia in neutropenic patients. Eur Radiol. 2004;14:256-71. 27. Aliberti S, Myers JA, Peyrani P, Blasi F, Menéndez R, Rossi P, et al. The role of neutropenia on outcomes of cancer patients with community-acquired pneumonia. Eur Respir J. 2009;33:142-7. 28. Franquet T. High-resolution computed tomography (HRCT) of lung infections in non-AIDS immunocompromised patients. Eur Radiol. 2006;16:707-18. 29. Coy DL, Ormazbal A, Godwin JD, Lalani T. Imaging evaluation of pulmonary and abdominal complications following hematopoietic stem cell transplantation. Radiographics. 2005;25:305-18. 30. Davila M, Bresalier RS. Gastrointestinal complications of oncologic therapy. Nat Clin Pract Gastroenterol Hepatol. 2008;5:682-96. 31. Cronin CG, O’Connor M, Lohan DG, Keane M, Roche C, Bruzzi JF, et al. Imaging of the gastrointestinal complications of systemic chemotherapy. Clin Radiol. 2009.64:724-33. 32. Kirkpatrick I D C , G re e n b e rg H M . G a s t ro i n t e s t i n a l complications in the neutropenic patient: characterization 0-3 01-37.indd 12 La imagen funcional en oncología and differentiation with abdominal CT. Radiology. 2003;226:668-74. 33. Spencer SP, Power N. The acute abdomen in the immune compromised host. Cancer Imaging. 2008;8:93-101. 34. Aksoy DY, Tanriover MD, Uzun O, Zarakolu P, Ercis S, Ergüven S, et al. Diarrhea in neutropénic patients: a prospective cohort study with emphasis on neutropenic enterocolitis. Ann Oncol. 2007;18:183-9. 35. Kim SW, Shin HC, Kim IY, Kim YT, Kim CH-J. CT findings of colonic complications associated with colon cancer. Korean J Radiol. 2010;1:211-21. 36. Kolomainem DF, Barton DPJ. Surgical management of bowel obstruction in gymaecological malignancies. Curr Opin Support Palliat Care. 2011;5:55-9. 37. Heiken JP. Contrast safety in the cancer patient: preventing contrast-induced nephropathy. Cancer Imaging. 2008;8:1247. 38. Karchewski M, Babb JS, Schweitzer ME. Can diffusionweighted imaging be used to differentiate benign from pathologic fractures? A meta-analysis. Skeletal Radiol. 2008;37:791-5. 39. Coleman RE. Clinical features of metastatic bone disease and risk of skeletal morbidity. Clin Cancer Res. 2006;12 20 Suppl:6243-9. 40. Fayad LM, Kamel IR, Kawamoto S, Bluemke DA, Frassica FJ, Fishman EK. Distinguising stress fractures from pathologic fractures: a multimodality approach. Skeletal Radiol. 2005;34:245-9. 23/11/12 11:48:57 La imagen funcional en oncología 2 Tratamiento intraarterial en las neoplasias hepáticas K. Memon y R. Salem* Department of Radiology, Section of Interventional Radiology and Division of Interventional Oncology, Robert H. Lurie Comprehensive Cancer Center, Northwestern University, Chicago, IL, USA Introducción La incidencia de tumores primarios y secundarios hepáticos está aumentando de forma significativa. La cirugía y el tratamiento sistémico con quimioterapia tienen sus limitaciones1. De ahí que las terapias locorregionales guiadas mediante técnicas de imagen estén adquiriendo un papel cada vez más importante en el manejo de la patología tumoral hepática. Este tipo de terapias diana disminuye la toxicidad del tratamiento sistémico sin que se reduzca el efecto de los agentes quimioterápicos sobre el tumor. Las terapias locorregionales han demostrado tener un papel paliativo y pueden ser también potencialmente curativas. Este capítulo está orientado a la descripción de las diferentes técnicas de embolización utilizadas para el tratamiento de los tumores hepáticos en el campo de la oncología intervencionista. Estas técnicas incluyen: la embolización transarterial, quimioembolización transarterial (TACE), quimioembolización mediante esferas con liberación de fármacos (DEB-TACE) y la radioembolización para tumores malignos hepáticos. Embolización transarterial Objetivo El objetivo es inducir una isquemia tumoral mediante la oclusión de los vasos que irrigan el tumor, inyectando material de embolización en los vasos aferentes tumorales a través de un catéter intraarterial. Este tipo de tratamiento fue utilizado por primera vez en el año 1950 y constituye la base y el inicio de las terapias con catéter. Procedimiento Después de la estadificación tumoral es necesario realizar un mapa arterial exhaustivo y detallado de la anatomía vascular regional mediante angiografía. Una vez localizado e identificado el aporte vascular del tumor, el material de embolización se inyecta dentro del tumor a través de los vasos aferentes. Algunos de los materiales de embolización utilizados son partículas de alcohol polivinílico (Embospheres; BioSphere Medical Inc, Rockland, MA) o gelfoam (Pharmacia and Upjohn Company, Kalamazoo, MI). Se ha visto que la embolización induce una isquemia tumoral y muerte celular, pero puede, al mismo tiempo, ocasionar una neoangiogénesis por aumento de los factores angiogénicos secundaria a la isquemia. Evidencia clínica Maluccio et al2 publicaron los hallazgos en 322 pacientes con hepatocarcinomas (HCC) irresecables tratados mediante embolización transarterial. La media de supervivencia desde el comienzo del primer tratamiento en este estudio fue de 21 meses. La tasa de supervivencia al primero, segundo y tercer años fue del 66, 46 y 33%, respectivamente. Los autores concluyeron que la embolización arterial con partículas es efectiva para el del HCC irresecable. Covey et3 al analizaron el uso de la embolización transarterial en 45 pacientes con recurrencia de HCC intervenidos. La media de supervivencia fue de 46 meses con una tasa de supervivencia al año, 2 y 5 años del 86, 74 y 47%, respectivamente. La media de estancia hospitalaria fue de 3,2 días tras el tratamiento. Estos autores concluyen que la embolización transarterial en recurrencias tumorales de HCC es un método efectivo de terapia de rescate. La embolización se ha utilizado también en tumores neuroendocrinos. En un estudio realizado en 84 pacientes, Strosberg et al encontraron una media de supervivencia de 36 meses con una respuesta terapéutica en 11 de los 23 pacientes. Concluyen que en pacientes con metástasis irresecables de tumores neuroendocrinos la terapia con embolización arterial consigue una respuesta clínica y radiológica, y en algunos casos incluso regresión de la enfermedad4. *Autor para correspondencia. Correo electrónico: r-salem@northwestern.edu (R. Salem). 0-3 01-37.indd 13 23/11/12 11:48:57 La imagen funcional en oncología 14 A B Figura 1. A) Resonancia magnética en la que se demuestra un hepatocarcinoma en segmento posterior del lóbulo hepático derecho previo al tratamiento con quimioembolización. B) Estudio tras quimioembolización con esferas cargadas con 3 fármacos, que demuestra una necrosis completa sin tejido residual viable captante. Eriksson et al analizaron la embolización arterial en una serie de 41 pacientes y encontraron una supervivencia media de 80 meses, con una respuesta tumoral del 50%5. La embolización arterial se ha utilizado también como técnica alternativa para la disminución del dolor y el control de los síntomas en metástasis hepáticas por sarcomas6. Complicaciones Los pacientes pueden presentar un síndrome postembólico moderado, que consiste en los siguientes síntomas clínicos; fatiga, náuseas, vómitos, anorexia, fiebre, dolor abdominal, malestar y caquexia. Generalmente, los síntomas son leves y se resuelven espontáneamente. Otras complicaciones incluyen los hematomas inguinales provocados por la vía de acceso vascular o los abscesos7. Quimioembolización transarterial Objetivo La quimioembolización permite la llegada de agentes quimioterápicos a altas dosis al seno del tumor con mínimo efecto sistémico. Se está utilizado desde el año 1980 y requiere hospitalización del paciente. Procedimiento Después de analizar las características y estadio tumoral utilizando los datos clínicos y radiológicos se debe realizar una arteriografía para obtener un mapa de la anatomía vascular regional y del tumor. El agente quimioterápico se mezcla con lipiodol y se inyecta en los vasos que irrigan al tumor durante la realización de la angiografía. El lipiodol es un aceite que se obtiene de la semilla de la amapola y contiene un 38% 0-3 01-37.indd 14 de yodo. Es una sustancia radiopaca que se visualiza en el estudio de control de la tomografía computarizada (TC) tras el tratamiento en el seno de la lesión tratada. Esto se sigue de una inyección de partículas embolizantes para prevenir el lavado del agente quimioterápico y evitar la necrosis isquémica (fig. 1). Evidencia clínica En general, las contraindicaciones absolutas a la quimioembolización incluyen la ausencia de flujo hepatópato, colaterales compensatorias, encefalopatía y obstrucción biliar. Las contraindicaciones relativas incluyen una cifra de bilirrubina en sangre > 2 mg/dl, lactato dehidrogenasa > 425 U/l, aspartato aminotransferasa > 100 U/l, carga tumoral > 50% del hígado, ascitis, sangrado de varices, trombocitopenia, o insuficiencia renal o cardíaca. La doxorrubicina sola se utiliza en muchos centros en diferentes países, en Estados Unidos se emplea en combinación con mitomicina C y cisplatino. Los mejores candidatos para la quimioembolización son aquellos con un buen estado clínico, con una función hepática preservada y sin invasión vascular o metástasis extrahepáticas. Llovet et al 8 estudiaron los resultados en pacientes tratados con quimioembolización, embolización y medidas conservadoras. Estos autores concluyeron que la quimioembolización y la embolización mejoraban significativamente la supervivencia en pacientes seleccionados con HCC irresecables. Takayasu et al9 publicaron los resultados de un estudio de cohorte en 8.510 HCC tratados con quimioembolización y demostraron que los principales datos pronósticos que influían en la supervivencia eran el grado de daño funcional hepático, el valor de la alfa-fetoproteína, el volumen tumoral, el número de lesiones y la invasión venosa portal. También se han publicado datos en pacientes con metástasis tratados con quimioembolización. 23/11/12 11:48:57 Tratamiento intraarterial en las neoplasias hepáticas Geschwind et al demostraron que la quimioembolización puede prolongar la supervivencia en pacientes con metástasis de carcinoma colorrectal, incluso en pacientes que no responden a la terapia sistémica10. Liapi et al analizaron la respuesta por imagen y determinaron los resultados clínicos en 26 pacientes con metástasis de tumores neuroendocrinos tratados con quimioembolización, y demostraron una supervivencia media de 78 meses11. La respuesta por imagen utilizando los criterios WHO y RECIST se vio en solamente un tercio del grupo cohorte. Burger et al publicaron su experiencia en 17 pacientes con colangiocarcinomas irresecables tratados con quimioembolización y concluyeron que ésta era efectiva y prolongaba la supervivencia media de estos pacientes12. 15 Las esferas con liberación de fármacos son agentes quimioterápicos cargados en microesferas que se administran por vía intraarterial. Esto permite una perfusión del fármaco de una forma controlada y mantenida caron un 63% de respuesta utilizando los criterios RECIST modificados que tienen en cuenta la necrosis tumoral. En un ensayo aleatorizado reciente en 200 pacientes comparando la quimioembolización convencional con las esferas cargadas, no se encontró una tasa de supervivencia superior (PRECISION V). El número de efectos adversos resultó ser inferior tras quimioembolización con esferas cargadas. Varela et al17 investigaron el uso de la quimioembolización DEB en una serie de 27 pacientes con HCC y Child-Pugh A cirrosis. Demostraron que el porcentaje de respuesta era de un 75% en los controles de TC realizados a los 6 meses; la concentración máxima de doxirrubicina en plasma y el área bajo la curva fueron significativamente inferiores que con la TACE convencional, y la supervivencia al año y 2 años fue del 92,5 y el 88,9%, respectivamente, con una media de seguimiento de 27,6 meses. En este trabajo concluyen que la quimioembolización utilizando DEB es un procedimiento efectivo con un perfil farmacocinético favorable. Malagari et al18 realizaron un ensayo prospectivo aleatorizado que comparaba DEB con simple quimioembolización en 2 grupos con 41 y 43 pacientes, respectivamente. Una respuesta completa y parcial medida según criterios EASL se vio en el 26,8 y el 46,3% de los pacientes tratados con DEB, respectivamente, frente al 14 y el 41,9% de los pacientes tratados con embolización. El porcentaje de recurrencia fue superior en el grupo tratado con embolización simple, mientras que el tiempo hasta la progresión tumoral fue superior en los pacientes tratados con DEB-TACE. La quimioembolización con esferas cargadas se ha utilizado también en casos de metástasis hepáticas por carcinoma colorrectal. En un trabajo multicéntrico reciente, en una serie de 55 pacientes con metástasis de carcinoma colorrectal tratados previamente con quimioterapia, Martin et al19 evaluaron 99 sesiones de tratamiento con DEBIRI (esferas de liberación de irinotecan). En un 28% de los casos se registraron efectos adversos y el porcentaje de respuesta fue del 66 y el 75% a los 6 y 12 meses; la supervivencia global y el tiempo libre de progresión fueron de 19 y 11 meses, respectivamente. Estos autores concluyen que el tratamiento intraarterial con DEBIRI es seguro y efectivo en pacientes con carcinoma metastásico colorrectal refractario a diversas líneas de tratamiento sistémico quimioterápico. Procedimiento Complicaciones El procedimiento es similar a la quimioembolización convencional y se administra tras la evaluación angiográfica de la anatomía vascular regional. Diversos trabajos han demostrado una disminución significativa de la concentración de fármaco en plasma con esferas liberadoras de fármacos comparativamente con la quimioterapia convencional15. El perfil de toxicidad es similar al objetivado en la quimiembolización convencional y los datos iniciales publicados en el ensayo clínico PRECISION V trial apuntan que puede ser una terapia más segura que la quimioembolización convencional. Complicaciones El síndrome postembolización tras el tratamiento con TACE requiere la hospitalización del paciente. Otras complicaciones pueden incluir: a) lesiones del conducto biliar7, hasta el 5,3% de los pacientes puede desarrollar complicaciones biliares13; b) abscesos hepáticos7; c) úlceras duodenales o gástricas por la introducción accidental del agente quimioterápico en el tracto gastrointestinal, que pueden dar lugar incluso a perforaciones en casos severos7; d) la vía intraarterial también provoca un aumento del riesgo de lesión vascular asociado a todas las técnicas con catéter7, así como el efecto del propio fármaco sobre el vaso14; e) rotura tumoral, que ocurre en un 0,15% de los casos 7, y f) embolia pulmonar7. Quimioembolización con esferas de liberación de fármaco Objetivo Evidencia clínica Las esferas cargadas con doxorrubicina tienen un papel prometedor en el tratamiento del HCC irresecable. La selección de pacientes es similar a la que se realiza para la quimioembolización convencional. Poon et al16 publi- 0-3 01-37.indd 15 Radioembolización Objetivo La radioembolización utiliza diferentes partículas vehiculizantes cargadas con radionúcleos con el objetivo 23/11/12 11:48:57 La imagen funcional en oncología 16 A B Figura 2. A) Resonancia magnética preradioembolización que muestra un hepatocarcinoma hipervascular en el lóbulo hepático derecho. B) Estudio realizado tras tratamiento con Ytrium, que demuestra una necrosis completa sin tejido residual viable captante. de administrar una dosis de radiación concentrada en la lesión diana. Hay una gran incidencia de enfermedades hepáticas inducidas por la radiación externa y la radioembolización minimiza esta incidencia; la ventaja respecto a la quimioembolización es que esta técnica puede realizarse en un entorno ambulatorio sin necesidad de ingreso del paciente. Procedimiento La radioembolización es un proceso diferente a cualquier otra embolización, la diseminación accidental de las microesferas cargadas con radionúcleos se previene mediante la realización de un estudio meticuloso del mapa anatómico vascular del hígado y de las colaterales. La embolización con coils de los vasos no diana puede ser necesaria para evitar el depósito accidental de microesferas. El tecnecio-99m marcado con macroagregados de albúmina (99mTc-MAA) se utiliza para demostrar los shunts del flujo esplácnico y pulmonar. Este estudio previo al tratamiento es importante realizarlo para prevenir complicaciones y calcular la fracción de shunt pulmonar (fig. 2). Evidencia clínica El uso de la radioembolización se ha visto que limita la progresión del hepatocarcinoma, esto permite que se pueda prolongar el tiempo de espera de los pacientes para la donación de órgano20 y aumentan sus posibilidades de ser sometidos a trasplante. Además, en los pacientes con un estadio tumoral que los excluye de la lista de trasplante, la radioembolización puede reducir el estadio y convertirlos en candidatos. También se ha visto que hay un aumento de la supervivencia global en estos pacientes20. 0-3 01-37.indd 16 En pacientes con invasión vascular tumoral se ha visto una mejora de la supervivencia con el uso de la radioembolización21. En un estudio comparativo reciente se ha visto que la radioembolización tiene una toxicidad menor y un aumento del tiempo hasta la progresión comparada con la quimiembolización convencional22. En otro estudio multicéntrico europeo reciente se analizó la radioquimioembolización en 325 pacientes con HCC y se demostró que la supervivencia aumentaba significativamente tras la radioembolización, incluso en los pacientes con enfermedad avanzada23. En un estudio piloto en el que se analizó el uso del 90Y en 24 pacientes con colangiocarcinoma intrahepático demostrado por biopsia, la respuesta al tratamiento resultó favorable con un aumento de la supervivencia global24. Los pacientes con carcinoma colorrectal metastásico con enfermedad hepática irresecable en tratamiento con quimioterapia o que no han respondido a la primera o segunda línea de quimioterapia se considera que son candidatos para este tipo de terapia con radioembolización. La combinación de radioembolización con quimioterapia sistémica produce una mayor respuesta tumoral y aumenta el tiempo hasta la progresión y la supervivencia con un perfil de seguridad aceptable25. El uso de radioembolización como único método de tratamiento se ha publicado en diferentes series con unos resultados prometedores26. Un ensayo clínico aleatorizado reciente ha sugerido que la combinación de radioembolización con fluorouracilo intravenoso es superior a la perfusión únicamente de fluorouracilo en cuanto a tiempo, progresión y mejora de la supervivencia27. La radioembolización de la enfermedad metastásica hepática de tumores neuroendocrinos se ha demostrado que es efectiva y segura. Se ha visto una respuesta al tratamiento superior a los 2 años28,29. 23/11/12 11:48:57 Tratamiento intraarterial en las neoplasias hepáticas Complicaciones El síndrome postembolización ocurre menos frecuentemente después de la radioembolización debido al pequeño tamaño de las partículas y, en general, no requiere hospitalización. Otros efectos adversos asociados a la radioembolización incluyen: a) enfermedad hepática radioinducida con ascitis; b) fibrosis que puede dar lugar a una hipertensión con un tiempo variable hasta el desarrollo; c) bilomas, abscesos, colecistitis; d) neumonitis postirradiación con alta fracción de shunt pulmonar; e) úlceras gastrointestinales; f) lesiones vasculares30. Conclusiones La selección cuidadosa de los pacientes y la preparación de las terapias diana pueden contribuir a una relación riesgo/beneficio óptima para el paciente. Para pacientes con hepatocarcinoma, el tratamiento de la enfermedad avanzada debe balancearse con la reserva funcional hepática debido a la cirrosis subyacente que suelen presentar estos pacientes. La selección de pacientes con una adecuada reserva funcional hepática y una buena situación clínica conduce a un mayor beneficio terapéutico con mínimo riesgo sobre el parénquima hepático normal. Este tipo de tratamientos se ha demostrado que son beneficiosos para pacientes con enfermedad metastásica que presentan progresión intrahepática a pesar del tratamiento estándar con quimioterapia. El beneficio clínico y la potencial mejora de la calidad de vida constituyen una oportunidad y un reto para todos los profesionales que participan en el manejo de los tumores hepáticos. Bibliografía 1. Llovet JM, Ricci S, Mazzaferro V, Hilgard P, Gane E, Blanc JF, et al. Sorafenib in advanced hepatocellular carcinoma. N Engl J Med. 2008;359:378-90. 2. Maluccio MA, Covey AM, Porat LB, Schubert J, Brody LA, Sofocleous CT, et al. Transcatheter arterial embolization with only particles for the treatment of unresectable hepatocellular carcinoma. J Vasc Interv Radiol. 2008;19: 862-9. 3. Covey AM, Maluccio MA, Schubert J, BenPorat L, Brody LA, Sofocleous CT, et al. Particle embolization of recurrent hepatocellular carcinoma after hepatectomy. Cancer. 2006;106:2181-9. 4. Strosberg JR, Choi J, Cantor AB, Kvols LK. Selective hepatic artery embolization for treatment of patients with metastatic carcinoid and pancreatic endocrine tumors. Cancer Control. 2006;13:72-8. 5. Eriksson BK, Larsson EG, Skogseid BM, Lofberg AM, Lorelius LE, Oberg KE. Liver embolizations of patients with malignant neuroendocrine gastrointestinal tumors. Cancer. 1998;83:2293-301. 6. Maluccio MA, Covey AM, Schubert J, Brody LA, Sofocleous CT, Getrajdman GI, et al. Treatment of metastatic sarcoma to the liver with bland embolization. Cancer. 2006;107: 1617-23. 0-3 01-37.indd 17 17 7. Xia J, Ren Z, Ye S, Sharma D, Lin Z, Gan Y, et al. Study of severe and rare complications of transarterial chemoembolization (TACE) for liver cancer. Eur J Radiol. 2006;59:407-12. 8. Llovet JM, Real MI, Montana X, Planas R, Coll S, Aponte J, et al. Arterial embolisation or chemoembolisation versus symptomatic treatment in patients with unresectable hepatocellular carcinoma: a randomised controlled trial. Lancet. 2002;359:1734-9. 9. Takayasu K, Arii S, Ikai I, Omata M, Okita K, Ichida T, et al. Prospective cohort study of transarterial chemoembolization for unresectable hepatocellular carcinoma in 8 510 patients. Gastroenterology. 2006;131:461-9. 10. Geschwind J, Hong K, Georgiades C. Utility of transcatheter arterial chemoembolization for liver dominant colorectal metastatic adenocarcinoma in the salvage setting. American Society of Clinical Oncology Gastrointestinal Cancers Symposium. San Francisco, CA. January 26-28, 2006. 11. Liapi E, Geschwind J-F, Vossen JA, Buijs M, Georgiades CS, Bluemke DA, et al. Functional MRI evaluation of tumor response in patients with neuroendocrine hepatic metastasis treated with transcatheter arterial chemoembolization. AJR Am J Roentgenol. 2008;190:67-73. 12. Burger I, Hong K, Schulick R, Georgiades C, Thuluvath P, Choti M, et al. Transcatheter arterial chemoembolization in unresectable cholangiocarcinoma: initial experience in a single institution. J Vasc Interv Radiol. 2005;16:353-61. 13. Kim HK, Chung YH, Song BC, Yang SH, Yoon HK, Yu E, et al. Ischemic bile duct injury as a serious complication after transarterial chemoembolization in patients with hepatocellular carcinoma. J Clin Gastroenterol. 2001;32:423-7. 14. Belli L, Magistretti G, Puricelli GP, Damiani G, Colombo E, Cornalba GP. Arteritis following intra-arterial chemotherapy for liver tumors. Eur Radiol. 1997;7:323-6. 15. Hong K, Georgiades CS, Geschwind JF. Technology insight: image-guided therapies for hepatocellular carcinoma-intra-arterial and ablative techniques. Nat Clin Pract Oncol. 2006;3:315-24. 16. Lo CM, Ngan H, Tso WK, Liu CL, Lam CM, Poon RT, et al. Randomized controlled trial of transarterial lipiodol chemoembolization for unresectable hepatocellular carcinoma. Hepatology. 2002;35:1164-71. 17. Varela M, Real MI, Burrel M, Forner A, Sala M, Brunet M, et al. Chemoembolization of hepatocellular carcinoma with drug eluting beads: efficacy and doxorubicin pharmacokinetics. J Hepatol. 2007;46:474-81. 18. Malagari K, Pomoni M, Kelekis A, Pomoni A, Dourakis S, Spyridopoulos T, et al. Prospective randomized comparison of chemoembolization with doxorubicin-eluting beads and bland embolization with BeadBlock for hepatocellular carcinoma. Cardiovasc Intervent Radiol. 2010;33:541-51. 19. Martin RC, Joshi J, Robbins K, Tomalty D, Bosnjakovik P, Derner M, et al. Hepatic intra-arterial injection of drugeluting bead, irinotecan (DEBIRI) in unresectable colorectal liver metastases refractory to systemic chemotherapy: results of multi-institutional study. Ann Surg Oncol. 2011;18:192-8. 20. Kulik LM, Atassi B, Van Holsbeeck L, Souman T, Lewandowski R J, M u l c a hy M F, e t a l . Y t t r i u m - 9 0 m i c r o s p h e r e s (TheraSphere®) treatment of unresectable hepatocellular carcinoma: Downstaging to resection, RFA and bridge to transplantation. J Surg Oncol. 2006;94:572-86. 21. Kulik LM, Carr BI, Mulcahy MF, Lewandowski RJ, Atassi B, Ryu RK, et al. Safety and efficacy of (90)Y radiotherapy for hepatocellular carcinoma with and without portal vein thrombosis. Hepatology. 2007;47:71-81. 23/11/12 11:48:57 18 22. Salem R, Lewandowski RJ, Kulik L, Wang E, Riaz A, Ryu RK, et al. Radioembolization results in longer time-to-progression and reduced toxicity compared with chemoembolization in patients with hepatocellular carcinoma. Gastroenterology. 2011;140:497-507, e492. 23. Sangro B, Carpanese L, Cianni R, Golfieri R, Gasparini D, Ezziddin S, et al. Survival after yttrium-90 resin microsphere radioembolization of hepatocellular carcinoma across Barcelona clinic liver cancer stages: A European evaluation. Hepatology. 2011;54:868-78. 24. Ibrahim SM, Mulcahy MF, Lewandowski RJ, Sato KT, Ryu RK, Masterson EJ, et al. Treatment of unresectable cholangiocarcinoma using yttrium-90 microspheres: results from a pilot study. Cancer. 2008;113:2119-28. 25. Gray B, Van Hazel G, Hope M, Burton M, Moroz P, Anderson J, et al. Randomised trial of SIR-Spheres plus chemotherapy vs. chemotherapy alone for treating patients with liver metastases from primary large bowel cancer. Ann Oncol. 2001;12:1711-20. 26. Kennedy A, Coldwell D, Nutting C, Overton C, Sailer S. Liver brachytherapy for unresectable colorectal metastases: US 0-3 01-37.indd 18 La imagen funcional en oncología results 2000-2004. ASCO GI Symposium. Miami, Florida. Jan 27-29, 2005. 27. Hendlisz A, Van den Eynde M, Peeters M, Maleux G, Lambert B, Vannoote J, et al. Phase III trial comparing protracted intravenous fluorouracil infusion alone or with yttrium-90 resin microspheres radioembolization for liverlimited metastatic colorectal cancer refractory to standard chemotherapy. J Clin Oncol. 2010;28:3687-94. 28. Rhee TK, Lewandowski RJ, Liu DM, Mulcahy MF, Takahashi G, Hansen PD, et al. 90Y Radioembolization for metastatic neuroendocrine liver tumors: preliminary results from a multi-institutional experience. Ann Surg. 2008;247:1029-35. 29. Kennedy AS, Dezarn WA, McNeillie P, Coldwell D, Nutting C, Carter D, et al. Radioembolization for unresectable n e u ro e n d o c r i n e h ep a t i c m e t a s t a s e s u s i n g re s i n 90Y-microspheres: early results in 148 patients. Am J Clin Oncol. 2008;31:271-9. 30. Riaz A, Lewandowski RJ, Kulik LM, Mulcahy MF, Sato KT, Ryu RK, et al. Complications following radioembolization with yttrium-90 microspheres: a comprehensive literature review. J Vasc Interv Radiol. 2009;20:1121-30; quiz 1131. 23/11/12 11:48:58 La imagen funcional en oncología 3 Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica P. Caro Mateo* y E. Navas Campos Radiología, DADISA, Grupo Healthtime, Cádiz, España Introducción El cáncer colorrectal es el tercer tumor no cutáneo más frecuente en el ámbito mundial y el segundo en mortalidad después del cáncer de pulmón cuando se incluyen ambos sexos. Un 30% se localiza en el recto. El cáncer de recto tiene peor pronóstico que el cáncer de colon por su mayor tasa de recidiva local y su mayor riesgo de enfermedad metastásica en el momento del diagnóstico, además de una mayor morbilidad. Esto es debido a su situación predominantemente extraperitoneal y a la íntima vecindad con otros órganos en un espacio restringido que exige estrategias de tratamiento específicas y cirugía especializada. La tasa de supervivencia está directamente ligada al estadio tumoral. Sin embargo, para cada estadio tumoral el rango de supervivencia es heterogéneo, por lo que es importante detectar la presencia de factores de mal pronóstico anatómicos, histológicos y dependientes de la propia biología tumoral, así como de la respuesta del tumor al tratamiento. En la actualidad ha mejorado de forma significativa la supervivencia tras la estandarización de la escisión total del mesorrecto (ETM) como técnica quirúrgica, la implementación de terapia neoadyuvante-adyuvante para tumores localmente avanzados y la evaluación personalizada de cada paciente por un equipo multidisciplinar que decide cuál es la estrategia más oportuna basada en una estadificación clínica lo más precisa posible. Los avances en la imagen diagnóstica permiten evaluar el recto con excelente resolución anatómica y de contraste permitiendo el análisis detallado del tumor y de los factores pronósticos, tanto en la estadificación inicial como en la valoración de la respuesta al tratamiento. Lo más habitual en la práctica clínica es evaluar la respuesta al tratamiento mediante aproximaciones anatómicas de medidas y volumen tumorales. Sin embargo, estas aproximaciones tienen limitaciones. Además, los tumores representan modelos biológicos muy complejos con características específicas como la alta celularidad, la angiogénesis tumoral, el metabolismo y la hipoxia, entre otras, que no son valoradas adecuadamente con la imagen radiológica convencional, y que son causa del fracaso del tratamiento. Con los nuevos tratamientos no son raras las remisiones patológicas completas y la disminución del estadio clínico. La indicación quirúrgica se basa en el estadio inicial del tumor, independientemente de la respuesta al tratamiento, si bien algunos estudios proponen tratamientos menos agresivos con preservación de esfínteres e incluso resección local para las remisiones completas o tumores limitados a la pared rectal. Para ello se necesita disponer de una adecuada reestadificación prequirúrgica una vez finalizado el tratamiento neoadyuvante1. Las medidas anatómicas tampoco sirven como biomarcadores de respuesta a las nuevas terapias citostáticas como las antiangiogénicas, que suprimen el crecimiento tumoral pero no tienen efecto citotóxico (muerte celular con regresión tumoral), por lo que los actuales criterios morfológicos no tienen correlación con la efectividad del tratamiento. Para evitar las limitaciones de los criterios anatómicos de respuesta cada vez se utilizan más las técnicas de imagen funcional, que son capaces de evaluar in vivo características tumorales, cuya determinación era dominio del examen histopatológico, y que permiten monitorizar precozmente la respuesta al tratamiento antes de que existan cambios de tamaño o volumen. Anatomía del recto Se define como cáncer de recto las tumoraciones cuyo margen inferior medido con el rectoscopio rígido se sitúa a 15-16 cm del margen anal. Los tumores de recto se dividen en función de la distancia de su extremo distal al margen anal en bajos (hasta 5 cm), medios (entre 5,1 y 10 cm) y altos (entre 10,1 y 15 cm). *Autor para correspondencia. Correo electrónico: pilar.e.caro@gmail.com (P. Caro Mateo). 0-3 01-37.indd 19 23/11/12 11:48:58 La imagen funcional en oncología 20 Tabla 1 − TNM (American Joint Committee on Cancer/International Union Against Cancer) 7.a edición (2010) Tumor primario (T) TX TO Tis T1 T2 T3 pT3a pT3b pT3c T4a T4b El tumor primario no puede evaluarse No hay evidencia de tumor primario Carcinoma in situ (carcinoma intraepitelial o intramucoso) El tumor invade la submucosa El tumor invade la muscular propia El tumor atraviesa la muscular propia e invade el mesorrecto Invasión < 5 mm Invasión 5-10 mm por fuera de la muscular propia Invasión > 10 mm por fuera de la muscular propia El tumor perfora el peritoneo visceral El tumor invade o se adhiere a otros órganos o estructuras Ganglios linfáticos regionales (N) NX N0 N1a N1b N1c N2a N2b Los ganglios linfáticos regionales no pueden evaluarse No hay metástasis en los ganglios linfáticos regionales Hay tumor en 1 ganglio linfático regional Hay tumor en 2 o 3 ganglios linfáticos regionales Depósitos tumorales en la subserosa, mesenterio o en tejidos no peritonealizados pericólicos o perirrectales sin metástasis ganglionares regionales Hay tumor en 4 a 6 ganglios linfáticos regionales Hay tumor en 7 o más ganglios regionales Metástasis a distancia (M) MX M0 M1a M1b La presencia de metástasis a distancia no puede evaluarse No hay metástasis a distancia Extensión tumoral a distancia limitada a un órgano o localización (hígado, pulmón, ovario, ganglio no regional) Extensión tumoral a más de un órgano, localización o al peritoneo cTNM: clasificación pretratamiento, basada en la exploración clínica, pruebas de imagen, endoscopia, biopsia o exploración quirúrgica; pTMN: clasificación histopatológica posquirúrgica; TNM: tumor, adenopatía, metástasis; ypTNM: clasificación histopatológica posquirúrgica efectuada tras tratamiento neoadyuvante. La inserción del peritoneo es más alta por su aspecto posterior y caras laterales que en su cara anterior, de ahí que el tercio superior del recto es intraperitoneal y los dos tercios inferiores corresponden a la porción extraperitoneal. La reflexión peritoneal anterior discurre por la superficie vesical en el varón y por el fundus uterino en la mujer hasta la cara anterior del recto. En este punto, el peritoneo se fusiona con la fascia mesorrectal (FMR) anterior y la fascia de Denonvilier. El recto extraperitoneal está rodeado por el tejido graso, que se conoce como mesorrecto, que contiene vasos y ganglios linfáticos. La FMR es la fascia visceral del recto extraperitoneal. Es una capa de tejido fibroareolar que rodea al mesorrecto y es una estructura anatómica muy importante, ya que representa, si bien no es lo mismo, el margen de resección circunferencial (MRC) y actúa como una barrera natural a la diseminación tumoral. El tercio inferior del recto corresponde a los últimos 5 o 6 cm. A este nivel, el mesorrecto va disminuyendo de tamaño en sentido descendente para fusionarse con el extremo superior del esfínter interno. El drenaje linfático de los dos tercios superiores del recto se hace a través de los ganglios del mesorrecto y de 0-3 01-37.indd 20 la arteria mesentérica inferior. El tercio distal puede drenar con los vasos rectos medios a la cadena ilíaca interna, siendo más frecuente la presencia de diseminación ganglionar extramesorrectal mediante diseminación lateral. También puede drenar a cadenas inguinales y diseminarse al pulmón sin pasar por el hígado2. Estadificación tumoral La evaluación de la extensión tumoral que define grupos de pacientes según estadios es el preámbulo ineludible para plantear las estrategias de tratamiento individualizado y estimar el pronóstico de cada paciente. La adecuada estadificación clínica es el objetivo fundamental del equipo multidisciplinar; una estadificación incompleta o inadecuada puede llevar a la selección de un tratamiento inadecuado. Para la estadificación del cáncer de recto se utiliza la clasificación TNM y la establecida por la International Union Against Cancer (IUAC) (tabla 1). Para la aplicación del sistema TNM a una lesión se debe disponer de la 23/11/12 11:48:58 Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica confirmación anatomopatológica de su naturaleza tumoral. Se distinguen 2 factores pronósticos independientes: la extensión local del tumor (T) y la ausencia/presencia de metástasis ganglionares (N). La valoración de la T se centra en la afectación de la lámina muscular propia. Los tumores T1 y T2 son lesiones precoces, limitadas a la pared rectal. La diferenciación entre lesiones T2 y T3 se basa en la afectación o no de la grasa perirrectal. Los tumores en estadio T3 son los más numerosos y tienen alta tasa de recidivas locales, sobre todo los situados en los dos tercios distales. Sin embargo, constituyen un grupo muy heterogéneo: desde los que infiltran mínimamente la grasa perirrectal a los que se extienden o infiltran la FMR3. Se ha demostrado que el pronóstico depende más de la distancia radial del tumor a la fascia que del estadio T. La presencia de un MRC invadido o amenazado puede ser anticipada por imagen si se identifica la presencia de tumor, focos tumorales discontinuos o ganglios metastásicos a menos de 1 o 2 mm de la FMR y es un factor predictivo potente de recidiva local. Mención especial tienen los tumores de recto inferior, que constituyen un grupo aparte por el escaso volumen del mesorrecto, pudiendo resultar en un MRC afectado, incluso en tumores en estadio precoz y por mayores tasas de recurrencia local, lo que obliga a tratamientos quirúrgicos más agresivos y al empleo de neoadyuvancia de manera más frecuente. El estadio T4 corresponde a las lesiones que infiltran órganos vecinos, al complejo esfinteriano o al peritoneo, en su reflexión en la cara anterior del recto o por encima de ella. Es factor predictivo de recurrencia a pesar de una resección quirúrgica en bloque y obliga a amputaciones más amplias y a tratamiento radioterápico con intensificación de dosis. La diseminación ganglionar es un factor de mal pronóstico independiente, tanto para la supervivencia como para la recaída local. Deben valorarse las vías de diseminación linfática, que varían según la localización del tumor. La invasión tumoral vascular de venas del mesorrecto ocurre en un 30% de tumores, suele asociarse a tumores localmente avanzados y lleva aparejada un mayor riesgo de afectación ganglionar y de enfermedad metastásica. Por este motivo, cuando se diagnostica, es obligado el tratamiento sistémico. Técnicas de imagen en la estadificación El papel del radiólogo es fundamental en la estadificación. Consiste en la valoración morfológica del tumor, de su extensión local y de los factores pronósticos, que orienten a la indicación quirúrgica y a la necesidad de neoadyuvancia/adyuvancia sistémicas de la forma más ajustada posible a la situación clínica del paciente y a las características del tumor. Ecografía endoanal La ecografía endoanal ha sido la más utilizada en la estadificación local de las lesiones, ya que permite una excelente 0-3 01-37.indd 21 21 delimitación de las capas de la pared rectal y la relación del tumor con éstas. Es una técnica de bajo coste e inocua, indicada para lesiones situadas hasta 12 cm del margen anal. No es apta para estenosis tumorales infranqueables. La ecografía endoanal está indicada fundamentalmente en la valoración de lesiones precoces (fig. 1A), siendo probablemente la mejor técnica de imagen para la distinción entre T1 y T2 (necesaria para decidir si es posible el tratamiento quirúrgico mediante técnicas endoanales). Por el contrario, su utilidad es más limitada para evaluar lesiones más avanzadas ya que no consigue valorar la FMR en todos los pacientes (fig. 1B). Se distinguen 5 capas: la primera y más próxima al transductor es hiperecogénica y representa la interfase entre la sonda y la mucosa; la segunda, hipoecoica, representa a la muscularis mucosa; la tercera, de mayor grosor e hiperecoica, representa a la submucosa; la cuarta es hipoecogénica y corresponde a la muscular propia. Distalmente se identifica la grasa mesorrectal hiperecogénica. El tumor es hipoecoico y puede estar rodeado de edema y fibrosis, también hipoecoicos, que pueden justificar una sobreestadificación de la lesión. Un tumor que no sobrepasa la lámina hiperecoica de la submucosa corresponde a un estadio T1. En el estadio T2, el tumor oblitera la submucosa y entra en contacto con la muscular propia sin atravesarla. En el estadio T3 la lesión hipoecoica atraviesa la muscular y penetra en la grasa mesorrectal. El estadio T4 con ecografía se establece cuando se identifica invasión de órganos pélvicos como la próstata (fig. 1). La fiabilidad diagnóstica de la ecografía para estimar la T oscila entre el 69 y el 97%2. Tomografía computarizada multidetector El avance tecnológico que ha supuesto la tomografía computarizada multidetector (TCMD) con su alta resolución espacial y temporal y, sobre todo, la posibilidad de obtener reconstrucciones multiplanares de alta calidad orientadas al tumor, la hace apta para la estadificación local de tumores avanzados con una precisión diagnóstica en rangos comprendidos entre el 83 y el 87% en diversas publicaciones2. Es posible evaluar los factores pronósticos más importantes cuando se considera la T, la progresión extramural y la relación del tumor con la FMR y con las estructuras pélvicas. Esto es especialmente relevante para los pacientes con contraindicaciones para la realización de la resonancia magnética (RM). También es una técnica de gran disponibilidad y permite el cribado de enfermedad en el pulmón e hígado con alta fiabilidad. Resonancia magnética Es indiscutible que la RM es la modalidad de imagen de mayor resolución de contraste. En la actualidad, el desarrollo técnico, fundamentalmente las antenas de superficie phased-array de alta resolución, la imagen en paralelo y gradientes más potentes, permiten estudiar mediante secuencias de alta resolución y campos de visión amplios las lesiones rectales en tiempos de adquisición razonables, habiéndose mejorado significativamente las precisiones diagnósticas publicadas2. 23/11/12 11:48:58 La imagen funcional en oncología 22 A B Figura 1. Ecografía endoanal. A) Tumor T1: la lesión hipoecoica no rebasa la submucosa hiperecoica. B) Tumor T3 hipoecoico que invade la grasa mesorrectal anterior. No se distingue la FMR. T: tumor; U: útero. Casos cedidos por el Dr. Ramón Botella, Hospital Universitario Gregorio Marañón de Madrid. Consideraciones técnicas. El recto es relativamente fijo, lo que permite adquirir secuencias de alta resolución espacial. El protocolo básico para la estadificación local se basa fundamentalmente en secuencias turbo-espín-eco T2. La secuencia fundamental es un plano axial oblicuo perpendicular al eje mayor del tumor o a la luz rectal adyacente, con voxel reducido de 0,6-0,8 mm3, que debe incluir todo el tumor. En esta secuencia se evaluará la infiltración mural/extramural del tumor y la distancia radial a la FMR, la invasión de órganos y del peritoneo. En tumores del tercio distal debe programarse una secuencia coronal paralela al canal anal para evaluar la relación del tumor con el complejo esfinteriano y los músculos elevadores. En la actualidad existe la posibilidad de adquirir una secuencia axial pura T2-TSE de voxel isotrópico, la cual puede ser reconstruida posteriormente en todos los planos que sean necesarios. La RM con antena endorrectal es capaz de evaluar la estructura laminar del recto de forma similar a la ecografía endoanal y presenta una precisión diagnóstica similar. Están disponibles antenas endorrectales y phased-array integradas que superan las desventajas del campo de visión reducido de la antena endorrectal y permite la evaluación de la FMR y la existencia de adenopatías. No obstante, la mayoría de los grupos de trabajo utiliza las antenas phased-array. En estudios comparativos con equipos de 3T, no se han encontrado diferencias significativas en la estadificación 0-3 01-37.indd 22 T2 y T3, aunque los equipos de 3T son superiores en la evaluación de la pared y en las técnicas funcionales. Valoración de la T con resonancia. En RM no siempre es posible discriminar todas las capas de la pared rectal; la mucosa presenta baja señal, la submucosa suele ser hiperintensa en T2 y la muscular propia es hipointensa. Los tumores suelen ser ligeramente hiperintensos en T2, en relación con la muscular propia. Se considera T1 cuando se identifica la señal hiperintensa en T2 de la mucosa; estadio T2 cuando la señal tumoral entra en contacto o incluso reemplaza la hiposeñal en T2 de la muscular propia sin rebasarla; estadio T3 cuando se observa señal tumoral de base nodular en la grasa del mesorrecto, no sólo una espiculación fina; estadio T4a, cuando exista infiltración de la superficie peritoneal anterior por señal tumoral de morfología nodular, y T4b cuando se identifica señal tumoral infiltrando órganos pélvicos, musculatura pélvica o el esfínter anal. A pesar del empleo de antenas de superficie, la fiabilidad diagnóstica de la RM para valorar la T en estudios recientes sólo es del 67-85%4. La resonancia tiene dificultades para diferenciar entre tumores T1 y T2, ambos confinados a la pared rectal, de los tumores T3 mínimamente invasivos. Esto se debe principalmente a las dificultades para evaluar la reacción desmoplástica que aparece en ocasiones de forma reactiva al tumor. No es posible diferenciar si es una reacción no tumoral 23/11/12 11:48:58 Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica A B C 23 D E F Figura 2. Tumor de recto medio T4. A, B y C) T2-TSE pre-QRT muestran invasión de la FMR, vesícula seminal derecha y de venas extramurales; D, E y F) Las secuencias T2-TSE post-QRT muestra reducción de volumen y fibrosis, no siendo posible descartar restos tumorales extramurales. Estadio ypT3. Flecha blanca: invasión de una vena extramural; FMR: fascia mesorrectal; T: tumor; VS: vesícula seminal. (pT2) o si hay células tumorales en su interior (pT3). De todas formas, esta discriminación no es muy significativa desde el punto de vista del pronóstico y también plantea problemas diagnósticos a la ecografía endoanal. También pueden darse falsos positivos y falsos negativos en la estadificación T4a. 0-3 01-37.indd 23 Valoración de la invasión de venas extramurales. La valoración de la invasión vascular extramural era dominio del examen patológico. La RM es la única modalidad de imagen capaz de evaluarlo preoperatoriamente al identificar la presencia de una vena extramural aumentada de calibre con señal heterogénea endoluminal (fig. 2). 23/11/12 11:48:59 24 La imagen funcional en oncología Estimación del estadio N con técnicas de imagen Opciones terapéuticas La identificación de la afectación ganglionar es el principal desafío para la estadificación prequirúrgica del cáncer de recto, independientemente de la modalidad de imagen empleada. Es importante una estadificación precisa ya que el pronóstico depende del número de ganglios afectados. Además, la vecindad de un ganglio afectado con el MRC aumenta el riesgo de recidiva local. La RM y la TCMD pueden evaluar las vías de drenaje linfático identificando adenopatías extramesorrectales, que necesitarán técnicas quirúrgicas ampliadas con extirpación de cadenas ilíacas internas. La diferenciación entre ganglio benigno y maligno se ha basado principalmente en el tamaño del diámetro del eje corto axial. Esta medida es limitada para la estimación de la N, ya que pueden existir micrometástasis en ganglios de tamaño normal. Las precisiones diagnósticas publicadas para las diferentes técnicas de imagen son variables (ecografía endoanal 61-80%; TC 56-79%; RM 5785%), no existiendo diferencias estadísticamente significativas entre ellas5. Brown et al6 obtienen una sensibilidad del 85% y una especificidad del 97% valorando la morfología y señal de los ganglios. Así, una morfología espiculada y una señal heterogénea serían un predictor de afectación más potente que el tamaño. Mejores resultados se han conseguido mediante la utilización de medios de contraste con partículas de hierro ultrapequeñas (ultrasmall particles of iron oxide, USPIO). Los ganglios infiltrados por tumor pierden la capacidad de captar el medio de contraste, por lo que no muestran pérdida de señal en secuencias de susceptibilidad, frente a los ganglios normales cuyos macrófagos acumularían dichas partículas. Lamentablemente, estos medios de contraste no han sido aprobados para el uso clínico. La tomografía por emisión de positrones (PET/TC) es capaz de detectar la presencia de adenopatías afectadas; no obstante, hay limitaciones por ser una técnica cara y de poca disponibilidad. También existe la limitación por la resolución espacial de la técnica en relación a las adenopatías de tamaño < 1 cm1. Cada vez hay más estudios dirigidos a evaluar la capacidad para caracterizar los ganglios de secuencias de RM potenciadas en difusión, tanto en la estadificación inicial como en respuesta al tratamiento, existiendo resultados dispares. Los ganglios normales son muy celulares y, por tanto, de alta señal en difusión, siendo fácilmente detectados en RM-difusión. Algunos estudios refieren una mayor restricción de la difusión en ganglios afectados que en ganglios normales, y otros que obtienen mejores resultados valorando conjuntamente el tamaño del ganglio y la relación entre el coeficiente de difusión aparente (ADC) del ganglio y el del tumor7. Un estudio reciente muestra que la RM potenciada en difusión es más sensible que la FDG-PET en la detección de metástasis ganglionares, basándose en criterios anatómicos (grupo de 3 o más ganglios independientemente del tamaño o, si eran menos de 3, uno de ellos mostraba eje corto > 1 cm)8. No obstante, son necesarios más estudios que valoren la capacidad de la imagen de difusión para discriminar ganglios malignos de benignos. La piedra angular del control locorregional del cáncer de recto es la cirugía. En concreto se ha mejorado la supervivencia libre de enfermedad y las recidivas locales con la implantación de la ETM, de tal forma que conseguir una ETM con MRC íntegro es el objetivo de todo el equipo multidisciplinario. Es muy importante conocer preoperatoriamente la extensión tumoral circunferencial y el estado del MRC; un MRC infiltrado o amenazado tiene una mayor probabilidad de recaída local, por lo que se recomienda neoadyuvancia. La ETM es una técnica quirúrgica consistente en la extirpación en bloque del recto, grasa perirrectal con ganglios y vasos siguiendo la FMR, con preservación la fascia parietal y de nervios esplácnicos. Debe realizarse por cirujanos especializados, ya que la ETM debe ser de alta calidad; un MRC completo puede convertirse en incompleto por una baja calidad técnica. También se ha mejorado la supervivencia y han disminuido las recidivas locales añadiendo tratamiento radioterápico (RT), radioquimioterápico (QRT) neoadyuvante/ adyuvante en pacientes con tumores localmente avanzados. El motivo de combinar QRT neoadyuvante con cirugía se basa en que el mecanismo del fallo de las 2 técnicas es diferente: la RQT rara vez falla en la periferia o márgenes del tumor, donde hay pocas células tumorales y están bien oxigenadas, y sí en el centro, por el gran número de células tumorales hipóxicas; lo contrario ocurre con la cirugía, donde el intento de preservar estructuras adyacentes puede limitar la extensión de la resección. Un gran número de ensayos clínicos muestra que la eficacia de los fármacos citotóxicos se ve aumentada, en gran medida, con la combinación de agentes quimioterápicos estándares con fármacos cuya diana son las moléculas que intervienen en el mecanismo de crecimiento y progresión del cáncer de recto. Entre ellos destacan las moléculas dirigidas al factor de crecimiento del endotelio vascular (VEGF) y a los receptores del factor de crecimiento epidérmico (EGFR). El EGFR juega un papel en factores críticos de la biología del cáncer colorrectal como son la proliferación, la apoptosis, la angiogénesis y la metastatización, influyendo en el crecimiento tumoral y la progresión. La sobreexpresión de EGFR se da en el 25-82% del cáncer colorrectal humano y se correlaciona con enfermedad más agresiva, aumento del riesgo de metástasis, estadio tumoral avanzado y afectación ganglionar. La vía del EGFR es la diana de nuevos tratamientos anti-EGFR9. La angiogénesis es un proceso dinámico esencial para el crecimiento tumoral. El VEGF juega un papel crucial en la proliferación, migración, invasión y diferenciación de las células endoteliales durante la angiogénesis a través de su unión a los receptores VEGFR-1 y VEGFR-2. Se ha encontrado sobreexpresión de VEGF en el 40-60% de los cánceres colorrectales y se asocia a una densidad vascular aumentada, enfermedad avanzada y pobre supervivencia. La clara correlación de la angiogénesis en el desarrollo tumoral ha abierto la vía al desarrollo de nuevos fármacos 0-3 01-37.indd 24 23/11/12 11:48:59 Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica que actúen frenándola; en estudios preclínicos, agentes que tienen como diana selectiva el VEGF y sus receptores han mostrado efectos antitumorales significativos en el cáncer colorrectal. El uso del anticuerpo monoclonal anti-VEGF bevacizumab ya está establecido en el tratamiento del cáncer de recto metastásico10. Esquema de tratamiento actual 1. Tumores T1-T2 N0 con MRC libre: cirugía; no necesitan QT/RT neoadyuvante. 2. Tumores T3 N0, T4 N0, Tx N1-2 e irresecables: QT/RT neoadyuvante. Se valorará esta indicación para T1-T2 N0 de recto inferior (0-5 del margen anal), dado el alto porcentaje de margen afectado y de recidivas locales. Tumores T4 y con MRC en riesgo o invadida serán sometidos a QRT con escalonamiento de dosis antes de la cirugía. Algunos autores abogan por la inclusión de los tumores T3ab dentro de los tumores de buen pronóstico, en los que una EMR completa sería suficiente. Incluso tumores T3ab y N1, pero sin factores pronósticos adversos, como el compromiso del MRC, ni invasión venosa dentro del grupo que es tratado sólo con cirugía, evitando sobretratamiento11. Sin embargo, otros ensayos indican QT/RT preoperatoria siempre que existan ganglios positivos12. Los esquemas de RT neoadyuvante son: esquema largo de RT preoperatoria con fraccionamiento convencional (180 cGy/fracción; 45-50 Gy total), con un intervalo de 5-10 semanas hasta la cirugía y un esquema corto de RT preoperatoria con hipofraccionamiento (500 cGy/fracción; 45-50Gy total), con intervalo de 7-10 días hasta la cirugía, que se utiliza en pacientes de riesgo de obstrucción o hemorragia o en los que no se pueda administrar QT preoperatoria. Es menos tóxico al no añadir QT. La QT concomitante con la RT se realiza con 5-FU en perfusión continua. Puede sustituirse por la capecitabina. Se administrará QT adyuvante incluso en pT1-2. La administración de QT adyuvante en remisiones completas patológicas es controvertida, debiéndose valorar el estadio clínico inicial. La aplicación de RT preoperatoria seguida de cirugía frente a la cirugía sola ha demostrado una disminución en la tasa de recidiva local (el 11 frente al 27%) y una mejoría de la supervivencia. Asimismo, la QRT neoadyuvante es superior a la RT sola, tanto de ciclo largo como de ciclo corto, en términos de respuestas completas patológicas (el 11 frente al 3%) y recidiva local (el 8 frente al 16%), y a la QRT postoperatoria en términos de recidivas locales, preservación de esfínteres y menor toxicidad13. Principios de cirugía – Resección transanal. La escisión local mediante cirugía transanal está limitada para tumores T1-T2 N0, situados 0-3 01-37.indd 25 25 en recto inferior hasta 8 cm. Otros datos que favorecen la resección transanal son un tamaño < 3 cm, naturaleza exofítica y que no sean fijos. La microcirugía endoscópica transanal es una técnica menos agresiva que la resección transabdominal, que permite la resección de tumores en estadios iniciales T1N0, situados hasta 16 cm del margen anal por vía transanal, pudiendo realizar resecciones transmurales. No permite la extirpación de los ganglios. Si el resultado patológico son márgenes afectados o el tumor es pobremente diferenciado debe procederse a ETM. – Resección transabdominal (amputación abdominoperineal, resección baja anterior, anastomosis coloanal). En tumores de recto superior se indica escisión parcial del mesorrecto al menos 5 cm por debajo del tumor, que asegura un margen inferior libre. En tumores de recto medio se indicará ETM con conservación del complejo esfinteriano si la distancia del polo inferior del tumor al esfínter es de 1 cm, ya que la progresión tumoral ocurre principalmente en sentido radial y no longitudinal. Se practica escisión abdominoperineal con ETM o escisión abdominoperineal extraelevadora/extraesfinteriana en tumores de recto inferior, dado su mayor riesgo de recidivas locales. – Escisión en bloque para tumores T4, con extirpación de órganos afectados. – Linfadenectomía pélvica ampliada si se identifican adenopatías por fuera de la fascia en la estadificación preoperatoria. Características histopatológicas de los tumores sometidos a neoadyuvancia En respuesta a la QRT preoperatoria, las células tumorales son sustituidas por tejido fibrótico o fibroinflamatorio. En el análisis patológico de los tumores tratados puede encontrarse: a) fibrosis marcada con o sin sustitución de células tumorales por células inflamatorias, y b) ausencia de necrosis tumoral con presencia de lagos de mucina en la estroma. La presencia de mucina se considera un modo de respuesta al tratamiento y la presencia de mucina acelular indica ausencia de tumor residual. La diferenciación mucinosa no implica mal pronóstico, a diferencia de los tumores mucinosos primarios. El estadio histopatológico postratamiento (ypT) se establece en relación con el núcleo de células patológicas situadas más profundamente en la pared rectal o en el mesorrecto. El grado de regresión tumoral obtenido impacta en el pronóstico de estos pacientes, ya que su supervivencia se acerca al estadio patológico y no al clínico14. Los ganglios se categorizan como positivos o negativos y la persistencia de adenopatías positivas tras QRT neoadyuvante es el principal factor de mal pronóstico. Para considerar N0 deben evaluarse 12 ganglios, lo cual no suele ser posible en especímenes tratados con neoadyuvancia, por lo que debe sobreestadificarse como Nx. 23/11/12 11:48:59 26 Valoración por imagen de la respuesta al tratamiento neoadyuvante en tumores avanzados Los abordajes quirúrgicos actuales no están exentos de morbimortalidad, por lo que algunos grupos de investigación abogan por tratamientos menos agresivos en los pacientes que tras la QRT muestran enfermedad limitada al recto (T0-T2N0) y plantean si la cirugía podría evitarse en pacientes que logren la respuesta completa. Para ello se necesita monitorizar de forma no invasiva la respuesta al tratamiento, tanto del tumor como de los ganglios afectados14. Además, la valoración precoz de la respuesta ayudaría a personalizar el tratamiento y, de esta forma, los pacientes respondedores podrían continuar el mismo régimen terapéutico mientras que en pacientes no respondedores debería interrumpirse un tratamiento inefectivo y potencialmente tóxico, o deberían ser sometidos a tratamientos más agresivos. Valoración de respuesta del tamaño y volumen tumoral. La valoración de la respuesta al tratamiento QRT neoadyuvante se viene realizando habitualmente mediante aplicación de aproximaciones morfológicas de tamaño tumoral. En 1979, la Organización Mundial de la Salud estableció criterios de respuesta que se basaban en las medidas de 2 diámetros en plano axial. Para estandarizar y unificar criterios se introdujeron en el año 2000 los criterios RECIST (Response Evaluation Criteria in Solid Tumor), cuya última revisión ha sido publicada en 2009, que evalúa la respuesta basándose en la disminución del eje máximo en plano axial. En el primero de los casos se considera que hay respuesta tumoral si existe una reducción del 50% en el producto de las 2 dimensiones. En los criterios RECIST se considera respuesta una disminución del 30% del diámetro máximo. Estos criterios se establecieron para disponer de un lenguaje común que permitiera comparar resultados de diferentes ensayos clínicos y su uso se ha generalizado en la práctica clínica de la imagen oncológica. Los criterios RECIST tienen limitaciones: tumores que no pueden ser medidos, masas que persisten después del tratamiento y una baja reproducibilidad. Para superar estas limitaciones se introdujeron, gracias a la llegada de la imagen digital y nuevos software, el cálculo del volumen tumoral. Se trazan los contornos del tumor en un plano axial oblicuo perpendicular al tumor y el volumen se calcula sumando las áreas trazadas multiplicadas por el grosor de corte. Se considera respuesta parcial la disminución de volumen de un 65%. Esta aproximación es mejor en el cáncer de recto al ser tumores irregulares. En el cáncer de recto localmente avanzado, Barbaro et al1 estiman que una reducción de un 70% o más del volumen tumoral tras la QRT tiene un alto valor predictivo positivo pero un bajo valor predictivo negativo para distinguir entre respondedores y no respondedores. Valoración de respuesta basada en cambios morfológicos. La resolución en contraste de la RM permite inferir los cambios 0-3 01-37.indd 26 La imagen funcional en oncología descritos anteriormente en el examen histopatológico. El tumor residual mantiene una intensidad de señal en T2 estable con respecto al estudio inicial; se muestra hiperintenso con relación al músculo, pero de señal inferior a la grasa. Tras la neoadyuvancia, la mayoría de los tumores disminuye de tamaño y desarrolla fibrosis, lo que se traduce en una disminución de señal en T2 con respecto al estudio previo a la neoadyuvancia. También pueden aparecer cambios mucinosos, que se traducen en alta señal en T2, superior a la grasa (fig. 3). Se considera estadio yT0-T2 en la RM de reestadificación cuando no se identifica el tumor o se aprecia un engrosamiento mural hipointenso en T2 por fibrosis. Esta fibrosis oblitera la estructura laminar de la pared rectal, por lo que no es posible diferenciar un T0 de un T2; se considera enfermedad limitada a la pared y pueden aparecer espiculaciones finas hipointensas que se extienden a la grasa perirrectal. Se estima un estadio yT3 cuando se aprecia crecimiento nodular en la grasa mesorrectal de señal hiperintensa en T2 con respecto al músculo y un estadio yT4 cuando se identifica crecimiento nodular de la pared, hiperintenso con respecto al músculo que entra e invade estructuras o vísceras vecinas. La RM es la mejor técnica para la revaluación del cáncer de recto, aunque no puede descartar la presencia de células tumorales dentro de la fibrosis ni diferenciar los estadios yT0, yT1 e yT2. Tiende a sobreestadificar las lesiones con cambios inflamatorios y diferenciación mucinosa, las cuales presentan mayor señal similar a la del tumor original. Se consigue una precisión razonable cuando se trata de diferenciar entre tumores yT0-T2 y tumores yT3 y se combinan criterios volumétricos con morfológicos1. Las variantes histopatológicas del cáncer de recto están asociadas a cursos clínicos diferentes, y casi siempre a un peor pronóstico para un mismo estadio. El adenocarcinoma mucinoso se caracteriza por exceso de mucina y es más agresivo que el adenocarcinoma ordinario. Afecta a pacientes más jóvenes y se asocia más frecuentemente a peor respuesta a la QRT. La RM puede sugerir la estirpe mucinosa, ya que el exceso de mucina hace a estos tumores más hiperintensos en T2. Tras la QRT mantienen alta señal en T2, siendo difícil diferenciar entre persistencia tumoral y mucina acelular. Si se sospecha adenocarcinoma mucinoso en la RM de estadificación, podría valorarse en primer lugar el manejo quirúrgico dada la posibilidad de pobre respuesta a la QRT neoadyuvante. La QRT neoadyuvante da lugar a una disminución de tamaño y de número de ganglios mesorrectales. Estudios comparativos de RM de alta resolución pre y posneoadyuvancia permiten comparar número, tamaño, morfología e intensidad de señal de los ganglios. A diferencia de la situación previa a la QRT, el tamaño < 5 mm y el número de ganglios tienen sensibilidad y especificidad del 80% para predecir respuesta15. Valoración de respuesta mediante técnicas funcionales. Entre las características biológicas más relevantes del cáncer de recto que pueden evaluarse con la imagen funcional se 23/11/12 11:48:59 Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica A 27 B Figura 3. Valoración de respuesta anatómica. Tumor de recto medio ulcerado (flechas) A) Resonancia magnética (RM) pre-QRT cT3b. B) RM post-QRT; engrosamiento hipointenso en T2 limitado a la pared (yT0-T2). encuentran la proliferación celular excesiva, el incremento de actividad metabólica y la angiogénesis. Alguna de las técnicas de imagen funcional de que se dispone está clínicamente avalada en el manejo de pacientes con carcinoma colorrectal, como la PET. En otras, como la imagen potenciada en difusión, la TC-perfusión y la RM-dinámica está cada vez más establecida su utilidad. Otras, como la imagen de la hipoxia (BOLD) y la imagen metabólica del cáncer de recto (espectroscopia), están en fase experimental (tabla 2). A. Secuencias de RM potenciadas en difusión. La RM-difusión es una modalidad de imagen funcional sensible al movimiento aleatorio o browniano de las moléculas de agua presentes en los tejidos. La RMI-difusión es una herramienta clínica cada vez más consolidada en oncología. Sus mayores ventajas consisten en que carecen de radiaciones ionizantes, no necesitan administración de isótopos ni de contrastes, el tiempo de adquisición de la secuencia es razonablemente corto y puede repetirse y cuantificarse16. La sensibilidad a la difusión varía cambiando el parámetro conocido como valor b. La adquisición de secuencias de difusión con varios valores b permite la cuantificación de la difusión mediante el cálculo del ADC en mm2/s. Pueden obtenerse mapas paramétricos que representan los valores de ADC en cada píxel, y permiten analizar la distribución de este parámetro dentro de una lesión así como compararlo antes y después del tratamiento. Se considera un coeficiente aparente ya que no diferencia el movimiento microscópico del agua (difusión tisular) 0-3 01-37.indd 27 de los efectos de la perfusión de las moléculas de agua dentro de los capilares incluidos en el mismo voxel16. Se hace necesario estandarizar los protocolos de imagen y los métodos de análisis de datos en la RM-difusión, ya que son los principales inconvenientes que limitan su uso de manera más generalizada. Esto incluye el trazado de la región de interés (ROI) para el cálculo del ADC que debe incluir toda la lesión, evitando áreas de necrosis y artefactos de susceptibilidad. El uso del ADC medio es una aproximación simplista dada la heterogeneidad de los tumores rectales y probablemente sea mejor utilizar el histograma de valores de ROI. Además, se están evaluando softwares complejos conocidos como mapas funcionales de la difusión, que reflejan cambios en la difusión cuantificada y que son muy útiles en el seguimiento postratamiento17. Una de las características de la mayoría de los tumores es la alta densidad celular en un entorno intersticial de tamaño variable. La RM-difusión es capaz de determinar de forma indirecta el grado de celularidad de una lesión, ya que cuanto más celular sea una lesión mayor será la restricción del agua libre en el espacio intersticial. Los tumores malignos generalmente son más celulares que los tumores benignos/tejidos sanos, por lo que el movimiento del agua está más restringido y muestran bajo ADC con respecto a la mucosa normal. En lo que respecta al cáncer colorrectal, la RM-difusión es útil para su detección, para delimitar el volumen tumoral, para valorar la respuesta al tratamiento y para la estadificación a distancia (fig. 4). 23/11/12 11:48:59 La imagen funcional en oncología 28 Tabla 2 − Técnicas de imagen funcional en el cáncer de recto Técnica imagen funcional Propiedades biológicas Parámetros cuantitativos en las que se basa o biomarcadores la imagen Datos fisiopatológicos representados Perfusión TC Captación de contraste Flujo sanguíneo, volumen por los tejidos, que depende sanguíneo, tiempo de de la perfusión de la tránsito medio densidad de vasos y de la permeabilidad de dichos vasos Densidad vascular, permeabilidad de los vasos, presión de perfusión, grado tumoral RM dinámica (RM-D) Captación tisular de contraste Área bajo la curva de gadolinio, constantes de transferencia (Ktrans, Kep), fracción de espacio de fuga (Ve), volumen de plasma (Vp) Difusión (RM-dif) Movimiento browniano Coeficiente de difusión del agua aparente (ADC) Densidad vascular, permeabilidad de los vasos Densidad celular, integridad de las membranas, tortuosidad del espacio extracelular, formación de glándulas, necrosis RM: resonancia magnética; TC: tomografía computarizada. Figura 4. MPR coronal de DWIBS de 2 estaciones, b = 1.000: M1 hepática (flecha grande). Pequeña tumoración en recto medio que restringe la difusión (flecha pequeña). 0-3 01-37.indd 28 Aunque no está bien establecido el valor b óptimo para el cáncer de recto, se acepta un valor b de 1.000 s/mm2; los valores más bajos son menos específicos dado que la mucosa rectal normal tiene una alta señal intrínseca en difusión, por lo que con valores b altos la hiperseñal de la mucosa normal disminuye. Hay otras características microscópicas que afectan la difusión del agua, incluyendo densidad celular, ratio núcleo-citoplasma, distribución de tamaños celulares dentro del tejido, tortuosidad del espacio intersticial, integridad de las membranas celulares, formación glandular y perfusión tisular. El ADC también se relaciona con el índice de proliferación tisular, el grado tumoral, la presencia de necrosis y la apoptosis celular; esta última se relaciona a su vez con la respuesta al tratamiento16,17. La RM-difusión en el cáncer de recto es un biomarcador precoz de respuesta a la QRT; el ADC aumenta a los 3-7 días del inicio del tratamiento en respuesta a la muerte celular y alteraciones vasculares antes de que haya cambios de tamaño. En los no respondedores, el ADC no se modificará significativamente. Posteriormente, los valores de ADC se reequilibran y vuelven a bajar como reflejo de la aparición de fibrosis (fig. 5). El edema y la inflamación peritumoral que pueden aparecer postratamiento y que son causa de falsos positivos en la PET pueden ser correctamente evaluados con difusión, ya que daría lugar a un aumento del ADC1,18. De Vries et al19 muestran que el ADC pretratamiento se correlaciona con respuesta a la QRT. Los respondedores tienen más bajo ADC que los no respondedores. Los altos valores de ADC en los no respondedores pueden traducir 23/11/12 11:49:00 Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica A D B E 29 C F Figura 5. Adenocarcinoma de recto. A) T2-TSE. B) Resonancia magnética (RM)-difusión (b = 800). C) Coeficiente de difusión aparente (ADC) pre-QRT: se estima un estadio cT4a N1 M0. D) T2-TSE. E) RM-difusión (b = 800). F) ADC post-QRT: se observa una disminución de señal en T2 y ADC en el estudio post-QRT limitada a la pared sugestiva de fibrosis. El estadio posquirúrgico fue ypT2. Caso cedido por el Dr. García Figueiras. Complexo Hospitalario Universitario de Santiago de Compostela. necrosis tumoral que explicaría la resistencia al tratamiento por la hipoxia en los tejidos necróticos. La RM-difusión también se ha demostrado útil en la reestadificación del cáncer de recto después de la neoadyuvancia. Es difícil distinguir fibrosis postratamiento de tumor residual en estudios morfológicos de revaluación, incluyendo estudios con contraste, ya que la fibrosis precoz puede realzar de forma similar al cáncer recurrente (fig. 6). El ADC post-QRT del cáncer de recto puede diferenciar respondedores de no respondedores. Kim et al20 han propuesto un valor de corte entre 1,2 y 1,3 × 10–3 s/ mm2, con valores predictivos negativos cercanos al 100%. Sin embargo, esta serie también ha mostrado un valor predictivo positivo bajo, de aproximadamente el 50-60%, probablemente relacionado con la limitación de la RMdifusión para diferenciar respuesta completa de respuesta 0-3 01-37.indd 29 casi completa, y en la diferenciación entre áreas de mucina inactiva y tumor residual. La RM-difusión ha mostrado su papel en la monitorización de respuesta a los fármacos antiangiogénicos en varios órganos y tipos de tumores; la respuesta positiva se traduce en una disminución rápida pero transitoria de los valores de ADC, que se explica por la disminución de flujo, edema celular y disminución del espacio extracelular. En el caso de los tumores GIST tratados con imatinib, que produce una transformación quística del tumor en respuesta al tratamiento, el ADC aumenta17 (fig. 7). La RM-difusión permite la estadificación a distancia al mismo tiempo que la local, así como la monitorización de respuesta local y a distancia mediante estudios RMdifusión de cuerpo entero con supresión del fondo tisular (difusion-weighted whole-body imaging with background body 23/11/12 11:49:00 30 A B Figura 6. A y B) T2-TSE y resonancia magnética-difusión (b = 1.000). Carcinoma de recto posneoadyuvancia. La difusión identifica un resto tumoral que pasa desapercibido en la secuencia T2 (flecha). signal supresión, DWIBS); se adquieren de 2 a 4 estaciones consecutivas con un valor b alto (entre 800 y 1.000 s/mm2) y con supresión grasa STIR, que suprime el fondo tisular. Habitualmente se hace un análisis cualitativo mediante el análisis visual de los cambios de intensidad de señal asociados a los cambios de carga tumoral. Puede considerarse un tratamiento exitoso cuando disminuye la intensidad de señal en b-altas; con progresión aparecen nuevas áreas de alteración de la señal, cambios en la extensión, simetría e intensidad de señal. También permite el cálculo del ADC si se obtiene una b baja (entre 0 y 50 s/mm2). 0-3 01-37.indd 30 La imagen funcional en oncología El cálculo del ADC en los tumores está muy influenciado por fenómenos de perfusión. Los tumores malignos están más perfundidos que los benignos, por lo que la perfusión intravascular influirá más en el ADC medio. Esto puede manejarse desde una aproximación monoexponencial del descenso de señal. Se puede calcular el ADC rápido usando sólo valores b bajos (0-100 s/mm2), que está dominado por el componente de la perfusión de la difusión total, y puede calcularse el ADC lento usando los valores b altos (> 100 s/mm2), en los que se habrá minimizado el efecto de la perfusión, por lo que domina la difusión del agua. También puede calcular la fracción de perfusión (Fp) y la difusión libre de perfusión (D) aplicando el modelo biexponencial IVIM (intravoxel incoherent motion). El descenso rápido de la señal con valores b bajos depende de la perfusión microvascular y permite el cálculo aislado de la Fp y de la D. Generalmente, el ADC lento es más alto que la D, siendo esta última una medida más real de la difusión. La fracción de perfusión permite evaluar la agresividad tumoral (fig. 8)21. Aunque la RM-difusión ha demostrado ser una técnica de imagen prometedora para la estadificación ganglionar preneoadyuvancia, en el momento actual sólo hay un estudio publicado sobre la eficacia de la RM-difusión en la evaluación de respuesta ganglionar a QRT22; encuentran diferencias pero no significativas entre el ADC de ganglios normales y patológicos. Estos últimos muestran ADC más alto, que atribuyen a necrosis por RT. La RM-difusión tampoco mejora la precisión diagnóstica de la valoración anatómica con secuencias T2. No obstante, la ausencia de ganglios en secuencias de difusión confirma estadio ganglionar N0 (fig. 9). B. Perfusión: TC-perfusión y RM. La génesis tumoral es un proceso diverso que afecta a un amplio espectro de células tumorales y de alteraciones genéticas. Sin embargo, todas las neoplasias tienen en común la incapacidad para formar vasos. Esto hace que a partir de que un tumor crece más allá de 1-2 mm3 necesite del desarrollo de nuevos vasos para su progresión. El desarrollo de la vascularización tumoral o angiogénesis depende de la formación de vasos sanguíneos por el huésped. Este proceso es dirigido por los efectos mitogénicos de un grupo de mediadores locales elaborados por las células tumorales, siendo el más importante el VEFG. Los nuevos vasos son anómalos, frágiles y tortuosos, con múltiples cortocircuitos arteriovenosos, permeabilidad aumentada y un flujo inestable e intermitente. Presentan además una distribución anárquica dentro del tumor, con áreas de alta y baja densidad de vasos. La densidad de microvasos es un criterio histológico que representa los vasos sanguíneos tumorales, y se considera el patrón oro para la cuantificación y monitorización de la angiogénesis. Se relaciona con el grado y estadio del tumor, y es otro factor pronóstico para la supervivencia del paciente con cáncer colorrectal. Sin embargo, es un criterio estático que no aporta información sobre el funcionalismo ni la heterogeneidad de los neovasos y que se obtiene mediante biopsia. 23/11/12 11:49:01 Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica A B C D E F 31 Figura 7. Tumor GIST en tratamiento con imatinib; A y D) Octubre de 2008 (coeficiente de difusión aparente [ADC] 0,6). B y E) Febrero de 2009 (ADC 0,8). C y F) Julio de 2009 (ADC 1,6). Hay una buena respuesta a pesar del aumento de tamaño tumoral, ya que el ADC aumenta en el primer control. En el control posterior aumenta el ADC y disminuye el volumen tumoral. 0-3 01-37.indd 31 23/11/12 11:49:01 La imagen funcional en oncología 32 A C D B D 4×104 + ++ 3×104 + 2×104 + + + 1×104 0 0 500 1.000 b factor (a/mm2) 1.500 2.000 Figura 8. Comparación entre el cálculo del coeficiente de difusión aparente (ADC) y cálculo de fracción de difusión (D) con IVIM. A) Cálculo del ADC con todos los valores b. B) Cálculo del ADC sólo con valores b de 100-2.000. C) Mapa paramétrico de difusividad (D). D) Curva caída-caída de la señal en el tumor rectal según modelo bicompartimental IVIM. El ADC lento es más bajo (0,60 mm2/s) que el ADC global (0,67 mm2/s), lo cual puede estar motivado por la perfusión. Por otra parte, el ADC lento es más alto que la D (0,34 mm2/s). El valor D es más real, ya que no se encuentra influenciado por la perfusión. Por otra parte, el tumor tiene una Fp del 30%, que indica alta vascularización. La angiogénesis tumoral se traduce en un aumento de la permeabilidad, de la presión en el intersticio y de la perfusión tumoral, que pueden ser evaluados con distintas modalidades de imagen funcional de forma no invasiva. Las principales son la TC-perfusión y la RM. Esta última puede evaluar la neoangiogénesis sin el uso de medios de contraste, mediante ASL (arterial spin labelling) o IVIM, y también mediante la RM-dinámica con contrate. 0-3 01-37.indd 32 Además permiten evaluar el efecto que tienen las distintas terapias sobre el funcionalismo vascular, siendo ésta una de las principales indicaciones de estas modalidades de imagen en la actualidad23. – TC-perfusión. Se basa en el cambio temporal de la atenuación de los tejidos tras la administración de contraste yodado intravenoso. El realce de los tejidos depende de la concentración tisular de yodo y refleja de forma indi- 23/11/12 11:49:02 Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica recta la vascularización tisular y la fisiología vascular. Se pueden distinguir 2 fases en la TC-perfusión. Una primera, que dura entre 40 y 60 s, en la que el realce se debe a la distribución del contraste en el espacio intravascular y a su paso rápido al espacio extravascular extracelular y que requiere alta resolución temporal (una adquisición por segundo). Y una segunda en la que el realce depende de la distribución del agente de contraste entre los compartimientos intra y extracelular y en la que la adquisición es más espaciada y dura entre 2 y 5 min24. Aplicando un modelo farmacocinético es posible obtener distintos parámetros vasculares cuantitativos, que varían según el equipo de que se disponga, como son el flujo sanguíneo (se correlaciona con la densidad vascular), el volumen sanguíneo (se correlaciona con la permeabilidad), el tiempo de tránsito medio (se correlaciona con la presión de perfusión) y la superficie de permeabilidad (se correlaciona con el grado tumoral). También se obtienen parámetros cualitativos como la morfología de la curva densidad/tiempo y pico de realce. La principal ventaja de la TC-perfusión sobre la RMdinámica es la relación directa entre densidad tumoral y concentración tisular de yodo. Esta relación directa hace que la aplicación de modelos matemáticos sea más simple y directa que en RM. Como contrapartida emplea radiaciones ionizantes y no es posible una gran cobertura anatómica (4 cm con 64 detectores), aunque estas limitaciones se han superado en los equipos de energía-dual y de mayor número de detectores25. La TC-perfusión puede reflejar la angiogénesis en el carcinoma colorrectal, por lo que puede ser usada como biomarcador subrogado. Algunos estudios han correlacionado parámetros de perfusión con densidad de microvasos en el cáncer de recto24,25. La densidad de microvasos está aumentada en el cáncer de recto comparada con la mucosa normal, lo cual se traduce en un flujo sanguíneo elevado y un tiempo de tránsito medio más corto. De igual modo, la TC-perfusión puede distinguir cáncer de recto de enfermedad diverticular por los valores de perfusión más elevados del primero24. Puede ser un biomarcador predictivo de respuesta aunque con resultados contradictorios: Sahani26 encontró en su estudio inicial de 15 pacientes tumores rectales con alto flujo y tiempo de tránsito medio más corto que respondían peor a la QRT, atribuyéndolo a la presencia de cortocircuitos intratumorales de baja resistencia. Por otra parte, Bellomi et al27, en su serie de 17 pacientes con el mismo estadio tumoral, encontraron que los tumores rectales con flujo sanguíneo y volumen sanguíneo altos parecían tener mejor respuesta a la QRT neoadyuvante, atribuyéndolo a un mejor acceso a la QT y mayor sensibilidad a la RT al estar mejor oxigenados. Se pone de manifiesto la utilidad de la técnica, aunque se necesitan estudios más extensos para confirmar los resultados. La valoración de la respuesta al tratamiento del cáncer de recto se basa en la disminución de los parámetros de 0-3 01-37.indd 33 33 A B Figura 9. A) Tumor T3a de recto inferior post-QRT (no incluido). B) Se identifica una adenopatía hipogástrica izquierda (flecha), inespecífica en T2 y de alta señal en b = 1.000 (coeficiente de difusión aparente 0,6 mm2/s) y que imposibilita la estimación de estadio N0 por resonancia. perfusión tumoral en respuesta a la QRT y a los fármacos antiangiogénicos, que además se produce de forma precoz durante el curso del tratamiento. Sahani26 encontró un descenso del flujo sanguíneo y elevación de tiempo de tránsito medio después de QRT en cáncer de recto. Bellomi27 encontró un descenso del flujo sanguíneo, del volumen sanguíneo y de la superficie de permeabilidad; Willet28 encontró un descenso del flujo sanguíneo y del 23/11/12 11:49:02 La imagen funcional en oncología 34 A B C D E F Figura 10. Tomografía computarizada-perfusión. Evaluación de respuesta al tratamiento; A-C) Pre-QRT: imagen base (A); mapa paramétrico de flujo (89 ml/100 ml/min) (B), y mapa paramétrico de volumen sanguíneo (7,3 ml/100 ml) (C). D-F) Post-QRT: imagen base (D); mapa paramétrico de flujo (32 ml/100 ml/min) (E), y mapa paramétrico de volumen (3,1 ml/100 ml) (F). Se identifica una disminución de tamaño tumoral así como de los parámetros de perfusión en respuesta al tratamiento QRT neoadyuvante. Caso cedido por el Dr. García Figueiras. Complexo Hospitalario Universitario de Santiago de Compostela. volumen sanguíneo como respuesta a terapias antiangiogénicas (fig. 10). – RM-dinámica. La aparición de contrastes de bajo peso molecular, que difunden libremente desde los vasos al espacio extracelular extravascular, y el desarrollo de secuencias de alta resolución temporal han permitido el análisis de la perfusión tumoral con RM. Tras la administración de un bolo de medio de contraste se produce el paso del mismo a través de la red capilar (primer paso) y de un modo rápido difunde al espacio extravascular, provocando un acortamiento del tiempo de relajación T1 de los tejidos. En esta segunda fase, el incremento de señal se debe a la presencia de contraste, tanto en el espacio vascular como en el intersticial. Posteriormente, según disminuye la concentración plasmática del medio de contraste por excreción renal, se produce la vuelta del contraste al espacio vascular hasta que es eliminado. Los principales determinantes de la captación de contraste por el tejido tumoral son el flujo sanguíneo, la densidad de microvasos, la permeabilidad del vaso y la fracción 0-3 01-37.indd 34 de volumen del espacio extravascular extracelular. La estimación individualizada de estos factores depende del empleo de secuencias de alta resolución temporal que permiten la caracterización de los patrones dinámicos de captación de gadolinio por el tumor. Los principales parámetros que describen este proceso dinámico son la constante de transferencia entre el plasma y el espacio extravascular extracelular (Ktrans), el volumen fraccional del espacio extravascular extracelular (Ve), ratio de extracción del contraste desde el espacio extravascular extracelular hacia el plasma (Kep) y volumen de espacio vascular (Vp). Se obtienen aplicando un modelo farmacocinético bicompartimental a los datos de realce dinámico, y aportan información cuantitativa sobre características anatómicas y funcionales de la microvasculatura tumoral, permitiendo mejorar la detección y caracterización tumoral así como valorar su pronóstico y la respuesta a los tratamientos QRT y antiangiogénico. En la evaluación del cáncer de recto está mucho más extendida en la práctica clínica una aproximación más 23/11/12 11:49:04 Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica simplista, que es la aplicación de un modelo monocompartimental. Éste utiliza el método de perfusión T1, que está basado en los efectos del contraste sobre la relajación T1 durante la adquisición dinámica de los datos. Se obtienen curvas de señal/tiempo que pueden analizarse de forma cualitativa mediante la observación del perfil de la curva; de forma semicuantitativa evaluando cambios de la intensidad de señal, o de forma cuantitativa. Las medidas semicuantitativas como la intensidad de señal relativa, la pendiente de la curva intensidad/tiempo (refleja la velocidad del realce) o el área bajo la curva intensidad de señal/tiempo son simples de obtener, pero tienen limitaciones: no reflejan de forma precisa la concentración de contraste en los tejidos de interés, a diferencia de la TC-perfusión, y son influenciados por los parámetros del tomógrafo. Además, carecen de explicación fisiológica clara. Como resultado, estos métodos muestran una gran variabilidad entre las distintas máquinas y entre exploraciones individuales, que dificulta los estudios comparativos, y son menos sensibles y reproducibles que las medidas farmacocinéticas. A pesar de las limitaciones, estos métodos son valiosos, sobre todo en la caracterización tumoral. La obtención de parámetros cuantitativos es compleja puesto que en RM no hay relación lineal entre la concentración de contraste y la señal, como en la TC. Lo más sencillo es la cuantificación de la cinética de la acumulación del medio de contraste mediante la integración de la concentración de contraste observado en un tejido de interés a lo largo del tiempo, el área bajo la curva inicial (IAUC). IAUC es fácil de calcular y reproducible, y ha demostrado parámetros de permeabilidad similares a los obtenidos con otros modelos matemáticos más complejos. Una desventaja es que la IAUC es un parámetro que representa múltiples procesos fisiológicos, incluyendo flujo sanguíneo, volumen sanguíneo, permeabilidad endotelial y volumen del espacio extravascular extracelular. La cuantificación basada en la aplicación de modelos farmacocinéticos permite la conversión de los valores de intensidad de señal a datos de concentración, ajustando las curvas a un modelo bicompartimental (hay 2 compartimientos, el vascular y el extravascular-extracelular) y obteniendo curvas concentración/tiempo. Para ello es necesario cuantificar la concentración de contraste en el plasma a lo largo del tiempo, lo que se conoce como función de entrada arterial, que se obtiene a partir de un vaso sanguíneo incluido dentro del campo de visión, y que permite la estimación de los cambios de concentración de contraste en los vasos tumorales. El Ktrans es el parámetro de interés en la mayoría de estudios y está determinado por el flujo por unidad de volumen, la permeabilidad y el área de superficie de los capilares; traduce una combinación variable de flujo y permeabilidad. En vasos donde la permeabilidad es alta, como en los tumorales, la perfusión determina la distribución del contrate y el Ktrans se aproxima al flujo sanguíneo por unidad de volumen. En situaciones de 0-3 01-37.indd 35 35 baja permeabilidad con una menor fracción de extracción durante el primer paso, como ocurre típicamente en el tratamiento con QT, de forma tardía después de RT o en lesiones fibróticas, la permeabilidad se convierte en el factor determinante del Ktrans, que se aproxima al producto de la permeabilidad y área de superficie29. Tumores rectales con mayor Ktrans al diagnóstico parecen responder mejor a la QRT que aquellos con valores bajos (fig. 11). Después de la QRT el Ktrans generalmente se reduce, mientras que valores elevados persistentemente indican enfermedad residual activa29. La angiogénesis tumoral puede analizarse, además de con contrastes de bajo peso molecular de distribución tumoral inespecífica, utilizando contrastes basados en macromoléculas con vida media intravascular mucho más larga. Con estos contrastes los valores de Ktrans son proporcionales a la permeabilidad capilar y relativamente insensibles al flujo sanguíneo. La TC-perfusión proporciona información principalmente sobre el primer paso del bolo de contraste aportando datos sobre la perfusión absoluta y el volumen sanguíneo, mientras que la RM-dinámica estudia el volumen tumoral durante más tiempo, permitiendo por ello establecer información que refleja mejor la perfusión de microvasos, la permeabilidad y el espacio extracelular de fuga30. Nuevas aproximaciones del análisis de la angiogénesis con RM como el ASL o los parámetros de perfusión derivados del análisis de la difusión con el modelo IVIM, que ya han sido probadas con éxito en otros tumores como el glioblastoma o el carcinoma de células renales, abren nuevas opciones en el estudio de las propiedades farmacocinéticas del cáncer de recto en un futuro cercano. Además, el estudio de la hipoxia tumoral con técnicas BOLD es una alternativa potencialmente atractiva para identificar las zonas hipóxicas intratumorales, que están íntimamente relacionadas con la resistencia a la QRT. Conclusiones El manejo de los pacientes con cáncer de recto ha dado un giro cualitativo en la última década debido a la evaluación multidisciplinar y personalizada, la implantación de la ECM como técnica quirúrgica, la neoadyuvancia QRT y la aparición de nuevos tratamientos antiangiogénicos. Pero el cáncer de recto es una entidad muy heterogénea en cuanto a pronóstico y respuesta al tratamiento que depende, además del estadio local, ganglionar y sistémico, de la propia histología y biología tumorales. El papel del radiólogo es esencial en la toma de decisiones y en la monitorización de los pacientes valorando los cambios en cuanto a tamaño y volumen mediante medidas cada vez más reproducibles. Además de la evaluación anatómica, la imagen funcional posibilita valorar la respuesta al tratamiento de los tumores rectales evaluando cambios en la propia biología tumoral mediante el análisis y cuantifica- 23/11/12 11:49:04 La imagen funcional en oncología 36 A B C Figura 11. A-C) T2-TSE axial. Voluminoso tumor que invade la fascia mesorrectal (T). Muestra una gran vascularización en los estudios de resonancia magnética-dinámica, que puede ser valorado mediante un análisis semicuantitativo (realce relativo máximo [B]) o mediante análisis bicompartimental (K-trans, valor medio 9,5 [C]). ción de diferentes parámetros o biomarcadores tumorales. Esto hará posible detectar precozmente a los pacientes no respondedores y también someter a tratamientos menos agresivos a los que logren una respuesta completa o una disminución de estadio. 0-3 01-37.indd 36 Bibliografía 1. Barbaro B, Vitale R, Leccisotti L, Vecchio FM, Santoro L, Valentini V, et al. Restaging locally advanced rectal cancer with MR imaging after chemoradiation therapy. Radiographics. 2010:30:699-716. 2. Ayuso JR, Pagés M, Ayuso C. Estadificación del cáncer de recto. Radiología. 2010;52:18-29. 3. MERCURY Study Group. Diagnostic accuracy of preoperative magnetic resonance imaging in predicting curative resection of rectal cancer: Prospective observacional study. BMJ. 2006;333:779-84. 4. Beets-Tan RG, Beets GL. Rectal cancer: review with emphasis on MR imaging. Radiology. 2004;232:335-46. 5. Bipat S, Glas AF, Slors FJM, Zwinderman AH, Bossuyt PMM, Stoker J. Rectal cancer: local staging and assesment of lymph node involvement with endoluminal US, CT, and MR imaging-a meta-analisis. Radiology. 2004;232:773-83. 6 . Brown G, Richards CJ, Bourne MW, Newcombe RG, Radcliffe AG, Dallimore NS, et al. Morphologic predictors limph node status in rectal cancer with use of high-spatial-resolution MR imaging with histopathologic comparision. Radiology. 2003;227:371-7. 7. Yasui O, Sato M, Kamada A. Diffusión- weighted imaging in the deteccion of lymph node metastases in colorectal cancer. Tohoku J Expert Med. 2009;218:177-83. 8. Ono K, Ochiai R, Yoshida T, Kitagawa M, Omagari J, Kobayashi H, et al. Comparision of diffusión-weighted MRI and 2-(fluorine-18)-fluoro-2-deoxy-D-glucose positron emission tomography (FDG-PET) for detecting primary colorectal cancer and regional lymph node metastases. J Magn Reson Imaging. 2009;29:336-40. 9. Wan CW, McKnight MK, Brattain DE, Brattain MG, Yerman LC. Different epidermal growth factor growth responses and receptor levels in human colon carcinoma lines. Cancer Lett. 1988;43:139-43. 10. Koukourakis MI, Mavanis I, Kouklakis G, Pitiakoudis M, Minopoulos G, Manolas C, et al. Early antivascular effects of bevacizumab anti-VEGF monoclonal antibody on colorrectal carcinomas assessed with functional CT imaging. Am J Clin Oncol. 2007;30:315-8. 11. Taylor F, Quirke PH, Heald R, Moran B, Blomqvist L, Swift I, et al. Preoperative high-resolution magnetic resonante imaging can identify good prognosis stage I, II and III rectal cancer best manager by surgery alone: a prospective, multicenter, European study that recruited consecutive patients with rectal cancer. Annals of Surgery. 2011;00:1-9. doi:10.1097/SLA.0b013e31820b8d52. 12. Marijnen CA, Van Gijn W, Nagtegaal ID, Klein Kranenbarg E, Putter H, Wiggers T, et al. The TME Trial after a Median Follow-up of 11 years. Proceedings of the 52nd annual ASTRO Meeting; 2010. S1. 13. Sauer R, Becker H, Hohenberger W, Rödel C, Wittekind C, Fietkau R, et al. Preoperative versus postoperative chemoradiotherapy for rectal cancer. N Engl J Med. 2004;351:1731-40. 14. Shia J, Guillem JG, Moore HG, Tickoo SK, Qin J, Ruo L, et al. Patterns of morphologic alterations in residual rectal carcinoma following preoperative chemoradiation and their association with long-term outcome. Am J Surg Pathol. 2004;28:215-23. 15. Lahaye MJ, Beets GL, Engelen SM, Kessels AG, De Bruïne AP, Kwee HW, et al. Locally advanced rectal cancer: MR imaging for restaging after neoadjuvant radiation therapy with concomitant chemotherapy. Part II. What are the criteria to predict involved lymph nodes? Radiology. 2009;252:81-91. 23/11/12 11:49:05 Cáncer de recto: evaluación de la respuesta tumoral y su influencia en la decisión terapéutica 16. Pahdani AR, Liu G, Koh DM, Chenevert TL, Thoeny HC, Takahara T, et al. Diffusion weighted magnetic resonance imaging as cancer biomarker: consensus and recommendations. Neoplasia. 2009;11:102-25. 17. Pahdani AR, Koh DW. Diffusion MR imaging for monitoring of treatment response. Magn Reson Imaging Clin N Am. 2011;19:181-209. 18. Sun YS, Zhan XP, Tang L, Ji JF, Gu J, Cai Y, el al. Locally advanced rectal carcinoma treated with preoperative chemotherapy and radiation therapy: Preliminary analysis of diffusion-weighted MR imaging for early detection of tumor histopathologic downstaging. Radiology. 2010;254:170-7. 19. De Vries AF, Kremser C, Hein PA, Griebel J, Krezcy A, Öfner D, et al Tumor microcirculation and difusion predict theraphy outcome for primary rectal carcinoma. Int J Radiat Oncol Biol Phys. 2003;56:958-65. 20. Kim SH, Lee JM, Hong SH, Kim GH, Lee JY, Han JK. Locally advanced rectal cancer: Added value of difusiónweighted MRimaging in the evaluation of tumor response to neoadyuvant chemoradiation therapy. Radiology. 2009;253:116-25. 21. Riches SF, Hawtin K, Charles-Edwuards EM, De Souza NM. Diffusion-weighted imaging of the prostate and rectal wall: comparison of biexponencial modelled diffusion and associated perfusion coefficient. R Biomed. 2009;22:318-25. 22. Lambregts DMJ, Mass M, Riedl RG, Bakers FCH, Verwoerd JL, Kessels AGH, et al. Value of ADC measurements for nodal staging after chemoradiation in locally advanced rectal cancer-a per lesion validation study. Eur Radiol. 2010;Doi:10.1007/s00330-010-1937-x. 0-3 01-37.indd 37 37 23. García Figueiras R, Goh V, Pahdani AR, Bermúdez Naviera A, Gómez Caamaño A, Villalba Martín C. The role of functional imaging in colorrectal cancer. AJR Am J Roentgenol. 2010;195:54-66. 24. García Figueiras R, Pahdani AR, Vilanova JC, Goh V, Villalba Martín C. Imagen tumoral funcional. Parte 1. Radiología. 2010;52:115-25. 25. Kambadakone AR, Sahani DV. Body perfusion CT: technique, clinical applications, and advances. Radiol Clin N Am. 2009;47:161-78. 26. Sahani DV, Kalva SP, Hamberg LM, Ham PF, Willet CG, Saini S, et al. Assesing tumor perfusion and treatment response in rectal cancer with multisection CT: initial observations. Radiology. 2005;234:785-92. 27. Bellomi M, Petralia G, Sonzogni A, Zampino MG, Rocca A. CT perfusion for the monitoring of neoadyuvante chemotherapy and radiation therapy in rectal carcinoma: initial experience. Radiology. 2007;244:486-93. 28. Willet CG, Boucher Y, Di Tomasso E, Duda DG, Munn LL, Tong RT, et al. Direct evidence that the VEGF-specific antibody bevacizumab has antivascular effects in human rectal cancer. Nat Med. 2004;10:145-7. 29. Paldino MJ, Barboriak DP. Fundamentals of quantitative dynamic contrast-enhanced MR imaging. Magn Reson Imaging Clin N Am. 2009;17:277-89. 30. De Vries AF, Griebel J, Kremser C, Judmaier W, Gneiting T, Kreczy A, et al. Tumor microcirculation evaluated by dynamic magnetic resonance imaging predicts therapy outcome for primary rectal carcinoma. Cancer Research. 2001;61:2513-6. 23/11/12 11:49:05 La imagen funcional en oncología 4 Cáncer de próstata. Papel de las técnicas funcionales en el diagnóstico y estadificación del cáncer de próstata: espectroscopia, difusión, perfusión. Seguimiento activo J.C. Vilanovaa,* y A. Luna Alcaláb aUnidad de Resonancia Magnética, Clínica Girona, Girona, España Servicio de Radiodiagnóstico, Hospital Sta. Caterina, Salt, Girona, España Departamento de Ciencias Médicas, Facultad de Medicina, Universidad de Girona, Girona, España bServicio de Radiología, Clínica Las Nieves, SERCOSA (Grupo Health Time), Jaén, España Introducción El cáncer de próstata es una de las neoplasias más frecuentes en la población masculina, pero no todos los tumores detectados serán sintomáticos en el transcurso de la vida si no hubieran sido tratados. Dependiendo de las condiciones de salud del paciente, edad, escala de Gleason, antígeno prostático específico (PSA) y preferencias personales, el tratamiento puede ser cirugía o radioterapia cuando el tumor es clínicamente significativo, o seguimiento activo cuando se considera insignificante de acuerdo a la calidad y esperanza de vida del paciente1. Precisamente, estas consideraciones requieren una valoración de los factores pronósticos de forma eficaz. En este contexto, las técnicas de imagen y especialmente la resonancia magnética (RM) funcional pueden tener un papel importante en la localización de zonas más sugestivas de la verdadera agresividad del tumor. Esta información tiene influencia en la valoración del paciente y puede implicar un cambio en la estrategia terapéutica, en lo que puede significar de eficacia o fracaso en el tratamiento2. Actualmente es posible utilizar distintas técnicas de imagen en el manejo del cáncer de próstata, ecografía, RM funcional (difusión, espectroscopia y difusión) o tomografía por emisión de positrones (PET/TC), en la detección, seguimiento y estadificación. Es preciso utilizar las técnicas de forma óptima y con las adecuadas indicaciones para facilitar al clínico el diagnóstico, estadificación y manejo del cáncer de próstata. Esta revisión pretende valorar y describir las técnicas funcionales disponibles y su correcta utilización, para mejorar la caracterización del cáncer y poder decidir entre tratamiento activo o seguimiento activo. Asimismo presentamos un algoritmo para optimizar la toma de decisiones en el manejo de los pacientes con riesgo de cáncer de próstata y el posible seguimiento activo, utilizando la imagen funcional, y compararlo con las guías clínicas Características del cáncer de próstata Es necesario conocer las características anatómicas, biológicas y patológicas del cáncer de próstata para poder interpretar de forma adecuada las distintas técnicas de imagen. La próstata consiste en 3 zonas: periférica posterior o glándula periférica, central-transicional y anterior fibroestromal. La zona central-transicional forma la glándula central. En la edad adulta, la zona transicional es el origen de la hipertrofia benigna prostática. La propia zona transicional recibe el nombre de forma indistinta como zona o glándula central en la edad adulta. La zona o glándula periférica se muestra homogénea. En cambio, la zona central generalmente es fisiológicamente heterogénea (fig. 1). Aproximadamente, más del 70% del cáncer de próstata se localiza en la glándula periférica y el resto en la glándula central. De todas formas es poco frecuente el cáncer aislado de la zona central, siendo en general frecuente la concurrencia con lesión periférica en los casos de cáncer de próstata central3. El sistema más comúnmente utilizado para clasificar y valorar la agresividad del tumor es el grado Gleason. Este *Autor para correspondencia. Correo electrónico: kvilanova@comg.cat (J.C. Vilanova). 4-9 38-101.indd 38 23/11/12 11:49:43 Cáncer de próstata. Papel de las técnicas funcionales en el diagnóstico y estadificación del cáncer de próstata: espectroscopia, difusión, perfusión. Seguimiento activo 39 Figura 1. Resonancia magnética funcional normal de la próstata. A) Corte axial ponderado en T2 mostrando la glándula periférica homogénea y la glándula central heterogénea. B) Mapa ADC en color mostrando señal heterogénea con valores elevados de difusión que se traduce por color rojo en la glándula periférica. C) Adquisición multivoxel en espectroscopia mostrando las curvas metabólicas. D) Curva normal de la glándula periférica derecha (flecha blanca en C) mostrando pico elevado de citrato y bajo de colina con ratio de colina + creatina/citrato < 0,7 (flecha negra). sistema da una puntuación entre 2 y 10, siendo el grado 2 el menos agresivo y el 10 el más agresivo. Esta puntuación es la suma de los 2 patrones histológicos más frecuentes (grados 1-5) encontrados en el tumor. La sospecha clínica del cáncer de próstata se basa en el tacto rectal y en las cifras elevadas del PSA, conjuntamente a la ratio PSA libre/PSA total < 20% y a una velocidad de PSA > 0,75 ng/ml. La conducta aceptada ante sospecha clínica de cáncer de próstata es la realización de biopsia prostática4. Actualmente, la detección precoz del cáncer de próstata conlleva detectar tumores más pequeños, de menor estadificación y de menor grado histológico que hace unas décadas. Muchos pacientes con cáncer de próstata no presentan sintomatología o son sometidos a tratamiento, pero fallecen por otras causas. La historia natural del cáncer de próstata es compleja y en muchos aspectos desconocida. Distintos estudios han mostrado que 1 de cada 3 varones > 50 años tiene cáncer de próstata, siendo la mayoría insignificantes, aunque algunos son agresivos1. La dificultad es poder diferenciar en el momento de la detección el cáncer insignificante, latente, del agresivo y letal. El cáncer de próstata se clasifica en grupos de riesgo (bajo, intermedio, elevado), basándose en las cifras de PSA, escala de Gleason 4-9 38-101.indd 39 y estadio clínico. Estos grupos de riesgo se utilizan para la selección terapéutica. De todas formas, estos 3 grupos de riesgo presentan variabilidad entre el mismo subgrupo e incluso pacientes en el grupo de bajo riesgo pueden presentar tanto un cáncer latente como letal. Las nuevas herramientas de imagen funcional muestran resultados esperanzadores en poder diferenciar el cáncer agresivo, letal, del latente o no agresivo2. La posibilidad de poder incluir información funcional, en forma de biomarcadores de imagen de difusión, perfusión o espectroscopia, puede ser útil en la decisión de considerar un cáncer latente. La posible decisión de considerar el seguimiento activo del paciente ante el resultado de tumor biológicamente latente, no agresivo, podría evitar el sobretratamiento y la consiguiente morbilidad. Técnicas de imagen funcional-molecular Ecografía transrectal La ecografía transrectal (ETR) es la técnica de imagen más utilizada para la glándula prostática. La ETR permite 23/11/12 11:49:43 La imagen funcional en oncología 40 Tabla 1 − Criterios de imagen paramétrica en resonancia magnética del cáncer de próstata Secuencia Significado biológico Ponderada en T2 Morfología Espectroscopia Metabolismo Difusión Densidad celular Perfusión Vascularización Hallazgos ↓ señal nodular ↓ ratio (colina + creatina)/citrato ↓ valor ADC ↑ pendiente inicial (> 200%) + lavado rápido ↑ kep, ktrans, Ve ADC: coeficiente de difusión aparente; kep: vuelta al espacio vascular; ktrans: paso de contraste a través del endotelio desde el compartimiento vascular al intersticio; Ve: fracción del espacio extracelular del tumor. valorar el tamaño y la anatomía zonal de la glándula. El cáncer de próstata generalmente se visualiza hipoecoico con relación a la zona periférica normal. De todas formas, la capacidad de detectar el cáncer de próstata mediante ETR es limitada. La mayoría de lesiones focales hipoecoicas detectadas en ETR no son malignas. Asimismo, la ETR es poco útil en la valoración extracapsular del cáncer de próstata5. La utilización del Doppler color y/o power Doppler incrementa la capacidad en detectar el tumor hipervascular. Sin embargo, la sensibilidad de la ETR no aumenta, debido a que la mayoría de tumores pequeños no son angiogénicos. La utilización de contrastes en ETR con microburbujas ha aumentado la capacidad de detección del cáncer de próstata agresivo o clínicamente significativo y la detección de cáncer en pacientes con cifras de PSA elevadas y biopsias previas negativas. De todas formas, los hallazgos de la ETR con contraste pueden ser similares a los pacientes con prostatitis y no existe su aprobación para uso clínico en el momento actual. Es necesario valorar los siguientes parámetros en el análisis ecográfico: tamaño y volumen prostático, protrusión prostática intravesical, lesiones hipoecoicas y asimetrías1. La ETR se utiliza habitualmente como guía para dirigir la biopsia prostática. El índice de falsos negativos en las biopsias con ETR es elevado, hasta del 40%. El rendimiento de la biopsia mejora aumentando el número de pases realizados, de aquí que es difícil comparar los resultados ante la variabilidad de metodología realizada en la biopsia con ETR. Resonancia magnética (tabla 1) La RM proporciona la mejor identificación de la anatomía prostática. Además, la RM permite valorar la imagen funcional de la próstata mediante técnicas como difusión (RMD), espectroscopia (RME) y perfusión con contraste dinámico (RMC) (fig. 1). El estudio óptimo de RM de próstata para localizar y detectar el cáncer de próstata requiere de bobina endorrectal combinada con la bobina multicanal en fase de pelvis, aunque la bobina endorrectal es más incómoda y encarece la exploración. El examen RM de próstata precisa de equipos de alto campo no inferior a 1,5T. La reciente incorporación de los equipos de 3T ofrece una mejor relación señal/ruido4. Dependiendo de las indi- 4-9 38-101.indd 40 caciones clínicas, como por ejemplo para realizar la estadificación ante cáncer de próstata previamente diagnosticado, puede ser suficiente un estudio morfológico con bobina multicanal en fase de pelvis. En equipos de 3T la necesidad de utilizar o no la bobina endorrectal para diagnóstico aún no ha sido definida. Es necesario conocer la posibilidad de haberse realizado biopsia previa. En este caso es imprescindible demorar en 8-10 semanas la exploración de RM para evitar los cambios de hemorragia glandulares o fibróticos periglandulares que interfieran la correcta interpretación del estudio6. El estudio de RM de próstata requiere valoración morfológica y funcional mediante RMD, RME o RMC. Resonancia magnética morfológica Las secuencias morfológicas consisten en adquisiciones espín eco (SE) o fast espín eco (FSE) ponderadas en T1 y T2. La secuencia ponderada en T1 permite la valoración de posibles adenopatías pélvicas, analizar la pelvis ósea para descartar metástasis y valorar la posibilidad de cambios hemorrágicos en la glándula prostática posbiopsia. La secuencia ponderada en T2 debe realizarse de alta resolución para poder valorar la anatomía normal de la próstata. La zona o glándula periférica se muestra homogéneamente hiperintensa separada de la zona central-transicional que se muestra de forma heterogénea e hipointensa, aunque pueden observarse áreas hiperintensas de adenoma en la misma zona central (fig. 1). El paquete neurovascular se localiza posterolateral a la glándula-zona periférica. El criterio patológico en la RM morfológica potenciada en T2 para cáncer se establece ante la presencia de áreas hipointensas nodulares en el interior de la hiperintensidad normal de la glándula o zona periférica6 (fig. 2). La secuencia en T2 muestra limitación en identificar el cáncer en la zona transicional debido a la dificultad en delimitar zonas hipointensas de cáncer en el seno del propio tejido normal hipointenso central. Los hallazgos que sugieren cáncer en la zona transicional son: hipointensidad difusa mal delimitada, sin el borde hipointenso visualizado en los adenomas y/o interrupción de la pseudocápsula quirúrgica. Además pueden observarse lesiones hipointensas en la zona o glándula periférica en situaciones no neoplásicas como: prostatitis, hiperplasia, fibrosis, hemorragia subaguda posbiopsia, cambios posradiación, hormonoterapia6. La 23/11/12 11:49:43 Cáncer de próstata. Papel de las técnicas funcionales en el diagnóstico y estadificación del cáncer de próstata: espectroscopia, difusión, perfusión. Seguimiento activo A B C D 41 Figura 2. Imagen multifuncional del cáncer de próstata. A) Corte axial ponderado en T2 mostrando la glándula heterogénea de forma global, tanto central como periférico. Se observan áreas más hipointensas en la glándula periférica bilateral que podrían ser de sospecha neoplásica. B) El estudio de espectroscopia demuestra zona de atrofia periférica derecha traducido por escasa presencia de metabolitos, sin elevación de la colina (flecha corta). En el lado izquierdo (flecha larga) se observa elevación de la colina, descenso del citrato e índice colina + creatina/citrato > 0,7 (1,04) sugestivo de neoplasia izquierda. C) Imagen del mapa ADC en color que demuestra reducción de la difusión en el lado izquierdo traducido por color azul y difusión normal en el lado derecho. D) Imagen paramétrica de perfusión en la que se observa una asimetría con curva de captación rápida y lavado rápido en el lado izquierdo (flechas); con curva en meseta y captación al contraste moderada en el lado derecho. La valoración funcional global traduce clara sospecha de neoplasia en el lado izquierdo. La biopsia y posterior prostatectomía mostró adenocarcinoma en el lado izquierdo con resultado negativo en el resto de la glándula. próstata no tiene una verdadera cápsula, sino una banda fibromuscular denominada cápsula prostática. La dificultad en localizar el cáncer de próstata es precisamente en glándulas con grandes hipertrofias de la zona transicional donde el tejido periférico queda comprimido, siendo difícil localizar el cáncer en biopsias sistemáticas a ciegas. Resonancia magnética funcional Resonancia magnética espectroscopia. La RME proporciona información metabólica de la glándula. El tejido prostático normal contiene cifras elevadas de citrato y cifras bajas de 4-9 38-101.indd 41 colina; en cambio, el tejido neoplásico tiene cifras elevadas de colina y reducidas de citrato (fig. 2). El criterio de sospecha es considerar el cociente (creatina + colina)/citrato ([CCo]/Ci) > 0,7 basándose en el análisis realizado en la glándula periférica en equipo de 1,5T7, aunque no hay consenso en el cociente metabólico que determine la presencia de cáncer de próstata debido a la propia variabilidad entre pacientes y equipos de exploración. Valores entre 0,5 y 0,7 se consideran indeterminados o con baja probabilidad de sospecha, y por debajo de 0,5 se consideran valores normales de índice metabólico de la glándula prostática6. 23/11/12 11:49:44 La imagen funcional en oncología 42 A B F E C D G H I Figura 3. Infiltración de vesículas seminales en ADC. A) corte axial ponderado en T2 mostrando hiposeñal en la raíz de las vesículas seminales. B) La correspondiente imagen en mapa ADC en color traduce restricción de la difusión por la presencia de color azul, indicativo de infiltración de cáncer de próstata. Los parámetros del cociente metabólico para la glándula central no han sido establecidos debido al solapamiento de los valores del cociente (CCo)/Ci en la zona central normal o con hipertrofia y el tejido neoplásico. Debe tenerse en cuenta que fisiológicamente la zona central y periuretral presenta menor concentración de citrato, con lo que los valores del índice metabólico (Cco)/Ci pueden ser normales > 0,7. De todas formas se considera como criterio más específico para neoplasia central la ausencia o cifras muy bajas de citrato y elevación de la colina4. Resonancia magnética difusión. La RMD aporta información acerca del movimiento browniano aleatorio de las moléculas de agua libre en el espacio intersticial y a través de la membrana celular. En general, el tejido neoplásico tiene más restricción de la difusión que el tejido normal debido a la mayor densidad celular, dificultando así la normal difusión de las moléculas de agua. La secuencia de difusión aporta información, aparte de la densidad celular, la tortuosidad del espacio extracelular, la integridad de las membranas celulares y el grado de organización glandular. La planificación de la secuencia de difusión debe incluir toda la pelvis además de la próstata y vesículas seminales para poder realizar al mismo tiempo estadificación regional4 (fig. 3) y detección de posible lesión glandular prostática en la misma secuencia de adquisición. La baja movilidad de las moléculas se refleja como alta señal en las imágenes en RMD y, por el contrario, las moléculas que tienen gran movilidad mostrarán una pérdida de señal. La interpretación de la secuencia requiere realizar el procesado y cuantificar la difusión mediante el ADC (coeficiente de difusión aparente) en el mapa paramétrico. La cuantificación se realiza colocando el área de interés (ROI) de 5-10 mm2 sobre la región a considerar. El valor del factor b a utilizar es variable sin que exista consenso. De todas formas se recomiendan valores = 0 y ≥ 1.000 s/mm2 a nivel prostático. La utilización de valores de factor b más elevados condiciona mayor sensibilidad de la secuencia al eliminar la hiperseñal de los tejidos con tiempo de relajación T2 más 4-9 38-101.indd 42 Figura 4. Modelo bicompartimental de la difusión para cálculo de ADC rápido y lento en el cáncer de próstata. A) corte axial ponderado en T2 sin bobina endorrectal en 3T. B-D) Cortes en la misma localización utilizando distintos valores b 0, 100 y 1.000 mm2/s, respectivamente. Se demuestra la mejor detección del tumor al incrementar el valor b. E) Mapa ADC en escala de grises que muestra la restricción de la difusión del tumor derecho traducido por hiposeñal. F) Fusión del mapa ADC en color con la secuencia morfológica. G) Mapa ADC rápido (b = 100 mm2/s) mostrando elevada fracción de perfusión (flecha) que se traduce por un descenso rápido de señal y de la pendiente (flecha corta en I). H) Mapa ADC lento (b = 1.000 mm2/s) mostrando restricción de la verdadera difusión (flecha), traducido por un descenso más lento de la señal (flecha larga en I). largos (edema o fluido debido a su alta densidad de protones), fenómeno denominado “T2 shine-through”. La relación entre la intensidad de señal y el factor b se describe por una curva de descenso biexponencial cuando se utilizan distintos valores b en la misma secuencia, basado en el principio de movimiento incoherente intravoxel8. A valores b bajos (< 150 s/mm2) la pendiente inicial cuantifica valores ADC rápidos (ADC rápido) al reflejar la microcirculación capilar en estructuras vascularizadas, produciéndose una pérdida de señal rápida y traduciendo una mayor pendiente a valores b bajos. El descenso de la pendiente de la curva cuantifica valores ADC lentos (ADC lento) al mostrar disminución de la señal de forma más lenta y una pendiente menor, reflejando en este caso el movimiento de los protones intracelulares. Es decir, utilizando valores b bajos (ADC rápido) permite valorar el efecto perfusión y con valores b elevados (ADC lento) permite medir el efecto real de la difusión (fig. 4). Se ha descrito la utilidad en utilizar los valores ADC lentos y rápidos como biomarcadores en el cáncer de próstata. La presencia de valores bajos, tanto en ADC lento como en ADC rápido, podría predecir la presencia de tumor agresivo, de alto grado histológico9 (aspecto que valoraremos con más detalle en el apartado de estadificación). Las lesiones con verdadera restricción de la difusión aparecerán con baja señal en el mapa de ADC de escala de grises 23/11/12 11:49:44 Cáncer de próstata. Papel de las técnicas funcionales en el diagnóstico y estadificación del cáncer de próstata: espectroscopia, difusión, perfusión. Seguimiento activo (fig. 4) o azul en el mapa en color. No hay un valor de ADC claro que distinga cáncer y no cáncer, aunque cifras < 1,2 × 10–3 mm2/s representan un umbral bastante significativo de proceso neoplásico10. Para evitar errores de interpretación de las imágenes de difusión resulta necesario valorar conjuntamente las imágenes anatómicas. Las ventajas de la secuencia de difusión son el tiempo de adquisición corto y la buena resolución del contraste entre tumor y tejido normal. Los inconvenientes son la escasa resolución espacial y los posibles artefactos de susceptibilidad por hemorragia posbiopsia. Resonancia magnética perfusión. La RMC permite la valoración de la vascularización de los tumores y de forma indirecta la angiogénesis. El análisis de los datos del valor de la señal de intensidad del contraste respecto al tiempo puede obtenerse de 3 formas: cualitativo (perfil de la curva), semicuantitativo (cambios en la intensidad de señal) o cuantitativo. Las medidas cualitativas miden el tipo de perfil de curva: tipo I (captación progresiva), tipo II (en meseta) o tipo III (lavado rápido), similar a los estudios de perfusión en la mama. Las medidas semicuantitativas miden y cuantifican la intensidad de señal relativa (la relación entre la mayor intensidad de señal poscontraste y la señal precontraste) o la pendiente de la curva intensidad/tiempo (que refleja la velocidad del realce) o el área bajo la curva intensidad de señal/tiempo. Estas medidas son simples de obtener mediante las estaciones de trabajo, pero no son comparables entre distintos equipos (fig. 2). La obtención de parámetros cuantitativos utiliza modelos farmacocinéticos que permiten cuantificar diversos parámetros: ktrans (paso de contraste a través del endotelio desde el compartimiento vascular al intersticio), kep (vuelta al espacio vascular) y Ve (fracción del espacio extracelular del tumor)11. Además, con estos datos es posible construir mapas paramétricos que representen la heterogeneidad intratumoral de la distribución vascular. Debemos, sin embargo, considerar la complejidad que hay detrás de estos parámetros, la falta de estandarización y la ausencia de programas de posprocesado de utilización universal. Así, en áreas en donde el tumor tiene una alta permeabilidad vascular (como en la periferia), los valores de ktrans van a depender principalmente del flujo, mientras que en el centro del tumor (en donde el factor limitante es la permeabilidad) dependerá de la superficie de permeabilidad. La dificultad de interpretación de la secuencia es su falta de estandarización. De todas formas, algunos autores han demostrado que el parámetro más fiable para detectar neoplasia es la presencia de una pendiente de captación elevada en los primeros segundos, acompañada de un lavado rápido12. Tomografía por emisión de positrones La PET/TC es una técnica novedosa en la investigación para el cáncer de próstata localizado. Aunque la resolución espacial de la PET es limitada, su eficacia radica en proporcionar la imagen del metabolismo de determinados trazadores para detectar los tumores. El trazador más utilizado 4-9 38-101.indd 43 43 es el 18F-FDG (18 fluor-fluorodeoxiglucosa), indicativo de la actividad glucolítica de las células cancerosas. El FDG no es eficaz en la localización del cáncer de próstata debido a la escasa actividad metabólica de la glucosa en el cáncer de próstata1. Además, los nódulos de la hipertrofia benigna de próstata también pueden mostrar aumento de la actividad metabólica. Nuevos radiofármacos basados en colina, fluorocolina, metionina, acetato, y L-leucina han mostrado resultados prometedores en estudios de investigación. El estudio PET/TC no está indicado como método de detección local, pero muestra resultados esperanzadores en la estatificación ganglionar y en la monitorización terapéutica ante evidencia de recidiva bioquímica. Actualmente, la PET/TC con 11C-colina muestra resultados de eficacia significativa en el manejo de la recidiva, aunque se requiere mayor experiencia para evitar falsos positivos y negativos que estudios iniciales habían mostrado, para de este modo poder ser una técnica eficaz en la monitorización terapéutica del cáncer de próstata13. Detección multiparamétrica La utilización de la secuencia ponderada en T2 de alta resolución es relativamente sensible pero poco específica para localizar el cáncer de próstata. La utilización de las secuencias funcionales, como la RME, RMD y RMC se muestran potencialmente útiles en complementar la secuencia ponderada en T2 y mejorar así la detección del cáncer de próstata mediante la combinación de 1 o 2 secuencias funcionales, RME, RMD o RMC (fig. 2). No se ha demostrado cuál podría ser la combinación más eficaz de las secuencias funcionales para complementar la secuencia ponderada en T2, ni tampoco la mayor eficacia en combinar todas las secuencias funcionales. Nuestro estudio, recientemente publicado, muestra similar eficacia combinando la secuencia morfológica T2 con la difusión y el parámetro clínico del cociente del PSA libre que la combinación de todas las secuencias funcionales14. Es decir, la posibilidad de poder excluir alguna secuencia funcional sin reducir de forma significativa la eficacia de la técnica funcional en RM para poder detectar el cáncer de próstata. La integración de la RMD en el protocolo de estudio debería incluirse de forma rutinaria, al haberse demostrado su utilidad combinada con la secuencia ponderada en T2 sin que ello represente un aumento del coste de la exploración, como así sucede en la espectroscopia o en la secuencia dinámica con contraste, y sin reducir la eficacia de detección. La integración de la información morfológica y funcional en un único estudio de RM hace prever una mejora en la capacidad diagnóstica de la técnica, especialmente en la zona central transicional15. Precisamente, la eficacia diagnóstica del cáncer mediante RM en la glándula central ha mostrado resultados inferiores a los descritos para la glándula periférica. Ello se debe a la presencia de hallazgos similares en RM morfológica y funcional entre la hipertrofia benigna, la prostatitis y el cáncer4. Una de las mayores dificultades en la valoración diagnóstica de la próstata es la distinción 23/11/12 11:49:44 44 entre prostatitis crónica y cáncer. En ambas situaciones, la glándula periférica muestra hiposeñal en secuencias ponderadas en T2. En la secuencia de espectroscopia hay aumento del cociente (CCo)/Ci, similar al tejido neoplásico. En las secuencias de contraste dinámico también puede haber solapamiento al producirse hipervascularización en la prostatitis y en el cáncer2. Existen hallazgos que permiten orientar el diagnóstico de prostatitis, especialmente la hipointensidad difusa o de forma parcheada bilateral de bordes regulares o en forma triangular en correlación a la imagen ponderada en T2. La secuencia de difusión puede ser útil en poder diferenciar la prostatitis del cáncer de próstata. Generalmente, la prostatitis crónica muestra unos valores de ADC intermedios, a diferencia de los valores más bajos en el cáncer, aunque hay solapamiento entre los valores de ADC entre la hipertrofia benigna y el cáncer y, especialmente, la glándula central6. Recientemente se ha demostrado la utilidad de combinar la información integrada en RM con parámetros clínicos como la ratio de PSA libre o densidad de PSA (relación entre el valor del PSA y el tamaño de la próstata) para así seleccionar mejor los pacientes candidatos a ser biopsiados, a diferencia de la indicación actual de biopsiar todos los pacientes con PSA > 4 ng/ml. Es decir, seleccionar los pacientes con mayor riego clínico de presentar cáncer para realizar una exploración de RM funcional y así intentar biopsiar con mayor precisión a los pacientes que hayan presentado sospecha en RM funcional14. La utilización de la RM funcional como herramienta prebiopsia permite obtener información topográfica de la localización del tumor para dirigir mejor la aguja sobre la lesión. Se trata de evitar la ineficacia de realizar las biopsias a ciegas, lo que supone un método poco preciso para identificar el cáncer de próstata (fig. 5). La elección del protocolo más adecuado dependerá de la disponibilidad de cada centro en poder utilizar más de una secuencia funcional. La variabilidad en los protocolos de adquisición en RM requiere optimizar el más adecuado para cada centro y equipo. Recientemente se ha publicado un documento de consenso como guía y recomendación para realizar y describir los hallazgos en RM funcional de próstata de forma óptima16. De todas formas, esta guía resulta de aplicación poco práctica para uso clínico al no proponer uno o varios algoritmos de utilización de imagen RM funcional. Asimismo, la guía es una valoración subjetiva de un escaso número de expertos en imagen RM, donde de los 16 expertos del documento únicamente 6 eran expertos en imagen RM. La última guía europea del cáncer de próstata incluye la RM como opción para detección en pacientes con PSA elevado y biopsias negativas. Para una buena eficacia en la detección es preciso utilizar la RM funcional. Estadificación funcional Es necesario caracterizar con precisión el tumor para seleccionar la mejor opción terapéutica o decidir segui- 4-9 38-101.indd 44 La imagen funcional en oncología miento activo. Generalmente se utilizan criterios clínicos para estadificación basados en nomogramas que integran las cifras de PSA, la agresividad del tumor (grado de Gleason) y el tacto rectal para considerar la extensión del tumor y la presencia de ganglios linfáticos1. Estos nomogramas muestran moderada eficacia, por lo que no siempre es posible tomar la decisión del tratamiento adecuado. La RM permite valorar la integración morfológica y funcional y, de esta forma, considerar la caracterización del tumor y diferenciar las lesiones intraglandulares de las localmente invasivas o metastásicas. El cáncer detectado sin extensión extraglandular se considera estadio T2 y cuando se extiende por fuera de la cápsula se considera T3. Los criterios utilizados para considerar extensión extracapsular del tumor prostático en RM incluyen protrusión focal irregular-espiculada de la cápsula, pérdida de la hiposeñal normal de la cápsula, obliteración del ángulo rectoprostático, asimetría y afectación del plexo neurovascular, y extensión del tumor a vesículas seminales6. La invasión de la vesícula seminal se demuestra por la presencia de hiposeñal en el seno de las vesículas. Se ha demostrado útil la utilización de la secuencia de difusión como criterio de infiltración de la vesícula seminal4 (fig. 3). Para obtener la máxima eficacia en la estadificación del cáncer de próstata en RM es imprescindible utilizar bobina endorrectal o de pelvis multicanal para obtener estudios de alta resolución de la pelvis. Los estudios que han analizado los criterios de selección para realizar un estudio en RM para estadificación del cáncer de próstata sugieren incluir pacientes con riesgo clínico intermedio de tener estadio T3 (PSA 10-20 ng/ml, Gleason 5-7)3. La inclusión en el protocolo de estudio de RM de próstata de la secuencia ponderada en T1 y difusión de toda la pelvis resulta imprescindible para la detección de posibles lesiones metastásicas óseas (fig. 6). A pesar del excelente contraste de los tejidos de partes blandas por parte de la RM, la técnica tiene valor limitado en la valoración metastásica ganglionar, siendo la fiabilidad similar a la TC. De todas formas, se ha demostrado la utilidad en combinar las tablas de Partin con la información en conjunto de la RM para valorar la extensión extracapsular, vesículas seminales y metástasis ganglionar al mostrar un elevado valor predictivo para el diagnóstico de metástasis ganglionares4. Para mejorar la fiabilidad se han desarrollado unos contrastes específicos del órgano. Se inyectan micropartículas de óxido de hierro superparamagnéticas (USPIO) de forma intravenosa que son fagocitadas por los macrófagos del sistema reticuloendotelial normal del ganglio, donde la señal RM se muestra hipointensa. Los nódulos metastásicos, donde los macrófagos normales son reemplazados por el tumor, no captan las partículas de hierro y, en consecuencia, no hay alteración en la señal RM17. La experiencia inicial sugiere que el contraste USPIO utilizando el método de RM linfografía mejora la sensibilidad y especificidad para la detección ganglionar metastásica. De todas formas, la utilización de este contraste específico del órgano no ha sido aprobada para la práctica clínica. 23/11/12 11:49:44 Cáncer de próstata. Papel de las técnicas funcionales en el diagnóstico y estadificación del cáncer de próstata: espectroscopia, difusión, perfusión. Seguimiento activo A 45 B Figura 5. Evolución del cáncer de próstata agresivo. Varón de 67 años, con PSA de 5,67 ng/ml. A) Corte axial ponderado en T2 y estudio de espectroscopia mostrando lesión hipointensa de predominio central anterior derecho con ratio metabólico de sospecha (= 1) (flecha). El resultado de la posterior biopsia fue negativo. B) El seguimiento anual mostró PSA de 9,54 ng/ml, indicando un nuevo estudio de resonancia magnética (RM). Se demuestra la progresión de la lesión en el corte morfológico y aumento de la ratio metabólica (> 2) (flecha). La segunda biopsia demostró cáncer de próstata con patrón de Gleason 8, de alto grado. La biopsia a ciegas previa no fue dirigida a la lesión valorada en la RM inicial como sospechosa de cáncer. Una de las ventajas de las técnicas funcionales es proporcionar información para predecir el grado de diferenciación tumoral y agresividad correlacionado con las propias cifras de los marcadores tumorales específicos prostáticos para diferenciar el cáncer agresivo del latente18-20. Estudios preliminares muestran valores bajos en ADC rápido y lento en cáncer de próstata agresivo indicativo de tumores con alta perfusión micropapilar y elevada celularidad. La RME también se ha correlacionado con el grado de Gleason9. La RME tiene la utilidad potencial de poder detectar los tumores agresivos de forma no invasiva21 (fig. 5). Precisamente nuestros resultados, pendientes de publicar, confirman la correlación entre los hallazgos de RME con el grado de Gleason, y en la decisión de hacer seguimiento activo en pacientes con RME negativa, por la escasa probabilidad de que éstos presenten un cáncer de próstata con un grado de Gleason alto (fig. 7). 4-9 38-101.indd 45 Figura 6. Metástasis óseas en difusión. A) Corte axial ponderado en T1 mostrando hiposeñal en la rama púbica derecha. B) Correspondiente corte axial en secuencia de difusión (b = 1.000 mm2/s) confirmando la metástasis, al mostrar hiperseñal en relación a restricción de la difusión. Monitorización terapéutica funcional Actualmente, el método para monitorizar la posible recidiva posterapéutica consiste en la detección de 23/11/12 11:49:45 46 Figura 7. Cáncer de próstata de bajo grado. Corte axial ponderado en T2 con la correspondiente adquisición en espectroscopia. Se demuestra una leve hiposeñal de la glándula periférica izquierda (flecha) con normalidad de la ratio metabólica (< 0,5) (flecha). La biopsia demostró un cáncer de próstata de bajo grado, Gleason 5. La imagen funcional en oncología cifras aumentadas de PSA, denominado recidiva bioquímica. Generalmente, la recidiva bioquímica precede a la recidiva clínica en varios años, aunque únicamente el 30% de pacientes con recidiva bioquímica progresará a recidiva clínica 22. El principal papel de la imagen es poder precisar si se trata de recidiva local o metastásica. La RM funcional puede ser útil para descartar, detectar y localizar el nivel de la recidiva local tanto para tratamiento quirúrgico como radiobraquiterapia, hormonoterapia, crioterapia o ultrasonido focal de alta intensidad (HIFU)6 (fig. 8). Los hallazgos en RM morfológica después de los distintos tratamientos pueden ser de difícil interpretación debido a la presencia de atrofia glandular y fibrosis inducida por la radiación, la presencia de semillas de braquiterapia, cicatriz o clips poscirugía. La secuencia ponderada en T2 es poco sensible a la detección por la presencia de hiposeñal difusa debido a la atrofia que impide diferenciar el tejido neoplásico del tejido atrófico. En estos casos conviene utilizar secuencias funcionales como la RME, la RMD y la RMC para mejorar la detección de la lesión e incluso para monitorizar la eficacia del tratamiento. Se ha demostrado la utilidad en localizar la posible recidiva posprostatectomía mediante secuencias convencionales, aunque es preciso utilizar bobina endorrectal 4. La utilización de la secuencia ponderada en T2 y RM funcional es eficaz en valorar la respuesta al tratamiento mediante radioterapia, hormonoterapia o HIFU. La secuencia de difusión tiene la capacidad de poder diferenciar recidiva tumoral de cambios posradiación basándose en la diferencia de los valores de ADC y la posibilidad de monitorizar la eficacia en el tratamiento con relación a los cambios en los valores de ADC 23. Las secuencias funcionales más eficaces para valorar recidiva resultan ser la difusión y la perfusión (fig. 9). La Figura 8. Seguimiento postratamiento de HIFU (ultrasonido focal de alta intensidad). A) Corte axial ponderado en T2 mostrando la neoplasia en el lado derecho. B) Corte axial ponderado en T2 mostrando la atrofia postratamiento con zona hipointensa inespecífica en el lado derecho (flecha). C-E) Las imágenes de espectroscopia, ADC y perfusión correspondiente no demuestran lesión en la zona descrita con relación a atrofia glandular y sin signos de recidiva. 4-9 38-101.indd 46 23/11/12 11:49:46 Cáncer de próstata. Papel de las técnicas funcionales en el diagnóstico y estadificación del cáncer de próstata: espectroscopia, difusión, perfusión. Seguimiento activo espectroscopia se muestra limitada, especialmente para poder detectar lesiones de pequeño tamaño, donde es difícil conseguir una buena adquisición en volúmenes de tejido pequeño. La experiencia para valorar la recidiva mediante PET/TC es aún limitada, mostrando los resultados más eficaces mediante 11C-colina. De todas formas se ha descrito variabilidad en la detección, al ser PSA dependiente y con mayor eficacia en la detección posprostatectomía que en la valoración posradioterapia13. Estrategia de imagen Recientemente se ha incluido la utilización de la RM en la última actualización de la guía europea del cáncer de próstata24. En esta inclusión consensuada se considera especialmente eficaz la RM para detectar y poder dirigir de forma focalizada la biopsia en pacientes con cifras de PSA elevadas y biopsias previas negativas, elevación progresiva de las cifras de PSA o en pacientes con riesgo clínico de presentar un cáncer de próstata. La aplicación de la RM como técnica previa a la biopsia en pacientes de riesgo de cáncer de próstata muestra ventajas y un beneficio significativo en el manejo del paciente2. La utilización de imagen funcional en RM permite mejorar la eficacia de la biopsia. El progresivo desarrollo de la mejora de la técnica y la evidencia científica debe aumentar la eficacia de la RM en el manejo del cáncer de próstata para que, de este modo, la RM pueda ser incluida incluso como selección de pacientes de riesgo previa a la biopsia. Empieza a ser relevante y admitido el papel de la RM en la monitorización terapéutica para localizar la posible recidiva local, como se describe en la última actualización de las guías europeas y americanas24,25, confirmando la utilidad de la espectroscopia y la perfusión como herramientas eficaces. Probablemente, en el futuro, se incluirá la secuencia de difusión como herramienta de uso universal para el manejo del cáncer de próstata en RM. Para ello es necesario validar de forma consensuada los estudios que recientemente parecen confirmar su utilidad 20. En la práctica clínica, el reto es valorar y decidir el criterio óptimo cuando hay discrepancia entre las distintas secuencias funcionales. Para ello es necesario disponer de la experiencia suficiente en las técnicas utilizadas, conocer las ventajas e inconvenientes y, sobre todo, combinar y fusionar la información de forma global (tablas 1 y 2) teniendo en cuenta siempre la importancia de la imagen morfológica, para evitar falsos diagnósticos debido al solapamiento que presenta especialmente el cáncer de próstata con la hipertrofia benigna en secuencias funcionales, como se ha especificado anteriormente. Es necesaria la implicación del radiólogo en el manejo clínico para consensuar con urólogos y oncólogos un algoritmo más lógico en pacientes con posible sospecha de cáncer de próstata basándose en cifras elevadas de PSA, donde la imagen tenga un papel relevante en la toma de decisiones (fig. 10). Asimismo, está prevista la publica- 4-9 38-101.indd 47 47 Figura 9. Recidiva bioquímica con lesión focal. Varón de 61 años, con PSA de 1,1 ng/ml. A) Axial en T2 con bobina endorrectal mostrando lesión hipointensa en el lado izquierdo del lecho quirúrgico (flecha) con restricción de la difusión en el mapa ADC en color (flecha) (B) e hipervascularización en el mapa en color de perfusión (C) (flecha). Sospecha clínica (PSA > 4 ng/ml, %PSA < 20%, elevación progresiva PSA) y/o biopsias previas negativas RM multiparamétrica + – Biopsia ecodirigida + Tratamiento o seguimiento activo según estadificación – Seguimiento clínico (PSA, marcadores) Recidiva bioquímica postratamiento Figura 10. Algoritmo de inclusión de la resonancia magnética funcional en el manejo del paciente con sospecha o seguimiento del cáncer de próstata. RM: resonancia magnética; PSA: antígeno prostático específico. ción en 2012 de la guía estandarizada del informe en RM de próstata, incluyendo criterios morfológicos y funcionales, denominada PI-RADS (Prostate Imaging Reporting and Data System). Conclusiones En la actualidad, el cáncer de próstata es uno de los problemas más importantes de la población masculina, don- 23/11/12 11:49:46 La imagen funcional en oncología 48 Tabla 2 − Ventajas e inconvenientes de la resonancia magnética (RM) funcional multiparamétrica en el cáncer de próstata Ventajas Inconvenientes Identificar pacientes de riesgo clínico Dificultad en correlacionar la imagen RM con la ETR Identificar zonas de mayor sospecha Complejidad en disponer de biopsia dirigida en equipo RM Mejorar el rendimiento de la biopsia dirigida con imagen Artefactos posbiopsia Evitar biopsias innecesarias y repetidas Dificultad en estandarizar, validar los parámetros de las secuencias Valoración global de la glándula Déficit de implementación universal de la RM de próstata Detección y estadificación en un único estudio Seguimiento postratamiento Posibilidad de gradación histológica ETR: ecografía transrectal. de el papel de la imagen había sido poco relevante hasta hace pocos años. El progresivo desarrollo y mejora de las técnicas de imagen, especialmente con la RM funcional, ha aumentando la eficacia en el manejo del cáncer de próstata. La posibilidad de incluir imagen morfológica y funcional permite seleccionar de forma más eficaz a los pacientes en riesgo de presentar cáncer de próstata, y de este modo dirigir de forma más óptima la biopsia. Las nuevas tecnologías funcionales y moleculares de RM y PET/TC pueden aumentar la eficacia en la estadificación y monitorización para que de este modo la RM pueda ser incluida en las guías de práctica clínica, como así se ha producido en las últimas actualizaciones. La utilización de un protocolo de imagen en RM y una guía adecuada según la indicación clínica específica puede ayudar a decidir la mejor opción terapéutica. Hay avances en imagen funcional para diferenciar el cáncer agresivo o letal del latente o insignificante, para así poder aumentar la eficacia en el manejo del cáncer de próstata y evitar sobretratamiento. Bibliografía 1. Hricak H, Choyke PL, Eberhardt SC, Leibel SA, Scardino PT. Imaging prostate cancer: a multidisciplinary perspective. Radiology. 2007;243:28-53. 2. Sciarra A, Barentsz J, Bjartell A, Eastham J, Hricak H, Panebianco V, et al. Advances in magnetic resonance imaging: how they are changing the management of prostate cancer. Eur Urol. 2011;59:962-77. 3. Kelloff GJ, Choyke P, Coffey DS. Challenges in clinical prostate cancer: role of imaging. AJR Am J Roentgenol. 2009;192:1455-70. 4. Bonekamp D, Jacobs MA, El-Khouli R, Stoianovici D, Macura KJ. Advancements in MR imaging of the prostate: from diagnosis to interventions. Radiographics. 2011;31:677703. 5. Heijmink SW, Futterer JJ, Strum SS, Oyen WJ, Frauscher F, Witjes JA, et al. State-of-the-art uroradiologic imaging in 4-9 38-101.indd 48 the diagnosis of prostate cancer. Acta Oncol. 2011;50 Suppl 1:25-38. 6. Vilanova JC, Comet J, García-Figueiras R, Barceló J, Boada M. Usefulness of magnetic resonance imaging in prostate cancer. Radiología. 2010;52:513-24. 7. Kurhanewicz J, Vigneron DB, Hricak H, Narayan P, Carroll P, Nelson SJ. Three-dimensional H-1 MR spectroscopic imaging of the in situ human prostate with high (0.240.7 cm3) . spatial resolution. Radiology. 1996;198:795-805. 8. Koh DM, Collins DJ, Orton MR. Intravoxel incoherent motion in body diffusion-weighted MRI: reality and challenges. AJR Am J Roentgenol. 2011;196:1351-61. 9. Giles SL, Morgan VA, Riches SF, Thomas K, Parker C, De Souza NM. Apparent diffusion coefficient as a predictive biomarker of prostate cancer progression: value of fast and slow diffusion components. AJR Am J Roentgenol. 2011;196:586-91. 10. Gibbs P, Tozer DJ, Liney GP, Turnbull LW. Comparison of quantitative T2 mapping and diffusion-weighted imaging in the normal and pathologic prostate. Magn Reson Med. 2001;46:1054-8. 11. Franiel T, Hamm B, Hricak H. Dynamic contrast-enhanced magnetic resonance imaging and pharmacokinetic models in prostate cancer. Eur Radiol. 2011;21:616-26. 12. Engelbrecht MR, Huisman HJ, Laheij RJ, Jager GJ, Van Leenders GJ, Hulsbergen-Van De Kaa CA, et al. Discrimination of prostate cancer from normal peripheral zone and central gland tissue by using dynamic contrast-enhanced MR imaging. Radiology. 2003;229:248-54. 13. Murphy RC, Kawashima A, Peller PJ. The Utility of 11C-Choline PET/CT for Imaging Prostate Cancer: A Pictorial Guide. AJR Am J Roentgenol. 2011;196:1390-8. 14. Vilanova JC, Barceló-Vidal C, Comet J, Boada M, Barceló J, Ferrer J, et al. Usefulness of prebiopsy multifunctional and morphologic MRI combined with free-to-total prostatespecific antigen ratio in the detection of prostate cancer. AJR Am J Roentgenol. 2011;196:W715-22. 15. Riches SF, Payne GS, Morgan VA, Sandhu S, Fisher C, Germuska M, et al. MRI in the detection of prostate cancer: combined apparent diffusion coefficient, metabolite ratio, and vascular parameters. AJR Am J Roentgenol. 2009;193:1583-91. 23/11/12 11:49:46 Cáncer de próstata. Papel de las técnicas funcionales en el diagnóstico y estadificación del cáncer de próstata: espectroscopia, difusión, perfusión. Seguimiento activo 16. Dickinson L, Ahmed HU, Allen C, Barentsz JO, Carey B, Futterer JJ, et al. Magnetic resonance imaging for the detection, localisation, and characterisation of prostate cancer: recommendations from a European consensus meeting. Eur Urol. 2011;59:477-94. 17. Hovels AM, Heesakkers RA, Adang EM, Barentsz JO, Jager GJ, Severens JL. Cost-effectiveness of MR lymphography for the detection of lymph node metastases in patients with prostate cancer. Radiology. 2009;252:729-36. 18. Van As NJ, De Souza NM, Riches SF, Morgan VA, Sohaib SA, Dearnaley DP, et al. A study of diffusion-weighted magnetic resonance imaging in men with untreated localised prostate cancer on active surveillance. Eur Urol. 2009;56:981-7. 19. Vargas HA, Akin O, Franiel T, Mazaheri Y, Zheng J, Moskowitz C, et al. Diffusion-weighted endorectal MR imaging at 3 T for prostate cancer: tumor detection and assessment of aggressiveness. Radiology. 2011;259:775-84. 4-9 38-101.indd 49 49 20.Morgan VA, Riches SF, Thomas K, Vanas N, Parker C, Giles S, et al. Diffusion-weighted magnetic resonance imaging for monitoring prostate cancer progression in patients managed by active surveillance. Br J Radiol. 2011;84:31-7. 21. Fradet V, Kurhanewicz J, Cowan JE, Karl A, Coakley FV, Shinohara K, et al. Prostate cancer managed with active surveillance: role of anatomic MR imaging and MR spectroscopic imaging. Radiology. 2010;256:176-83. 22. Ravizzini G, Turkbey B, Kurdziel K, Choyke PL. New horizons in prostate cancer imaging. Eur J Radiol. 2009;70:212-26. 23. Verma S, Rajesh A. A Clinically relevant approach to imaging prostate cancer: self-assessment module. AJR Am J Roentgenol. 2011;196:S11-4. 24. Heidenreich A, Aus G, Abbou C, Bolla M, Joniau S, Matveev V, et al. Guidelines on prostate cancer 2011. EUA 2011. Disponible en: http://www.uroweb.org 25. National Guideline Clearinghouse N. Prostate cancer. Diagnosis and treatment. Disponible en: http://www.guideline.gov 23/11/12 11:49:46 La imagen funcional en oncología 5 Tomografía por emisión de positrones/ tomografía computarizada en la estadificación del cáncer de pulmón A. Rodríguez Fernández* y R. Sánchez Sánchez Servicio de Medicina Nuclear, Hospital Universitario Virgen de las Nieves, Granada, España Introducción La incidencia de cáncer de pulmón se ha incrementado de manera significativa desde comienzos del siglo xx, y en la actualidad representa la principal causa de muerte por cáncer, tanto en varones como en mujeres. El cáncer de pulmón constituye la segunda causa más frecuente de cáncer para ambos sexos. A pesar de las mejoras obtenidas en la supervivencia de otros tumores en los últimos años, el cáncer de pulmón sigue presentando una supervivencia a los 5 años pequeña, en torno al 10%, principalmente debido a que su diagnóstico se realiza en fases avanzadas donde las opciones terapéuticas son ya limitadas1. El hábito tabáquico es el principal factor etiológico del cáncer de pulmón, siendo la asociación entre éste y el tabaco una de las más estudiadas en las investigaciones biomédicas2. El riesgo de cáncer de pulmón es 10 veces superior en personas fumadoras frente a las no fumadoras. No obstante, fumar no parece ser el único factor etiológico asociado al cáncer de pulmón, lo que explicaría el actual aumento de la incidencia de cáncer de pulmón en personas que nunca han fumado. Se han identificado numerosos factores medioambientales asociados a un incremento del riesgo de cáncer de pulmón, como la exposición a la radiación, el asbesto y enfermedades pulmonares como la tuberculosis, la bronquitis crónica y la fibrosis pulmonar idiopática. Tipos histológicos Las categorías histopatológicas actuales son un intento de acercar el diagnóstico histopatológico a un diagnóstico clínico real clasificando no sólo tipos histológicos, sino también orientando el tratamiento, el pronóstico y la evolución de la enfermedad. La tabla 1 muestra la clasificación del cáncer de pulmón llevada a cabo por la Organización Mundial de la Salud (OMS)3. Según esta clasificación, el cáncer de pulmón agrupa a todos los tumores primitivos epiteliales malignos de pulmón, excluyendo tumores pleomórficos, sarcomatoides, carcinoides y los derivados de glándula salivar. El cáncer de pulmón de célula no pequeña (CPCNP) supone el 85-90% de todos los cánceres de pulmón e incluye 3 tipos histológicos fundamentales: adenocarcinoma, escamoso o epidermoide, y el de célula grande. Los 2 primeros son los más frecuentes (80%). El carcinoma epidermoide es el que con más frecuencia aparece asociado al tabaco y suele presentar una localización central. Recientemente ha sido publicada una propuesta de nueva clasificación de adenocarcinoma realizada por un equipo multidisciplinario de expertos patólogos, neumólogos, oncólogos, radiólogos, cirujanos y biólogos moleculares, quienes se basaron en niveles de evidencia de los estudios de los últimos años con respecto al cáncer de pulmón4. Según esta clasificación hablaríamos de: lesiones preinvasivas, adenocarcinoma in situ (anteriormente bronquioloalveolar [CBA]), adenocarcinoma mínimamente invasivo, adenocarcinoma invasivo y otras de sus variantes, como el adenocarcinoma mucinoso con patrón de crecimiento “lepídico” (anteriormente CBA mucinoso), coloide, fetal y entérico. El cáncer de pulmón de célula pequeña (CPCP) es la forma más agresiva por su alto potencial de metastatización a distancia y su asociación al tabaco es evidente, presentándose en personas fumadoras o ex fumadoras en un porcentaje superior al 95%. El pulmón es la segunda localización en frecuencia de los tumores neuroendocrinos (TNE), después del tracto gastrointestinal. Estos tumores presentan un pronóstico más favorable si los comparamos con los anteriores tipos histológicos. Se caracterizan por tener un curso más indolente y una menor tasa de proliferación. *Autor para correspondencia. Correo electrónico: antonio.rodriguez.fernandez.sspa@juntadeandalucia.es (A. Rodríguez Fernández). 4-9 38-101.indd 50 23/11/12 11:49:46 Tomografía por emisión de positrones/tomografía computarizada en la estadificación del cáncer de pulmón 51 Tabla 1 − Clasificación de la Organización Mundial de la Salud del cáncer de pulmón Carcinoma broncogénico no microcítico/no células pequeñas (CBNM/CBNCP) Carcinoma de células adenoescamosas Papilar Células claras Células pequeñas Basaloide Carcinoma bronquioloalveolar No mucinoso Mucinoso Mixto Sólido Adenocarcinoma Acinares Papilar Adenocarcinoma con subtipos mixtos Variantes Adenocarcinoma fetal bien diferenciado Mucinoso (coloide) adenocarcinoma Cistoadenocarcinoma mucinoso Sello de adenocarcinoma anillo Adenocarcinoma de células claras Carcinoma adenoescamoso Carcinoma sarcomatoide o sarcomatoso Carcinoma huso y/o de células gigantes Carcinoma de células fusiformes Carcinoma de células gigantes Carcinosarcoma Blastoma pulmonar Carcinoma de células grandes Variantes Neuroendocrino de célula grande Mixto Carcinoma basaloide Carcinoma tipo linfoepitelioma Carcinoma de células claras Carcinoma de células grandes con fenotipo rabdoide Carcinomas de tipo glándula salival Carcinoma mucoepidermoide Carcinoma adenoide quístico Tumor carcinoide Carcinoides típicos Carcinoides atípicos Carcinoma microcítico o tipo células pequeñas (CBM/CBCP) Carcinoma no clasificado Tomografía por emisión de positrones La tomografía por emisión de positrones (PET) es un procedimiento no invasivo que detecta y cuantifica la actividad metabólica de los diferentes fenómenos fisiológicos o patológicos, dando una información funcional in vivo de dichos procesos, unas veces complementaria y otras adicional a las técnicas de imagen estructurales. Los cambios en la fisiología tumoral se presentan de forma más precoz que los cambios anatómicos, por lo que la PET permite detectar las alteraciones bioquímicas y fisiológicas ocasionadas por procesos tumorales cuando aún no se evidencian con otras técnicas de diagnóstico por imagen. Históricamente, el cáncer de pulmón fue la segunda indicación de la PET tras las neoplasias cerebrales. El radiofármaco más utilizado en PET para las aplicaciones oncológicas es un análogo de la glucosa, en la que se ha sustituido el grupo hidroxilo del carbono 2 por un átomo de 18F, denominado 2-[18F]fluoro-2-desoxi-D-glucosa (18F-FDG). El enorme incremento en la utilización clínica de la 18F-FDG se debe, en parte, a su elevada aplicabilidad para 4-9 38-101.indd 51 el estudio de un gran número de tumores y a su mayor disponibilidad, ya que su período de semidesintegración (110 min) permite su transporte a instalaciones alejadas del lugar de su producción (ciclotrón), mientras que esto no es posible con otros radiofármacos de uso clínico. Tras su administración por vía intravenosa, la 18F-FDG se distribuye por el sistema circulatorio y se incorpora a las células tumorales por los mismos mecanismos de transporte que la glucosa no marcada, mediante los transportadores sodio-glucosa a través de un gradiente de concentración, y por los transportadores específicos de membrana o GLUT, que permiten el paso de glucosa mediante transferencia pasiva y difusión facilitada. En el interior de la célula, mediante la acción de la enzima hexocinasa, la 18F-FDG se fosforila a 18F-FDG-6-fosfato que, a diferencia de su análogo no marcado, no puede ser metabolizada por las vías de la glucólisis o de la síntesis de glucógeno. Además, la enzima que cataliza el paso inverso a la hexocinasa, la glucosa-6-fosfatasa, se encuentra en muy baja concentración en la mayoría de los tejidos, en especial en los neoplásicos. 23/11/12 11:49:46 La imagen funcional en oncología 52 18F-FDG Glucosa Rs Glut 18F-FDG Glucosa Hexoquinasa G-6 Fosfatasa Glucoquinasa 18F-FDG-6-P Glucosa-6-P Isomerasa Fructosa-6-P Atrapamiento Ciclo de Krebs Figura 1. Esquema del metabolismo celular de la glucosa y de la flúor-deoxiglucosa. La glucosa entra en el interior de la célula gracias a los receptores GLUT, es fosforilada e introducida en el ciclo de Krebs. La FDG usa la misma vía de entrada en la célula, igualmente es fosforilada, pero no es sustrato para la isomerasa, por lo que no puede entrar en el ciclo de Krebs, produciéndose un atrapamiento metabólico de ésta. Por estas razones se puede afirmar que la 18F-FDG sufre un “atrapamiento metabólico en la célula” y éste es el fundamento que posibilita su detección (fig. 1). Por tanto, la 18F-FDG es un marcador del metabolismo glucídico celular y no de proliferación celular. La concentración de 18 F-FDG en la célula tumoral es un reflejo del aumento de su metabolismo glucídico para poder mantener una elevada tasa de crecimiento y/o proliferación. La captación de 18F-FDG varía mucho según la histología de cada tumor; sin embargo, una captación elevada se asocia, generalmente, a la existencia de un gran número de células viables, propia de un alto grado histológico. No todos los focos que muestran hipercaptación de 18F-FDG son de origen canceroso, ya que dicha hipercaptación no es específica de los tejidos tumorales. Cualquier proceso inflamatorio o infeccioso puede ser visualizado, probablemente debido al acúmulo del trazador en los macrófagos y en el tejido de granulación, como ocurre, por ejemplo, en la sarcoidosis o en los abscesos, siendo éstas las principales causas de estudios falsamente positivos. Por otro lado, podemos encontrar lesiones tumorales que no capten 18F-FDG. Dentro de las causas de la no visualización de las lesiones malignas se ha descrito la existencia de valores elevados de glucosa endógena, que compite con la 18F-FDG en su incorporación celular, el pequeño tamaño (inferior al límite de resolución de los sistemas detectores), la composición (mucinosa, necrótica, quística), las caracte- 4-9 38-101.indd 52 rísticas celulares del tumor (muy diferenciado, bajo grado, crecimiento lento) y la localización (periférica por el efecto parcial de volumen, cortical de actividad similar a la sustancia gris cerebral normal). Por tanto, muchos factores pueden afectar a la captación, distribución y eliminación de la 18F-FDG, y conducir a exploraciones falsamente negativas o positivas. En la tabla 2 se resumen las principales causas de falsos positivos y negativos en la patología torácica. El SUV (standardized uptake value) es un parámetro que cuantifica la actividad metabólica de un área, pero que no muestra un valor fijo para determinar la benignidad o malignidad de una lesión. Hasta ahora, el valor de corte usado para ello había sido 2,5. La insulina endógena circulante tras la ingesta o la administrada a los diabéticos aumentará la captación en el hígado y en las partes blandas, por lo que disminuirá en los tumores, ocasionando en algunas circunstancias falsos negativos. De ahí la importancia de que el paciente esté en ayunas antes de la exploración o que la administración de insulina en los pacientes diabéticos se adelante lo más posible antes de la exploración. Por otro lado, las células mediadoras de la inflamación (especialmente los granulocitos) estimuladas durante dichos procesos o en infecciones pueden captar 18F-FDG de forma similar o superior a una neoplasia, de ahí la posibilidad de provocar falsos positivos. Por todo ello, y para minimizar la probabilidad de estudios falsos positivos y negativos, es importante que: 23/11/12 11:49:47 Tomografía por emisión de positrones/tomografía computarizada en la estadificación del cáncer de pulmón 53 Tabla 2 − Causas de falsos positivos y falsos negativos en los estudios de tomografía por emisión de positrones (PET) con FDG Falsos positivos Falsos negativos Enfermedades granulomatosas Tuberculosis Histoplasmosis Sarcoidosis Aspergilosis Granulomatosis de Wegener Enfermedades inflamatorias Neumonías Bronquiectasias Abscesos Aspergilosis Pleurodesis Artefactos Tumores hipometabólicos Carcinomas bronquioloalveolares Tumores carcinoides Carcinomas mucinosos Nódulos subcentimétricos Altos niveles de glucemia – Los valores de glucemia estén, en el momento de la inyección del trazador, por debajo de 120 mg/dl. – Se evite la administración de insulina las horas antes de la exploración. – Se demore la exploración tras circunstancias que causen procesos inflamatorios, como cirugía, traumatismos o tratamientos quimio y radioterápicos. – No se realice la exploración en el curso de un proceso infeccioso activo. Por otro lado, también hay que tener en cuenta factores técnicos a la hora de valorar posibles falsos negativos de la exploración, como el límite de resolución de los equipos PET, de modo que lesiones por debajo de dicho límite pueden no ser detectadas. En este aspecto es donde los nuevos equipos multimodalidad han añadido un punto de ventaja sobre los antiguos equipos PET dedicados, y es que la resolución de dichos equipos está ya en torno a los 6-7 mm. De cualquier manera, a este límite de resolución hay que añadirle la densidad de células neoplásicas metabólicamente activas para que éstas sean detectables a pesar del tamaño que tengan. Además, ciertos tipos tumorales, a pesar de su agresividad, pueden no captar 18F-FDG debido a sus peculiaridades metabólicas o a su tipo de crecimiento. Éste es el caso de los adenocarcinomas in situ y mucinosos (antiguos tumores bronquioloalveolares), que debido a sus peculiaridades histopatológicas pueden dar estudios falsamente negativos. El desarrollo de equipos multimodalidad PET/TC (tomografía por emisión de positrones/tomografía computarizada) nos aporta un valor adicional en la valoración de patología neoplásica, sumando información funcional y anatómica. Pero, además, en un estudio PET/TC los datos de la TC se emplean para corregir la atenuación fotónica, la dispersión de la radiación y los errores por volumen parcial de la imagen de PET. 4-9 38-101.indd 53 Cáncer de pulmón de células no pequeñas En pacientes diagnosticados de CPCNP es importante la estadificación inicial de la enfermedad para poder seleccionar la opción terapéutica más apropiada. Asimismo es primordial diferenciar de manera correcta a los pacientes con enfermedad potencialmente curable, que pueden beneficiarse de la cirugía con intención curativa, de los que son irresecables y, por tanto, candidatos a tratamiento con quimioterapia, radioterapia o ambos. La resecabilidad depende del estadio y de la localización/extensión local. La clasificación más utilizada con este propósito es la TNM (tumor, node, metastases). La T se refiere al tumor primario en cuanto al tamaño, localización y posible invasión de estructuras de vecindad. La N hace referencia a la afectación ganglionar y la M a la presencia o ausencia de metástasis. Todos los autores coinciden en que hasta el estadio IIB el tumor es resecable, mientras que el IIIB y el IV son irresecables. El problema se plantea con los estadios IIIA, en que según escuelas se aconseja realizar la cirugía junto con quimioterapia adyuvante o bien quimioterapia neoadyuvante como paso previo a la cirugía. El objetivo fundamental de las técnicas de imagen es poder seleccionar a los pacientes en los que puede realizarse cirugía o radioterapia curativas. Por tanto hay que valorar adecuadamente el mediastino y excluir la posible existencia de metástasis. La TC es la técnica más utilizada en la evaluación de pacientes con carcinoma pulmonar. Es especialmente útil para la obtención de información sobre el tamaño de la lesión, sus características morfológicas y la relación con estructuras adyacentes. Sin embargo, presenta limitaciones para el diagnóstico de infiltración tumoral en ganglios de tamaño normal, ya que se basa en criterios exclusivamente morfológicos para dicho diagnóstico. 23/11/12 11:49:47 54 La imagen funcional en oncología Valoración del T Figura 2. Estudio de tomografía por emisión de positrones/ tomografía computarizada (PET/TC) con 18F-FDG, presentando proyecciones MIP (A) y cortes transaxiales de PET (B1), TC (B2, ventana de mediastino) e imagen de fusión (B3). Gran masa hipermetabólica, con centro ametabólico, en lóbulo inferior del pulmón derecho (A, B), que presenta extensión hacia el mediastino a través del espacio subcarinal (B2, B3). Hallazgos compatibles con una gran tumoración pulmonar, parcialmente necrosada, que invade el mediastino. Figura 3. Distribución por áreas y estaciones de los ganglios mediastínicos según la IASLC 2009. 4-9 38-101.indd 54 La incorporación de equipos multimodalidad PET/TC ha incrementado la exactitud diagnóstica en la detección del tumor primario, la afectación de la pared torácica y la determinación de la infiltración mediastínica (fig. 2) comparada con la de la PET sola5,6. No obstante, el papel de la PET/TC es limitado si lo comparamos con la TC con contraste, que sigue siendo el método más utilizado en la evaluación del tumor primario, ya que constituye una técnica excelente para determinar su localización, tamaño y su relación con estructuras anatómicas adyacentes7. La resonancia magnética (RM) puede proporcionar una información adicional en determinadas ocasiones, como la afectación del sulcus superior, la posible infiltración cardíaca y/o los grandes vasos y estructuras vecinas Valoración del N En ausencia de metástasis, la afectación de los ganglios linfáticos regionales es de gran relevancia a la hora de establecer el tratamiento más adecuado y el pronóstico de la enfermedad. Los pacientes sin ganglios regionales afectados o que sólo presentan afectación de ganglios hiliares o intrapulmonares homolaterales, son candidatos a resección quirúrgica. En los casos que presentan afectación ganglionar mediastínica ipsilateral (N2), la quimioterapia preoperatoria seguida de cirugía o la radioterapia radical son elecciones adecuadas. Finalmente, los pacientes con afectación ganglionar mediastínica contralateral (N3) serán candidatos a tratamiento quimioterápico combinado o no con radioterapia (fig. 3)8. Clásicamente se ha considerado la TC como la técnica no invasiva de elección para la valoración ganglionar. El criterio para determinar la infiltración ganglionar es el aumento de tamaño de los ganglios, considerando metastásicos aquellos con un tamaño > 1 cm en el eje corto. Como es bien conocido, este criterio adolece de la limitación de que nódulos más grandes pueden ser reactivos (30-40%) y, por otro lado, ganglios más pequeños, generalmente asociados a adenocarcinomas, pueden estar infiltrados. La imagen funcional, al utilizar un criterio metabólico para tipificar una adenopatía como metastásica, muestra, respecto a este propósito, una clara superioridad, con una sensibilidad (79-85%) y especificidad (89-92%) mayores que las de la TC (sensibilidad 57-61%, especificidad 77-82%)9,10. Las figuras 4 y 5 muestran 2 pacientes con afectación mediastínica homolateral y contralateral a la lesión pulmonar primaria. Los trabajos que comparan la PET/TC con la PET y/o la TC en la evaluación de la afectación ganglionar del CPCNP muestran también una mayor exactitud diagnóstica de la técnica combinada con valores entre el 78 y el 93%11-13, fundamentalmente basándose en 2 ventajas: por un lado, una mejor localización e identificación precisa de las estaciones ganglionares afectadas, que puede ser de especial interés en pacientes con variantes anatómicas, atelectasia 23/11/12 11:49:47 Tomografía por emisión de positrones/tomografía computarizada en la estadificación del cáncer de pulmón o desviación mediastínica importante; por otro, la técnica combinada evita algunos de los errores diagnósticos de la PET al localizar la actividad en estructuras vasculares mediastínicas, diferenciar entre adenopatías hiliares y mediastínicas próximas a los hilios, diferenciar entre un tumor de localización central y afectación hiliar, etc. Por tanto, podemos concluir que la PET aporta sensibilidad a la TC y la TC mejora la especificidad de la PET. No obstante, cabe reseñar que los valores de validez diagnóstica, tanto de la PET como de la PET/TC, se van a ver influidos por el tamaño que presentan los ganglios, siendo mayor la sensibilidad cuando se encuentren aumentados de tamaño (menor especificidad) y mayor la especificidad cuando presenten un tamaño normal (menor sensibilidad)13,14. Sin duda, uno los datos de mayor importancia que se desprende de estos estudios es el alto valor predictivo negativo (VPN), que alcanza el 90%, si bien el valor predictivo positivo (VPP) sigue siendo relativamente bajo (en torno al 70%). Como se ha comentado anteriormente, una de las características más importantes de la PET y la PET/TC es su elevado VPN, que permite que los pacientes con tumores T1-2 y ganglios de tamaño normal no sean sometidos a una estadificación ganglionar mediastínica invasiva cuando la PET determine la ausencia de captación de éstos, siempre y cuando el tumor primario haya demostrado su avidez por la FDG y no tenga una localización central15-17. Sin embargo, pese al valor adicional del estudio PET/ TC sobre otras técnicas de imagen en la valoración de la afectación ganglionar mediastínica, para algunos autores sigue siendo de obligado cumplimiento la confirmación histológica de los hallazgos positivos observados mediante PET/TC18,19. El algoritmo diagnóstico propuesto por estos autores se refleja en la figura 6. En la tabla 3 se recogen los datos de validez diagnóstica, en la correcta estadificación ganglionar mediastínica, obtenidos cuando se aplica el protocolo propuesto por la Sociedad Europea de Cirujanos Torácicos20 frente a los obtenidos mediante estudio de PET y la mediastinoscopia. No obstante, el VPP está sujeto a variaciones regionales en función de la prevalencia de enfermedad granulomatosa10. La técnica instrumental más utilizada para confirmar los hallazgos de la PET/TC es la mediastinoscopia. Aunque la mediastinoscopia tiene limitaciones para la valoración de algunas estaciones ganglionares (ventana aortopulmonar, espacio subcarinal), actualmente se la considera el patrón oro para confirmar la afectación ganglionar. Su sensibilidad es aproximadamente del 90%. Dado el alto VPN de la PET/TC, en los casos en los que esta exploración no objetive afectación ganglionar mediastínica se puede excluir la realización de la mediastinoscopia14. No obstante, en recientes estudios se ha visto que el VPN varía en función del tamaño del ganglio, siendo menor en los ganglios que están aumentados de tamaño. Esto podría deberse a una menor capacidad de detectar la carga tumoral baja en un volumen mayor. Este hecho ha llevado a algunos autores a establecer la necesidad de confirma- 4-9 38-101.indd 55 55 Figura 4. Estudio de tomografía por emisión de positrones/ tomografía computarizada (PET/TC) con 18F-FDG, presentando proyecciones MIP (A) y cortes transaxiales de PET (B1), TC (B2, ventana de mediastino) e imagen de fusión (B3). Masa hipermetabólica en el lóbulo superior del pulmón derecho (A) y 2 focos hipermetabólicos en mediastino en el espacio 4R (B1), que en las imágenes de la TC (B2) y de fusión (B3) se corresponden con adenopatías de 1 cm de eje corto. Hallazgos compatibles con tumor pulmonar derecho con afectación adenopática mediastínica ipsilateral. Figura 5. Estudio de tomografía por emisión de positrones/ tomografía computarizada (PET/TC) con 18F-FDG, presentando proyecciones MIP (A) y cortes transaxiales de PET (B1, C1), TC (B2, C2, ventana de mediastino) e imagen de fusión (B3, C3). Muestra una masa hipermetabólica en lóbulo superior del pulmón izquierdo (A, B) y un foco hipermetabólico en mediastino derecho, en el espacio 4R (B1), que en las imágenes de la TC (B2) y de fusión (B3) se corresponde con una adenopatía. Se observa, además, un foco hipermetabólico en la ventana aortopulmonar sobre grupo G5 (C). Hallazgos compatibles con un tumor pulmonar izquierdo con afectación adenopática mediastínica ipsi y contralateral. ción histológica en los ganglios que estén aumentados de tamaño en las imágenes de la TC independientemente de los hallazgos de la PET. A modo de resumen, podemos decir que la necesidad de estadificación ganglionar mediastínica de forma invasiva 23/11/12 11:49:48 La imagen funcional en oncología 56 PET/TC Positiva (N2-N3) Negativa (N0) Confirmación histológica EBUS/EUS Negativo Mediastinoscopia Positivo Negativo Tratamiento quirúrgico Positivo Tratamiento multimodal Figura 6. Algoritmo diagnóstico propuesto por la Sociedad Europea de Cirujanos Torácicos para la estadificación locorregional del cáncer de pulmón no microcítico. Tabla 3 − Valores de sensibilidad (S), especificidad (E), valor predictivo positivo (VPP), valor predictivo negativo (VPN) y exactitud para la estadificación mediastínica de la tomografía por emisión de positrones (PET), la mediastinoscopia y la Guía de la Sociedad Europea de Cirujanos Torácicos (ESTS) Sensibilidad (%) Especificidad (%) VPP (%) VPN (%) Exactitud (%) PET Mediastinoscopia ESTS guidelines 71 84 84 75 100 100 75 100 100 87 94 94 74 95 95 sigue siendo controvertida, si bien se aceptan las recomendaciones de la Sociedad Europea de Cirujanos Torácicos y del Colegio Americano de Cirujanos Torácicos. Así, es necesaria la confirmación histológica del estadio ganglionar mediastínico en los pacientes con ganglios aumentados de tamaño y de tamaño normal cuando sea un tumor central o asociado a adenopatías hiliares, independientemente de los hallazgos positivos o negativos evidenciados en el estudio PET/TC, así como en pacientes con tumores periféricos y ganglios mediastínicos que muestran captación de FDG. En la nueva normativa SEPAR (Sociedad Española de Neumología y Cirugía Torácica) se recomienda la incorporación de la ecobroncoscopia (EBUS) y de la ultrasonografía esofágica (EUS), para la obtención de muestra citohistológica, en el algoritmo de estadificación y se destaca la importancia de una reestadificación precisa después del tratamiento de inducción para tomar nuevas decisiones terapéuticas. Aunque no parece haber un consenso sobre cuál debe ser el estándar de una exploración ecoendoscópica, recomiendan explorar y puncionar todos los ganglios sospechosos en la PET/TC, descartando de forma secuencial N3, N2 y N1, y explorar las estaciones ganglionares N3 en todos los casos con intención curativa radical, y puncionar los ganglios ≥ 5 mm de diámetro21. 4-9 38-101.indd 56 Valoración del M La presencia de metástasis en el momento del diagnóstico es un hecho bastante frecuente en pacientes con cáncer de pulmón no microcítico, lo que obliga a excluir a estos pacientes de la posibilidad de realizar terapias con fines curativos. Por otra parte, tras el tratamiento radical, algunos pacientes desarrollan de forma precoz metástasis, lo que probablemente indicaría que en el momento del diagnóstico ya existía una diseminación micrometastásica de la enfermedad. La PET ofrece un valor adicional en la detección de metástasis en pacientes con cáncer de pulmón no microcítico potencialmente operable, por 2 motivos: por un lado, la PET ha demostrado en varios estudios que, tras una estadificación convencional negativa, es capaz de detectar metástasis no sospechadas en un 5-29% de los pacientes9,22; por otro, la PET es capaz de determinar la naturaleza de lesiones de significado incierto en las técnicas de imagen convencional23. La PET podría tener un papel preponderante en la valoración de la afectación pleural. La diferenciación entre benignidad/malignidad es primordial a la hora de determinar la resecabilidad del tumor y el posible uso de la radiote- 23/11/12 11:49:48 Tomografía por emisión de positrones/tomografía computarizada en la estadificación del cáncer de pulmón rapia. Aunque la presencia de nodularidad, engrosamiento y captación pleural son sugestivos de infiltración, tanto la TC como la RM tienen limitaciones para resolver este interrogante. Por otro lado, la toracocentesis tiene un 30-40% de resultados falsos negativos y es una técnica intervencionista24. La demostración de actividad metabólica en el engrosamiento y/o en la nodularidad pleural es sugestiva de malignidad. Gupta et al25 estudiaron a 35 pacientes con anormalidades pleurales en la TC, a los que se les realizó una PET. La sensibilidad, la especificidad, el VPP, el VPN y la exactitud diagnóstica fueron del 88,8, 94,1, 94,1, 88,8 y 91,4%, respectivamente. Erasmus et al26 aportan en su estudio valores similares. Este alto VPN de la PET podría ser útil para reducir el número de toracocentesis y biopsias por toracoscopia en los pacientes en los que el estudio de PET fuera negativo. La PET/TC es una técnica morfofuncional de “cuerpo entero” que combina la información proporcionada por las 2 técnicas, por lo que es ideal para el estudio de la enfermedad metastásica. Una exploración normal incluye desde la calota hasta la porción superior de los miembros inferiores, por lo que se incluyen las localizaciones en que con mayor frecuencia se producen metástasis en el CPCNP (suprarrenal, hueso, hígado, pulmón, tejidos blandos), con alguna excepción (cerebro) que será objeto de un comentario especial. Los pacientes con CPCNP presentan con relativa frecuencia (10-15%) adrenales aumentadas de tamaño en la TC (incidentalomas). Sin embargo, dos tercios de éstas son benignas. La información proporcionada por la PET tiene un alto rendimiento para confirmar o descartar dichas metástasis (fig. 7), lo que permite reducir el número de biopsias innecesarias27. Ante un nódulo adrenal hipermetabólico habrá que confirmar la existencia de metástasis mediante biopsia por aspiración si se trata del único hallazgo que contraindica la cirugía. Si el nódulo sólo se visualiza en la TC y es subcentimétrico (situación excepcional), hay que valorar la posibilidad de un falso negativo. Con relación a las metástasis óseas, la información proporcionada por la PET/TC tiene una sensibilidad y, sobre todo, una especificidad, muy superiores a las de la gammagrafía ósea, la cual puede ser eliminada del protocolo de estadificación cuando se dispone de PET/TC. Únicamente se debe tener en cuenta que en el estudio estándar de PET/TC no se incluyen de forma rutinaria las extremidades inferiores, pero sí en la gammagrafía ósea, por lo que en pacientes sintomáticos se recomienda ampliar el estudio PET/TC a dichas extremidades. Por otra parte, está descrita una menor actividad metabólica en las metástasis osteoblásticas, pero, sobre todo, en otros tipos tumorales como el cáncer de mama y el de próstata. Debido al menor número de falsos positivos y a la posibilidad de mostrar la afectación de tejidos blandos, el rendimiento de esta técnica se considera excelente para el estudio de este tipo de metástasis. La PET/TC también es una exploración útil para el cribado de metástasis hepáticas. La información proporcionada por la PET posee un valor añadido respecto a la obtenida 4-9 38-101.indd 57 57 Figura 7. Estudio de tomografía por emisión de positrones/ tomografía computarizada (PET/TC) con 18F-FDG, presentando proyecciones MIP (A) y cortes transaxiales de PET (B1 y C1), TC (B2 y C2) e imagen de fusión (B3 y C3). Masa hipermetabólica en lóbulo inferior del pulmón derecho (A, B) junto a un foco hipermetabólico en la glándula suprarrenal izquierda (A, C) compatibles con un tumor pulmonar derecho con una lesión metastásica única adrenal izquierda. mediante la TC, permitiendo reducir los posibles falsos positivos y confirmar los hallazgos dudosos. Las metástasis subcentimétricas pueden ser causa de falsos negativos. Con relación a las metástasis pulmonares (nódulos tumorales en el pulmón contralateral), la técnica de elección sigue siendo la TC con cortes finos, no superiores a 5 mm, y en inspiración para poder detectar nódulos < 1 cm, ya que la TC adquirida en el estudio de PET/TC se realiza con el paciente respirando y sin cortes finos. La presencia de una linfangitis carcinomatosa debe sospecharse ante la existencia en la TC de un patrón reticulonodular con engrosamiento de las líneas septales que muestra un incremento difuso de la captación con FDG. La PET/TC muestra una limitada utilidad para la valoración de las posibles metástasis cerebrales. La técnica de elección debe ser la RM, que debe realizarse en pacientes sintomáticos, pacientes con diagnóstico de adenocarcinoma o carcinoma de células grandes, pacientes con cualquier histología en estadios III y IV, susceptibles de tratamiento locorregional radical. La PET tiene una baja resolución espacial y, además, la captación intensa y fisiológica de la FDG por la cortical cerebral dificulta la objetivación de las posibles metástasis. Aunque el patrón normal de la metástasis es la visualización de un foco hipermetabólico, hay que ser precavido respecto a la valoración de los defectos ametabólicos debido a que, en ocasiones, el edema vasogénico que acompaña a la metástasis puede producir ese patrón. En ocasiones puede observarse un incremento de captación de FDG en una cuerda vocal. Este hecho se puede 23/11/12 11:49:48 58 La imagen funcional en oncología Figura 8. Estudio de tomografía por emisión de positrones/tomografía computarizada (PET/TC) con 18F-FDG, presentando proyecciones MIP (A) y cortes transaxiales de PET (B1 y C1), TC (B2, ventana de mediastino, y C2, ventana de parénquima) e imagen de fusión (B3 y C3). Se ve un área de moderada actividad metabólica en el lóbulo inferior del pulmón izquierdo (B1 y C1), que en las imágenes de la TC (B2 y C2) se corresponde con un área de infiltrado alveolar. El estudio anatomopatológico demostró que se trataba de un carcinoma bronquioloalveolar. deber a la afectación del nervio recurrente por el tumor o las adenopatías. Como consecuencia se produce una hiperutilización de la cuerda vocal sana (por compensación fisiológica), la que muestra la hipercaptación, y una parálisis de la afectada. Por último, en algunas ocasiones, la PET/TC permite objetivar la presencia de un tumor sincrónico, sobre todo a nivel colorrectal. De cualquier manera, la detección con la PET de una metástasis potencialmente resecable o cuyo descubrimiento implique que el tumor pulmonar que en un principio era resecable ya no lo sea, obliga a confirmarla mediante otras técnicas instrumentales y, a ser posible, mediante su biopsia. Carcinoma bronquioloalveolar Queremos hacer un apartado especial para el CBA debido a sus peculiaridades. La OMS3 define al CBA como un subtipo del adenocarcinoma que crece a lo largo de los septos alveolares sin evidencia de infiltración vascular, estromal o pleural y, a su vez, establece 2 subtipos histológicos: no mucinoso y mucinoso. 4-9 38-101.indd 58 Como se ha comentado anteriormente, hay una nueva clasificación de adenocarcinoma en la que el conocido como CBA se correspondería con las variantes de adenocarcinoma in situ (mucinoso/no mucinoso/mixto), adenocarcinoma invasivo predominantemente lepídico y adenocarcinoma invasivo mucinoso4. La PET/TC ha mostrado una utilidad limitada en el manejo de estos tumores, ya que la exactitud diagnóstica de ésta en las formas mucinosas es reducida, sobre todo en las lesiones hipocelulares con gran componente mucinoso, que pueden dar lugar a estudios falsamente negativos. La captación de FDG en el CBA puro es significativamente menor que en el adenocarcinoma y en el adenocarcinoma con característica de CBA, debido al patrón de crecimiento que presenta (fig. 8). Un estudio reciente28 establece una relación inversamente proporcional entre el valor estándar de captación máximo y el porcentaje del componente de CBA. Cáncer de pulmón de célula pequeña El CPCP supone aproximadamente el 10-15% de todos los cánceres de pulmón. Desde el punto de vista clínico 23/11/12 11:49:49 Tomografía por emisión de positrones/tomografía computarizada en la estadificación del cáncer de pulmón presenta una mayor agresividad que el CPCNP, con una gran tendencia a la diseminación metastásica y un pronóstico muy malo. Clásicamente, el CPCP se ha clasificado en 2 estadios, enfermedad limitada y enfermedad diseminada, si bien, actualmente, se aplica también el sistema de estadificación TNM. Al igual que en el CPCNP, la estadificación es crucial para determinar la aptitud terapéutica a seguir y constituye el factor pronóstico más importante. Las técnicas diagnósticas más utilizadas con este fin son la TC de abdomen y tórax, la TC y/o la RM para la valoración del cerebro, la gammagrafía ósea y la punción de médula ósea. El impacto de la PET/TC en la estadificación de pacientes recientemente diagnosticados de CPCP ha sido estudiado por múltiples autores, determinándose, en la mayoría de los estudios realizados, una modificación en el estadio y, por tanto, en el manejo de estos pacientes en torno al 10-33%29. La PET/TC también ha mostrado utilidad en la valoración de la respuesta al tratamiento administrado, siendo capaz de discriminar entre pacientes respondedores y no respondedores, con el consiguiente impacto en el manejo de estos últimos al permitir evitar tratamientos innecesarios. Tumores neuroendocrinos El parénquima pulmonar es la segunda localización en frecuencia de los TNE, representando el 1-2% de todas las neoplasias pulmonares. Presentan un pico de edad a los 60 años y suelen manifestarse como tumores bien diferenciados que raramente metastatizan. El pronóstico grave sólo se da en formas atípicas que presentan un alto potencial de metastatización, incluso años después de la resección del primario. La utilidad del estudio PET/TC con FDG en pacientes con TNE, fundamentalmente en formas bien diferenciadas, es limitada dado el bajo consumo de glucosa que presentan. Ello ocurre con los tumores carcinoides, que por su grado de diferenciación y actividad metabólica pueden dar exploraciones falsamente negativas. Actualmente, los radiotrazadores más utilizados con este fin son los péptidos análogos de la somatostatina (que se unen específicamente a su receptor de membrana) marcados con 68Ga-DOTA y la 18F-DOPA. Es sin duda el 68Ga-DOTApéptido el radiotrazador más prometedor para el estudio de las formas diferenciadas, dando una importante información acerca de la extensión de la enfermedad así como de la distribución y expresión de receptores de somatostatina, con las implicaciones terapéuticas que ello conlleva. Conclusión A modo de conclusión, podemos decir que la TC torácica, en la estadificación no invasiva del CPCNP, es una herramienta útil porque proporciona una información anatómi- 4-9 38-101.indd 59 59 ca muy precisa, si bien su precisión en la diferenciación entre benignidad/malignidad de las lesiones ganglionares detectadas es bastante limitada. En este sentido, la PET ha mostrado mayor sensibilidad y especificidad, tanto para la estadificación mediastínica como para la detección de metástasis a distancia. Es por ello que se ha convertido en una técnica esencial a la hora de evaluar a pacientes subsidiarios de tratamiento radical, en los que es fundamental determinar la afectación mediastínica y descartar la existencia de afectación metastásica30. Especial mención hay que hacer en los antiguos CBA, los cuales son la principal fuente de falsos negativos de la técnica, sobre todo cuando el componente mucinoso es predominante. Bibliografía 1. Sant M, Allemani C, Santaquilani M, Knijn A, Marchesi F, Capocaccia R; EURO-CARE Working Group. EUROCARE-4. Survival of cancer patients diagnosed in 1995-1999. Results and commentary. Eur J Cancer. 2009;45:931-91. 2. Youlden DR, Cramb SM, Baade PD. The International epidemiology of lung cancer geographical distribution and secular trends. J Thorac Oncol. 2008;3:819-31. 3. Travis WD, Brambilla E, Müller-Hermelink HK, Harris CC. Pathology and genetics of tumours of the lung, pleura, thymus and heart. Lyon, France: IARC Press; 2004. 4. Travis WD, Brambilla E, Noguchi M, Nicholson AG, Geisinger KR, Yatabe Y, et al. International association for the study of lung cancer/american thoracic society/european respiratory society international multidisciplinary classification of lung adenocarcinoma. J Thorac Oncol. 2011;6:244-85. 5. De Wever W, Ceyssens S, Mortelmans L, Stroobants S, Marchal G, Bogaert J, et al. Additional value of PET-CT in the staging of lung cancer: comparison with CT alone, PET alone and visual correlation of PET and CT. Eur Radiol. 2007;17:23-32. 6. Antoch G, Stattaus J, Nemat AT, Marnitz S, Beyer T, Kuehl H, et al. Non-small cell lung cancer: dual- modality PET/CT in preoperative staging. Radiology. 2003;229:526-33. 7. Bruzzi JF, Munden RF. PET/CT imaging of lung cancer. J Thorac Imaging. 2006;21:123-36. 8. Goldstraw P. The 7th edition of TNM in lung cancer: what now? J Thorac Oncol. 2009;4:671-3. 9. Rodríguez Fernández A, Gómez Río M, Llamas Elvira JM, Sánchez-Palencia Ramos A, Bellón Guardia M, Ramos Font C, et al. Diagnosis efficcacy of structural (CT) and functional (FDG-PET) imaging methods in the thoracic and extrathoracic staging of non small cell lung cancer. Clin Transl Oncol. 2007;9:32-9. 10. Sánchez Sánchez R, Rodríguez Fernández A, Gómez Río M, Alkurdi Martínez A, Castellón Rubio VE, Ramos Font C, et al. Utility of PET/CT for mediastinal staging of non-small cell lung cancer in stage III (N2). Rev Esp Med Nucl. 2011;30:211-6. 11. Halpern BS, Schiepers C, Weber WA, Crawford TL, Fuege RBJ, Phelps ME, et al. Presurgical staging of non-small cell lung cancer: positron emission tomography, integrated positron emission tomography/CT, and software image fusion. Chest. 2005;128:2289-97. 12. Shim SS, Lee KS, Kim BT, Chung MJ, Lee EJ, Han J, et al. Nonsmall cell lung cancer: prospective comparison of integrated FDG PET/CT and CT alone for preoperative staging. Radiology. 2005;236:1011-9. 23/11/12 11:49:49 60 13. Yang WY, Yu Z, Yuan S, Zhang B, Xing L, Zhao D, et al. Value of PET/CT versus enhanced CT for locoregional lymph nodes in non- small cell lung cancer. Lung Cancer. 2008;61:35-43. 14. Gould MK, Kuschner WG, Rydzak CE, Maclean CC, Demas AN, Shigemitsu H, et al. Test performance of positron emission tomography and computed tomography for mediastinal staging in patients with non-small cell lung cancer: a meta-analysis. Ann Intern Med. 2003;139:879-92. 15. Pieterman R, Van Putten JWG, Meuzelaar JJ, Mooyaart EL, Vaalburg W, Koëter GH. Preoperative staging of non-small cell lung cancer with positron emission tomography. N Engl J Med. 2000;343:254-61. 16. Farrell MA, Mc Adams HP, Herndon JE, Patz EF. Non-small cell lung cancer: FDG PET for nodal staging in patients with stage I disease. Radiology. 2000;215:886-90. 17. Al-Sarraf N, Aziz R, Gately K, Lucey J, Wilson L, Mc Govern E, et al. Pattern and predictors of occult mediastinal lymph node involvement in non-small cell lung cancer patients with negative mediastinal uptake on positron emission tomography. Eur J Cardiothoracic Surg. 2008;33:104-9. 18. Toloza EM, Harpole L, McCrory DC. Non invasive staging of non-small cell lung cancer: a review of the current evidence. Chest. 2003;123:137S-46S. 19. De Leyn P, Lardinois D, Van Schil PE, Rami-Porta R, Passlick B, Zielinski M, et al. ESTS guidelines for preoperative lymph node staging for non-small cell lung cancer. Eur J Cardiothorac Surg. 2007;32:1-8. 20. Gunluoglu MZ, Melek H, Medetoglu B, Demir A, Kara HV, Dincer SI. The validity of preoperative lymph node staging guidelines of European Society of Thoracic Surgeons in non-small-cell lung cancer patients. Eur J Cardiothorac Surg. 2011;40:280-1. 21. Sánchez de Cos J, Hernández Hernández J, Jiménez López MF, Padrones Sánchez S, Rosell Gratacós A, Rami Porta R. Normativa SEPAR sobre estadificación del cáncer de pulmón. Arch Bronconeumol. 2011:47:453-65. 4-9 38-101.indd 60 La imagen funcional en oncología 22. Saunders CA, Dussek JE, O’Doherty MJ, Maisey MN. Evaluation of fluorine-18 fluorodeoxyglucose whole body positron emission tomography imaging in the staging of lung cancer. Ann Thorac Surg. 1999;67:790-7. 23. Quint LE, Tummala S, Brisson LJ Francis IR, Krupnick AS, Kazerooni EA, et al. Distribution of distant metastases from newly diagnosed non-small cell lung cancer. Ann Thorac Surg. 1996;62:246-50. 24. Light RW, Erozan YS, Ball WC. Cells in pleural fluid. Their value in differential diagnosis. Arch Intern Med. 1973;132:854-60. 25. Gupta NC, Rogers JS, Graeber GM, Gregory JL, Waheed U, Mullet D, et al. Clinical role of F-18 fluorodeoxyglucose positron emission tomography imaging in patients with lung cancer and suspected malignant pleural effusion. Chest. 2002;122:1918-24. 26. Erasmus JJ, McAdams HP, Rossi SE, Goodman PC, Coleman RE, Patz EF. FDG PET of pleural effusions in patients with non-small cell lung cancer. AJR Am J Roentgenol. 2000;175:245-9. 27. Erasmus JJ, Patz EF, McAdams HP, Murray JG, Herndon J, Coleman RE, et al. Evaluation of adrenal masses in patients with bronchogenic carcinoma using 18F-fluorodeoxyglucose positron emission tomography. AJR Am J Roentgenol. 1997;168:1357-60. 28. Liu S, Cheng H, Yao S, Wang C, Han G, Li X, et al. The clinical application value of PET/CT in adenocarcinoma with bronchioloalveolar carcinoma features. Ann Nucl Med. 2010;24:541-7. 29. Azad A, Chionh F, ScottAM, Lee ST, Berlangieri SU, White S, et al. High impact of 18F-FDGPET on management and prognostic stratification of newly diagnosed small cell lung cancer. Mol Imaging Biol. 2010;12:433-51. 30. Silvestri GA, Gould MK, Margolis ML, Tanque LT, McCrory D, Tolozza E, et al. Noninvasive staging of non-small cell lung cancer, ACCP Evidenced-Based Clinical Practice Guidelines (2nd edition). CHEST. 2007;13 2:178S-201S. 23/11/12 11:49:49 La imagen funcional en oncología 6 Resonancia de cuerpo completo con difusión: aplicaciones oncológicas y en la evaluación de las metástasis óseas A. Luna Alcaláa,* y J.C. Vilanovab aServicio de Radiología, Clínica Las Nieves, SERCOSA (Grupo Health Time), Jaén, España bUnidad de Resonancia Magnética, Clínica Girona, Girona, España Servicio de Radiodiagnóstico, Hospital Sta. Caterina, Salt, Girona, España Departamento de Ciencias Médicas, Facultad de Medicina, Universidad de Girona, Girona, España Introducción Con el uso de un soporte complementario, la resonancia magnética (RM) ha podido formar parte de las técnicas capaces de realizar estudios del cuerpo entero. En la última década se han expandido las aplicaciones de la RM de cuerpo entero (RM-CC) en la estadificación y monitorización terapéutica oncológicas, con especial relevancia en la afectación de la médula ósea1. La RM-CC ha tenido un papel especialmente relevante en el estudio de las metástasis óseas y del mieloma, por su excelente resolución en contraste y gran capacidad de detección de lesiones óseas, incluso sin gran actividad osteolítica o metabólica1,2. Al mismo tiempo, el desarrollo de gradientes más potentes, antenas multicanal y de la imagen paralela, ha permitido que la utilización de la difusión con RM fuera del cerebro se haya convertido en algo habitual3,4. Esta técnica, que permite detectar y cuantificar el movimiento del H2O libre tisular a nivel microscópico, se ha posicionado como un robusto biomarcador oncológico4. Además, la difusión con RM se ha utilizado para varias aplicaciones del sistema osteomuscular como la caracterización del edema de médula ósea, la detección y caracterización de tumores óseos y de partes blandas, procesos infecciosos, las espondiloartropatías degenerativas e inflamatorias, y la monitorización terapéutica3,5. Además, tiene un papel prometedor en la evaluación del cartílago articular, los discos intervertebrales, la necrosis ósea y la afectación osteomuscular de enfermedades oncológicas y no oncológicas5,6. Con el desarrollo de la secuencia DWIBS (diffusion-weighted imaging with background suppression; imagen ponderada en difusión con supresión de fondo), Takahara et al7 posibilitaron la incorporación de la difusión a los protocolos de cuerpo completo. Esta secuencia utiliza el STIR como técnica de supresión grasa, lo que crea una homogénea supresión de fondo, contra la que destacan los focos hipercelulares con restricción de la difusión. Su presentación con ventana de grises invertidas crea una imagen que recuerda a la de la tomografía por emisión de positrones (PET). Con los datos existentes parece una opción válida en casos de estadificación tumoral, principalmente para la afectación ósea1,3,8-10. La información funcional que aporta tiene un futuro prometedor en la evaluación de la monitorización terapéutica y en el cribado1,3,6. En este campo hay datos prometedores en la evaluación postratamiento y de respuesta precoz de pacientes con metástasis óseas y mieloma6,11-14. De acuerdo a los datos de varias series, se puede concluir que las aplicaciones de la difusión de cuerpo entero deben realizarse junto a secuencias morfológicas y no de forma aislada1,3,6. En esta revisión vamos a repasar los conceptos técnicos y biofísicos de las secuencias de difusión, así como algunas de las bases para el diseño de secuencias y su cuantificación. En una segunda parte, nos centraremos en las aplicaciones en cuerpo entero de la difusión, con especial atención a la experiencia existente en patología de la médula ósea. Bases biofísicas de la difusión con resonancia magnética El concepto de la difusión se refiere al movimiento aleatorio de las moléculas de gases o líquidos a través de su agitación térmica. En el H2O puro, las colisiones entre las moléculas dan lugar a un movimiento aleatorio, sin dirección predefinida, llamado movimiento browniano. Si se modela este desplazamiento como un movimiento *Autor para correspondencia. Correo electrónico: aluna70@sercosa.com (A. Luna Alcalá). 4-9 38-101.indd 61 23/11/12 11:49:49 La imagen funcional en oncología 62 Tabla 1 − Secuencias DWIBS (imagen ponderada en difusión con supresión de fondo) realizadas en nuestros centros en 1,5 y 3T Tipo de secuencia/ Valores b TR/TE Resolución Sincronización factor de imagen (s/mm2) (ms) (mm3) paralela DWIBS 3T SS EPI/factor 2 0-1.000 5.000/55 2,5 × 2,5 × 7 DWIBS 1,5T SS EPI/factor 2 0-1.000 632/60 3 × 3 × 7 Respiración libre Respiración libre Técnica de Evaluación supresión de la imagen grasa STIR (TI: 260 ms) STIR (TI: 160 ms) ADC ADC TE: tiempo de eco; TR: tiempo de repetición. aleatorio, su medida refleja el desplazamiento efectivo de las moléculas que pueden trasladarse en un período efectivo. En los tejidos biológicos hay una gran posibilidad de que las moléculas de H2O interactúen con membranas celulares y macromoléculas que impedirán o limitarán ese desplazamiento. De esta manera, el cálculo de este movimiento del H2O libre reflejará la composición tisular4. La difusión RM aporta información funcional acerca de la composición tisular distinta de la información morfológica obtenida con secuencias convencionales. Esta técnica permite el estudio in vivo del desplazamiento efectivo de las moléculas de H2O en un tiempo dado. Incluso es posible realizar mediciones de los movimientos de la difusión del H2O mediante el cálculo del coeficiente de difusión aparente (ADC). Con la tecnología disponible en este momento se puede medir la difusión en una fracción temporal de entre 40 y 80 ms, con una resolución espacial de milímetros4. La difusión tisular in vivo se encuentra influenciada por varios factores, como temperatura, organización y estructura del tejido, intercambio de agua entre los compartimentos intra y extracelular, densidad celular, flujo, perfusión y movimiento macroscópico5. La temperatura no tiene una relevancia importante en la medición de la difusión del H2O libre con RM. El movimiento macroscópico puede compensarse con las técnicas de corrección de movimiento y sincronismo. La influencia del flujo y la perfusión se puede reducir si la señal de los valores b inferiores a 100 s/mm2 se elimina de las cuantificaciones del ADC o, incluso mejor, si se utiliza un modelo bicompartimental de la difusión que permite separar la perfusión de la difusión real15. El resto de factores limitantes de la difusión del H2O libre en el espacio extracelular se relaciona con las características de las células y la estructura tisular. Hay una importante correlación negativa entre los valores ADC y la densidad y tamaño celulares dentro de un tejido, como se ha demostrado en varios órganos, lo que ha convertido a la difusión con RM en un robusto biomarcador oncológico5,15. Sin embargo, esta correlación es más obvia en tumores como los gliomas, tumores de células redondas o linfomas que en adenocarcinomas5. Esta variabilidad se debe a que cada tumor y tejido demuestran diferentes 4-9 38-101.indd 62 descensos de señal de la difusión de manera multiexponencial sobre un amplio rango de valores b, y a que las bases biofísicas de la difusión no se conocen de forma completa en el momento actual15. De cualquier modo, las áreas más hipercelulares y, por tanto, con mayor número de componentes intracelulares y membranas celulares, demuestran una mayor restricción de la difusión que las zonas con pérdida de la integridad celular, como pueden ser las áreas de necrosis. Bases técnicas de la difusión con resonancia magnética El movimiento browniano es dependiente de la temperatura, y en los tejidos biológicos éste no es realmente aleatorio, ya que depende de la estructura del tejido. En 1965, Stejskal and Tanner introdujeron por primera vez una secuencia de RM sensible al movimiento browniano in vivo15. Aplicaron 2 gradientes simétricos de polaridad opuesta a una secuencia SE ponderada en T2 (pulso de radiofrecuencia de 90º seguido por otro pulso de radiofrecuencia de 180º), uno de ellos previo al pulso de 180º de la secuencia SE y otro posterior al pulso de 180º (fig. 1). Estos gradientes provocaban un desfase de la señal de los espines en movimiento. Tras la excitación de radiofrecuencia de 90º se aplica el primer gradiente, que produce un desfase en todos los espines proporcional al área del gradiente. Tras este primer gradiente, los espines se mueven libremente. Los espines estáticos permanecen en la misma posición, mientras que los espines en movimiento cambian su posición relativa. Al mismo tiempo se aplica un pulso de 180º cambiando la fase de todos los espines en 180º. La aplicación del segundo gradiente tras el pulso de 180º solamente producirá el refase de los protones que tengan la misma posición a la presentada previa al primer gradiente. Los espines estáticos tras el segundo gradiente se encuentran en la misma situación que con el pulso de 90º, evitando cualquier efecto T2. Los espines dinámicos no recuperan la fase tras el segundo gradiente, por que han cambiado su posición. Además, estos gradientes introdu- 23/11/12 11:49:49 Resonancia de cuerpo completo con difusión: aplicaciones oncológicas y en la evaluación de las metástasis óseas 63 A B Figura 1. La porción superior de esta figura representa el esquema de la secuencia de difusión de Stejskal y Tanner. Esta secuencia se basa en 2 gradientes de polaridad opuesta que producen un desfase de la señal de los espines en movimiento, lo que permite que sea sensible al movimiento browniano del H2O en aplicaciones in vivo. La porción inferior de la figura pone de manifiesto la obtención de la dirección de difusión. Se puede apreciar que es posible obtener la difusión en cualquier dirección del espacio cambiando la intensidad de los gradientes X, Y o Z. Dxyz: dirección de la difusión en los 3 ejes del espacio; RF: radiofrecuencia; TE: tiempo de eco. Cedida por Javier Sánchez, científico clínico de Philips Healthcare Ibérica. C D cen un mayor desfase entre los espines. Por ello, la señal adquirida de los espines con desplazamiento es menor que la de los estáticos (fig. 2). En la secuencia de StejskalTanner, la pérdida de señal producida por el desfase de los espines se puede controlar por el factor de difusión b, que depende de los parámetros de adquisición: b = g2 G2 d2 (D – d/3) donde g es la constante giromagnética (42,57 MHz/T, para los protones); G representa la intensidad del gradiente; d es el tiempo de aplicación de los gradientes lobulares, y D representa la separación entre los gradientes aplicados. El factor b se influencia principalmente por el área del gradiente, ya que a mayor área del gradiente los espines se desfasan más y el descenso de la señal de la difusión por su movimiento será también mayor. Por ello, para obtener valores b más altos lo mejor es aumentar el área de los gradientes aplicados. Además, es preferible acortar el TE tanto como sea posible para reducir la pérdida de señal debida al descenso del T2. Otro factor a considerar en la secuencia de difusión es la dirección de la difusión que depende de la estructura tisular. El área de cada uno de los gradientes de polaridad opuesta se puede originar con diferentes intensidades en cada dirección del espacio. Cambiando el área en el eje X, Y o Z es posible conseguir la difusión en la dirección deseada (fig. 2A). Por ello, si no se necesita estudiar la estructura tisular, sino tan sólo el movimiento del H2O libre, sólo se necesita obtener 3 direcciones ortogo- 4-9 38-101.indd 63 Figura 2. Representación esquemática de la evolución en fase de los espines estáticos y móviles durante la secuencia de Stejskal y Tanner. Tras la excitación de radiofrecuencia representada por un pulso de 90º (A), se produce un desfase de todos los espines de manera proporcional al área del primer gradiente de desfase aplicado (B). Después de este gradiente, los espines evolucionan de manera libre. Los espines estáticos se hallan en la misma posición, mientras que los móviles cambian su posición relativa (C). Al mismo tiempo, la aplicación de un pulso de 180º provoca el cambio en fase de todos los espines también en 180º. Después, la aplicación de un segundo gradiente de desfase de la misma intensidad que el primero, pero de polaridad opuesta, provoca que los espines móviles no recuperen la fase por el cambio en su posición relativa entre ambos gradientes, mientras que los espines estáticos no modifican su posición (D). Además, ambos gradientes incrementan el desfase entre los espines. Como resultado, la señal adquirida del movimiento promedio de los espines es más baja que la resultante de uno solo de los espines estáticos. Cedida por Javier Sánchez, científico clínico de Philips Healthcare Ibérica. nales de la difusión, consiguiendo una imagen combinada de las 3, llamada imagen isotrópica, que permite el cálculo del ADC. La imagen isotrópica representa el efecto promedio del movimiento del H2O libre en un tejido isotrópico, independientemente de la dirección de difusión, que es una propiedad invariable de los tejidos isotrópicos no relacionada con la dirección de la difusión aplicada durante 23/11/12 11:49:50 La imagen funcional en oncología 64 la adquisición. Sin embargo, cuando se requiere conocer la organización tisular es necesario calcular si el H2O libre difunde de forma predominante en alguna dirección6-15. Si se quiere obtener información de la dirección privilegiada de la difusión deben obtenerse, al menos, 6 direcciones mediante el tensor de difusión (DTI), que tiene poca relevancia actual fuera del cerebro. Secuencias de difusión con resonancia magnética En el momento actual, la estrategia más utilizada en las adquisiciones de difusión es la basada en secuencias EPI (echo planar imaging), bien de disparo único o múltiple, estas últimas también conocidas como segmentadas. Se pueden considerar a las secuencias SS-EPI como la primera opción para las aplicaciones fuera del cerebro, incluyendo los estudios de cuerpo completo. Estas secuencias son muy rápidas y poco sensibles al movimiento permitiendo, al mismo tiempo, una gran cobertura anatómica. Además disponen de una buena relación señal-ruido (RSR) con baja deposición de energía, ya que se adquieren varios ecos tras el pulso único de excitación. Para evitar los artefactos de susceptibilidad, que producen por ejemplo las interfases aire-tejido o huesopartes blandas, o los materiales metálicos, y la distorsión geométrica típica de esta secuencia, es imprescindible utilizar la imagen paralela y la fuerza máxima de los gradientes1,15. La aproximación MS-EPI reduce también los artefactos de susceptibilidad, aunque incrementa la sensibilidad a los artefactos de movimiento y el tiempo de adquisición. En las secuencias MS-EPI es posible utilizar una aplicación especial conocida como PROPELLER, que organiza la adquisición segmentada de una forma radial alrededor del centro del espacio k, siendo menos sensible a artefactos de movimiento y reduciendo la necesidad de sincronizar la adquisición15. También se han utilizado secuencias RARE o HASTE, que son muy rápidas con menor sensibilidad a los artefactos de susceptibilidad. Sin embargo se encuentran limitadas por su pobre RSR y la típica borrosidad en la dirección de la codificación de fase, precisando de un tren de ecos mayor que el de las secuencias EPI y de varias repeticiones para obtener una calidad clínica5. La utilización de la tecnología PROPELLER en este tipo de secuencias también incrementa su solidez y reproducibilidad. Asimismo se han utilizado secuencias SSFP para la difusión del sistema osteomuscular, sobre todo en la columna vertebral. Esta aproximación utiliza sólo un gradiente de difusión en cada TR (gradiente monopolar) que lleva a la potenciación en difusión de varios ecos consecutivos (ecos de espín o ecos estimulados) en condiciones de estado estacionario. Estas secuencias son rápidas e insensibles al movimiento, aunque la cuantificación ADC es difícil, ya que es complicado determinar el valor b empleado, que habitualmente es bajo. La más común es la conocida como PSIF, que es una secuencia FISP invertida5. 4-9 38-101.indd 64 Técnicas de supresión grasa en las secuencias de difusión Lo más adecuado para obtener la mejor RSR posible en un tiempo de adquisición corto es utilizar técnicas selectivas espectrales de supresión grasa como SPIR o SPAIR15. Estas técnicas se diferencian en el pulso de inversión aplicado, que en ambas se sintoniza con la frecuencia de la grasa para saturar la señal de ésta antes de la adquisición. Estas técnicas de saturación espectral son muy sensibles a las variaciones del campo magnético, lo que hace necesario aplicar una homogeneización localizada del campo magnético en el área de estudio. En los casos donde no es posible una homogeneización correcta, es preferible utilizar como supresión grasa el STIR15. El problema es que esta técnica de supresión grasa tiene una menor RSR, incrementando el número de repeticiones necesarias para obtener una resolución espacial similar a las adquisiciones con saturación espectral de la grasa. La difusión con STIR ha tenido mucha extensión gracias a las aplicaciones de cuerpo completo, en la secuencia conocida como DWIBS6,7. Esta secuencia tiene menos problemas para evitar los problemas de homogeneidad del campo y presenta una gran sensibilidad para detectar áreas hipercelulares contra un fondo suprimido. Además permite el estudio de regiones anatómicas mayores que las secuencias de difusión con saturación espectral de la grasa, por su menor sensibilidad a las inhomogeneidades del campo magnético. Por todo ello, su uso se ha centrado principalmente en aplicaciones oncológicas, principalmente de varias regiones anatómicas o incluso del cuerpo completo. Sincronismo Las secuencias DWIBS se suelen realizar con respiración libre y varias repeticiones. Otro tipo de secuencias de difusión en territorio abdominal o torácico requieren del uso de sincronismo respiratorio, apnea o econavegadores. El sincronismo cardíaco puede ser necesario en las adquisiciones torácicas. Cuantificación El ADC representa el descenso exponencial de la señal de difusión mientras se incrementa el valor b. El cálculo del ADC compensa el efecto T2 en la evaluación de la restricción del movimiento del H2O, conocido como efecto T2 shine-through, una de las fuentes de error más comunes en la difusión3,9. Para conseguir una estimación adecuada del ADC es necesario adquirir al menos 2 valores b, aunque se puede obtener una mejor estimación cuando se adquieren más de 2 valores b. El rango completo de valores b se ajusta a un modelo monoexponencial de descenso de la señal de la difusión, donde la constante de descenso representa el valor ADC estimado. Aunque se pueden utilizar modelos de análisis más sofisticados del descenso de señal de la difusión, como el movimiento incoherente intravoxel 23/11/12 11:49:50 Resonancia de cuerpo completo con difusión: aplicaciones oncológicas y en la evaluación de las metástasis óseas (IVIM), que permite medir la perfusión a partir de la señal de difusión15, el modelo monoexponencial de la difusión es el mejor preparado para las aplicaciones clínicas actuales. Medidas y herramientas de cuantificación El ADC habitualmente se mide dibujando una o varias regiones de interés (ROI), proceso operador dependiente y no estandarizado. Tampoco hay un consenso sobre la medida del ADC más válida, siendo frecuente el uso del valor medio, mediana o mínimo6,15. La medida más utilizada es el ADC medio, que representa la magnitud promedio del movimiento de las moléculas de H2O en un volumen tisular, aunque no refleja la heterogeneidad de las lesiones. Más práctico es el uso de los histogramas para representar la heterogeneidad del ADC dentro de una ROI. Los histogramas permiten la diferenciación de los componentes de lesiones con ADC medio, similar pero con distinta distribución de los valores ADC6. Recientemente, se han empezado a utilizar programas de software complejos para comparar los cambios en el ADC con el tratamiento, conocidos como mapas funcionales de difusión o mapas paramétricos de ADC6. Consideraciones técnicas de los estudios de resonancia de cuerpo completo con difusión La posibilidad de realizar estudios de resonancia de cuerpo completo con difusión (RM-CC-D) en la última década ha abierto nuevas puertas a sus aplicaciones, especialmente en oncología. Se puede realizar con la antena integrada de cuerpo o con múltiples antenas multicanal asociadas. Se obtienen varias estaciones, dependiendo del campo de estudio, con desplazamiento automático de la mesa, desde la cabeza a los pies. En un principio, tan sólo se utilizaban secuencias morfológicas, pero desde hace unos años es posible realizar RM-CC-D utilizando secuencias DWIBS, lo que proporciona nuevas capacidades funcionales a los estudios morfológicos iniciales. Incluso es posible realizar estudios dinámicos de perfusión de forma selectiva en alguna de las estaciones. Habitualmente, las adquisiciones con DWIBS se realizan en axial en 4 o 5 estaciones, dependiendo de la altura del paciente, incluyendo: cabeza-cuello, tórax, abdomen, pelvis y muslos. Con la última generación de tomógrafos de RM, es posible realizar la adquisición en coronal utilizando factores muy altos de imagen paralela, con la potencialidad de disminuir tanto el tiempo de adquisición como el número de estaciones. Al menos se obtiene un valor b alto entre 600 y 1.400 s/mm2, dependiendo de la aplicación clínica y el tipo de tomógrafo utilizado, aplicando gradientes en los ejes X, Y y Z. Algunos autores utilizan adquisiciones de RM-CC-D con secuencias de difusión con técnicas de saturación espectral de la grasa en vez de STIR, aunque son poco frecuentes16. Hay controversia sobre la necesidad de adquirir además un valor b bajo, habitualmente 0 s/mm2, que permite calcular el ADC. Nosotros somos partidarios de adquirir 2 valores b, ya que las ventajas de disponer del ADC superan las del aumento del tiempo de adquisición. Todas las adquisicio- 4-9 38-101.indd 65 65 nes se realizan con mayor frecuencia en plano axial para minimizar la distorsión geométrica típica de las secuencias EPI, con un grosor de corte de entre 4 y 7 mm sin separación entre cortes, y de una forma intercalada. La secuencia DWIBS en cada estación puede durar entre 90 y 180 s, dependiendo del número de señales promedio adquiridas, ya que suele ser necesario adquirir de 2 a 5 por la baja resolución espacial intrínseca de esta secuencia. La aproximación más extendida es la de respiración libre, ya que reduce el cambio de posición de las referencias anatómicas respecto a las secuencias morfológicas17. A este respecto es importante señalar que en las diversas series evaluando distintas aplicaciones de la RM-CC-D se ha incidido de forma prácticamente unánime en la necesidad de integrar la adquisición DWIBS con secuencias morfológicas, ya que se mejora la localización anatómica y detección y caracterización de lesiones1-3,9,18. Algunos autores prefieren realizar las adquisiciones DWIBS con sincronismo respiratorio y/o cardíaco, ya que se incrementa la calidad de las estaciones de tórax y abdomen, evitando sobre todo los artefactos relacionados con el latido cardíaco y el movimiento del diafragma aunque, eso sí, incrementando de manera importante el tiempo de adquisición15,17. Las adquisiciones en apnea son poco habituales por limitaciones en el grosor de corte17. La mayor parte de las series que utilizan estudios RMCC-D se ha realizado con imanes de 1,5T. Recientemente se ha empezado a explorar las posibilidades de equipos de 3T, siendo muy atractiva su mayor resolución espacial, permitiendo disminuir el tiempo de adquisición, si se utiliza la misma resolución espacial que en un tomógrafo de 1,5T, o alternativamente incrementar la resolución espacial en el mismo tiempo de adquisición que en 1,5T1 (fig. 3). La mayor sensibilidad de los imanes de 3T a la susceptibilidad magnética, distorsión geométrica y artefactos de movimiento y respiratorios, hace que la optimización del diseño de la secuencia DWIBS sea crítica, siendo aconsejable utilizar técnicas de supresión grasa avanzadas, como la técnica de inversión de gradientes de corte selectivo (slice-selective gradient-reversal) y la tecnología de fuentes múltiples de transmisión de radiofrecuencia. Como se ha comentado anteriormente, la secuencia DWIBS utiliza el STIR como técnica de supresión grasa, consiguiendo una buena supresión de fondo, que incrementa la detección de lesiones. Se debe tener en cuenta que hay estructuras normales hipercelulares que suelen presentar una relativa restricción de la difusión, como: cerebro, médula espinal, nervios periféricos, glándulas salivares, mucosa intestinal, anillo linfático de Waldeyer, bazo, adenopatías, riñones, adrenales, próstata, testículos, ovarios, endometrio y médula ósea. Estas estructuras deben reconocerse como posibles áreas de restricción, para evitar un incremento de los falsos positivos4 (fig. 3). Tras la adquisición de las distintas estaciones es necesario su posproceso en la estación de trabajo. Se realiza la unión de todas las adquisiciones en plano axial, pudiendo presentarse como imágenes de cuerpo completo en plano sagital o, de forma más habitual, en el coronal. Se pueden realizar reconstrucciones multiplanares o proyecciones de 23/11/12 11:49:50 66 La imagen funcional en oncología poco, incluso se puede realizar fusión con otras técnicas de imagen como la TC o la PET. Si se han adquirido 2 valores b se pueden realizar cuantificaciones ADC. Se debe tener en cuenta que los valores ADC obtenidos de secuencias DWIBS son habitualmente más bajos, tanto en tejidos normales como en lesiones, que los obtenidos con secuencias de difusión con técnicas de supresión selectiva de la grasa19. Aplicaciones oncológicas de los estudios de resonancia de cuerpo completo con difusión Diseño de los protocolos Figura 3. Resonancia de cuerpo completo con difusión en 1,5 y 3T. Proyección de máxima intensidad (MIP) coronal de adquisición DWIBS de cuerpo completo y MIP sagital de columna cervical en un voluntario sano en 1,5 y 3T. Ambas secuencias se realizaron con un valor b de 1.000 s/mm2 y el mismo tiempo de adquisición. La adquisición en 3T tiene mayor resolución espacial y mayor susceptibilidad magnética y distorsión, como se aprecia en la columna cervical (flechas amarillas). Se identificó un ganglio axilar derecho no patológico de forma incidental (flechas rojas). máxima intensidad del volumen completo o de manera parcial. Se suele aplicar una inversión de la escala de grises para presentar las imágenes de manera similar a la PET y con la misma semiología, demostrándose las áreas de restricción de la difusión como focos hipointensos. Si se realizan estudios comparativos del mismo individuo en el tiempo, por ejemplo en casos de monitorización terapéutica, idealmente deben normalizarse las imágenes originales antes de realizar reconstrucciones para la comparación lo más fiable posible, o al menos definir la ventana de visualización respecto a órganos que no cambien sus características entre los estudios comparados5,6. Además, es posible fusionar las series morfológicas con la difusión, lo que permite aumentar la precisión en la localización anatómica. Desde hace 4-9 38-101.indd 66 La RM-CC con secuencias morfológicas se ha utilizado con éxito en la última década para la estadificación oncológica, el seguimiento terapéutico y la detección de recidiva local o a distancia1-3,9. La secuencia DWIBS se ha integrado en la mayor parte de los protocolos, ya que añade una información funcional adicional. Los protocolos de RM-CC deben ajustarse en secuencias y extensión a la patología e indicación clínica del estudio, con la ventaja de poder individualizarse llegado el caso. Por ejemplo, en patología ósea osteomuscular deben incluirse secuencias potenciadas en T1, T2 y STIR, además de la secuencia de difusión, incluyendo secuencias sagitales selectivas de la columna completa si se tiene que estudiar el esqueleto axial (imprescindibles por ejemplo en la estadificación del mieloma múltiple) y valorando si es necesario o no incluir las extremidades (p. ej., se pueden obviar en la estadificación ósea del carcinoma de mama o próstata por la baja prevalencia de metástasis ósea más allá de la porción proximal del fémur)2,20. En caso de sospecha de metástasis óseas, en nuestra experiencia se puede obviar el contraste. Sin embargo, en la estadificación de tumores pélvicos, abdominales o torácicos, deben adquirirse secuencias de alta resolución para la estadificación local en la localización del tumor primario, realizar secuencias dinámicas hepáticas en caso de alta probabilidad de metástasis a este nivel (p. ej., en la estadificación del carcinoma colorrectal o pulmonar), siendo suficiente, habitualmente, con una extensión del estudio de cráneo a muslos. Para la valoración de metástasis cerebrales es fundamental la adquisición de una secuencia potenciada en T1 con supresión grasa poscontraste6-18. También es importante en el diseño de los protocolos tener en cuenta el equipo en el que se realizan los estudios, si se hace con la bobina integrada de cuerpo o con múltiples antenas multicanal, el número de antenas disponibles y cuántas de ellas podemos conectar al mismo tiempo. Aplicaciones clínicas La RM-CC se ha utilizado desde sus primeros momentos en la estadificación oncológica, mejorando su sensibilidad con la adición de las secuencias de difusión3. La secuencia DWIBS permite detectar focos tumorales milimétricos que pueden pasar desapercibidos en las secuencias mor- 23/11/12 11:49:50 Resonancia de cuerpo completo con difusión: aplicaciones oncológicas y en la evaluación de las metástasis óseas fológicas; esto es especialmente relevante en la detección de adenopatías, metástasis peritoneales y hepáticas. Las metástasis aparecen como focos de restricción de la difusión contra un fondo suprimido. Habitualmente, el grado de restricción aumenta de forma paralela al grado de indiferenciación histológica y agresividad biológica1,3. Sin embargo, debe tenerse en cuenta que la presencia de edema tumoral, necrosis o degeneración quística puede reducir el grado de restricción5,6. Por ello es conveniente el uso de mapas ADC, que permiten cuantificar el grado de restricción de la difusión de una lesión y diferenciar el comportamiento de sus distintos componentes. La detección de metástasis pulmonares es la más problemática para la RM, sobre todo teniendo en cuenta que los artefactos por movimientos respiratorios y la pulsación cardíaca limitan su detección en los lóbulos inferiores15. Para minimizar esta limitación, en tumores con incidencia alta de metástasis pulmonares se puede realizar una adquisición complementaria de difusión con supresión selectiva de la grasa o una secuencia sangre negra con doble inversión potenciada en T1 o STIR, utilizando sincronismo respiratorio y cardíaco, o alternativamente secuencias 3D con voxel isotrópico y supresión selectiva de la grasa poscontraste en apnea. La secuencia DWIBS tiene una gran capacidad para la detección de ganglios linfáticos y adenopatías patológicas, incluso de muy pequeño tamaño3. Un tema candente es la posibilidad de diferenciar las adenopatías patológicas de las normales mediante cuantificaciones ADC. Datos recientes apoyan que esta distinción es posible para metástasis ganglionares de tumores de cabeza y cuello, carcinoma de pulmón, ginecológicos, de próstata y recto15,19. Sin embargo, la mayor parte de estas series utilizó secuencias de difusión con supresión selectiva de la grasa y dirigidas a un área anatómica concreta y, por ello, con mayor resolución espacial que las adquisiciones DWIBS convencionales, y en el caso de algunos tumores los resultados sólo pueden considerarse como preliminares. En la estadificación inicial del linfoma, las secuencias DWIBS de cuerpo completo incrementan la tasa de detección de lesiones sobre los protocolos RM sólo con secuencias morfológicas3 (fig. 4). Además, en los ganglios aumentados de tamaño, la cuantificación ADC permite la diferenciación entre los inflamatorios y los que presentan infiltración linfomatosa21. Una serie reciente ha demostrado una correlación excelente entre la PET/TC y la RM-CC-D, utilizando tan sólo una secuencia de difusión con saturación espectral de la grasa y cuantificaciones ADC, en la valoración de la afectación ganglionar y orgánica del linfoma difuso de células B grandes22. Existe poca experiencia en la búsqueda de tumor primario oculto en pacientes con metástasis, aunque en una serie reciente la RM-CC-D demostró una sensibilidad del 95,8% y una especificidad del 90%8 (fig. 5). Otras aplicaciones de los estudios de RM-CC-D han sido la valoración de respuesta a tratamiento (figs. 4 y 6) y la detección de recidiva tumoral (fig. 7)1,3,9. Por tanto, las aplicaciones de la RM-CC y RM-CC-D entran en campos habitualmente reservados para la PET y la PET/TC, lo que ha hecho inevi- 4-9 38-101.indd 67 67 table la comparación de ambas técnicas. Por el momento se ha realizado de forma limitada, tanto en el número de pacientes como de indicaciones, y la mayor parte de ellas con importantes limitaciones metodológicas, sobre todo teniendo en cuenta que no se dispone de un verdadero patrón de oro, ya que en los casos de neoplasias diseminadas no se puede obtener muestras histológicas de todas las lesiones9. En general, los datos existentes apoyan la superioridad de la PET/TC en la estadificación de distintos tumores al compararla con los estudios RM-CC o RM-CC-D de forma aislada. Sin embargo, en una serie reciente que comparó directamente el número de lesiones detectadas en 43 pacientes oncológicos, se demostró una mayor tasa de detección media de una adquisición DWIBS de cuerpo completo frente a la PET/TC, aunque de forma no significativa23. En las pocas series disponibles comparando la detección de metástasis mediante RM-CC-D frente a PET/ TC, la sensibilidad es algo superior para la RM (fig. 8)9. En cualquier caso, con los datos existentes parecen tener un papel complementario, ya que exploran propiedades funcionales diferentes de los tumores17,18. Ventajas inherentes a la RM son la no utilización de radiación ionizante, su mayor rapidez respecto a la PET e incluso su mayor resolución espacial1. Además, la evaluación de tumores de bajo grado, mucinosos y bien diferenciados que muestran bajo consumo de glucosa, puede beneficiarse de su estudio con RM1,3,9. En el caso concreto de los tumores uroteliales, la RM con difusión es superior a la PET, debido a la acumulación en orina del isótopo 18-FDG17. En localizaciones específicas como la médula ósea, hígado, peritoneo y cerebro la RM-CC-D permite una estadificación más precisa que la PET y/o la PET/TC3. En este sentido, una serie reciente ha demostrado una sensibilidad del 82% y una especificidad del 97% para la RM-CC-D en la estadificación de pacientes con melanoma maligno avanzado, superiores a los de la PET/TC, que fueron concretamente del 72,8 y el 92,7%, respectivamente24. En esta serie, la RM fue claramente superior en la evaluación de la médula ósea, hígado, tejido subcutáneo y afectación peritoneal. Por los artefactos respiratorios y de pulsación cardíaca, la PET es superior a la RM en la evaluación de lesiones esplénicas o paracardíacas, aunque se puede considerar que tienen resultados equivalentes en la detección global de metástasis pulmonares17,18. En la estadificación del carcinoma de pulmón no microcítico, las series disponibles demuestran una sensibilidad y precisión diagnóstica similares para ambos métodos, con un menor número de falsos positivos para la RM con difusión9,15,18. Sin embargo, en la serie de Heusner et al, donde se compararon ambas técnicas en la estadificación del cáncer de mama en 20 pacientes, la sensibilidad fue equivalente pero la especificidad y el valor predictivo positivo fueron significativamente superiores para la PET/TC debido, sobre todo, a falsos positivos con la RM-CC-D en ganglios linfáticos y en lesiones óseas benignas25. En cuanto a la estadificación N (ganglionar), hay un alto grado de concordancia en los resultados para la RM-CC-D y la PET/TC en la estadificación del linfoma difuso de células B grandes, en 23/11/12 11:49:50 La imagen funcional en oncología 68 A B C Figura 4. Monitorización terapéutica de linfoma no hodgkiniano. A, B y C) Proyección de máxima intensidad parcial coronal de una secuencia DWIBS pretratamiento y a las 4 y 8 semanas del inicio de la quimioterapia, respectivamente. A) Se identifican 3 lesiones hepáticas y afectación ganglionar mediastínica. B) Tras 4 semanas de quimioterapia se siguen apreciando las mismas lesiones con un volumen similar, pero con menor restricción de la difusión visualmente, indicativo de respuesta precoz favorable, como se confirma con la desaparición de unas y disminución de volumen de otras de las lesiones a los 2 meses posquimioterapia en relación con respuesta parcial. En este caso hubo un aumento progresivo de los valores del coeficiente de difusión aparente de las lesiones hepáticas y mediastínicas, que confirmaba la respuesta al tratamiento. A y C) Se aprecia de forma incidental la restricción de la difusión normal de los testículos. la estadificación ganglionar del carcinoma de cérvix y en la detección y cribado ganglionar del carcinoma colorrectal15,17,22. La PET/TC no puede detectar ganglios necróticos ni metástasis submicroscópicas, y además demuestra una tasa importante de falsos positivos debido a linfadenitis inflamatoria 15. Como ya se ha comentado, la RM-CC-D presenta más limitaciones en la detección de adenopatías, principalmente relacionadas con artefactos respiratorios a nivel mediastínico, aunque presenta un papel potencial en la diferenciación entre ganglios benignos y metastásicos que necesita ser confirmado. 4-9 38-101.indd 68 Evaluación de las metástasis óseas con resonancia de cuerpo completo con difusión Los datos disponibles apoyan la utilidad de la secuencia DWIBS en los protocolos de RM-CC en la detección de las metástasis óseas (figs. 6-9)9. La difusión con RM es muy sensible en la detección de las lesiones de médula ósea, especialmente de las malignas, incluso antes que las secuencias morfológicas. Un metaanálisis reciente ha confirmado la excelente sensibilidad en la detección de metástasis óseas de la RM-CC-D, aunque a costa de una 23/11/12 11:49:51 Resonancia de cuerpo completo con difusión: aplicaciones oncológicas y en la evaluación de las metástasis óseas A B Figura 5. Varón de 58 años, con lumbalgia intensa y aplastamiento de L5 agudo. A) Proyección de máxima intensidad sagital de la secuencia DWIBS que pone de manifiesto la restricción severa de L5 (asterisco) y focos adicionales en C7 y D6 (flechas), sugiriendo un origen metastásico. B) La secuencia de fusión del DWIBS con b = 1.000 s/mm2 y la secuencia T2 de turbo espín eco pone de manifiesto un área de restricción de la difusión basal derecha prostática en relación con un primario prostático, anteriormente no conocido. menor especificidad de los protocolos de RM-CC utilizando tan sólo secuencias morfológicas10. De cualquier modo, los resultados de la especificidad de las secuencias DWIBS 4-9 38-101.indd 69 A 69 B Figura 6. Seguimiento posterapéutico de metástasis lumbar de carcinoma de mama. A y B) Proyección de máxima intensidad coronal de una secuencia DWIBS antes y después del tratamiento con anticuerpos monoclonales de una metástasis ósea lumbar (flechas), que desaparece completamente en el control posterapéutico. En hemitórax derecho hay un artefacto de susceptibilidad magnética por el expansor mamario (asterisco en B). son contradictorios, ya que la mayor parte de las series se han centrado en la detección de metástasis óseas, utilizando tan sólo un análisis visual. La RM-CC-D es superior a la gammagrafía en la estadificación tumoral ósea, por tanto, con el potencial para sustituirla como herramienta diagnóstica de primer orden (fig. 7)2,10,20. Takenaka et al compararon la PET/TC y la RM-CC-D en la valoración de las metástasis óseas del cáncer de pulmón no microcítico, con sensibilidad y especificidad similares. En la comparación aislada de las secuencias de difusión y morfológicas de RM había una diferencia significativa en la sensibilidad a favor de la difusión, con una especificidad similar y muy alta para ambas, aunque los mejores resultados se obtenían valorando las 2 en conjunto. Además, la RM-CC-D ha demostrado ser tan efectiva como la PET/TC con 11C-colina en la detección de metástasis óseas de carcinoma de próstata26. Una limitación evidente de la RM-CC-D en la evaluación de la médula ósea son las lesiones osteoblásticas, que aparecen como hipointensas con valores b altos por 23/11/12 11:49:51 La imagen funcional en oncología 70 A B A Figura 7. Metástasis óseas de carcinoma de próstata. A) Gammagrafía ósea con dudosa afectación metastásica en pelvis y fémur derecho. B) Sin embargo, la proyección de máxima intensidad coronal de la secuencia DWIBS pone de manifiesto la afectación ósea de la cabeza humeral derecha y cuerpos vertebrales dorsales y lumbares. Adicionalmente se detecta una extensa recidiva pélvica (asterisco) y adenopatías pélvicas. su bajo contenido en H2O. Sin embargo, como la secuencia de difusión se realiza junto a secuencias morfológicas con gran sensibilidad para detectar alteraciones en la médula ósea, como secuencias TSE potenciadas en T1 o STIR, esta limitación se puede soslayar por la adecuada detección de este tipo de lesiones en secuencias potenciadas en T1 (fig. 9)20. Un problema similar puede ocurrir en caso de metástasis o lesiones óseas tratadas con éxito con radioterapia, quimioterapia o bifosfonatos, que provocan la aparición de hueso escleroso, lo que suele indicar el éxito del tratamiento6. Otro problema en la estadificación ósea con los estudios RM-CC-D es la alteración de señal fisiológica que se produce en la médula ósea, según el componente predominante en ésta, que varía con la localización anatómica y la edad. La difusión del H2O libre es mayor en la médula hematopo- 4-9 38-101.indd 70 B D Figura 8. Metástasis vertebrales de carcinoma parotídeo derecho evaluadas con tomografía por emisión de positrones (PET/ TC) y resonancia de cuerpo completo con difusión. A y B) Metástasis única en S2, tanto en la adquisición del 18-18-fluorodesoxigucosa-PET como en la fusión del PET/TC (flechas). C) Sin embargo, la reconstrucción multiplanar sagital de la secuencia DWIBS pone de manifiesto la misma metástasis y otras adicionales en D9, L2 y L3 (flechas). yética que en la grasa, que disminuye en el esqueleto con la edad. El contenido en grasa de la médula ósea incrementa con la edad y se relaciona negativamente con los valores ADC5. Así, mientras la médula grasa aumenta, los valores ADC descienden. Los valores ADC se relacionan positivamente con la celularidad de la médula ósea, aunque inesperadamente el ADC de la médula grasa que es hipocelular es más bajo que el de médula ósea normocelular de los adultos o de la médula hipercelular de los niños6,18. Podemos encontrar la explicación en un nivel microscópico, ya que las células grasas medulares son grandes y limitan más la difusión del H2O libre extracelular que las células hematopoyéticas normales. Se debe prestar atención cuando se utilizan las secuencias de difusión para evaluar patología ósea en niños, ya que la presencia de áreas de hiperseñal en los huesos pélvicos y de la columna lumbar es común. En casos de aumento de células en la médula ósea que no contengan células grasas, como en la hiperplasia de médula ósea o infiltración tumoral, se incrementa paralelamente la intensidad de señal ósea en secuencias de difusión con valores b altos y disminuyen progresivamente sus valores ADC6. 23/11/12 11:49:52 Resonancia de cuerpo completo con difusión: aplicaciones oncológicas y en la evaluación de las metástasis óseas A B C 71 D Figura 9. Metástasis vertebrales osteolíticas y osteoesclerótica de carcinoma de próstata. Apreciamos metástasis osteolíticas con restricción de la difusión a nivel dorsal superior y en L5 (flechas) y una metástasis osteoblástica en L2 (asterisco), que no presenta ninguna restricción de la difusión (C) y es marcadamente hipointensa en T1 (A) y STIR (B). D) La fusión de la difusión con valor b = 1.000 s/mm2 y del T1 pone de manifiesto el distinto comportamiento de las metástasis según su origen. En la secuencia de difusión se aprecia también una metástasis esternal (flecha), no visualizable en STIR y difícilmente en la secuencia T1. Una de las aplicaciones clínicas más estudiadas ha sido el papel de la difusión en la distinción entre fracturas vertebrales benignas y patológicas. Visualmente, las fracturas benignas son hipointensas (fig. 10) y las malignas hiperintensas con valores b altos (fig. 5), debido a que en las fracturas osteoporóticas se incrementa la difusión por el edema en el hueso trabecular y la disrupción de la microestructura ósea, y en las malignas se produce un incremento de la celularidad con la restricción de la difusión consiguiente27. En varias series, esta distinción ha sido más obvia utilizando secuencias SSFP. A veces, las fracturas benignas pueden mostrar hiperseñal en difusión por la presencia de edema o hemorragia extensos. Para evitar este problema, deben analizarse las secuencias morfológicas y la integridad de la trabeculación ósea con secuencias eco de gradiente potenciadas en susceptibilidad o TC5. Aunque los mapas ADC pueden ayudar en esta diferenciación, hay un solapamiento en los valores ADC de las fracturas vertebrales benignas y malignas, lo que impide la consideración de esta herramienta como un arma definitiva en 4-9 38-101.indd 71 este momento, ya que no se puede determinar un valor de corte claro (fig. 10). Habitualmente, las fracturas metastásicas y malignas presentan valores ADC más bajos (entre 0,7-1 × 10-3 mm2/s) que las osteoporóticas (entre 1-2 × 10-3 mm2/s)5. Los valores ADC de ambas son más altos que los de las vértebras normales, que oscilan entre 0,2-0,5 × 10–3 mm2/s. Los valores ADC de las vértebras normales varían de acuerdo con el tipo de secuencia, valores b usados y la utilización o no de supresión grasa. Los valores ADC de las fracturas vertebrales de cualquier origen son generalmente más altos que los de las vértebras normales, ya que disminuye el contenido en grasa, que presenta un valor ADC muy bajo. Las fracturas secundarias a enfermedades inflamatorias e infecciosas suelen demostrar ADC intermedios, lo que hace difícil su diferenciación de cualquier tipo de fractura en secuencias de difusión5. Se ha constatado un solapamiento entre las fracturas malignas y la espondilitis tuberculosa, que suele demostrar también valores ADC bajos20. Por tanto, los valores ADC deben analizarse junto a la intensidad de señal en las secuencias de difusión con 23/11/12 11:49:53 La imagen funcional en oncología 72 A B C D Figura 10. Aplastamiento vertebral subagudo benigno. Paciente con antecedente de carcinoma de pulmón resecado con posterior radioterapia, con lumbalgia actual. A) En la gammagrafía hay una hipercaptación en L1 sospechosa de metástasis. En el estudio de resonancia magnética de cuerpo completo se aprecia un acuñamiento con expansión de muro posterior de L1, con leve hiposeñal en T1 (B) e hiperseñal franca en STIR (C). La morfología es de acuñamiento osteoporótico en las secuencias morfológicas de resonancia magnética. En la secuencia DWIBS muestra una restricción moderada de la difusión (D), que favorece un origen osteoporótico, aunque con un coeficiente de difusión aparente muy bajo, de 1 × 10–3 mm2/s (no mostrado), que favorece un origen metastásico. El origen benigno de la lesión pudo demostrarse en posteriores controles. valores b altos, siendo especialmente útiles cuando el valor ADC es muy alto, lo que indicará con alta probabilidad una etiología osteoporótica. Aunque no hay datos concluyentes, los estudios publicados indican un valor añadido en la incorporación de la difusión a los protocolos de estudio de las fracturas vertebrales, ya que, en ocasiones, los hallazgos en la difusión modifican el diagnóstico derivado del análisis aislado de las secuencias morfológicas5. La RM-CC-D permite de una manera rápida y visual la valoración de la extensión de un tumor, especialmente de la afectación ósea. Por ello, se ha investigado su uso en la monitorización postratamiento de las metástasis óseas (figs. 6 y 11). Aunque la experiencia es limitada, la mayor parte de las series se ha centrado en las metástasis óseas del carcinoma de próstata. Por ejemplo, Reischauer et al11 demostraron en 9 pacientes con 20 metástasis pélvicas una correlación positiva entre el descenso de los valores de PSA con un incremento en el ADC medio a los 1, 2 y 3 meses postratamiento antiandrogénico comparado con el ADC medio pretratamiento. Además, en esta serie analizaron la respuesta mediante métodos de cuantificación más sofisticados, como los mapas cuantitativos funcionales de difusión, demostrándose una respuesta heterogénea con 4-9 38-101.indd 72 un predominio de los vóxeles con aumento del ADC en todos los puntos temporales de análisis, aunque el porcentaje de vóxeles con aumento del ADC disminuyó entre el primer y el tercer mes postratamiento. Sin embargo, en la serie de Messiou et al12, que incluía 26 pacientes con 100 metástasis de carcinoma de próstata pélvicas y lumbares, se demostró un aumento significativo del ADC medio y del ADC lento, tanto en respondedores como en no respondedores, a las 12 semanas tras el inicio del tratamiento quimioterápico, no variando en los pacientes con enfermedad estable, tomando como referencia los valores de PSA y la estadificación RECIST en TC. El aumento y el número de lesiones con progresión fueron mucho más frecuentes en el grupo de respondedores. Tanto en el grupo de respondedores como en los que presentaron progresión hubo casos con descensos del ADC más allá de los límites de la reproducibilidad, por lo que los autores no consideraron el ADC como una medida apropiada de la respuesta de las metástasis óseas. Estos datos, aunque limitados, confirman que la valoración de la respuesta al tratamiento en la médula ósea con difusión es compleja. En un primer momento tras el inicio del tratamiento, un incremento del ADC puede correlacionarse con respuesta positiva, con comportamien- 23/11/12 11:49:53 Resonancia de cuerpo completo con difusión: aplicaciones oncológicas y en la evaluación de las metástasis óseas A 73 B D C F E Figura 11. Control postratamiento de metástasis ósea de carcinoma de próstata. A, C y E) Secuencias de difusión con saturación espectral de la grasa y valor b = 1.000 s/mm2, realizadas en noviembre de 2009, abril de 2010 y febrero de 2011, respectivamente. En ellas se puede ver la evolución de una metástasis en la tuberosidad isquiática izquierda, que disminuye su tamaño y señal en el segundo control tras iniciar tratamiento antiandrogénico, y un posterior aumento de volumen en señal en el tercer control, indicativo de progresión. B, D y F) Mapas correspondientes al coeficiente de difusión aparente (ADC) con histograma de la región de interés sobre la lesión, demostrando el ascenso inicial del ADC con posterior descenso, indicando primero buena respuesta y después progresión. tos variables en la intensidad de señal de las lesiones con valores b altos5. Sin embargo, a medio plazo la situación se complica, ya que la respuesta positiva al tratamiento incluye 2 mecanismos paralelos: la esclerosis ósea y la sustitución de los focos tumorales por médula amarilla (grasa) normal6. Ambos mecanismos, junto a la necrosis, apoptosis y mielofibrosis, inducen reducciones de señal en difu- 4-9 38-101.indd 73 sión y de los valores ADC en pacientes respondedores. Este patrón lo vemos con frecuencia en las metástasis óseas de carcinoma de mama y próstata tratadas con éxito, aunque su patrón temporal de establecimiento es variable y puede ocurrir tras meses de tratamiento6. Estas reducciones en el ADC pueden también detectarse en la médula ósea normal debido al efecto de los fármacos citotóxicos. Recientemen- 23/11/12 11:49:54 74 te, Padhani et al28 han descrito los patrones de respuesta precoz de las metástasis óseas a este tipo de terapias. De manera similar, la médula ósea puede también demostrar atrofia grasa de manera secundaria a la radioterapia, disminuyendo su señal en difusión con valores b altos. La valoración de la respuesta al tratamiento puede hacerse de forma cualitativa o cuantitativa. El análisis visual es más fácil de realizar y funciona bien para la médula ósea en la mayor parte de las ocasiones. Esta aproximación es la más extendida en la práctica clínica diaria en la evaluación de mieloma múltiple o metástasis óseas. Las limitaciones de esta aproximación son la presencia de algunos factores que pueden llevar a confusión, como la presencia de edema tras radioterapia o cirugía, que puede incrementar la intensidad de señal de la médula ósea en difusión o la visualización de estructuras hipercelulares normales6. El uso de cuantificaciones ADC y la correlación de los hallazgos con secuencias morfológicas pueden minimizar estas limitaciones. Como se comentó anteriormente, probablemente, el uso de histogramas o de mapas funcionales de difusión pueda representar mejor la heterogeneidad de las lesiones en la médula ósea que el ADC medio. Otra posible situación que puede llevar a error es la evaluación de pacientes que reciben factor estimulador de las colonias de granulocitos utilizado junto a la quimioterapia para minimizar la neutropenia6. Este fármaco incrementa la médula ósea roja esquelética, lo que no debe interpretarse como progresión de la enfermedad en pacientes oncológicos con afectación ósea. Evaluación del mieloma múltiple y otros procesos malignos hematológicos con resonancia de cuerpo completo con difusión En el mieloma múltiple se produce una infiltración de la médula ósea por clones de células plasmáticas malignas, que provocan destrucción de la arquitectura. Hasta el 40% de los pacientes están asintomáticos en el momento del diagnóstico, siendo el síntoma más frecuente la presencia de dolor óseo. La distribución de la enfermedad es variable, pero afecta principalmente al esqueleto axial, siendo posible también la afectación de las costillas, escápulas, húmeros y clavículas, cráneo y porción proximal de los fémures. La estadificación inicial se sigue realizando con radiología simple integrada en una serie ósea de acuerdo a las recomendaciones del International Myeloma Working Group en 2009, pero no es una técnica lo suficientemente sensible para detectar lesiones osteolíticas tempranas1. La RM-CC es más sensible en la detección de lesiones y en la valoración de su extensión de forma significativa, como se ha demostrado en diversas series1,29. Por ello, entre las conclusiones de este grupo se incluyó la recomendación de incluir los estudios de RM-CC en pacientes con estudios radiológicos simples negativos o con plasmocitoma aparentemente solitario. Además, la RM permite la detección de afectación extraósea6-20. En distintas series, la RM-CC, 4-9 38-101.indd 74 La imagen funcional en oncología incluyendo secuencias potenciadas en T1 y T2 con supresión grasa o STIR, también se ha demostrado superior a la PET, la gammagrafía ósea o la TC en la estadificación del mieloma múltiple1. Por ello, estas técnicas sólo deben utilizarse si la RM no está disponible o en casos seleccionados. La estadificación del mieloma múltiple se realiza por el sistema Durie/Salmon PLUS, que es una modificación realizada en 2003 del sistema inicial de Durie y Salmon de 197529. En este sistema se incluyen los hallazgos de la radiología simple y la RM-CC. El criterio de imagen clave es el número de lesiones óseas focales detectadas. Las secuencias STIR son las mejores para la detección de lesiones focales y las potenciadas en T1 para la infiltración ósea difusa. El problema con la RM es que la apariencia de las lesiones por mieloma múltiple no es específica y los hallazgos pueden superponerse a los de otras patologías óseas; por ello no es infrecuente que se produzcan casos tanto de sobre como de infraestadificación13. El papel de la RM-CC-D en la evaluación del mieloma múltiple se ha estudiado poco, pero con los escasos datos disponibles ha demostrado potencial para mejorar la especificidad de la RM-CC para el estudio tanto de lesiones focales como de la infiltración difusa, así como un papel en la monitorización posterapéutica (fig. 12)12-14,29,30. En una serie muy reciente de Sommer et al29, la RM-CC-D, con valores b de 0 y 800 s/mm2, demostró ser una herramienta muy potente en la estadificación y seguimiento terapéutico del mieloma múltiple, ya que mejoró la detección de lesiones tanto en pacientes con enfermedad recién diagnosticada como recurrente. En esta serie se evaluó de forma retrospectiva a 81 pacientes con mieloma múltiple con 79 lesiones focales en pelvis o columna vertebral, bien para estadificación inicial o para seguimiento terapéutico. Se analizaron de forma independiente los pacientes con valores séricos de componente M altos (> 20 g/dl) y bajos (< 20 g/dl), indicativos de enfermedad activa o inicial e inactiva o en remisión, respectivamente. El índice de contraste/ruido de las lesiones no varió en ambos grupos en las secuencias potenciadas en T1 ni en las de difusión. Sin embargo, con la secuencia STIR se evidenció una diferencia estadísticamente significativa en este índice entre ambos grupos, siendo mayor en el grupo con componente M bajo. Esto puede explicarse porque en las fases activas de la enfermedad las lesiones óseas son más sólidas e hipercelulares, y en las fases de remisión o de inactividad se producen defectos quísticos en la esponjosa, rellenos de líquido o detritus celulares. Por esta evolución, podemos justificar que en esta serie, en los pacientes con una concentración baja sérica de componente M, los valores ADC de las lesiones fueron significativamente más altos que en los pacientes con niveles altos de este marcador. Además, el alto índice de contraste/ruido que demostraron las lesiones en difusión, independientemente de la fase de la enfermedad, compensa la menor visibilidad de las lesiones en STIR en los estadios activos e iniciales. En otra serie, Horger et al 14 demostraron de forma preliminar que la RM-CC-D con cuantificación ADC permite la valoración a corto plazo de la respuesta terapéutica en pacientes con mieloma múltiple. Estos autores 23/11/12 11:49:54 Resonancia de cuerpo completo con difusión: aplicaciones oncológicas y en la evaluación de las metástasis óseas 75 pacientes respondedores mostraron un incremento medio del ADC del 63,9% y en los no respondedores un descenso del 7,8%, con una correlación adecuada con el gradiente sérico del componente M. La amplitud de la respuesta medida por el curso de los valores ADC fue mayor en el esqueleto apendicular que en el axial. Estos resultados son similares a los resultados previos de Fenchel et al30. En otra serie reciente se evaluó con una secuencia de difusión y cuantificación ADC la columna lumbar y la pelvis ósea de 25 pacientes con mieloma múltiple o gammapatía monocolonal, a los que se les realizó una biopsia de médula ósea en comparación con 30 voluntarios sanos 13. Los valores ADC se correlacionaron de manera positiva con la celularidad de la médula ósea y la densidad microvascular. Entre los valores ADC de los controles sanos y enfermos hubo una diferencia estadísticamente significativa, al igual que en sus valores antes y después del tratamiento en los 15 pacientes en los que se pudo realizar seguimiento terapéutico. Estos datos otorgan un posible papel a la difusión en la valoración de pacientes con mieloma múltiple y enfermedad infiltrativa, al igual que en su monitorización. El linfoma óseo aparece como áreas de restricción de la difusión, con resultados similares a las secuencias STIR y algo mejores que las potenciadas en T1, aunque con mayor tendencia a artefactos y menor resolución espacial5. En casos de mieloma múltiple o linfoma tratados puede producirse una necrosis licuefactiva masiva en las lesiones óseas, lo que provoca un incremento tanto de la intensidad de señal en secuencias de difusión con valores b altos como de los valores ADC de la médula ósea. En ocasiones, estas alteraciones pueden observarse de manera persistente y otras con una distribución heterogénea, demostrando en los mapas ADC una señal predominantemente alta entremezclada con áreas de hiposeñal (fig. 13). Todos estos patrones sugieren enfermedad inactiva6. Otras aplicaciones en el sistema osteomuscular de los estudios de resonancia de cuerpo completo con difusión Figura 12. Estadificación de mieloma múltiple con resonancia de cuerpo completo con difusión. Se objetivan focos líticos de destrucción de la difusión a nivel de escápula izquierda, ambos huesos ilíacos, cuarto arco costal derecho y cabeza femoral izquierda. Las lesiones de la escápula y de los ilíacos presentan extensión extraósea. evaluaron de forma prospectiva 12 pacientes con diagnóstico inicial de mieloma múltiple con estudios de RM-CC-D, incluyendo una secuencia DWIBS con valores b de 0 y 800 s/mm2 en el momento del diagnóstico y 3 semanas tras el inicio del tratamiento. En el momento del diagnóstico, todas las lesiones mostraron restricción de la difusión. Los hallazgos en la secuencia de difusión se correlacionaron en el 100% de los casos con el curso clínico. Las lesiones en 4-9 38-101.indd 75 Aparte de las aplicaciones oncológicas, los estudios RMCC-D tienen un papel en el estudio de la patología benigna multifocal y/o sistémica, como las entidades inflamatorias o infecciosas, por ejemplo, la osteomielitis crónica multifocal recurrente o la neurofibromatosis (fig. 14)20. Además, la difusión con RM presenta un papel prometedor en la monitorización terapéutica y detección temprana de enfermedades reumáticas, como la espondilitis anquilosante. Conclusiones La RM-CC-D aporta información funcional a las series morfológicas de la RM-CC, mejorando la sensibilidad en la detección de lesiones oncológicas, en particular de las lesiones de médula ósea. A la vista de los datos publicados, 23/11/12 11:49:54 La imagen funcional en oncología 76 A B Figura 13. Varón de 67 años con mieloma múltiple en tratamiento. Secuencias sagital STIR (A) y proyección coronal de máxima intensidad de secuencia de difusión de cuerpo completo (B) demuestran cambios postratamiento con un patrón mixto en médula ósea. Tan sólo se detecta un foco de enfermedad activa en D3 (flechas), que aparece como un área hiperintensa en STIR y con restricción de la difusión. Incidentalmente se encontró un nódulo subcutáneo benigno paravertebral dorsal izquierdo con restricción de la difusión (cabeza de flecha). parece claro que las secuencias DWIBS deben interpretarse en conjunto con las secuencias morfológicas para incrementar la especificidad y evitar falsos negativos, como las metástasis completamente osteoblásticas. El cálculo de las cuantificaciones ADC también es útil en general para incrementar la especificidad en la caracterización de lesiones, aunque hay que definir un parámetro métrico que represente la heterogeneidad en la composición de la médula ósea y sus patologías. La RM-CC-D es una alternativa válida a la gammagrafía ósea y PET/TC en la valoración de la afectación metastásica ósea, del mieloma múltiple y del linfoma. Aunque la monitorización terapéutica de las alteraciones de la médula ósea es muy compleja con la difusión con RM, tanto por la heterogénea composición de la médula ósea normal como por la variabilidad de los procesos de respuesta postratamiento, las series publicadas indican resultados muy prometedores tanto para las metástasis óseas del cáncer de próstata como para el mieloma múltiple. 4-9 38-101.indd 76 Figura 14. Proyección de máxima intensidad coronal de secuencia DWIBS en paciente con neurofibromatosis tipo 2 en estudio por mieloma múltiple. Aparte de las múltiples lesiones óseas en esqueleto axial, costales, femorales y humerales, apreciamos la presencia de neurofibromas dorsales (flechas) y uno de gran tamaño en región escapular izquierda (asterisco). Bibliografía 1. Schmidt GP, Reiser MF, Baur-Melnyk A. Whole-body MRI for the staging and follow-up of patients with metastasis. Eur J Radiol. 2009;70:393-400. 2. Balliu E, Boada M, Peláez I, Vilanova JC, Barceló-Vidal C, Rubio A, et al. Comparative study of whole-body MRI and bone scintigraphy for the detection of bone metastases. ClinRadiol. 2010;65:989-96. 3. Low RN. Diffusion-weighted MR imaging for whole body metastatic disease and lymphadenopathy. Magn Reson Imaging Clin N Am. 2009;17:245-61. 23/11/12 11:49:54 Resonancia de cuerpo completo con difusión: aplicaciones oncológicas y en la evaluación de las metástasis óseas 4. Padhani AR, Liu G, Koh DM, Chenevert TL, Thoeny HC, Takahara T, et al. Diffusion-weighted magnetic resonance imaging as a cancer biomarker: consensus and recommendations. Neoplasia. 2009;11:102-25. 5. Khoo MM, Tyler PA, Saifuddin A, Padhani AR. Diffusionweighted imaging (DWI) in musculoskeletal MRI: a critical review. Skeletal Radiol. 2011;40:665-81. 6. Padhani AR, Koh DM. Diffusion MR imaging for monitoring of treatment response. Magn Reson Imaging Clin N Am. 2011;19:181-209. 7. Takahara T, Imai Y, Yamashita T Yasuda S, Nasu S, Van Cauteren M. Diffusion weighted whole body imaging with background body signal suppression (DWIBS): technical improvement using free breathing, STIR and high resolution 3D display. Radiat Med. 2004;22:275-82. 8. Gu TF, Xiao XL, Sun F, Yin JH, Zhao H. Diagnostic value of whole body diffusion weighted imaging for screening primary tumors of patients with metastases. Chin Med Sci J. 2008;23:145-50. 9. Lambregts DMJ, Maas M, Cappendijk VC, Prompers LM, Mottaghy FM, Beets GL, et al. Whole-body diffusionweighted magnetic resonance imaging: Current evidence in oncology and potential role in colorectal cancer staging, Eur J Cancer. 2011;doi:10.1016/j.ejca.2011.05.013. 10. Wu LM, Gu HY, Zheng J, Xu X, Lin LH, Deng X, et al. Diagnostic value of whole-body magnetic resonance imaging for bone metastases: a systematic review and meta-analysis. J Magn Reson Imaging. 2011;34:128-35. 11. Reischauer C, Froehlich JM, Koh DM, Graf N, Padevit C, John H, et al. Bone metastases from prostate cancer: assessing treatment response by using diffusion-weighted imaging and functional diffusion maps--initial observations. Radiology. 2010;257:523-31. 12. Messiou C, Collins DJ, Giles S, De Bono JS, Bianchini D, De Souza NM. Assessing response in bone metastases in prostate cancer with diffusion weighted MRI. EurRadiol. 2011;doi:10.1007/s00330-011-2173-8. 13. Hillengass J, Bäuerle T, Bartl R, Andrulis M, McClanahan F, Laun FB, et al. Diffusion-weighted imaging for non-invasive and quantitative monitoring of bone marrow infiltration in patients with monoclonal plasma cell disease: a comparative study with histology. Br J Haematol. 2011;153:721-8. 14. Horger M, Weisel K, Horger W, Mroue A, Fenchel M, Lichy M. Whole-body diffusion-weighted MRI with apparent diffusion coefficient mapping for early response monitoring in multiple myeloma: preliminary results. AJR Am J Roentgenol. 2011;196:790-5. 15. Luna A, Sánchez-González J, Caro P. Diffusion-weighted imaging of the chest. Magn Reson Imaging Clin N Am. 2011;19:69-94. 16. Ballon D, Watts R, Dyke JP, Lis E, Morris MJ, Scher HI, et al. Imaging therapeutic response in human bone marrow using rapid whole-body MRI. Magn Reson Med. 2004;52:1234-8. 17. Kwee TC, Takahara T, Ochiai R, Koh DM, Ohno Y, Nakanishi K, et al. Complementary roles of whole-body diffusion- 4-9 38-101.indd 77 77 weighted MRI and 18F-FDG PET: the state of the art and potential applications. J Nucl Med. 2010;51:1549-58. 18. Padhani AR, Koh DM, Collins DJ. Whole-body diffusionweighted MR imaging in cancer: current status and research directions. Radiology. 2011;261:700-18. 19. Herneth AM, Mayerhoefer M, Schernthaner R. Diffusion weighted imaging: lymph nodes. Eur J Radiol. 2010;76:398-406. 20. Vilanova JC, Barceló J. Diffusion-weighted whole-body MR screening. Eur J Radiol. 2008;67:440-7. 21. Kwee TC, Takahara T, Vermoolen MA, Bierings MB, Mali WP, Nievelstein RA. Whole-body diffusion-weighted imaging for staging malignant lymphoma in children. Pediatr Radiol. 2010;40:1592-602. 22. Lin C, Luciani A, Itti E, El-Gnaoui T, Vignaud A, Beaussart P, et al. Whole-body diffusion-weighted magnetic resonance imaging with apparent diffusion coefficient mapping for staging patients with diffuse large B-cell lymphoma. EurRadiol. 2010;20:2027-38. 23. Wang N, Zhang M, Sun T, Chen H, Huang Z, Yan L, et al. A comparative study: Diffusion weighted whole body imaging with background body signal suppression and hybrid positron emission computed tomography on detecting lesions in oncologic clinics. Eur J Radiol. 2011;doi:10.1016/j. ejrad.2011.03.047. 24. Laurent V, Trausch G, Bruot O, Olivier P, Felblinger J, Régent D. Comparative study of two whole-body imaging techniques in the case of melanoma metastases: advantages of multi-contrast MRI examination including a diffusionweighted sequence in comparison with PET-CT. Eur J Radiol. 2010;75:376-83. 25. Heusner TA, Kuemmel S, Koeninger A, Hamami ME, Hahn S, Quinsten A, et al. Diagnostic value of diffusion-weighted magnetic resonance imaging (DWI) compared to FDG PET/ CT for whole-body breast cancer staging. Eur J Nucl Med Mol Imaging. 2010;37:1077-86. 26. Luboldt W, Küfer R, Blumstein N, Toussaint TL, Kluge A, Seemann MD, et al. Prostate carcinoma: diffusion-weighted imaging as potential alternative to conventional MR and 11C-choline PET/CT for detection of bone metastases. Radiology. 2008;249:1017-25. 27. Baur A, Dietrich O, Reiser M. Diffusion-weighted imaging of the spinal column. Neuroimaging Clin N Am. 2002;12:147-60. 28. Padhani AR, Gogbashian A. Bony metastases: assessing response to therapy with whole-body diffusion MRI. Cancer Imaging. 2011;11:S129-45. 29. Sommer G, Klarhöfer M, Lenz C, Scheffler K, Bongartz G, Winter L. Signal characteristics of focal bone marrow lesions in patients with multiple myeloma using whole body T1w-TSE, T2w-STIR and diffusion-weighted imaging with background suppression. Eur Radiol. 201;21:857-62. 30. Fenchel M, Konaktchieva M, Weisel K, Kraus S, Claussen CD, Horger M. Response assessment in patients with multiple myeloma during antiangiogenic therapy using arterial spin labeling and diffusion-weighted imaging: a feasibility study. Acad Radiol. 2010;17:1326-33. 23/11/12 11:49:55 La imagen funcional en oncología 7 Papel de la resonancia magnética en el seguimiento de los gliomas J. Álvarez-Linera Prado Sección de Neurorradiología, Hospital Ruber Internacional, Madrid, España Introducción Los gliomas son los tumores cerebrales primarios más frecuentes en adultos, con una incidencia anual aproximada de 5/100.000 habitantes. A pesar del progreso en los últimos 10 años en el diagnóstico y tratamiento de los tumores cerebrales, los gliomas continúan siendo uno de los mayores retos en neurooncología. Aunque se han producido grandes avances en el diagnóstico, tanto en el ámbito histológico, molecular y genético como en el diagnóstico por imagen, el tratamiento de los gliomas ha avanzado sólo moderadamente en términos de supervivencia y los criterios de respuesta al tratamiento continúan presentando importantes limitaciones. Los gliomas son tumores con gran tendencia infiltrante y con una arquitectura heterogénea, que mezcla poblaciones celulares de diferente grado de agresividad en distintas localizaciones que a su vez coexisten con áreas de necrosis en el caso de lesiones más agresivas. Además, es frecuente la existencia de edema y, en menor medida, de sangrado o calcificación, que contribuye a producir una imagen muy compleja, de difícil interpretación. La clasificación de los gliomas se basa en criterios histológicos, siendo la más utilizada la clasificación de la Organización Mundial de la Salud (OMS), que distingue 4 grados de menor a mayor agresividad. Dejando de lado los gliomas clasificados como grado I, por sus características específicas y su menor interés desde el punto de vista del seguimiento, los gliomas se suelen clasificar como de bajo grado (grado II de la OMS) y de alto grado (grados III y IV de la OMS), dependiendo de la presencia de atipia/indiferenciación celular, proliferación vascular y necrosis, en combinaciones que varían ligeramente dependiendo de la histología del glioma (los más frecuentes son los derivados de astrocitos y de oligodendrocitos). Aunque hay cierta correlación entre el grado de agresividad y la manifestación en imagen estructural (la heterogeneidad de la señal, la existencia de edema y la de realce poscontraste sugieren agresividad), no hay criterios fiables para determinar el grado de agresividad de los gliomas que, además, tienen tendencia a aumentar el grado de agresividad al cabo del tiempo. Todo esto hace que el seguimiento de los gliomas sea especialmente difícil, a lo cual se une el hecho de que los diferentes tratamientos provocan alteraciones, tanto en el tumor como en el parénquima sano, muchas veces muy similares a las que produce la recurrencia o la progresión del propio tumor. La mayor parte de las recomendaciones de grupos de trabajo de las diferentes sociedades neurooncológicas se refieren a gliomas de alto grado, ya que además de ser más frecuentes son los que más se someten a quimio/radioterapia y necesitan una evaluación detenida de la respuesta tumoral, así como de la aparición de posibles complicaciones del tratamiento. La EMSO (Sociedad Europea de Oncología Médica) recomienda seguir los gliomas de alto grado con resonancia magnética (RM) estructural con contraste cada 3-4 meses si los datos clínicos no indican la realización de una RM más precoz. Aunque no hay una recomendación detallada para los gliomas de bajo grado, la práctica más habitual es realizar la RM cada 4-6 meses si no hay cambios en la clínica. El seguimiento de los gliomas, incluyendo el de la respuesta al tratamiento, se ha centrado siempre en los gliomas de alto grado debido a múltiples factores, entre ellos el hecho de tratarse de lesiones con crecimiento lento, frecuentemente sin asociar claros cambios en la clínica y con escasos criterios para identificar el significado de los cambios que se pueden producir en la imagen, bien por la progresión del tumor, por los efectos del tratamiento o por una mezcla de ambos1. El criterio más importante en el control de los gliomas de bajo grado es el tamaño de la lesión. Las secuencias T2, especialmente con secuencias FLAIR, son las más utilizadas para evaluar cambios en el tamaño lesional y se han mostrado incluso más eficaces que las técnicas avanzadas en el seguimiento2. Las técnicas volumétricas en FLAIR son superiores a las técnicas uni o bidimensionales para valorar pequeños cambios en el tamaño de la lesión, ya que además de poder medir lesiones irregulares pueden valorar mejor el crecimiento, ya que frecuentemente éste es anisotrópico. El principal inconveniente sigue siendo la dificultad para diferenciar el tumor de los efectos del tratamiento o del propio tumor. Correo electrónico: jalinera@ruberinternacional.es 4-9 38-101.indd 78 23/11/12 11:49:55 Papel de la resonancia magnética en el seguimiento de los gliomas 79 Tabla 1 − Criterios de McDonald Respuesta completa Respuesta parcial Desaparición del realce durante más de 4 semanas No aparición de nuevas lesiones Clínica estable o mejor, sin corticoides > 50% de disminución No criterios de lesión medible de progresión > 4 semanas No aparición de nuevas No criterios de lesiones con realce respuesta parcial Corticoides y clínica Clínica estable estables Las técnicas avanzadas son poco útiles en los gliomas de bajo grado, excepto en el caso de evolucionar a un glioma de alto grado en el que se plantea el diagnóstico diferencial con radionecrosis. En estos casos se aplican los criterios establecidos para gliomas de alto grado (v. más adelante). Los gliomas de bajo grado tienden a tener una perfusión similar a la sustancia blanca, por lo que debido al efecto suelo es difícil identificar signos de mejoría, aunque se ha visto que la disminución del volumen sanguíneo regional (VSR) en gliomas de bajo grado es un factor de buen pronóstico3. Por otro lado, alrededor del 30% de los oligodendrogliomas tiene una perfusión similar a los gliomas de alto grado, lo cual añade un factor de confusión. La espectroscopia puede mostrar disminución del pico de Cho, pero éste no suele ser muy alto en los gliomas de bajo grado4. Además, la gliosis también produce ligero aumento de la Cho, por lo que es difícil diferenciar cambios postratamiento de tumor. El único criterio fiable sería el aumento importante de Cho en el caso de progresión. En cuanto a la difusión, los gliomas de bajo grado suelen tener discreto aumento de la difusión respecto a la sustancia blanca y los efectos del tratamiento no han sido bien estudiados5, aunque la aparición de áreas de marcada reducción en la difusión ha de hacer sospechar progresión. Los criterios de respuesta al tratamiento más utilizados son los llamados criterios de McDonald, que consideran signos de imagen junto con datos clínicos y tienen en cuenta la dosis de corticoides. Sin embargo, como se analizará más adelante, estos criterios presentan serias limitaciones en el caso de los gliomas, lo que ha motivado una reciente modificación. Por otro lado, el efecto de nuevas combinaciones terapéuticas como la quimio/radioterapia y la aparición de fármacos antiangiogénicos como el bevacizumab, están provocando importantes cambios en la imagen que han motivado la aparición de nuevos términos como seudoprogresión o seudorrespuesta6, que hablan por sí mismos de las nuevas dificultades diagnósticas que conllevan los avances en el tratamiento. El objetivo de este capítulo es revisar los criterios de respuesta tumoral y los cambios que produce el tratamiento de los gliomas (especialmente de los gliomas de alto grado), así como mostrar las posibilidades de técnicas más avanzadas de RM como la perfusión, difusión y espectroscopia, para mejorar la efi- 4-9 38-101.indd 79 Enfermedad estable Progresión > 25% de aumento de lesión medible Aparición de nuevas lesiones con realce Deterioro clínico ciencia en el seguimiento de los gliomas, especialmente en el diagnóstico diferencial entre recurrencia tumoral y radionecrosis así como en la seudoprogresión y la seudorrespuesta. Criterios de respuesta tumoral La evaluación del tratamiento en gliomas se basa tanto en la supervivencia global como, sobre todo, en los pacientes con recurrencia, en la respuesta radiológica o supervivencia libre de progresión. Para ello, en los años noventa se establecieron los llamados criterios de McDonald7, intentando obtener una evaluación objetiva que se basaba en el cálculo de área de realce tumoral utilizando la suma del producto de los diámetros máximos de las lesiones medibles y valorando, también, el estado clínico y el tratamiento concomitante con corticoides (tabla 1). Se consideran lesiones medibles las lesiones bidimensionales con realce de borde bien definido y diámetro > 1 cm, visibles en más de 2 cortes de 5 mm sin espacio entre cortes. Los pacientes con lesiones no medibles no pueden incluirse en ensayos clínicos que evalúen la respuesta tumoral, aunque sí en estudios de supervivencia. La principal limitación que presentan los criterios de McDonald es que se basan en la existencia de realce poscontraste6. La inmensa mayoría de los tumores malignos del cuerpo se realza con contraste, al menos en la periferia, y suele ser homogénea, lo cual permite medirlos de forma eficiente con imagen. Éste no es el caso de los gliomas, que son heterogéneos y pueden no realzarse significativamente o hacerlo de forma tan heterogénea que hace imposible obtener un diámetro fiable. Además, el realce poscontraste puede producirse por otras razones, entre otras como respuesta al propio tratamiento8. Los criterios de McDonald, al igual que los criterios RECIST en tumores sistémicos, fueron diseñados para la evaluación de ensayos clínicos, pero en la práctica clínica se emplean los mismos conceptos: respuesta completa o parcial, enfermedad estable y progresión, aunque con criterios no tan estrictos en cuanto a la imagen, que en la mayoría de los casos utiliza estimaciones subjetivas en la evaluación del tamaño de la lesión, incluyendo lesiones no 23/11/12 11:49:55 80 La imagen funcional en oncología Figura 1. Seudoprogresión. Cortes axiales con secuencias T1-poscontraste y FLAIR después de la cirugía (A y B), a los 2 meses del tratamiento con radioterapia (60 Gy) y temozolamida (C y D) y 3 meses más tarde (E y F). En el control a los 2 meses se observa aumento del edema y del área de realce poscontraste, que disminuye 3 meses más tarde. medibles, tanto las áreas de realce mal definidas o pequeñas como las áreas de alteración de señal sin realce. Seudoprogresión El tratamiento inicial de los gliomas es la resección quirúrgica lo más completa posible, ya que está demostrado que el grado de resección es uno de los principales factores que mejoran la supervivencia. En el caso de los gliomas de alto grado, el tratamiento quirúrgico va seguido de radioterapia y quimioterapia con temozoloamida concurrente y adyuvante. La asociación de quimio y radioterapia da lugar hasta en un 15-25% a un aumento transitorio del efecto expansivo, con aumento en el realce poscontraste en el área del tumor y del edema vasogénico (fig. 1), que suele producirse en los 2-3 meses posteriores al inicio del tratamiento y que cumple criterios de McDonald de progresión 4-9 38-101.indd 80 tumoral. Este porcentaje de pacientes no tiene criterios histológicos de progresión, sino que presenta necrosis y lesiones del endotelio vascular que son los causantes del fenómeno que se ha denominado seudoprogresión, ya que suele disminuir en los meses siguientes sin dejar secuelas9. Es importante reconocer este fenómeno ya que estos pacientes no deberían interrumpir el tratamiento; por otro lado, estos casos no deben incluirse en ensayos clínicos de tratamiento de gliomas en recurrencia ya que darán lugar a falsos índices de respuesta. Para identificar estos pacientes y diferenciarlos de aquellos con auténtica progresión, la RM estructural presenta importantes limitaciones8, por lo que se están proponiendo técnicas avanzadas de RM o bien de tomografía por emisión de positrones (PET)10, aunque por el momento los paneles de expertos recomiendan que para establecer progresión en las 12 semanas después de quimio/radioterapia ha de demostrarse nuevo realce por 23/11/12 11:49:55 Papel de la resonancia magnética en el seguimiento de los gliomas 81 Figura 2. Seudorrespuesta. Cortes axiales con secuencias T1 poscontraste en el momento de la recurrencia (A y B), a las 4 semanas de tratamiento con bevacizumab e irinotecán (C y D) y 3 meses más tarde (E y F). Se observa desaparición del realce poscontraste desde el primer control. El área de alteración de señal en FLAIR, con efecto expansivo, continúa aumentando desde el primer control. fuera del área de radioterapia o bien realizarse biopsia de confirmación si se trata de un ensayo clínico. En la práctica clínica, muy probablemente, las técnicas avanzadas de RM pueden ser de utilidad (v. más adelante) y si no muestran signos de progresión, los que permanezcan clínicamente estables podrían continuar el tratamiento a pesar de presentar seudoprogresión en la RM estructural. Hay otras causas de realce precoz poscontraste, como los cambios posquirúrgicos, por lo que para definir resto tumoral se aconseja obtener una RM con contraste en las primeras 72 h tras la intervención11. También puede producir realce poscontraste transitorio la administración local de tratamientos como braquiterapia o radiocirugía. En estos casos puede ser útil la realización de técnicas avanzadas de RM o PET12. Seudorrespuesta Los fármacos antiangiogénicos se basan habitualmente en la inhibición del factor de crecimiento endotelial vas- 4-9 38-101.indd 81 cular (VEGF) y tienen un rápido efecto sobre la vasculatura tumoral, inhibiendo la angiogénesis y normalizando la circulación, con estabilización de la barrera hematoencefálica. A partir de los 2 días del tratamiento, la terapia con antiangiogénicos puede producir marcada disminución del realce poscontraste así como del edema vasogénico. Este efecto da lugar a una imagen con signos de respuesta al tratamiento según criterios de McDonald en un 25-50%, lo que no significa necesariamente que haya una verdadera respuesta, ya que la supervivencia global sólo aumenta discretamente13. La progresión tumoral suele producirse en estos casos debido al crecimiento de poblaciones celulares con distinto fenotipo, sin marcada angiogéneis y sin realce poscontraste. La imagen muestra disminución o desaparición del realce poscontraste y del edema vasogénico a pesar del deterioro progresivo del paciente, situación que se denomina seudorrespuesta14 (fig. 2). La duración de la respuesta es un indicador robusto de efecto antitumoral, por lo que se ha propuesto que para considerarse respuesta, si hay tratamiento antiangiogéni- 23/11/12 11:49:55 La imagen funcional en oncología 82 Tabla 2 − Nuevos criterios de respuesta Criterios RANO Respuesta completa Respuesta parcial Enfermedad estable (Response Assesment in Neuro-Oncology) Progresión T1 post-Gd No < 50% disminución < 50% disminución, < 25% aumento < 25% aumento T2/FLAIR Igual o menor Igual o menor Aumento Igual o menor Corticoides No Estable o menor Estable o menor Clínica Igual o mejor Igual o mejor Igual o mejor Deterioro Requerimiento Todos Todos Todos Cualquiera Tabla 3 − Lesiones posradiación Lesión posradiación Tiempo de aparición Características sobresalientes Aguda Crónica precoz Edema Crónica tardía Necrosis 1-2 meses 3 semanas-meses Edema vasogénico Desmielinización 6 meses-años Desmielinización co, ésta debe prolongarse más de 4 semanas. Además, la respuesta en este caso no debe valorarse únicamente con criterios de McDonald. El Grupo de Trabajo de la RANO (Response Assesment in Neuro-Oncology) recomienda considerar también las áreas de alteración de señal en T2/FLAIR15. De esta forma, durante el tratamiento con antiangiogénicos, aunque haya disminución en el de realce poscontraste, debe valorarse el posible aumento del área de alteración de señal en T2/FLAIR, y si hay efecto expansivo (borrado de surcos, compresión ventricular) o engrosamiento del córtex/cuerpo calloso, debe sospecharse progresión tumoral y se recomienda confirmarla con un nuevo estudio de control (tabla 2). De nuevo, este tipo de pacientes probablemente se beneficiará de otras técnicas de imagen, aunque deberá precisarse su papel mediante nuevas investigaciones16. En los gliomas abundan las lesiones no medibles según los actuales criterios. Los estudios volumétricos seguramente serán muy útiles para determinar progresión radiológica, tanto en lesiones con realce como en lesiones sin realce, aunque debido a la escasa estandarización de los métodos, actualmente no se recomienda emplearlos en ensayos clínicos, si bien pueden ser validados en cada centro para uso clínico ya que se reconoce su utilidad. También se reconoce en los paneles de expertos el valor de las técnicas avanzadas de RM así como el PET, pero para incluirlas como herramientas de ensayos clínicos se requiere una validación más amplia. 4-9 38-101.indd 82 Alteraciones postratamiento Las principales alteraciones secundarias al tratamiento de los gliomas son debidas a la radioterapia, sola o en combinación con quimioterapia. Los factores que influyen en el desarrollo de estas lesiones incluyen la dosis total de radiación, el tamaño del campo y la pauta de administración, la combinación con quimioterapia, la edad en la que se administró el tratamiento y la duración de la supervivencia. Los mecanismos de lesión incluyen daño vascular, lesión celular (células madre, neuronas, células gliales) y efectos sobre los sistemas inmune y enzimático. Se distinguen lesiones agudas, crónicas precoces y crónicas tardías (tabla 3). Las lesiones agudas suelen ser leves y transitorias, habitualmente debidas a edema vasogénico. Las lesiones crónicas precoces suelen ser debidas a desmielinización y/o edema y pueden dejar secuelas. Las lesiones crónicas son más severas e irreversibles y se caracterizan por la desmielinización o, en el caso más grave, por necrosis. El daño vascular es uno de los factores más importantes desde el punto de vista de la imagen, tanto en las lesiones agudas como crónicas, ya que entre otras cosas condiciona la aparición de edema y/o realce poscontraste, tanto en las lesiones precoces como en las tardías. Las células más sensibles a la radiación son los oligodendrocitos, que se relacionan tanto con la desmielinización en las lesiones subagudas como con desmielinización focal o difusa y la 23/11/12 11:49:55 Papel de la resonancia magnética en el seguimiento de los gliomas 83 Figura 3. Radionecrosis. Cortes axiales con secuencias T2 y T1 poscontraste en paciente con antecedentes de carcinoma nasofaríngeo sometido a radioterapia hace 12 meses. Se observa lesión hiperintensa en T2 en protuberancia (A), con discreto efecto expansivo y área de intenso realce poscontraste (B). atrofia de la encefalopatía crónica o leucopatía postirradiación. La radionecrosis puede desarrollarse meses o años después del tratamiento (aunque típicamente se produce después del primer año), siendo el riesgo a los 5 años del 5% después de un tratamiento de radioterapia convencional y es frecuentemente irreversible y a veces progresiva. Se caracteriza por necrosis fibrinoide en la pared vascular rodeada por necrosis coagulativa en el parénquima (sobre todo en la sustancia blanca, más frecuentemente en las zonas sometida a mayores dosis), formando focos que confluyen y dan lugar a lesiones serpiginosas o geográficas. También pueden producirse telangiectasias, bien en el foco de necrosis, que puede producir zonas hemorrágicas, como de forma aislada, dando lugar a lesiones similares a cavernomas. Más raramente puede haber microangiopatía mineralizante, con necrosis de pequeñas arterias, proliferación endotelial y depósitos de calcio. Las características de imagen de la radionecrosis 17 (fig. 3) pueden ser idénticas a la recurrencia tumoral: suelen localizarse cerca del lecho tumoral, producen efecto de masa, con edema, y se realzan intensamente en el estudio poscontraste. La manifestación más típica en RM es como una lesión focal mal definida, con discreto efecto de masa y edema vasogénico. La señal en T2 suele ser hipo/ isointensa y la aparición de nódulos bien definidos se ha considerado como sospecha de coexistencia de tumor. En el estudio poscontraste suele haber realce intenso de predominio periférico y puede haber lesiones múltiples, más frecuentes cerca del área de irradiación, aunque a veces pueden aparecer nódulos periventriculares que simulan una recurrencia multifocal. No hay criterios fiables en la RM estructural para diferenciar la radionecrosis de la recurrencia tumoral8, por lo que se recomiendan otras técnicas (v. más adelante) y en casos dudosos la biopsia. Perfusión La técnica de perfusión con RM más utilizada se basa en los cambios de señal en T2*, que produce el paso de un 4-9 38-101.indd 83 Figura 4. Perfusión. Cortes axiales con secuencia T1-poscontraste y mapa de volumen sanguíneo regional (VSR), en un caso de recurrencia tumoral (A y B) y en un caso de radionecrosis (C y D). En el caso de recurrencia hay aumento de VSR en el área de realce mientras que en el caso de radionecrosis el VSR es similar a la sustancia blanca normal. bolo de contraste (DSC o contraste dinámico por susceptibilidad) y permite medir el VSR relativo cerebral. Múltiples estudios han probado la utilidad de esta técnica para diferenciar los gliomas de alto y bajo grados18-20, aunque sería deseable una mayor estandarización de los valores observados por diferentes autores. El valor más reconocido para la estratificación de gliomas es el VSR máximo observado en la lesión, normalizado con el VSR en la sustancia blanca normal (VSRn), que suele ser > 1,7 en los gliomas de alto grado. Las radionecrosis, aunque presentan intenso realce debido a la lesión del endotelio vascular, no presentan angiogénesis, al contrario que los gliomas de alto grado21, por lo que los valores de VSRn suelen ser < 1,5 (fig. 4). No obstante puede haber solapamiento en los valores del VSRn no solamente debido a razones técnicas, sino a la frecuente coexistencia de necrosis y resto tumoral, por lo que solamente son más fiables los valores extremos (> 2,5 para recurrencia y < 0,7 para radionecrosis)21. La técnica DSC, que globalmente es la más fiable en la tipificación de los gliomas, tiene el inconveniente de ser deteriorada cuando hay una importante lesión de la barrera hematoencefálica, que provoca importante salida del contraste del compartimiento intravascular. En estos 23/11/12 11:49:56 84 La imagen funcional en oncología debido al efecto de los antiangiogénicos22 sin que ello descarte progresión de un fenotipo tumoral con menor vascularización, por lo que aunque la perfusión podría valorar la respuesta al tratamiento23 no hay actualmente suficientes datos para determinar su posible utilidad. Figura 5. Glioma de alto grado con alta permeabilidad. Cortes axiales sobre lesión cerebelosa, con técnicas de perfusión con contraste dinámico por susceptibilidad (DSC) (A) y etiquetado de spines (ASL) (B), y tomografía por emisión de positrones con flúor-deoxiglucosa (PET-FDG) (C). La lesión presenta alto metabolismo en PET, que se correlaciona mejor con la secuencia ASL que con la secuencia DSC, debido a la excesiva permeabilidad que deteriora el análisis de la curva señal/tiempo (no mostrada). casos, puede ser de utilidad la perfusión con técnica de etiquetado de spines (Arterial Spin Labeling o ASL), que no se deteriora con el aumento de la permeabilidad, aunque tiene el inconveniente de la menor resolución espacial y la menor disponibilidad actual (fig. 5). La técnica DSC es muy útil para diferenciar alteración vascular debido al tratamiento de recurrencia tumoral. Esto incluye la seudoprogresión, ya que se comporta de forma muy similar a la radionecrosis, aunque es imprescindible disponer de estudios previos, ya que la clave diagnóstica está en demostrar que hay disminución del VSRn respecto al estudio previo, ya que en los primeros controles el VSRn puede ser > 1,7 si en el estudio previo era muy alto. En el caso de la seudorrespuesta el VSRn puede disminuir Espectroscopia de hidrógeno La espectroscopia también se ha utilizado ampliamente en el estudio de los gliomas, considerándose que hay una relación directa entre el aumento de concentración de Cho, la disminución de NAA y el grado de agresividad. Sin embargo, la coexistencia de necrosis con el tumor, que es habitual en glioblastomas, puede hacer que el pico de Cho descienda debido al predominio de la necrosis sobre el tejido tumoral. Los picos de lípidos libres y lactato, que son muy usados para identificar signos de agresividad, tienen menos utilidad en el seguimiento de los gliomas de alto grado, ya que los cambios que provoca el propio tratamiento contribuyen a la aparición de ambos picos24. Se ha preconizado que una relación Cho/NAA > 2 es indicativa de lesión tumoral frente a una lesión inflamatoria, mientras que la radionecrosis se caracteriza por la disminución global de metabolitos, salvo el pico de lípidos en relación con necrosis, aunque en las fases iniciales puede haber un aumento transitorio de Cho debido a la rotura de membranas celulares y/o desmielinización. Por otro lado, el volumen parcial con el parénquima cerebral suele provocar que el espectro muestre cantidades variables de otros metabolitos como Cho y NAA (fig. 6), por lo que en el Figura 6. Espectroscopia en control posradioterapia con buena respuesta. Cortes axiales con secuencias FLAIR en estudio inicial y de control con su correspondiente espectroscopia, en el caso de un glioma de bajo grado (A-D) y de un glioma de alto grado (E-H). En el glioma de bajo grado se observa discreta disminución de Cho y aparición de picos en la frecuencia de Lip/Lact. En el glioma de alto grado se observa marcado descenso de Cho, permaneciendo un gran pico de lípidos/lactato. 4-9 38-101.indd 84 23/11/12 11:49:56 Papel de la resonancia magnética en el seguimiento de los gliomas 85 diagnóstico diferencial entre radionecrosis y recurrencia se recomienda trabajar con la máxima resolución espacial, habitualmente mediante técnicas multivoxel25, que en 3T pueden obtener resoluciones por debajo de 1 ml, lo que aumenta la fiabilidad (fig. 7). Al igual que con las técnicas de perfusión, es muy conveniente disponer de estudios previos para comparación, ya que si el pico de Cho aumenta o disminuye indicaría progresión o respuesta, respectivamente, aunque hay que cuidar especialmente la localización de los espectros para que la comparación sea valorable (fig. 6). Aunque la espectroscopia tiene mucho menos valor que la perfusión para el estudio de la radionecrosis y la seudoprogresión debido, sobre todo, a una mejor resolución espacial, sin olvidar que mediante perfusión es posible estudiar todo el cerebro, lo que es muy difícil mediante espectroscopia, la seudorrespuesta probablemente será mucho mejor estudiada mediante espectroscopia26, ya que el aumento del tumor, independientemente del componente vascular, provocaría aumento del pico de Cho. No obstante serán necesarios estudios específicos para su validación. Difusión La difusión ha sido la técnica menos utilizada en el estudio de los gliomas, ya que los trabajos iniciales ofrecieron resultados contradictorios debido, en su mayor parte, al escaso dominio de la técnica, especialmente en lo referente a la forma de medición de los parámetros. El coeficiente de difusión aparente (ADC) se ha relacionado con la celularidad en los gliomas, lo que puede utilizarse para su tipificación19. La forma más eficiente para estudiar los gliomas es utilizar una técnica similar a la de la perfusión, es decir, normalizar el ADC respecto a la sustancia blanca normal y elegir el área con el ADC más bajo como la más significativa. Se ha considerado como indicador de agresividad un ADCn < 1,2. Cuando se dispone de secuencias con alto valor b (2.500-3.000) (fig. 8) es posible trabajar con imágenes isotrópicas y valorar la hiperintensidad, ya que no hay contaminación por la señal en b = 0 (“T2-shiningthrough”), lo que permite un análisis cualitativo que es más practico en la rutina clínica. En el seguimiento de los gliomas hay mucha menos experiencia, ya que puede haber situaciones en las que se produzca una disminución del ADC sin que eso indique la existencia de tumor agresivo. La principal causa no tumoral de disminución del ADC es la presencia de una lesión isquémica o de edema citotóxico de otra etiología, lo cual es frecuente en el borde tumoral en los días siguientes a la cirugía. De hecho, la aparición de áreas con disminución del ADC que no estaban presentes en el estudio prequirúrgico en el primer control posquirúrgico sirve para diagnosticar estas lesiones, que no indican persistencia tumoral y que pueden ser motivo de realce poscontraste transitorio que plantearía el diagnóstico diferencial con resto tumoral. En las fases tardías, sin embargo, la aparición de áreas con disminución del ADC ha de hacer sospechar la presencia de recurrencia tumoral. 4-9 38-101.indd 85 Figura 7. Valor de la espectroscopia multivoxel. Recurrencia de glioma de alto grado, con alta perfusión (A) y espectroscopia de voxel simple (2 ml) en el área de realce muestra baja Cho (B). El estudio de alta resolución (0,8 ml) (C y D) muestra múltiples áreas de aumento de Cho. Los estudios de difusión se han utilizado para evaluar la respuesta tumoral, ya que la disminución de la celularidad en relación con la respuesta tumoral provoca aumento del ADC y viceversa27. De nuevo es conveniente disponer de estudios previos para determinar si hay aumento o disminución del ADC respecto a los estudios anteriores. Teniendo en cuenta las ventajas e inconvenientes de cada técnica, si es posible es conveniente combinarlas (figs. 9 y 10), ya que cuando hay coincidencia entre ellas aumenta la fiabilidad y si hay incongruencias habrá que valorar otras posibilidades y plantear otras exploraciones, como los estudios metabólicos con PET-flúor-deoxiglucosa (PETFDG) (fig. 4). Algunos casos de radionecrosis pueden producir de forma transitoria descenso del ADC, ya que puede haber edema citotóxico en las primeras fases y, ocasionalmente, puede haber sangrado que en la fase subaguda provoca descenso del ADC (esta situación es válida para todas las circunstancias en las que se estudian los gliomas, por lo que siempre hay que comparar con otras secuencias para descartar la presencia de sangrado subagudo). La presencia de edema citotóxico es especialmente frecuente después de la radiocirugía, aunque ésta es una técnica más utilizada en las metástasis que en los gliomas; no obstante, la aparición de áreas con descenso del ADC indicaría un estudio exhaustivo de esa lesión utilizando otras técnicas para confirmación. 23/11/12 11:49:56 86 La imagen funcional en oncología Figura 8. Difusión en seguimiento de gliomas. Cortes axiales con mapas de difusión isotrópica con valor b = 3.000 en el caso de progresión tumoral (A y B), donde se observa aumento de señal en relación con restricción de la difusión, y en el caso de buena respuesta a tratamiento (C-E), donde se observa paulatina disminución de señal por aumento del coeficiente de difusión. Figura 9. Recurrencia de glioma de alto grado. Cortes axiales con secuencias FLAIR (A), T1 poscontraste (B), difusión isotrópica (b = 3.000) y perfusión (D), así como espectroscopia de voxel simple (1,4 ml) en el área de realce (E). Se observa lesión nodular con edema vasogénico e intenso realce, que presenta marcada restricción de la difusión (C) y aumento de vascularización (D). La espectroscopia muestra grandes picos en las frecuencias de Cho y lípidos/lactato. 4-9 38-101.indd 86 23/11/12 11:49:57 Papel de la resonancia magnética en el seguimiento de los gliomas 87 Figura 10. Respuesta completa en glioma de alto grado. Cortes axiales con secuencia T1 poscontraste (A), perfusión (B), difusión (C) y espectroscopia (D), y estudio de control a los 3 meses con la misma técnica (E-H). Se observa desaparición del realce, normalización de la vascularización, desaparición de la restricción de la difusión y marcada disminución de Cho con aparición de picos prominentes en la frecuencia de lípidos/lactato. Figura 11. Seudoprogresión. En la fila superior, estudio antes de tratamiento con radioterapia (60 Gy) y temozolamida con la misma técnica que la figura 10. En la fila intermedia, control a los 3 meses y en la fila inferior control a los 6 meses. En el primer control se observa aumento de tamaño de la lesión, que sugiere progresión, pero la difusión, perfusión y espectroscopia indican buena respuesta. Se continuó el tratamiento y 3 meses más tarde la lesión comenzó a presentar signos de respuesta en el estudio estructural. 4-9 38-101.indd 87 23/11/12 11:49:58 La imagen funcional en oncología 88 Figura 12. Seudorrespuesta. Recurrencia tumoral en tratamiento con bevacizumab e irinotecán. En la fila superior, estudio inicial con la misma técnica que las figuras anteriores, que muestra lesión con signos de agresividad. En la fila intermedia, el estudio a los 2 meses muestra criterios de McDonald de respuesta completa y signos de mejoría en perfusión, aunque la señal en FLAIR aumenta su volumen ligeramente y hay signos de progresión en difusión y espectroscopia. En el control a los 2 meses continúan los criterios de respuesta completa en T1 poscontraste y perfusión, pero hay claros signos de progresión en FLAIR, difusión y, en menor medida, en espectroscopia. El paciente fallece 4 semanas más tarde y la necropsia confirma progresión tumoral. En el tratamiento con antiangiogénicos no está claro el papel de las técnicas de difusión: en los primeros días se ha descrito descenso del ADC en relación con los cambios en la vascularización28, aunque posteriormente se ha descrito aumento del ADC relacionado con el efecto antitumoral, sobre todo cuando se asocian fármacos citotóxicos como irinotecán, lo cual ocurre frecuentemente. Hay poca experiencia acerca del efecto sobre el ADC de la progresión del fenotipo tumoral sin realce que se produce en la seudorrespuesta, aunque la restricción de la difusión sugiere progresión. No obstante, en los siguientes días del tratamiento antiangiogénico se han descrito áreas de restricción de la difusión que podrían estar relacionadas con los fenómenos vasculares y no con la respuesta tumoral28, por lo que es importante valorar siempre los estudios previos. Por otro lado, el análisis de histogramas, tanto del ADC como de la difusibilidad media y la anisotropía, utilizando secuencias de tensor de difusión son prometedoras29, pero requieren una más amplia validación. Conclusiones El seguimiento de los gliomas presenta especiales dificultades desde el punto de vista de la imagen no sólo por 4-9 38-101.indd 88 la complejidad propia de estos tumores, sino por los múltiples cambios que provocan los distintos tratamientos, incluyendo nuevas combinaciones de radio/quimioterapia y el uso de fármacos antiangiogénicos. Hay un claro consenso entre las diferentes especialidades implicadas en la neurooncología que admite las importantes limitaciones que presenta la RM estructural, aunque ésta continúa siendo la herramienta fundamental a la espera de una mayor estandarización y validación de las técnicas avanzadas en RM, sin olvidar las técnicas de medicina nuclear que, aunque no han sido objeto de esta revisión, probablemente jugarán un papel importante. El seguimiento de los gliomas necesitará un abordaje multidisciplinar y multimodal30, que incluirá nuevas combinaciones y fusiones de las técnicas emergentes (figs. 11 y 12), entre las que se encuentran la perfusión, la espectroscopia y la difusión. Bibliografía 1. Mullins ME, Barest GD, Schaefer PW, Hochberg FH, González RG, Lev MH. Radiation necrosis versus glioma recurrence: conventional MR imaging clues to diagnosis. AJNR Am J Neuroradiol. 2005;26:1967-72. 2. Brasil Caseiras G, Ciccarelli O, Altmann DR, Benton CE, Tozer DJ, Tofts PS, et al. Low-grade gliomas: six-month 23/11/12 11:49:58 Papel de la resonancia magnética en el seguimiento de los gliomas tumor growth predicts patient outcome better than admission tumor volume, relative cerebral blood volume, and apparent diffusion coefficient. Radiology. 2009;253:505-12. 3. Danchaivijitr N, Waldman AD, Tozer DJ, Benton CE, Brasil Caseiras G, Tofts PS, et al. Low-grade gliomas: do changes in rCBV measurements at longitudinal perfusion-weighted MR imaging predict malignant transformation? Radiology. 2008;247:170-8. 4. Murphy PS, Viviers L, Abson C, Rowland IJ, Brada M, Leach MO, et al. Monitoring temozolomide treatment of low-grade glioma with proton magnetic resonance spectroscopy. Br J Cancer. 2004;90:781-6. 5. Van den Bent MJ, Wefel JS, Schiff D, Taphoorn MJ, Jaeckle K, Junck L, et al. Response assessment in neuro-oncology (a report of the RANO group): assessment of outcome in trials of diffuse low-grade gliomas. Lancet Oncol. 2011;12:58393. 6. Brandsma D, Van den Bent MJ. Pseudoprogression and pseudoresponse in the treatment of gliomas. Curr Opin Neurol. 2009;22:633-8. 7. Macdonald DR, Cascino TL, Schold SC Jr, Cairncross JG. Response criteria for phase II studies of supratentorial malignant glioma. J Clin Oncol. 1990;8:1277-80. 8. Young RJ, Gupta A, Shah AD, Graber JJ, Zhang Z, Shi W, et al. Potential utility of conventional MRI signs in diagnosing pseudoprogression in glioblastoma. Neurology. 2011;76:1918-24. 9. Brandes AA, Tosoni A, Spagnolli F, Frezza G, Leonardi M, Calbucci F, et al. Disease progression or pseudoprogression after concomitant radiochemotherapy treatment: pitfalls in neurooncology. Neuro Oncol. 2008;10:361-7. 10. Jain R, Narang J, Sundgren PM, Hearshen D, Saksena S, Rock JP, et al. Treatment induced necrosis versus recurrent/progressing brain tumor: going beyond the boundaries of conventional morphologic imaging. J Neurooncol. 2010;100:17-29. 11. Hygino da Cruz LC Jr, Rodríguez I, Domingues RC, Gasparetto EL, Sorensen AG. Pseudoprogression and pseudoresponse: imaging challenges in the assessment of posttreatment glioma. AJNR Am J Neuroradiol. 2011;32:1978-85. 12. Barajas RF, Chang JS, Sneed PK, Segal MR, McDermott MW, Cha S. Distinguishing recurrent intra-axial metastatic tumor from radiation necrosis following gamma knife radiosurgery using dynamic susceptibility-weighted contrast-enhanced perfusion MR imaging. AJNR Am J Neuroradiol. 2009;30:367-72. 13. Batchelor TT, Sorensen AG, Di Tomaso E, Zhang WT, Duda DG, Cohen KS, et al. AZD2171, a pan-VEGF receptor tyrosine kinase inhibitor, normalizes tumor vasculature and alleviates edema in glioblastoma patients. Cancer Cell. 2007;11:83-95. 14. Norden AD, Young GS, Setayesh K, Muzikansky A, Klufas R, Ross GL, et al. Bevacizumab for recurrent malignant gliomas: efficacy, toxicity, and patterns of recurrence. Neurology. 2008;70:779-87. 15. Wen PY, Macdonald DR, Reardon DA, Cloughesy TF, Sorensen AG, Galanis E, et al. Updated response assessment criteria for high-grade gliomas: response assessment in neuro-oncology working group. J Clin Oncol. 2010;28:1963-72. 16. Brandsma D, Stalpers L, Taal W, Sminia P, Van den Bent MJ. Clinical features, mechanisms, and management of 4-9 38-101.indd 89 89 pseudoprogression in malignant gliomas. Lancet Oncol. 2008;9:453-61. 17. Kumar AJ, Leeds NE, Fuller GN, Van Tassel P, Maor MH, Sawaya RE, et al. Malignant gliomas: MR imaging spectrum of radiation therapy- and chemotherapy-induced necrosis of the brain after treatment. Radiology. 2000;217:377-84. 18. Nelson SJ, McKnight TR, Henry RG. Characterization of untreated gliomas by magnetic resonance spectroscopic imaging. Neuroimaging Clin N Am. 2002;12:599-613. 19. Arvinda HR, Kesavadas C, Sarma PS, Thomas B, Radhakrishnan VV, Gupta AK, et al. Glioma grading: sensitivity, specificity, positive and negative predictive values of diffusion and perfusion imaging. J Neurooncol. 2009;94:87-96. 20. Law M, Yang S, Wang H, Babb JS, Johnson G, Cha S, et al. Glioma grading: sensitivity, specificity, and predictive values of perfusion MR imaging and proton MR spectroscopic imaging compared with conventional MR imaging. AJNR Am J Neuroradiol. 2003;24:1989-98. 21. Sugahara T, Korogi Y, Tomiguchi S, Shigematsu Y, Ikushima I, Kira T, et al. Posttherapeutic intraaxial brain tumor: the value of perfusion-sensitive contrast-enhanced MR imaging for differentiating tumor recurrence from nonneoplastic contrast-enhancing tissue. AJNR Am J Neuroradiol. 2000;21:901-9. 22. Sorensen AG, Batchelor TT, Zhang WT, Chen PJ, Yeo P, Wang M, et al. A “vascular normalization index” as potential mechanistic biomarker to predict survival after a single dose of cediranib in recurrent glioblastoma patients. Cancer Res. 2009;69:5296-300. 23. Essock-Burns E, Lupo JM, Cha S, Polley MY, Butowski NA, Chang SM, et al. Assessment of perfusion MRI-derived parameters in evaluating and predicting response to antiangiogenic therapy in patients with newly diagnosed glioblastoma. Neuro Oncol. 2011;13:119-31. 24. Weybright P, Sundgren PC, Maly P, Hassan DG, Nan B, Rohrer S, et al. Differentiation between brain tumor recurrence and radiation injury using MR spectroscopy. AJR Am J Roentgenol. 2005;185:1471-6. 25. Zeng QS, Li CF, Zhang K, Liu H, Kang XS, Zhen JH. Multivoxel 3D proton MR spectroscopy in the distinction of recurrent glioma from radiation injury. J Neurooncol. 2007;84:63-9. 26. Kim H, Catana C, Ratai EM, Andronesi OC, Jennings DL, Batchelor TT, et al. Serial magnetic resonance spectroscopy reveals a direct metabolic effect of cediranib in glioblastoma. Cancer Res. 2011;71:3745-52. 27. Hein PA, Eskey CJ, Dunn JF, Hug EB. Diffusion-weighted imaging in the follow-up of treated high-grade gliomas: tumor recurrence versus radiation injury. AJNR Am J Neuroradiol. 2004;25:201-9. 28. Rieger J, Bahr O, Muller K, Franz K, Steinbach J, Hattingen E. Bevacizumab-induced diffusion-restricted lesions in malignant glioma patients. J Neurooncol. 2010;99:49-56. 29. Xu JL, Li YL, Lian JM, Dou SW, Yan FS, Wu H, et al. Distinction between postoperative recurrent glioma and radiation injury using MR diffusion tensor imaging. Neuroradiology. 2010;52:1193-9. 30. Matsusue E, Fink JR, Rockhill JK, Ogawa T, Maravilla KR. Distinction between glioma progression and post-radiation change by combined physiologic MR imaging. Neuroradiology. 2010;52:297-306. 23/11/12 11:49:58 La imagen funcional en oncología 8 Modificaciones en la estadificación por imagen de los tumores malignos pediátricos del SNC M.I. Martínez León Radiología Pediátrica, Hospital Materno-Infantil, Complejo Hospitalario Universitario Carlos Haya, Málaga, España Introducción La valoración de una serie de datos de imagen prequirúrgicos ayuda en la exactitud diagnóstica de la gradación de los tumores pediátricos malignos del sistema nervioso central (SNC); para ello se utiliza la combinación de la información de la resonancia magnética (RM) convencional o basal sumada a la de la difusión y su correlativo mapa de coeficiente de difusión aparente (mapa ADC), y otras técnicas avanzadas de difusión, espectroscopia de protón (ERM) y perfusión por resonancia (PRM)1. En el estudio de RM se realizan una serie de secuencias básicas para el diagnóstico tumoral (T1, T2, FLAIR, puede añadirse en determinadas secuencias la valoración con supresión grasa, sumando además el estudio con gadolinio) en los 3 planos del espacio. El estudio mediante difusión se realiza con factores b que oscilan entre 1.000 y 2.500 s/mm2. Se valora el ADC relativo (valores del mapa ADC) y pueden realizarse técnicas más complejas, como la imagen tensor de difusión, la imagen “q-ball”, la imagen del espectro de difusión y la tractografía2. La ERM se puede adquirir con voxel único o univoxel con tiempo de eco (TE) corto (23 ms) y largo (136-144 ms) y también con estudio multivoxel. Se valoran de forma aislada los diferentes metabolitos, siendo los principales en el contexto tumoral la colina (Cho), el N-acetil aspartato (NAA), la creatina, la taurina, los lípidos y el lactato, así como las ratios entre ellos. En la PRM se valora una serie de medidas, entre las que destaca por su utilidad el volumen sanguíneo cerebral relativo (rCBV). información limitada que ha de ser completada en relación al grado y el tipo tumoral3. La difusión realza el diagnóstico en este punto2 al valorar el estado “fisiológico” del tejido4,5. En un contexto tumoral, una difusión restringida, hiperintensa o brillante, con inversión de la señal en el mapa ADC o baja señal, es altamente predictiva de un tumor de alto grado (grados III y IV de la World Health Organization (WHO)6. Factores causantes de la restricción de la difusión en los tumores de alto grado son3: – Aumento de la celularidad. – Disminución del espacio extracelular3,7. – Alto porcentaje núcleo/citoplasma. Parece haber una clara correlación entre el mapa ADC, la celularidad y el grado tumoral (figs. 1 y 2). Esto permite en determinados casos el diagnóstico diferencial tumoral mediante la ayuda de los diferentes mapas ADC8: Difusión – M eduloblastoma, tumor neuroectodérmico primitivo (PNET) y pineoblastoma presentan menor señal en mapa ADC que el ependimoma. – Cuanto mayor es el grado del tumor astrocitario menor es el ADC, cumpliéndose, según la bibliografía, en los astrocitomas grados II a IV, excluyendo los astrocitomas grado I. – Los linfomas presentan menor señal en el mapa ADC que los glioblastomas y las metástasis (aunque éstos no suelen ser tumores pediátricos). – Los tumores disembrioplásicos neuroepiteliales tienen señal ADC mayor que otros tumores glioneurales de mayor grado, debido a su baja celularidad y al elevado espacio extracelular que muestran. La RM basal caracteriza de forma excelente la localización y extensión del tumor cerebral, pero proporciona una Algunos otros puntos a destacar referentes a la difusión8: Correo electrónico: marcela338@hotmail.com 4-9 38-101.indd 90 23/11/12 11:49:58 Modificaciones en la estadificación por imagen de los tumores malignos pediátricos del SNC A B C D A B C D 91 Figura 2. Restricción de la difusión en diseminación de tumores pediátricos de alto grado. Resonancia magnética (RM) plano axial secuencia T1 con contraste (A) y RM axial difusión b = 1.000 (B), realce con contraste (flecha blanca) y restricción de la difusión (flecha negra) en un nódulo correspondiente a diseminación intracraneal de meduloblastoma anaplásico. RM plano axial secuencia T2 (C) y RM axial difusión b = 1.000 en meduloblastoma atípico (D), alteración de la morfología de folias e infiltración subaracnoidea por el meduloblastoma, que presenta diseminación a líquido cefalorraquídeo con nódulos que restringen en la difusión (flechas largas). E F Figura 1. Restricción de la difusión en tumores pediátricos de alto grado. Resonancia magnética (RM) plano axial secuencia T1 con contraste (A) y RM difusión axial b = 1.000 (B), restricción marcada de la difusión (flechas cortas) de un tumor de fosa posterior correspondiente a meduloblastoma. RM plano axial secuencia T2 (C) y RM mapa de coeficiente de difusión aparente (mapa ADC) en tumor teratoide rabdoide atípico (D), baja señal en mapa ADC con relación a restricción de la difusión del componente sólido del tumor supratentorial maligno (flecha larga). RM plano axial secuencia FLAIR (E) y RM difusión axial b = 1.000 en pinealoblastoma (F), acentuado brillo por restricción de la difusión (flechas cortas) en este tumor de alta celularidad, que presenta señal intermedia homogénea en secuencias IR. – Cuanto mayor sea el grado tumoral de la WHO, menor será la señal del mapa ADC en tumores glioneurales, especialmente en los astrocitarios. – El mapa ADC puede ayudar a diferenciar ependimomas supratentoriales (especialmente los grado III) de astro- 4-9 38-101.indd 91 citomas grado II (difusos) supratentoriales, dado que los ependimomas tienen una clara menor señal en el mapa ADC. – Distinción muy precisa entre 2 tumores infratentoriales de alto grado de malignidad: meduloblastoma y ependimoma (mayor ADC los ependimomas, especialmente en los no anaplásicos o grado II). – En la bibliografía se refiere la menor restricción de la difusión de los ependimomas grado II con relación a los ependimomas grado III, hecho que no es una constante pero que puede ayudar en la diferenciación de grado de este tumor9. – El linfoma (maligno) tiene ADC muy bajo, menor que otros tumores grado IV como puedan ser el glioblastoma o las metástasis. La difusión sirve, además, no sólo en el diagnóstico, sino en la monitorización de la respuesta al tratamiento, dado que se ha comprobado que el mapa ADC aumenta de señal durante la quimioterapia, porque con ésta se reduce la celularidad y aumenta el espacio extracelular y, al contra- 23/11/12 11:49:59 92 rio, vuelve a tornarse de señal más hipointensa si hay una recidiva tumoral3. Sin embargo, la difusión y el mapa ADC no son de tanta ayuda en la distinción entre diferentes tumores del mismo grado, por ejemplo: PNET, tumor de células germinales maligno, astrocitoma grado IV, infiltración leucémica, todos ellos con la misma gradación, grado IV3. Resaltar que todos los PNET/meduloblastomas restringen. Por eso, es una forma excelente de diferenciar entre 2 frecuentes tumores de fosa posterior pediátricos, los meduloblastomas y los ependimomas; los meduloblastomas siempre restringen y los ependimomas generalmente no lo hacen, especialmente los no anaplásicos, grado II9. Al igual que en otros tumores, la información de cada una de las técnicas ha de englobarse en un contexto, y la difusión es de ayuda o apoyo en esta distinción, siempre incluida con el resto de técnicas y en el contexto clínico, epidemiológico y genético del paciente. Por ejemplo, la diferenciación entre tumor teratoide rabdoide atípico (ATRT) y meduloblastoma ha de ayudarse de otros datos además de en la restricción de la difusión de ambos10: – Edad de presentación: de 0-1 año el ATRT, alrededor de los 6 años el meduloblastoma. – Localización predominante: supratentorial, infratentorial o ambas el ATRT, sólo infratentorial el meduloblastoma. – Producción de hidrocefalia: ambos. – Diseminación (leptomeníngea y subaracnoidea): ambos. – Hemorragia intratumoral: más en los ATRT. – Heterogeneidad tumoral: más heterogéneos los ATRT. – Predominantemente sólido o sólido: meduloblastoma. – Difusión: en ambos está restringida. – Señal en secuencias potenciadas en T2: ambos presentan señal media o baja en la parte sólida del tumor, por elevado índice núcleo/citoplasma y por su hipercelularidad. Otro dato en el que la difusión puede dar información relevante es en la distinción de los límites tumorales. Se sugiere que tanto los tumores que realzan con gadolinio como los que no, pueden distinguirse del edema porque éste tiene índices de difusión mayores, por tanto, menor restricción cuando se compara con el tumor adyacente, presumiblemente debido a la mielina intacta del edema4, aunque, según determinados estudios7, es cuestionable que la difusión delimite mejor los límites entre edema y tumor que la combinación de señal T2 y realce con gadiolinio. La delimitación entre el tumor y el edema vasogénico adyacente mediante la ayuda de la difusión es importante para determinar con mayor exactitud el tamaño tumoral, los márgenes quirúrgicos, la toma de biopsia y el campo de radiación4,7. El edema citotóxico tiene señal baja en el mapa ADC y el edema vasogénico muestra señal alta en el mapa ADC con relación al parénquima adyacente. Esto puede ayudar en el estudio posquirúrgico tumoral inmediato complicado 4-9 38-101.indd 92 La imagen funcional en oncología con déficit neurológico agudo, puesto que teóricamente el edema posquirúrgico sería vasogénico y el isquémico, citotóxico, alto y bajo en ADC, respectivamente (ambos hiperintensos en SE T2)4. Espectroscopia La espectroscopia de protón es un método no invasivo, in vivo y no radiante para valorar los biomarcadores tumorales; permite predecir de forma muy acertada el grado de los tumores cerebrales pediátricos11. La espectroscopia permite la obtención no invasiva (sin biopsia) de moléculas o metabolitos intracelulares tumorales que definen estas neoplasias. Algunos autores publican que la espectroscopia “promete una nueva era en el manejo tumoral”11. El listado de metabolitos valorados por orden de aparición en el eje horizontal y con lectura de derecha a izquierda11 es el siguiente: 1. Lípidos: localización en 0,9 (1,3) ppm. Aparece en los tumores con necrosis, por ejemplo en el glioblastoma12 (fig. 3). 2. Alanina: localización en 1,47 (1,5) ppm. Es un marcador casi exclusivo de meningiomas, poco habituales en la edad pediátrica (pueden presentarse en contexto posradiación o englobados en las manifestaciones de la neurofibromatosis). 3. Lactato: 1,35. Aparece en glucólisis anaeróbica, su presencia es siempre patológica. Se muestra en cuadros de hipoxia o en consumo hipermetabólico de glucosa13. Puede presentarse en el contexto tumoral en determinadas ocasiones. 4. NAA o componentes de N-acetil: localización en 2,02 ppm. Es un marcador de neuronas y de sus prolongaciones o apéndices (dendritas)13. Disminuye de forma generalizada en los tumores. 5. Glutamato-glutamina: localización en 2,35 ppm. 6. Creatina (creatina y fosfocreatina): localización en 3,03 ppm. Es un metabolito indicador del metabolismo de energía14. 7. Cho: localización en 3,20 ppm. Los valores de Cho parece que se correlacionan directamente con la celularidad tumoral15 (fig. 4). Da idea de la estructura y función de membranas celulares a través del metabolismo de fosfolípidos y por eso se eleva en los tumores proliferantes con “turnover” celular elevado o en cualquier tejido que prolifera 13. Aunque los valores de Cho se aparejen con la celularidad tumoral, la celularidad no se correlaciona tan directamente con el grado tumoral en el contexto de los gliomas. Por eso, aunque la Cho es muy buen marcador para diferenciar entre los diferentes grados de glioma (a mayor malignidad mayor elevación de Cho), se necesitan otros datos como necrosis, atipia celular, mitosis e hiperplasia vascular para determinar malignidad16. Según otros autores, el marcador histológico de proliferación en gliomas es el 23/11/12 11:49:59 Modificaciones en la estadificación por imagen de los tumores malignos pediátricos del SNC 93 Figura 3. Estudio de espectroscopia en glioblastoma pediátrico. Resonancia magnética plano sagital secuencia T1 con contraste, realce heterogéneo con áreas de necrosis e invasión del cuerpo calloso. Espectroscopia univoxel con TE corto localizada en la masa tumoral muestra un elevado pico de lípidos (flecha) con disminución del resto de metabolitos; este patrón es uno de los más frecuentemente encontrados en los glioblastomas, en los que el aumento de lípidos es indicativo de necrosis intratumoral. Figura 4. Estudio de espectroscopia de pinealoblastoma. Estudio espectroscópico univoxel con TE corto muestra elevado pico de colina con un porcentaje Cho/Cr (creatina) > 2, así como llamativa reducción del pico de N-acetil aspartato en el interior del tumor. 4-9 38-101.indd 93 23/11/12 11:49:59 94 La imagen funcional en oncología Figura 5. Estudio de espectroscopia en meduloblastoma. Espectroscopia de hidrógeno, adquisición univoxel con TE corto (23). Flecha horizontal: colina (3,22 ppm). Elevado pico de colina, marcada reducción de N-acetil aspartato (NAA) y disminución de creatina. A este patrón indicativo de patología tumoral se suma la presencia de un pequeño pico de taurina cuya elevación está descrita en el meduloblastoma. Flecha larga: NAA (2,02 ppm); asterisco: taurina (3,36 ppm). Ki-67, y la Cho y el ki-67 van parejos en su elevación con el grado histológico del glioma12,15. Conforme más agresividad tiene el tumor, menor es el cociente NAA/ Cho, porque la disminución de NAA se incrementa y la elevación de Cho se aumenta. Los valores más altos de Cho se encuentran en los PNET, siendo el meduloblastoma el tumor pediátrico con mayor elevación de Cho, dado que es un tumor con rápido crecimiento y alta tasa de proliferación13,16. 8. Taurina (Tau): localización en 3,4 ppm. La Tau se eleva en meduloblastomas, PNET y pineoblastomas17 (fig. 5). Es un metabolito bastante específico de estos tipos tumorales. La conjunción de un tumor de línea media en fosa posterior asociado a elevación del metabolito Tau en la ERM es altamente específica de meduloblastoma. 9. Glicina y/o mioinositol: localización en 3,55 ppm. génesis tumoral. Un aumento de la micro y neovascularización tumorales conlleva un aumento del rCBV. El rCBV puede mostrar la vascularización tumoral de forma tanto cuantitativa como cualitativa19. La perfusión tumoral puede valorarse mediante 2 tipos diferentes de técnicas de PRM: En resumen, la ERM es más precisa que la RM convencional para definir los márgenes tumorales y cuantificar el grado de infiltración tumoral. Entre otras utilidades, la ERM está indicada para seleccionar el lugar donde se debe realizar la biopsia (en caso de tumores en los que no pueda realizarse resección), así como para definir la zona para mayor irradiación18. La angiogénesis y el incremento de la permeabilidad vascular son características de las neoplasias cerebrales; esto se puede reproducir con la utilización de la PRM. El CBV se incrementa con el grado tumoral, pudiendo servir de ayuda para identificar recidivas tumorales o edema perilesional, y diferenciar lesiones malignas de benignas18. La morfología vascular y el grado de angiogénesis son datos para evaluar el tipo de tumor y determinar su agresividad; la agresividad y el crecimiento tumorales se asocian con la neovascularización. Es la medida comparativa entre la hemodinámica vascular tumoral frente a la del parénquima normal19. La perfusión mediante el rCBV sirve para: Perfusión La perfusión proporciona información fisiológica de los tejidos con relación a la proliferación vascular y la angio- 4-9 38-101.indd 94 1. Contraste de susceptibilidad dinámica RM T2 (DSC). La DSC mide la farmacocinética del primer paso del contraste a través de un volumen determinado20, son imágenes rápidas en gradiente T2 durante el paso de un bolo de contraste paramagnético intravenoso18. 2. S ecuencias de contraste dinámico T1 (DCE). La DCE mide la permeabilidad capilar, derivándola mediante un modelo compartimental de series de imágenes en secuencias T119. 23/11/12 11:49:59 Modificaciones en la estadificación por imagen de los tumores malignos pediátricos del SNC – Señalar el área óptima donde ha de realizarse la biopsia tumoral (si es requerida biopsia por incompatibilidad para resección). – Diferenciar necrosis posradiación de resto tumoral. – Asesorar en la respuesta tumoral al tratamiento. Pero la perfusión en sí misma no es el principal dato diferenciador inicial en el diagnóstico del tumor, tiene mayor utilidad en el manejo y monitorización del tratamiento de los tumores19. El aumento de la vascularización no es sinónimo de malignidad. Sí lo es si se encuentra en el contexto de tumores gliales, pero no lo es en otros casos, por ejemplo, en el meningioma y en los tumores de plexos coroideos, que pueden ser altamente vasculares pero no tienen una conducta agresiva, no son tumores malignos de alto grado19. Como se ha comentado, en el caso de los diferentes grados de glioma y entre glioblastoma, metástasis y linfoma, sí presenta una función diagnóstica importante, mayor que la espectroscopia según algunos autores21. Sin embargo, esta última es una disquisición diagnóstica rara en la época pediátrica, dado que es infrecuente la presentación de glioblastomas en pediatría frente a otros tipos tumorales, y las metástasis al SNC tampoco son habituales a esta edad. Estudiando de forma independiente los resultados de la resonancia convencional, el valor rCBV de la perfusión y la espectroscopia, se observa que la medida de rCBV aislada es la que mayor capacidad diagnóstica presenta para predecir el grado en el caso de los gliomas14,15,19. El realce con contraste y el grado de perfusión (estudios T1 con contraste paramagnético y mapa rCBV, respectivamente) no van parejos, tienen un significado diferente. El realce está en relación con la rotura de la barrera hematoencefálica, de modo que a mayor ruptura mayor realce, mientras que la perfusión está en relación con el grado de hiperplasia (proliferación vascular) o neoformación vascular (angiogénesis vascular). Por eso, un tumor con poco realce puede presentar signos de intensa neovascularización en rCBV y viceversa, elevado realce mostrar bajos valores rCVB15,19. Conclusiones La RM tiene una serie de parámetros que, en principio, están asociados a elevación en el grado tumoral: edema importante, heterogeneidad lesional (sangrado, necrosis), efecto masa, foco tumoral a distancia, realce con contraste. En la espectroscopia, la elevación de Cho y disminución de NAA, presencia de lípidos o lactato, son signos de malignidad. Hay metabolitos bastante específicos de determinados tipos tumorales, como la Tau o la alanina. El valor de rCBV en el estudio de perfusión se correlaciona con la aproximación al grado tumoral en los gliomas. Según refleja la bibliografía, los datos más fidedignos para diagnosticar los tumores de alto grado corresponden principalmente a la necrosis intratumoral, el realce con gadolinio y los bajos valores del mapa ADC, aunque hay 4-9 38-101.indd 95 95 numerosas excepciones en el contexto de tumores del SNC pediátrico. Bibliografía 1. Guzmán de Villoria Lebiedziejewski JA. Combinación de la imagen, perfusión y espectroscopia de protón por resonancia magnética en la determinación del grado de agresividad en tumores cerebrales intraaxiales. Tesis Doctoral. 2. Hagmann P, Jonasson L, Maeder P, Thiran JP, Wedeen VJ, Meuli R. Understanding diffusion MR imaging techiques: from scalar diffusion-weighted imaging to diffusion tensor imaging and beyond. Radiographics. 2006;26:S205-23. 3. Kan P, Liu JK, Hedlund G, Brockmeyer DL, Walker ML, Kestle JRW. The role of diffusion-weighted magnetic resonance imaging in pediatric brain tumors. Childs Nerv Syst. 2006;22:1435-9. 4. Schaefer PW, Grant PE, González RG. Diffusion-weighted MR imaging of the brain. State of the art. Radiology. 2000;217:331-45. 5. Vázquez E, Delgado I, Sánchez-Montáñez A, Barber I, Sánchez-Toledo J, Enríquez G. Side effects of oncologic therapies in the pediatric central nervous system: update on neuroimaging findings. Radiographics. 2011;31:1123-39. 6. Louis DN, Ohgaki H, Wiestler OD, Cavenee WK, Burger PC, Jouvet A, et al. The 2007 WHO classification of tumours of the central nervous system. Acta Neuropathol. 2007;114: 97-109. 7. Stadnik TW, Chaskis C, Michotte A, Shabana WM, Van Rompaey K, Luypaert R, et al. Diffusion-weighted MR imaging of intracerebral masses: comparison with conventional MR imaging and histologic findings. AJNR Am J Neuroradiol. 2001;22:969-76. 8. Yamasaki F, Kurisu K, Satoh K, Arita K, Sugiyama K, Ohtaki M, et al. Apparent diffusion coefficient of human brain tumors at MR imaging. Radiology. 2005;235:985-91. 9. Martínez León MI, Vidal Denis M, Weil Lara B. Resonancia magnética en el ependimoma anaplásico infratentorial pediátrico. Radiología. 2012;54:59-64. 10. Koral K, Gargan L, Bowers DC, Gimi B, Timmons CF, Weprin B, et al. Imaging characteristics of atypical teratoid-rhabdoid tumor in children compared with medulloblastoma. AJR Am J Roentgenol. 2008;190:809-14. 11. Astrakas LG, Zurakowski, D, Tzika AA, Zarifi MK, Anthony DC, Girolami UD, et al. Noninvasive magnetic resonance spectroscopic imaging biomarkers to predict the clinical grade of pediatric brain tumors. Clin Cancer Res. 2004;10:8220-8. 12. Majós C, Alonso J, Aguilera C, Serrallonga M, Pérez Martín J, Acebes JJ, et al. Proton magnetic resonance spectroscopy (1H MRS) of human brain tumours: assessment of differences between tumour types and its applicability in brain tumour categorization. Eur Radiol. 2003;13:582-91. 13. Möller-Hartmann W, Herminghaus S, Krings T, Marquardt G, Lanfermann H, Pilatus U, et al. Clinical application of proton magnetic resonance spectroscopy in the diagnosis of intracranial mass lesions. Neuroradiology. 2002;44:371-81. 14. Law M, Young R, Babb J, Rad M, Sasaki T, Zagzag D, et al. Comparing perfusion metrics obtained from a single compartment versus pharmacokinetic modelin methods using dynamic susceptibility contrast-enhanced perfusion MR Imaging with glioma grade. AJNR Am J Neuroradiol. 2006;27:1975-82. 15. Law M, Yang S, Wang H, Babb JS, Johnson G, Cha S, et al. Glioma grading: sensitivity, specificity, and predictive 23/11/12 11:50:00 96 values of perfusion mr imaging and proton MR spectroscopic imaging compared with conventional MR imaging. AJNR Am J Neuroradiol. 2003;24:1989-98. 16. Martínez León MI. Meduloblastoma pediátrico: revisión y puesta al día. Radiología. 2011;53:134-45. 17. Chawla A, Emmanuel JV, Seow WT, Lou J, Teo HE, Lim CCT. Paediatric PNET: pre-surgical MRI features. Clin Radiol. 2007;62:43-52. 18. Fayed-Miguel N, Morales-Ramos H, Modrego-Pardo PJ. Magnetic resonance imaging with spectroscopy, perfusion and cerebral diffusion in the diagnosis of brain tumours. Rev Neurol. 2006;42:735-42. 4-9 38-101.indd 96 La imagen funcional en oncología 19. Hakyemez B, Edrogan C, Bolca N, Yildrim N, Gokalp G, Parlak M. Evaluation of different cerebral mass lesions by perfusion-weighted MR Imaging. J Magn Reson Imaging. 2006;24:817-24. 20. Fayed-Miguel N, Castillo-Blandiono J, Medrano-Lin J. Perfusion by magnetic resonance imaging: its physical foundations and clinical application. Rev Neurol. 2010;50: 23-32. 21. Weber MA, Zoubaa S, Schlieter M, Jüttler E, Huttner HB, Geletneky K, et al. Diagnostic performance of spectroscopic and perfusion MRI for distinction of brain tumors. Neurology. 2006;66:1899-906. 23/11/12 11:50:00 La imagen funcional en oncología 9 Cáncer de mama: aportación de la imagen funcional E. Pérez Gómez Unidad de Patología Mamaria, Hospital Universitario Dr. Josep Trueta, Girona, España Introducción En los últimos años han aparecido múltiples técnicas, como la resonancia magnética (RM) con realce de contraste1,2, la espectroscopia por RM (MRS) y la medicina nuclear sestamibi con tecnecio-99m metoxiisonitrilo, así como la tomografía por emisión de positrones (PET), que proporcionan información más allá de la imagen morfológica mediante la visualización de procesos biológicos como la neoangiogénesis tumoral, los metabolitos del tumor (MRS), un mayor número de mitocondrias celulares tumorales (sestamibi), y el metabolismo de las células tumorales (fluorodesoxiglucosa [FDG]). Wagenaar et al3 definen la imagen molecular como “la caracterización in vivo y la medición de los procesos biológicos a nivel celular y molecular”. Estos métodos de imágenes a nivel molecular han sido aclamados como el próximo gran avance para la imagen mamaria4. Estos avances de las técnicas de imagen pueden proporcionar detalles específicos del tumor que podrían llevar a la evaluación temprana de la respuesta al tratamiento, la individualización de las opciones de tratamiento y la detección incluso antes de que se desarrolle la enfermedad, como ahora se reconoce5. A continuación se expone un breve resumen de las principales técnicas de imagen funcional que tienen un papel relevante en el diagnóstico y seguimiento del cáncer de mama. Resonancia magnética-difusión Basada en el movimiento aleatorio (browniano) de las moléculas de agua bajo el campo magnético. Este movimiento puede ser transcelular, intracelular, extracelular o intracapilar, básicamente. Son secuencias EPI potenciadas en T2 con un factor b distinto para cada órgano a estudiar, recomendándose alrededor de b = 700 para mama. Es importante el concepto de efecto T2 (los cambios en la señal T2 influirán en las imágenes de difusión, señal independiente de la difusión del tejido). Puede objetivarse mediante un valor cuantitativo en mm2/s (el coeficiente de difusión aparente o ADC) creado por el equipo mediante un análisis de regresión a partir de los valores numéricos de señal de difusión, eliminando el efecto T2. Pueden crearse mapas con una intensidad de señal proporcional al grado de difusión del agua (fig. 1). Los valores elevados de ADC indicarán menor compactación celular y los bajos, mayor compactación. Por tanto pueden relacionarse con la celularidad, así como las características intrínsecas de las estructuras a estudio. Sus principales utilidades son: – Detección. Pueden identificarse imágenes dentro del parénquima mamario (alteraciones en la difusión) que podrán ser analizadas posteriormente. – Caracterización. En lesiones benignas o malignas; según dónde se establezca el umbral variará la sensibilidad y especificidad de esta técnica. Un umbral de 1,1 × 10–3 mm2/s presenta una sensibilidad del 80% y una especificidad del 81%. Un umbral en 1,31 × 10–3 mm2/s presenta una sensibilidad del 100% y una especificidad del 60%. También puede determinarse el subtipo histológico según los valores de ADC (tabla 1). A modo de ejemplo se muestran los valores estudiados por Kuroki et al6, donde se aprecia que la media de valor de ADC en las masas benignas es de 1,41 × 10–3 mm2/s, mientras que en las malignas es de 1,021 × 10–3 mm2/s. Dentro de las malignas, los valores varían en función de si es un carcinoma infiltrante, con una media de ADC de 0,91 × 10–3 mm2/s, o no infiltrante, con una media de ADC de 1,21 × 10–3 mm2/s. Además, estableció diferentes medias de ADC para los diversos subtipos. – Seguimiento posquirúrgico, facilitando la detección de recidivas. – Valoración del parénquima sano en diferentes condiciones (diabetes, lactancia, tratamiento hormonal sustitutivo, etc.). – Predicción de la respuesta a la quimioterapia (biomarcador “surrogate end point”)7-9. – Seguimiento de la respuesta a la quimioterapia, apreciando cambios precoces (primer ciclo) antes que los cambios morfológicos (RECIST)7-9. Correo electrónico: pgelsa@yahoo.com 4-9 38-101.indd 97 23/11/12 11:50:00 La imagen funcional en oncología 98 – Diferenciar entre lesiones benignas y malignas. En la tabla 2, extraída de un artículo de Bartella y Huang10, se describen la sensibilidad y especificidad según diferentes autores. La sensibilidad estudiada varía entre el 70 y el 100%, siendo más homogénea la especificidad, que oscila entre el 83 y el 88%, excepto en el caso de Tse et al, que la describieron del 100%. Los estudios realizados son escasos y con muestras relativamente pequeñas, pero coinciden en un alto valor predictivo positivo, del 82 al 100%. – Seguimiento en la respuesta a la quimioterapia. Pudiendo detectar descensos en el pico de colina antes que la reducción del volumen tumoral11. Figura 1. Mapa de coeficiente de difusión aparente en plano sagital de pecho derecho, con su correspondencia en el mismo corte en secuencia T1 poscontraste con supresión grasa. – Valoración de la persistencia de la enfermedad después del tratamiento neoadyuvante (fig. 2). Las principales ventajas radican en que mediante una técnica muy rápida, sin uso de contraste, se aumenta notablemente la especificidad de la RM convencional. Como limitaciones destacar la escasa resolución espacial de las imágenes resultantes, que puede compensarse mediante la fusión de imágenes con otras secuencias, la difusión es sensible a artefactos de movimiento, metálicos, de flujo. Además hay un solapamiento entre los valores de benignidad y malignidad. Resonancia magnética-espectroscopia La espectroscopia es un método no invasivo para obtener información a nivel molecular, basándose en el valor de colina (Cho) (trimetilamina) y sus metabolitos, componentes implicados en la síntesis de fosfolípidos de membrana. La Cho es prácticamente indetectable en el tejido mamario normal, pero se encuentra presente en la neoplasia mamaria. Los valores elevados de Cho indican elevada actividad y viabilidad. Las principales aplicaciones son: Podemos encontrarnos con falsos positivos por mejoría de la técnica, ya que detecta mínimas cantidades de Cho en lesiones benignas, como fibroadenomas o el adenoma tubular. Además, la mama lactante presenta valores elevados de Cho, lo que también puede originar falsos positivos. Como limitaciones, destacar que requiere una bobina y un software adaptados, el posprocesado no está automatizado, lo que implica tiempo y entreno del técnico y el radiólogo. Tanto la difusión como la espectroscopia no requieren el uso de contraste y presentan un prometedor futuro para su empleo de forma aislada (en combinación con T2 o STIR). Resonancia magnética-perfusión Es la evaluación funcional de la vascularización del tejido mamario y la lesión a estudio. Se basa en la neovascularización existente en las lesiones malignas, que condiciona un aumento del flujo sanguíneo y del volumen de sangre, midiendo el componente intravascular. Son secuencias GRE EPI T2* sensibles al descenso de señal T2* poscontraste. Es útil en la caracterización de lesiones y muy útil en la valoración de la respuesta a la quimioterapia, ya que detecta cambios en el flujo antes de que aparezcan los cambios morfológicos. La limitación principal es la complejidad de la técnica, que requiere una alta resolución espacial y temporal para obtener imágenes de calidad interpretables, además de un posprocesado específico, por lo que no está muy difundida. Tabla 1 − Media de valor de coeficiente de difusión aparente (ADC) de masas mamarias (× 10–3 mm2/s) Tipo de lesión Media ADC Desviación estándar Masa benigna Masa maligna Carcinoma ductal infiltrante Papilotubular Escirro Sólido-tubular Carcinoma no infiltrante 1,448 1,021 0,968 1,007 0,882 0,989 1,218 0,453 0,23 0,194 0,287 0,102 0,173 0,266 Extraída de Kuroki et al6. 4-9 38-101.indd 98 23/11/12 11:50:00 Cáncer de mama: aportación de la imagen funcional 99 Figura 2. A) Reconstrucción volumétrica con sustracción a los 70 s de inyección de contraste paramagnético, en una paciente en seguimiento de tratamiento neoadyuvante por T4 en mama izquierda. Se aprecia persistencia parcheada de la enfermedad en pecho izquierdo. B y C) Secuencias de difusión en plano sagital de mama derecha (B) e izquierda (C). En C se objetiva persistencia tumoral parcheada y engrosamiento cutáneo patológico. Tabla 2 − Metaanálisis de los estudios publicados sobre espectroscopia mamaria Estudio Lesiones malignas Lesiones benignas Sensibilidad (%) Especificidad (%) VPP ) (% Roebuck et al, 1998 Kvistad et al, 1999 Cecil et al, 2001 Young et al, 2001 Jagannathan et al, 2001 Tse et al, 2003 Huang et al, 2004 Bartella et al, 2006 Total 10 11 23 24 32 19 18 31 168 7 11 15 6 14 21 12 26 112 70 82 83 92 81 89 100 100 87 86 82 87 83 86 100 87 88 87 88 82 90 97 93 100 82 91 90 VPP: valor predictivo positivo. Destaca la elevada especificidad y el alto VPP en todos ellos. 4-9 38-101.indd 99 23/11/12 11:50:00 100 La imagen funcional en oncología Mamografía con contraste Consiste en la inyección de contraste yodado combinado con la realización de mamografía digital para el estudio del comportamiento dinámico de lesiones no concluyentes, la detección de lesiones ocultas, la descripción de la neoangiogénesis, la extensión de la enfermedad, así como la valoración de la respuesta a la quimioterapia y la detección de posibles recurrencias12. Las lesiones identificadas presentan un comportamiento dinámico de captación y eliminación de contraste, objetivable y medible. De modo similar a la semiología de la RM, las lesiones con captación de contraste precoz e intensa son, con mayor probabilidad, más malignas. Tomografía por emisión de positrones Figura 3. Adenopatía axilar derecha en el contexto de neoplasia mamaria ipsilateral, con resultado de punción negativa para metástasis. Después de administrar contraste ultrasonográfico se identifica un área hipoecogénica cortical cuya punción resultó positiva para metástasis. Ecografía con contraste Mediante la inyección intravenosa de microburbujas de gas (perfluorocarbonos) obtendremos una señal de forma repetida bajo la onda incidente de ultrasonidos. Obtendremos un área de perfusión y curvas de intensidad de señal/ tiempo que se correlacionan de forma estricta con el lecho neoangiogénico y no con el espacio tumoral extravascular (la RM dinámica con contraste refleja la extravasación al espacio tumoral extravascular). Es útil en el diagnóstico de lesiones mamarias, el estudio de su arquitectura vascular, la detección de recidivas y el seguimiento en el tratamiento quimioterápico. De especial interés es su uso en el estudio de extensión de enfermedad linfática. El contraste es retenido por el sistema reticuloendotelial ganglionar, el cual se encuentra sustituido por tejido neoplásico en las adenopatías metastásicas y, por tanto, no capta contraste; esta característica permite una mayor precisión para obtener material diagnóstico en la punción-aspiración con aguja fina (fig. 3). Está contraindicada en gestantes y durante la lactancia materna, en casos de angina inestable y en las 24 h postangina, así como en las 24 h previas a litotricia extracorpórea. 4-9 38-101.indd 100 El trazador usado es habitualmente la 18F-FDG. La intensidad de señal refleja la concentración del trazador, objetivable mediante el SUV (standard uptake value). Es útil en la estadificación locorregional y a distancia. Puede ayudar en la caracterización de lesiones, sospecha de recidivas, en pacientes con riesgo elevado de cáncer de mama, en la monitorización de la respuesta al tratamiento y se ha planteado como referencia útil en las terapias dirigidas, como por ejemplo en los tumores dependientes de hormonas (usando 18F-ES). Como limitaciones hay que destacar la irradiación que comporta este estudio y la no detección de tumores de pequeño tamaño13. Puede usarse también en combinación con la tomografía computarizada (PET-TC) y, aunque actualmente no se encuentra ampliamente disponible, se han diseñado equipos híbridos de RM y PET, muy útiles para el seguimiento del tratamiento neoadyuvante. Mamografía por emisión de positrones Equipo específico para el estudio de la mama, que se basa en el uso de un radiotrazador. Es un aparato manejable que se sitúa inmovilizando el pecho con la paciente sentada. El detector está próximo al pecho, obteniendo imágenes tomográficas en 3 dimensiones con proyecciones superponibles a la mamografía, y una resolución espacial de hasta 1,5 mm. Aporta información del metabolismo celular y no del componente neovascular. Puede usarse para detectar lesiones, adenopatías, seguimiento en el tratamiento neoadyuvante, detección de recidivas, etc. Con el soporte adecuado es útil para guiar biopsias y la localización prequirúrgica. Se ha descrito una especificidad superior a la RM (el 92,3 frente al 89,7%)14. Como inconveniente principal destaca la irradiación y el hecho de ser un soporte dedicado específicamente a la mama, lo que puede condicionar su adquisición masiva para realizar estudios con mayor número de pacientes. 23/11/12 11:50:00 Cáncer de mama: aportación de la imagen funcional Hay numerosas técnicas funcionales más allá del propósito de este artículo, ya que se encuentran en fase experimental o en centros de investigación (BOLD, ODI, tensor, elastografía dinámica, etc.). Conclusión Se describen brevemente las técnicas funcionales aplicadas a la patología mamaria más accesibles en nuestro entorno, enfatizando su aportación al aumento de la especificidad en la caracterización de lesiones, la monitorización precoz de la respuesta a la quimioterapia y su papel como biomarcador o surrogate end point. Bibliografía 1. Padhani AR, Hayes C, Assersohn L, Powles T, Makris A, Suckling J, et al. Prediction of clinicopathologic response of breast cancer to primary chemotherapy at contrastenhanced MR imaging: initial clinical results. Radiology. 2006;239:361-74. 2. Loo CE, Teertstra HJ, Rodenhuis S, Van de Vijver MJ, Hannemann J, Muller SH, et al. Dynamic contrastenhanced MRI for prediction of breast cancer response to neoadjuvant chemotherapy: initial results. AJR Am J Roentgenol. 2008;191:1331-8. 3. Wagenaar DJ, Weissleder R, Hengerer A. Glossary of molecular imaging terminology. Acad Radiol. 2001;8:409e20. 4. Birdwell RL, Mountford CE, Iglehart JD. Molecular Imaging of the Breast. AJR Am J Roentgenol. 2009;193:367-76. 5. Sardanelli F, Boetes C, Borisch B, Decker T, Federico M, Gilbert FJ, et al. Magnetic resonance imaging of the breast: recommendations from the EUSOMA working group. EJC. 2010;46:1296-316. 4-9 38-101.indd 101 101 6. Kuroki Y, Nasu K, Kuroki S, Murakami K, Hayashi T, Sekiguchi R, et al. Diffusion-weighted imaging of breast cancer with the sensitivity encoding technique: analysis of the apparent diffusion coefficient value. Magn Reson Med Sci. 2004;3:79-85. 7. Fangberget A, Nilsen LB, Hole KH, Holmen MM, Engebraaten O, Naume B, et al. Neoadjuvant chemotherapy in breast cancer-response evaluation and prediction of response to treatment using dynamic contrast-enhanced and diffusion-weighted MR imaging. Eur Radiol. 2011;21: 1188-99. 8. Iacconi C, Giannelli M, Marini C, Cilotti A, Moretti M, Viacava P, et al. The role of mean diffusivity (MD) as a predictive index of the response to chemotherapy in locally advanced breast cancer: a preliminary study. Eur Radiol. 2010;20: 303-8. 9. Pickles MD, Gibbs P, Lowry M, Turnbull LW. Diffusion changes precede size reduction in neoadjuvant treatment of breast cancer. Magn Reson Imaging. 2006;24:843-7. 10. Bartella L, Huang W. Proton (1H) spectroscopy of the breast. Radiographics. 2007;27:241-52. 11. Precht L, Lowe K, Atwood M, Beatty D. Neoadjuvant chemotherapy of breast cancer: tumor markers as predictors of pathologic response, recurrence, and survival. Breast J. 2010;16:362-8. 12. Schmitzberger FF, Fallenberg EM, Lawaczeck R, Hemmendorff M, Moa E, Danielsson M, et al Development of lowdose photon-counting contrast-enhanced tomosynthesis with spectral imaging. Radiology. 2010;259:558-64. 13. Brem RF, Rechtman LR. Nuclear medicine imaging of the breast: a novel, physiologic approach to breast cancer detection and diagnosis. Radiol Clin N Am. 2010;48: 1055-74. 14. Schilling K, Narayanan D, Kalinyak JE, The J, Velasquez MV, Kahn S, et al. Positron emission mammography in breast cancer presurgical planning: comparisons with magnetic resonance imaging. Eur J Nucl Med Mol Imaging. 2010;38:23-36. 23/11/12 11:50:00 4-9 38-101.indd 102 23/11/12 11:50:01