[editar]Definición
Anuncio
![[editar]Definición](http://s2.studylib.es/store/data/008533524_1-f53108428f2c43501e4a8807a3697a86-768x994.png)
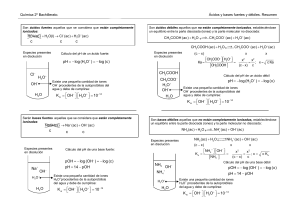
pH Para otros usos de este término, véase PH (desambiguación). El pH (potencial de hidrógeno) es una medida de acidez o alcalinidad de una disolución. El pH indica la concentración de ioneshidronio [H3O+] presentes en determinadas sustancias. La sigla significa "potencial de hidrógeno" (pondus Hydrogenii o potentiaHydrogenii; del latín pondus, n. = peso; potentia, f. = potencia; hydrogenium, n. = hidrógeno). Este término fue acuñado por el químicodanés Sørensen, quien lo definió como el logaritmo negativo en base 10 de la actividad de los iones hidrógeno. Esto es: Desde entonces, el término "pH" se ha utilizado universalmente por lo práctico que resulta para evitar el manejo de cifras largas y complejas. En disoluciones diluidas, en lugar de utilizar la actividad del ion hidrógeno, se le puede aproximar empleando la concentración molar del ion hidrógeno. Por ejemplo, una concentración de [H3O+] = 1 × 10–7 M (0,0000001) es simplemente un pH de 7 ya que: pH = –log[10–7] = 7 La escala de pH típicamente va de 0 a 14 en disolución acuosa, siendo ácidas las disoluciones con pH menores a 7 (el valor del exponente de la concentración es mayor, porque hay más iones en la disolución) , y alcalinas las que tienen pH mayores a 7. El pH = 7 indica la neutralidad de la disolución (cuando el disolvente es agua). Índice [ocultar] 1 Definición 2 Medida del pH 3 Solución “Buffer” 4 pH de algunas sustancias 5 Véase también 6 Referencias 7 Enlaces externos [editar]Definición El pH se define como el logaritmo negativo de base 10 de la actividad de los iones hidrógeno: Se considera que p es un operador logarítmico sobre la concentración de una solución: p = – log[...] , también se define el pOH, que mide la concentración de iones OH−. Puesto que el agua está adulterada en una pequeña extensión en iones OH– y H3O+, tenemos que: K(constante)w(water; agua) = [H3O+]·[OH–]=10–14 en donde [H3O+] es la concentración de iones hidronio, [OH−] la de ioneshidroxilo, y Kw es una constante conocida como producto iónico del agua, que vale 10−14. Por lo tanto, log Kw = log [H3O+] + log [OH–] –14 = log [H3O+] + log [OH–] 14 = –log [H3O+] – log [OH–] pH + pOH = 14 Por lo que se puede relacionar directamente el valor del pH con el del pOH. En disoluciones no acuosas, o fuera de condiciones normales de presión y temperatura, un pH de 7 puede no ser el neutro. El pH al cual la disolución es neutra estará relacionado con la constante de disociación del disolvente en el que se trabaje. [editar]Medida del pH Dependiendo del pH del suelo, la hortensia (Hydrangea) puede poseer flores rosas o azules. En suelos ácidos (pH < 7) las flores son azules, mientras que en suelos básicos (pH > 7) son rosas.1 El valor del pH se puede medir de forma precisa mediante un potenciómetro, también conocido como pH-metro, un instrumento que mide la diferencia de potencial entre doselectrodos: un electrodo de referencia (generalmente de plata/cloruro de plata) y un electrodo de vidrio que es sensible al ion de hidrógeno. También se puede medir de forma aproximada el pH de una disolución empleandoindicadores, ácidos o bases débiles que presentan diferente color según el pH. Generalmente se emplea papel indicador, que se trata de papel impregnado de una mezcla de indicadores cualitativos para la determinación del pH. El papel de litmus o papel tornasoles el indicador mejor conocido. Otros indicadores usuales son la fenolftaleína y el naranja de metilo. A pesar de que muchos potenciómetros tienen escalas con valores que van desde 1 hasta 14, los valores de pH también pueden ser aún menores que 1 o aún mayores que 14. Por ejemplo el ácido de batería de automóviles tiene valores cercanos de pH menores que uno, mientras que el hidróxido de sodio 1 M varía de 13,5 a 14. Un pH igual a 7 es neutro, menor que 7 es ácido y mayor que 7 es básico a 25 °C. A distintas temperaturas, el valor de pH neutro puede variar debido a la constante de equilibrio del agua (Kw). La determinación del pH es uno de los procedimientos analíticos más importantes y más usados en ciencias tales como química, bioquímica y la química de suelos. El pH determina muchas características notables de la estructura y actividad de las biomacromoléculas y, por tanto, del comportamiento de células y organismos. En 1909, el químico danés Sorensen definió el potencial hidrógeno (pH) como el logaritmo negativo de la concentración molar (más exactamente de la actividad molar) de los iones hidrógeno. [editar]Solución “Buffer” Diversas reacciones químicas que se producen en solución acuosa necesitan que el pH del sistema se mantenga constante, para evitar que ocurran otras reacciones no deseadas. Las soluciones reguladoras o "buffer" son capaces de mantener la acidez o basicidadde un sistema dentro de un intervalo reducido de pH. Estas soluciones contienen como especies predominantes, un par ácido/base conjugado en concentraciones apreciables. La reacción de neutralización: Es una reacción entre un ácido y una base, generalmente en las reacciones acuosas ácido-base se forma agua y una sal. El organismo posee tres mecanismos para mantener el pH en valores compatibles con la vida: 1. Los Amortiguadores. 2. La regulación pulmonar de la pCO2. 3. La resorción y eliminación renal de bicarbonato y la excreción de ácidos.2 [editar]pH de algunas sustancias El pH de la leche es de 6,5 , el pH de la sangre es aproximadamente entre 7,35 y 7,45. El pH de detergentes es de 10,5. El pH del zumo de limón es de 2. Para obtener un indicador orgánico se puede utilizar col morada siguiendo estos pasos: 1. Cortar la col en tiras. 2. En un mortero colocar la col morada y molerla. 3. Colocar alcohol en la disolución. 4. Filtrar la sustancia con un filtro de papel. 5. Colocar sustancias en varios recipientes como: bicarbonato de sodio, limón, pomelo, vinagre, agua o limpiador de horno. 6. Agregar en cada recipiente el indicador. Si los resultados son los siguientes se extrajo el indicador con éxito: Vinagre: color rosado (sustancia ácida) Bicarbonato de sodio: color verde (sustancia alcalina) Pomelo: color fucsia (sustancia ácida) Alcohol: color verde azulado (sustancia alcalina) Limpiador de horno: color amarillento (sustancia alcalina) Limón: color fucsia (sustancia ácida) . Agua: color violeta (sustancia neutra) [editar]Véase también Acidemia Alcalosis Anexo:Indicadores de pH Equilibrio químico Grado Dornic (otra medida de acidez) pKa pOH [editar]Referencias 1. ↑ Hydrangea - HGIC @ Clemson University (en inglés) 2. ↑ «pH Neutro» (en español) págs. 2 y 3. México: Investigación realizada por la Dirección Médica de Esteripharma. Consultado el 11 de julio de 2011. [editar]Enlaces externos