PRAKTIKA:
Anuncio

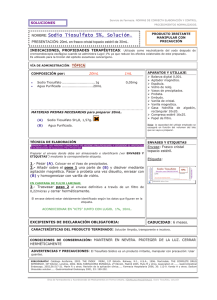
Colegio Urdaneta Ikastetxea . Técnicas de laboratorio PRÁCTICA: ESTUDIO DE LA FUSIÓN Y LA SOLIDIFICACIÓN OBJETIVO Estudiar el proceso de fusión y solidificación de una sustancia. INTRODUCCIÓN Al calentar una sustancia sólida con un foco de calor uniforme su temperatura se eleva linealmente con el tiempo hasta alcanzar la de fusión. Mientras dura el cambio de estado la temperatura permanece constante, y hasta que no se ha fundido toda la masa de sustancia la temperatura no vuelve a aumentar. La determinación del punto de fusión de una sustancia permite identificarla, pues toda sustancia pura tiene un punto de fusión fijo a la presión atmosférica, o comprobar su pureza, ya que las impurezas rebajan la temperatura de fusión. REACTIVOS Y MATERIAL *mechero *soporte *aro * rejilla *nuez doble (2) * vaso de precipitados * tubo de ensayo grande * varilla * pinzas * termórnetro de O a PROCEDIMIENTO 1. Poner agua en un vaso de precipitados hasta sus 2/3 partes aproximadamente. 2. Introducir en un tubo de ensayo grande el tiosulfato sódico hasta una altura de unos 2 cm y colocar dentro del tubo el termómetro, cuidando que el bulbo este completamente cubierto por el tiosulfato. 3. Introducimos el tubo en el vaso de precipitados hasta que el tiosulfato quede completamente sumergido en el agua y el tubo no toque el fondo del vaso. 4. Con todo ello hacemos el montaje de la figura: 5. Encendemos el mechero y calentamos el agua midiendo la temperatura cada minuto. 6. A partir de los 35ºC agitamos el agua y anotamos la temperatura cada 1/2 minuto, poniendo especial cuidado en anotar la temperatura a la que funde el tiosulafto, y anotando todas las observaciones de interés. 100ºC * cronóretro * tiosulfato sódico * espátula Colegio Urdaneta Ikastetxea . Técnicas de laboratorio 7. Cuando haya fundido todo el tiosulfato apagamos el mechero y retiramos el vaso de precipitados, sacando el tubo de ensayo fuera del vaso. Volvemos a anotar las temperaturas cada minuto observando bien cuando se empiezan a formar los primeros cristales. Dejamos de anotar sobre los 35ºC. PREGUNTAS 1.- Completa las siguientes tablas con los datos obtenidos: Calentamiento t (s) T ( º C) observaciones Enfriamiento t (s) T (°C) observaciones 2.- ¿Cuáles son los puntos de fusión y solicüficacidn del tiosulfato sódico? 3.- ¿Coinciden el punto de fusión por ti obtenido y el que nos da el fabricante del producto en la etiqueta del envase?. Si no es así, ¿cuál crees que es el motivo de la diferencia?. 4.- Dibuja en el mismo gráfico las curvas de calentamiento y enfriamiento del tiosulfato, representa el tiempo en abcisas y la temperatura en ordenadas. \