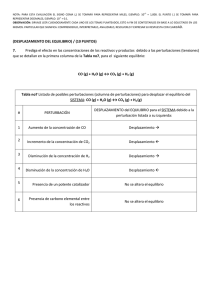
Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia EJERCICIO NÚMERO 108 Se va a diseñar una Planta Completa para la Producción de Óxido de Etileno y Etilenglicol. Como se muestra en el Diagrama de flujo, la Planta tendrá Cuatro Secciones Principales: El Ciclo de Oxidación Parcial de C2H4, la Sección de Purificación de C2H4O, el Reactor de Hidratación y la Sección de Purificación de Glicol. La Información Detallada de Proceso para cada Unidad es la siguiente: 1º. Reactor de Oxidación: Reacción Principal: Reacción Secundaria: 2 C2 H 4 + O 2 C2 H4 + 3 O2 → → 2 C2 H4 O 2 CO2 + 2 H2 O Con una corriente de Alimentación al Reactor de 5% de C2H4, 10% de O2 y 0,25% de CO2, la Conversión de C2H4 es de 40% y la Selectividad de C2H4O es de 70% (Selectividad=(moles de C2H4 convertidas a C2H4O)/(moles totales de C2H4 convertidas). 2º. Absorbedor: Todo el C2H4O y la mayor parte del CO2 se Absorbe de la corriente (4) y sale con la corriente (8). Veinte por ciento de la corriente (5) se Purga y abandona el Proceso en la corriente (6). 3º. Agotador: La corriente (8), que contiene 4% de CO2 y algo de H2O y C2H4O, se Agota con Vapor de Agua, corriente (11), para eliminar todo el CO2 y el C2H4O (junto con algo de agua), a través de la corriente superior (10). El agua restante se Recircula al Absorbedor, mediante la corriente (9). 4º. Condensadores Parciales: La corriente de Gas (10) que sale del Agotador, que contiene 30% de C2H4O, se enfría en el Condensador Parcial I para Eliminar por Condensación 50% del agua. El Gas Restante se enfría aún más en el Condensador Parcial II, en donde se licúa todo el agua y casi todo el C2H4O. El Gas de Descarga a la atmósfera del Condensador Parcial II contiene una cantidad despreciable de agua, todo el CO2 y una pequeña cantidad de C2H4O (0,4%). La Disolución de C2H4O/H2O que sale de la Unidad se Divide en el punto C en dos corrientes, una de las cuales se Purifica posteriormente para obtener el Producto C2H4O; la otra se Envía al Reactor de Hidratación, para Producir Etilenglicol. 5º. Deshidratador I: La corriente (16) se separa en un Producto C2H4O (con 99,5% de C2H4O) y una Corriente de Fondos (20) que contiene 40% de C2H4O. 6º. Reactor de Hidratación: Las corrientes (17) y (20) (que contienen C2H4O y H2O) junto con el Agua Condensada en el Condensador Parcial I, se Mezclan con Agua Fresca Adicional para obtener la corriente de Alimentación al Reactor de Hidratación, con una 161 Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia proporción molar de C2H4O a H2O de 1 a 20. En el Reactor, Todo el Óxido se Convierte a través de la reacción primaria: C2 H4 O + H2 O C2 H4 (OH)2 → y la reacción secundaria: C2 H4 O + C2 H4 (OH)2 → (C2 H4 OH)2 O La formación de Diglicol en la segunda reacción no es deseable; por lo tanto, se ajustan las condiciones de reacción de manera que se logra una Selectividad de 90% para el C2H4(OH)2 (etilenglicol). 7º. Tren de Separación: Como el etilenglicol debe ser 99% puro, la Corriente de Producto que sale del Reactor, corriente (22), que contiene una gran cantidad de agua, debe someterse a Varias Etapas de Purificación. En la Primera Etapa se Elimina suficiente agua por Evaporación para reducir el porcentaje en mol de H2O en la corriente (24) hasta 75%. El Agua Restante se Elimina por Destilación en el Deshidratador II. La Corriente de Domos de esta Unidad contendrá 2% de glicol y el resto es agua. La Corriente de Fondos (26) contendrá únicamente 0,5% de H2O y se Purificará aún más en la Columna de Terminado para producir una corriente de Fondos con 1% de glicol (el resto es diglicol). La Corriente de Producto (28) contiene algunas impurezas de H2O y diglicol, pero tiene una pureza del 99%. La Planta deberá producir 20000000 de libras de C2H4O/año y 25000000 de libras de C2H4(OH)2/año. a) Efectúe un análisis de Grados de Libertad para demostrar que el Proceso está especificado correctamente. b) Calcule todos los flujos y composiciones desconocidos. SOLUCIÓN: 1. DIAGRAMA CUALITATIVO: Puede verse en la página siguiente. 2. DIAGRAMA CUANTITATIVO: Puede verse después del Diagrama Cualitativo. Se asume que todos los porcentajes de las corrientes son molares. Las reacciones que ocurren en el Proceso son: Reactor de Oxidación: 2 C2 H4 + O2 C2 H4 + 3 O2 r2 → 162 r1 → 2 C2 H4 O 2 CO2 + 2 H2 O Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia C2 H4 Fresco Aire O2 , 21% N2 , 79% 1 M 1 2 C2 H4 , 5% CO2 , 0,25% N2 O2 , 10% H2 O C2 H4 CO2 N2 O2 H2 O C2 H4 CO2 N2 O2 H2 O 7 C2 H4 O, 30% CO2 H2 O D1 C2 H4 CO2 N2 O2 H2 O 3 REACTOR DE OXIDACIÓN Condensador Parcial 1 6 C2 H4 C2 H4 O CO2 N2 O2 H2 O 11 5 H2 O 10 9 A B S O R B E D O R A G O T A D O R 15 20 H2 O 21 COLUMNA DE TERMINADO 26 27 C2 H4 (OH)2 (C2 H4 OH)2 H2 O, 0,5% Poliglicoles C2 H4 (OH)2 , 1% C2 H4 O, 40% H2 O 24 EVAPORADOR 22 C2 H4 (OH)2 (C2 H4 OH)2 H2 O C2 H4 (OH)2 (C2 H4 OH)2 H2 O, 75% II (C2 H4 OH)2 163 C2 H4 O H2 O REACTOR DE HIDRATACIÓN 23 D E S H I D R A T A D O R D E S H I D R A T A D O R I M 2 Vapor de agua C2 H4 O CO2 , 4% H2 O C2 H4 O H2 O 18 25 28 16 17 H2 O C2 H4 O H2 O D2 C2 H4 O H2 O C2 H4 O H2 O CO2 19 H2 O C2 H4 (OH)2 , 2% H2 O Glicol Producto C2 H4 (OH)2 , 99% (C2 H4 OH)2 H2 O 12 11 8 4 13 C2 H4 O CO2 , 0,4% Condensador 14 Parcial 2 Producto C2 H4 O, 99,5% H2 O Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia 19 F =20000000 w19 C2 H4 O = 0,995 6 N x6C2H4 7 N x7C2H4 x7CO2 x7N2 1 NC2 H4 2 N 1 x2O2 = 0,21 (x2N2 = 0,79) 2 x7O2 (x7H2O ) M 1 6 5 x5CO2 3 x3O2 = 0,100 12 9 4 4 NC2 H4O 4 NCO2 4 NN2 4 NH2 O 4 NO2 Condensador Parcial 2 14 A G O T A D O R 13 20 M 2 20 N x20 C2 H4 O = 0,4 (x20 H2 O ) 21 N x8C2 H4O NC2 H4O 21 11 NH2 O 21 NH2 O 25 (x25 H2 O ) (x28 (C H4 OH) O ) 2 D E S H I D R A T A D O R 28 COLUMNA DE TERMINADO 27 27 N x27 C2 H4 (OH)2 = 0,01 (x27 (C H4 OH) O ) 2 2 23 NH2 O 25 2 26 23 24 22 EVAPORADOR 24 N x22 C2 H4 (OH)2 (x24 (C2 H4 OH) O ) (x22 H2 O ) x22 (C H4 OH) x24 C2 H4 (OH)2 2 2 26 N x26 H2 O = 0,005 x26 C2 H4 (OH)2 2 2 22 N x24 H2 O = 0,75 II (x26 (C H4 OH) O ) REACTOR DE HIDRATACIÓN 164 2 O D E S H I D R A T A D O R I 18 NH2 O 11 8 N x17 C2 H4 O (x17 H2 O ) 18 N x25 C2 H4 (OH)2 = 0,02 x28 H2 O 17 17 13 NH2 O (x8H2O ) 28 16 (x15 H2 O ) x8CO2 = 0,04 N x28 C2 H4 (OH)2 = 0,99 D2 15 N x15 C2 H4 O 12 16 N x16 C2 H4 O (x16 H2 O ) 15 NC2 H4O 8 4 19 12 NCO2 12 NH2 O A B S O R B E D O R NC2 H4 REACTOR DE OXIDACIÓN 10 (x10 H2 O ) 9 x5O2 (x5H2O ) 3 x3CO2 = 0,0025 x3N2 (x3H2O ) Condensador Parcial 1 NH2 O x5N2 N x3C2 H4 = 0,050 10 N x10 C2 H4 O = 0,3 x10 CO2 N x5C2 H4 (w19 H2 O ) (x14 CO2 ) D1 5 7 14 N x14 C2 H4 O = 0,004 x6CO2 x6N2 x6O2 (x6H2O ) Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia Reactor de Hidratación: r3 C2 H4 O + H2 O → C2 H4 (OH)2 r4 C2 H4 O + C2 H4 (OH)2 → (C2 H4 OH)2 O. 3. RELACIONES: R1: Reacciona el 40% del C2H4O. Lo que no reacciona es el 60%: 4 3 NC2 H4 = 0,6 NC2 H4 4 NC2 H4 = 0,6 * 0,05 N R2: 3 La Selectividad del C2H4O es del 70%: 4 NOE 0,7 = 3 0,4 NC2 H4 4 NOE 0,7 = R3: R4: 0,4 * 0,05 N 3 Se Purga el 20% de la corriente (5): N 6 N 5 = 0,2 En el Condensador Parcial I se elimina el 50% del agua: 13 10 13 10 10 NH2 O = 0,5 * (1 - x10 OE - xCO2 ) N 10 NH2 O = 0,5 * (1 - x10 OE - xCO2 ) N R5: La Proporción molar entre el C2H4O y el H2O a la salida del Mezclador 2 es de 1 a 20: 21 NOE 1 = 21 20 N H2 O R6: Reacciona todo el C2H4O y la Selectividad para el etilenglicol es del 90%: La Conversión del C2H4O es del 100% y el 90% forma C2H4(OH)2. Expresando la Selectividad en función de las velocidades de las dos reacciones en el Hidratador se obtiene que: 165 Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia r3 R7: r3 = 0,9 + r4 Restricciones del Divisor I: RDI = (5 - 1) (2 - 1) = 4 R8: Restricciones del Divisor II: RDII = (2 - 1) (2 - 1) = 1 4. GRADOS DE LIBERTAD DEL PROCESO: NVI: 77 (N1C H , N2 , x2O , N3 , x3C H , x3O , x3CO , x3N , N4C H , N4N , N4O , N4CO , 2 4 2 4 2 2 2 2 2 2 4 2 2 4 4 5 6 NOE , NH2 O , N , x5C2 H4 , x5O2 , x5CO2 , x5N2 , N , x6C2 H4 , x6O2 , x6CO2 , x6N2 , 7 8 9 10 10 N , x7C2 H4 , x7O2 , x7CO2 , x7N2 , N , x8OE , x8CO2 , NH2 O , N , x10 OE , xCO2 , 11 12 12 12 13 14 15 16 17 15 16 NH2 O , NCO2 , NOE , NH2 O , NH2 O , N , x14 OE , N , xOE , N , xOE , N , 18 20 21 21 22 23 24 19 20 22 22 19 x17 OE , NH2 O , F , wOE , N , xOE , NOE , NH2 O , N , xG , xD , NH2 O , N , 25 26 27 28 26 28 24 25 26 27 28 x24 H2 O , xG , N , xG , N , xH2 O , xG , N , xG , N , xG , xH2 O , r1, r2, NBMI: NFC: NCC: r3 , r 4 ) 50 (Mezclador 1: 5(C2H4, O2, N2, H2O, CO2); Divisor: 5(C2H4, O2, N2, H2O, CO2); Reactor de Oxidación: 6(C2H4, O2, N2, H2O, CO2, OE); Absorbedor: 6(C2H4, O2, N2, H2O, CO2, OE); Agotador: 3(H2O, CO2, OE); Condensador I: 3(H2O, CO2, OE); Condensador II: 3(H2O, CO2, OE); Divisor: 2(H2O, OE); Deshidratador I: 2(H2O, OE); Mezclador 2(H2O, OE); Reactor de Deshidratación: 4(H2O, OE, G, D); Evaporador: 3(H2O, G, D); Deshidratador II: 3(H2O, G, D) Columna de Terminado: 3(H2O, G, D)) 2 (F19 = 20000000, F28 = 25000000) 14 (x1O = 0,21; x3C H = 0,05; x3O = 0,1; x3CO = 0,0025; 2 2 4 2 2 19 14 x8CO2 = 0,04; x10 OE = 0,3; xOE = 0,004; xOE = 0,995; 24 25 x20 OE = 0,4; xH2 O = 0,75; xG = 0,02; NRC: G de L: 28 x27 G = 0,01; xG = 0,99) 11 (R1, R2, R3, R4, R5, R6, 4 R7, 1 R8) 0 166 x26 H2 O = 0,005 Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia Con la determinación de la diferencia entre el Número de Incógnitas y el Número de Ecuaciones se corroboran los Grados de Libertad y con el número de ecuaciones se conoce el tamaño del sistema que debe formularse para hallar las variables desconocidas del Proceso. INCÓGNITAS = (NVI - NFC - NCC) = 77 - 2 - 14 = 61 ECUACIONES = (NBMI + NRC) = 50 + 11 = 61 Las especificaciones del ejercicio son correctas. El Proceso tiene 0 Grados de Libertad. Se debe formular y resolver un sistema de 61 ecuaciones con 61 incógnitas. Base de Cálculo: 1 día. Los flujos conocidos para un año se pasan a flujo por día. Se asume un año comercial de 360 días. Como el flujo conocido de la corriente (28) es másico y se tomaron el flujo y sus fracciones molares como variables, debe hallarse su masa molecular media y con ella calcular el flujo 28 molar N . Sin embargo, la masa molecular media de la corriente (28) queda en función de x28 H2 O , que 28 es una variable desconocida. Por tanto, el flujo N se asume como una Relación, R9, para disminuir la complejidad de las ecuaciones de balance. Desaparece un flujo (pasan de 2 a 1) y aparece una Relación (pasan de 11 a 12): Los Grados de Libertad siguen valiendo CERO. Se tiene, en definitiva, un sistema de 62 ecuaciones con 62 incógnitas. Este es un caso interesante, porque un flujo, aparentemente conocido, debe ser tratado como una Relación. Similar a cuando se tomó como Base el componente C en el problema de Destilación Simple que se propuso y resolvió al comienzo de este trabajo. Dividiendo el flujo másico diario por la masa molecular media se encuentra que: R9: N 28 = 25000000 360 28 0,99 * 62 + x28 H2 O * 18 + (1 - 0,99 - xH2 O ) * 106 El flujo másico diario de la corriente (19) será: F 19 = 20000000 360 5. ECUACIONES DEL PROCESO: Ecuaciones en el Mezclador 1: Total: N 3 1 = N C 2 H4 + N 167 2 + N 7 (1) Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia 0,1 N C2H4: 3 = x2O2 N + x7O2 N 3 = 0,21 N + x7O2 N x3O2 N O2 : x3C2 H4 N 3 2 2 1 = 0,05 N 3 N C 2 H4 N 3 = x7CO2 N x3N2 N 3 3 3 = 0,79 N 2 2 7 7 (3) 7 = x7CO2 N = (1 - x2O2 ) N x3N2 N (2) + x7C2 H4 N 1 0,0025 N N2 : 3 7 = NC2 H4 + x7C2H4 N x3CO2 N CO2: 7 7 (4) + x7N2 N + x7N2 N 7 7 (5) Ecuaciones en el Divisor I: Total: C2H4: N x6C2 H4 N 6 + N 7 = N + x7C2 H4 N 6 + x7O2 N 6 + x7CO2 N O2 : x6O2 N 5 (6) = x5C2H4 N + x7N2 N x6N2 N x6CO2 N 7 6 N2: CO2: 6 7 = x5N2 N 7 = x5O2 N 7 5 5 (8) 5 = x5CO2 N (7) (9) 5 (10) Ecuaciones en el Reactor de Oxidación: Las reacciones son: r1 2 C2 H4 + O2 C2 H4 + 3 O2 4 NOE C2H4O: 4 NCO2 CO2: 4 NCO2 C2H4: 2 C2 H 4 O → r2 2 CO2 + 2 H2 O → = 2 r1 (11) 3 = x3CO2 N + 2 r2 = 0,0025 N 4 3 + 2 r2 (12) 3 NC2 H4 = x3C2 H4 N - 2 r1 - r2 4 N C 2 H4 3 = 0,05 N - 2 r1 - r2 168 (13) Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia 4 3 N2 : NN2 = x3N2 N O2 : NO2 = x3O2 N - r1 - 3 r2 4 3 4 3 (14) NO2 = 0,1 N - r1 - 3 r2 (15) 4 3 NH2 O = (1 - x3C2 H4 - x3O2 - x3CO2 - x3N2 ) N + 2 r2 H2O: 4 3 NH2 O = (1 - 0,05 - 0,1 - 0,0025 - x3N2 ) N + 2 r2 (16) Ecuaciones en el Absorbedor: x5C2H4 N C2H4: x8OE N C2H4O: x5CO2 CO2: N x5CO2 N 5 5 N2 : (1 - x8OE - x8CO2 ) 8 8 4 = N C 2 H4 + 8 = NOE N 8 + 0,04 N N + (1 - N 5 x5C2 H4 (17) 4 x8CO2 x5N2 H2O: 5 = 8 = 4 = NCO2 (19) 4 NN2 x5O2 - (18) 4 NCO2 (20) x5CO2 - - x5N2 ) N 5 = 5 = (1 - x8OE - 0,04) N + (1 - x5C2 H4 - x5O2 - x5CO2 - x5N2 ) N 4 N H2 O 4 + 9 N H2 O 9 N H2 O + N H2 O O2 : x5O2 N 5 = 4 NO2 (21) (22) Ecuaciones en el Agotador: N Total: 10 9 8 10 = x8OE N 10 = x8OE N 10 = x8CO2 N 10 = 0,04 N x10 OE N C2H4O: 0,3 N x10 CO2 N CO2: 11 + N H2 O = N + N H2 O x10 CO2 N (23) 8 8 (24) 8 8 (25) Ecuaciones en el Condensador Parcial I: 12 12 12 13 Total: NOE + NCO2 + NH2 O + NH2 O = N C2H4O: NOE = x10 OE N 12 169 10 10 (26) Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia 12 10 (27) 12 10 (28) NOE = 0,3 N CO2: NCO2 = x10 CO2 N Ecuaciones en el Condensador Parcial II: Total: N 15 + N 14 x15 OE N C2H4O: x15 OE N 12 15 15 x14 OE N + 14 0,004 N + 14 CO2: 12 12 = NOE + NCO2 + NH2 O (1 - xOE ) N 12 = NOE 14 12 = NOE 14 = NCO2 14 = NCO2 (1 - 0,004) N (29) (30) 12 12 (31) Ecuaciones en el Divisor II: Total: N C2H4O: x16 OE N 16 16 + N 17 + x17 OE N = N 17 15 (32) = x15 OE N 15 (33) Ecuaciones en el Deshidratador I: 19 Total: (1 - w19 OE )F + MMH2 O w19 OE F MMOE 19 + N 20 = N 16 0,995 * 20000000 0,005 * 20000000 20 16 + + N = N 44 * 360 18 * 360 19 w19 OE F MMOE C2H4O: + x20 OE N 20 = x16 OE N (34) 16 0,995 * 20000000 20 16 + 0,4 ∗ N = x16 OE N 44 * 360 (35) Ecuaciones en el Mezclador 2: Total: C2H4O: 21 21 13 18 NOE + NH2 O = NH2 O + NH2 O + N 21 17 + x20 OE N 21 17 + 0,4 N NOE = x17 OE N NOE = x17 OE N 170 17 + N 20 (36) 20 20 (37) Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia Ecuaciones en el Reactor de Hidratación: x22 G N Glicol: 22 = r3 - r4 x22 D N Diglicol: 22 (38) = r4 (39) 21 (40) 0 = NOE - r3 - r4 C2H4O: 22 (1 - x22 G - xD ) N H2O: 2 21 = NH2 O - r3 (41) Ecuaciones en el Evaporador: N Total: 23 + N H2 O = N x24 G N Glicol: H2O: 24 24 = x22 G N 22 (42) 22 (43) 23 24 22 = (1 - x22 G - xD ) N 23 24 22 = (1 - x22 G - xD ) N NH2 O + x24 H2 O N NH2 O + 0,75 N 22 22 (44) Ecuaciones en el Deshidratador II: N Total: H2O: Glicol: 25 + N 26 = N (1 - x25 G )N 25 + x26 H2 O N (1 − 0,02) N 25 + 0,005 N x25 G N 25 0,02 N + x26 G N 25 26 26 + x26 G N 24 = x24 H2 O N 26 24 = 0,75 N = x24 G N 26 (45) 24 (46) 24 = x24 G N 24 (47) Ecuaciones en la Columna de Terminado: Total: Glicol: N + N 28 = N 27 + x28 G N 27 + 0,99 N x27 G N 0,01 N H2O: 27 x28 H2 O N 28 28 28 26 = x26 G N 26 26 = x26 G N = x26 H2 O N 171 (48) 26 (49) Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia x28 H2 O N 28 = 0,005 N 26 (50) Ecuaciones de las Relaciones: 4 3 De R1: NC2 H4 = 0,6 * 0,05 * N De R2: NOE = 0,7 * 0,4 * 0.05 N De R3: N = 0,2 * N De R4: NH2 O = 0,5 * (1 - 0,3 - x10 CO2 ) * N 4 6 21 20 * NOE r3 = De R6: De R7: De R8: N = (52) (53) 10 (54) 21 (55) = N H2 O 0,9 * (r3 + r4 ) (56) x5C2 H4 = x6C2 H4 (57) x5N2 = x6N2 (58) x5O2 = x6O2 (59) x5CO2 = x6CO2 (60) 16 x15 OE = xOE (61) De R9: 28 5 5 13 De R5: (51) (0,99 * 62 + x28 H2 O 25000000 360 * 18 + (1 - 0,99 - x28 H2 O ) * 106 (62) 6. LA SOLUCIÓN AL SISTEMA DE ECUACIONES ES: 1 2 N = 201983,3689 NC2 H4 = 6059,5011 4 NCO2 = 3068,5313 NN2 = 154597,4934 NO2 = 14974,0371 NC2 H4 = 5251,5676 N = 39138,6059 x3N2 = 0,76539714 4 NH2 O = 191469846 4 4 5 4 4 x5C2 H4 = 0,03076022 NOE = 2757,8809 N x5CO2 = 0,00320419 x5N2 = 0,78479273 x5O2 = 0,07601362 x6C2 H4 = 0,03076022 x6CO2 = 0,00320419 x6N2 = 0,78479273 x6O2 = 0,07601362 x7C2 H4 = 0,03076022 x7CO2 = 0,00320419 N = 157593,1954 x7N2 = 0,78479273 x7O2 = 0,07601362 N = 60933,3328 NH2 O = 57320,3986 9 N 11 NCO2 = 2437,3333 N 6 = 39398,2988 NH2 O = 5580,0022 = 196991,4942 3 8 10 = 9192,9364 12 172 7 x8OE = 0,04526063 x10 CO2 = 0,26513110 12 NH2 O = 1998,8611 Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia 13 12 NH2 O = 1998,8611 N N = 4746,9535 x16 OE = 0,57891707 15 x15 OE = 0,57891707 N = 4178,5562 x17 OE = 0,57891707 18 N H2 O = 21 N H2 O = 25853,2959 N = 2906,8110 29835,5860 N NOE = 2757,8809 N 17 = 2447,1218 16 = 568,3973 20 22 14 21 NOE = 1491,7793 x22 G = 0,04000000 = 29835,5860 23 N = 5370,4055 25 N N = 145,7588 27 N = 1121,1061 x28 H2 O = 0,00565007 r1 = 1378,9405 r2 = 1281,7865 r3 = 1342,6014 r4 = 149,1779 x22 D = 0,00500000 NH2 O = 24465,1805 x24 G = 0,22222222 N = 4103,5406 x26 G = 0,87724638 24 26 = 1266,8649 28 5. RESUMEN DEL BALANCE DE MATERIA: COMPONENTES C2H4 O2 N2 C2H4O H2O CO2 Glicol Diglicol TOTAL COMPONENTES C2H4 O2 N2 C2H4O H2O CO2 Glicol Diglicol TOTAL 1 147043,893 _________ _________ FLUJOS MÁSICOS 2 3 _________ 282776,716 263011,432 646346,780 865745,963 4328729,800 4 169666,031 479169,184 4328729,815 121346,760 344645,723 135015,377 _________ _________ _________ _________ _________ _________ _________ 298501,421 22218,171 _________ _________ _________ _________ _________ _________ _________ _________ 147043,893 5 169666,048 479169,171 4328729,791 _________ 373126,774 27772,720 1128757,395 5578572,888 FLUJOS MÁSICOS 6 7 33933,209 135732,838 95833,834 383335,337 865745,957 3462983,833 _________ 74625,355 5554,544 _________ 298501,419 22218,176 5578572,890 8 _________ _________ _________ 121346,765 1003286,132 107242,666 _________ _________ _________ _________ _________ _________ _________ _________ 5378464,504 1075692,899 173 4302771,603 1231875,563 Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia COMPONENTES C2H4 O2 N2 C2H4O H2O CO2 Glicol Diglicol TOTAL COMPONENTES C2H4 O2 N2 C2H4O H2O CO2 Glicol Diglicol TOTAL COMPONENTES C2H4 O2 N2 C2H4O H2O CO2 Glicol Diglicol TOTAL 9 FLUJOS MÁSICOS 10 11 12 _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ 121346,760 71958,999 107242,667 _________ 121346,760 35979,500 107242,665 _________ _________ _________ _________ _________ _________ _________ _________ 300548,426 100440,038 264568,925 1031767,175 _________ 1031767,175 13 100440,038 _________ FLUJOS MÁSICOS 14 15 16 _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ 120916,066 35979,500 106437,651 31671,336 _________ 430,693 35979,500 _________ _________ 107242,666 _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ 35979,500 107673,359 156895,566 138108,987 17 FLUJOS MÁSICOS 18 19 20 _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ 14478,416 4308,163 _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ 18786,579 465359,326 465359,326 174 55277,778 277,778 55555,556 51159,874 31393,556 82553,430 Ben-Hur Valencia Valencia Profesor Titular Universidad Nacional Balance de Materia COMPONENTES C2H4 O2 N2 C2H4O H2O CO2 Glicol Diglicol TOTAL COMPONENTES C2H4 O2 N2 C2H4O H2O CO2 Glicol Diglicol TOTAL 21 FLUJOS MÁSICOS 22 23 24 _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ 65638,289 537040,548 512873,723 440373,249 _________ _________ _________ _________ _________ 73992,253 15812,861 602678,837 _________ 73992,253 15812,862 162305,589 _________ 602678,837 25 _________ 440373,249 FLUJOS MÁSICOS 26 27 72500,474 28 _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ _________ 72386,456 _________ 5088,390 _________ 77474,846 114,018 _________ 68903,864 15812,860 84830,742 175 _________ _________ 90,370 15295,928 15386,298 114,018 _________ 68813,492 516,934 69444,444