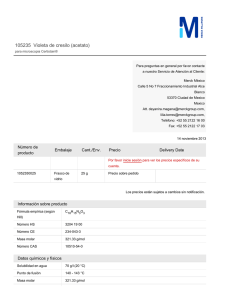
EQUILIBRIO QUÍMICO VELOCIDAD DE REACCIÓN COMPLEJO ACTIVADO TEORÍA DE LAS COLISIONES: LOS REACTIVOS DEBEN CHOCAR DEBEN ALINEARSE DE MANERA ADECUADA PARA ROMPER Y FORMAR ENLACES: FORMACIÓN DEL COMPLEJO ACTIVADO COMPLEJO ACTIVADO: ASOCIACIÓN DE ÁTOMOS TRANSITORIA DE ALTA ENERGÍA LA COLISIÓN DEBE APORTAR LA ENERGÍA MÍMINA: ENERGÍA DE ACTIVACIÓN. VELOCIDAD DE REACCIÓN Diferencia entre una reacción exotérmica y endotérmica VELOCIDAD DE REACCIÓN PUEDE DECIRSE QUE ES LA RAPIDEZ EN QUE LOS REACTIVOS SE TRANSFORMAN EN PRODUCTO, ES DECIR EL CAMBIO DE CONCENTRACIÓN POR UNIDAD DE TIEMPO LA CINÉTICA QUÍMICA ES LA PARTE DE LA QUÍMICA QUE ESTUDIA LA VELOCIDAD O RAPIDEZ EN LAS REACCIONES QUÍMICAS SI HABLAMOS DE RAPIDEZ SIMPLEMETE ES EL CAMBIO DE CONCENTRACIÓN ENTRE EL CAMBIO DE TIEMPO SI ES VELOCIDAD ENTONCES, APLICAMOS LA LEY DE VELOCIDAD ORDEN DE UNA REACCIÓN QUÍMICA El término "orden de reacción" se refiere a cómo la concentración de uno o más reactivos (químicos) afectan la velocidad de reacción Se denomina orden parcial respecto a la sustancia j al exponente a que aparece elevada la concentración de dicha sustancia. El orden total, n es la suma algebraica de los exponentes: n = α + β + ... Los ´ordenes de reacción pueden ser números positivos o negativos, enteros o fraccionarios y no están ligados a los coeficientes estequiométricos de la reacción (global). Sus valores no dependen de como se ajuste la reacción. La k que aparece en la ecuación cinética recibe el nombre de constante de velocidad y es función de la temperatura. Al aumentar la temperatura, la constante de velocidad también aumenta. La constante de velocidad tiene unidades que, en el caso de ecuaciones en términos de concentraciones molares, son: s −1 · mol1−n · L n−1 EJEMPLOS 1. Determina los órdenes de reacción total y parciales de las reacciones anteriores: a) H2 (g) + I2 (g) ---------- 2 HI (g) v = k x [H2] x [I2] b) H2 (g) + Br2 (g) ---------- 2 HBr (g) v = k x [H2] x [Br2]1/2 En la obtención del ácido nítrico, una de las etapas principales es la oxidación del óxido nítrico a dióxido de nitrógeno: 2 NO(g) + O2(g) --------- 2 NO2(g). Para esta reacción, se ha determinado experimentalmente que su ecuación de velocidad es: v = k [NO]2 ·[O2] y que la constante de velocidad, a 250 ºC, vale: k = 6,5 . 10 -3 mol-2L2s-1. Calcular la velocidad de oxidación del NO, a dicha temperatura, cuando las concentraciones iniciales (mol L-1) de los reactivos son: a) [NO] = 0,100 M ; [O2] = 0,210 M b) [NO] = 0,200 M; [O2] = 0,420 M. Determinar el orden de reacción: CH3-Cl(g) + H2O(g) ------- CH3-OH(g) + HCl(g) usando los datos de la tabla. Experiencia 1 2 3 [CH3-Cl] (mol/l) 0,25 0,50 0,25 [H2O] (mol/l) 0,25 0,25 0,5 v (mol·l–1·s–1) 2,83 5,67 11,35 FACTORES QUE AFECTAN LA VELOCIDAD DE LAS REACCIONES QUÍMICAS