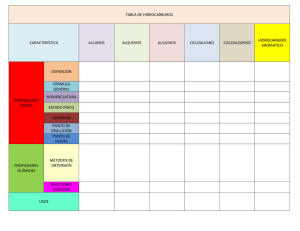
Los Alcanos son hidrocarburos, es decir que tienen sólo átomos de carbono e hidrógeno. También reciben el nombre de hidrocarburos saturados. Los Alquenos son hidrocarburos insaturados que tienen varios dobles enlaces carbono-carbono en su molécula. Los Alquinos son hidrocarburos alifáticos con al menos un triple enlace entre dos átomos de carbono Propiedades físicas----------------------------------------------Alcanos Los alcanos son compuestos que tienen hibridación sp3 en cada uno de sus carbonos. Estos presentan una densidad mucho menor que el agua. Se trata de hidrocarburos compuestos por átomos de hidrógeno y de carbono. Los alcanos de menor tamaño, metano, etano, propano y butano son gases a temperatura ambiente. Los alcanos lineales desde C5H12 hasta C17H36 son líquidos. Alcanos de y mayor número de carbonos son sólidos a temperatura ambiente. Los puntos de fusión y ebullición de los alcanos aumentan con el número de carbonos de la molécula. También se observa que los alcanos ramificados presentan un punto de ebullición menor que sus isómeros lineales. En fase líquida existen fuerzas de atracción entre moléculas que las mantiene unidas. Para pasar a fase gas la sustancia es necesario vencer estas fuerzas intermoleculares mediante el aporte de energía. Solubilidad Los alcanos solo se disuelven en disolventes no polares o que tienen baja polaridad debido a su baja polaridad, ejemplo de ello es el éter etílico, el tetracloruro de carbono y el cloroformo. No poseen polaridad Los alcalinos son compuestos no polares, debido a que solo están conformados por hidrógeno y por carbono. Estos no pueden disolverse en agua, pero si lo hace en grasas y en ciertas ceras. Densidad Estos compuestos llegan a ser los menos densos de todo el grupo de moléculas orgánicas. Presentan densidades menores que la densidad del agua, o sea, nunca supera 1g/cm3. Según va aumenta el alcano también lo hace la densidad. Alquenos Las propiedades físicas de los alquenos son comparables a las de los alcanos. Los alquenos más sencillos eteno, propano y buteno son gases, los alquenos de cinco átomos de carbono hasta quince son líquidos y los alquenos con más de quince átomos de carbono son sólidos Los puntos de fusión de los alquenos se incrementan al aumentar el tamaño de la cadena. La densidad de los alquenos es menor a la del agua y solamente son solubles en solventes no polares. Alquinos Los alquinos tienen unas propiedades físicas similares a los alcanos y alquenos. Son poco solubles en agua, tienen una baja densidad y presentan bajos puntos de ebullición. Sin embargo, los alquinos son más polares debido a la mayor atracción que ejerce un carbono sp sobre los electrones, comparado con un carbono sp3 o sp2. Los puntos de fusión y ebullición de los alquinos son ligeramente superiores a los de los alcanos y alquenos correspondientes. Reacciones--------------------------------------------------------Alcanos Si bien es cierto que los alcanos, a condiciones moderadas no reaccionan con la mayoría de reactivos, bajo condiciones especiales presentan las siguientes reacciones: Combustión Los alcanos son buenos combustibles al contacto con la llama, se incendian en oxígeno del aire y desprenden anhídrido carbónico y H2O, además de abundante calor. Halogenación Los alcanos reaccionan con los halógenos, principalmente cloro y bromo; la reacción es fotoquímica, es decir necesita presencia de luz, pudiendo realizarse también en la oscuridad a altas temperaturas (de 250°C o mayor). La halogenación es una reacción de sustitución, logrando sustituirse en la molécula del alcano, átomos de hidrógeno por átomos de halógeno. Nitración Los alcanos logran nitrarse, al reaccionar con ácido nítrico concentrado, sustituyendo hidrogeno por el grupo Nitro (-NO2). Esta reacción a presión atmosférica, en fase vapor o temperaturas entre 420 a 475°C y en presencia de ácido sulfúrico. Ciclación Los alcanos a temperaturas entre 500 y 700°C, logran deshidrogenarse en presencia de catalizadores especiales que son Cr2O3 ó Al2O3 ; los alcanos de seis a diez átomos de carbono dan hidrocarburos aromáticos monocíclicos. Alquenos Reacciones de adición electrófila La reacción característica de los alquenos es la adición de sustancias al doble enlace, según la ecuación. Hidrogenación de Alquenos La hidrogenación es la adición de hidrógeno al doble enlace para formar alcanos. Platino y paladio son los catalizadores más comúnmente usados en la hidrogenación de alquenos. El paladio se emplea en forma de polvo absorbido en carbón (Pd/C). El platino se emplea como PtO2 (Catalizador de Adams). Adición de HX Los haluros de hidrógeno se adicionan a alquenos, formando haloalcanos. El protón actúa como electrófilo, siendo atacado por el alqueno en la primera etapa. En esta reacción se pueden utilizar como reactivos HF, HCl, HBr, HI. Regla de Markovnikov - Regioselectividad Cuando un alqueno no tiene los mismos sustituyentes en sus carbonos sp2 puede formar dos tipos de productos en reacciones de sustitución electrófila. El producto mayoritario es el que se obtiene por adición del protón al carbono sp2, que genera el carbocatión de mayor estabilidad. Por ejemplo, cuando el propeno reacciona con HBr, el protón puede unirse al carbono 1 formándose el carbocatión en el carbono 2. Este carbocatión es secundario y la hiperconjugación le da una importante estabilidad. Si el protón se une al carbono 2, se obtiene un carbocatión primario sobre el carbono 1. La estabilidad del carbocatión primario es muy inferior a la del secundario y se formará más lentamente, dando lugar a un pequeño porcentaje del 1-bromopropano. Hidratación de Alquenos El agua es un ácido muy débil, con una concentración de protones insuficiente para iniciar la reacción de adición electrófila. Es necesario añadir al medio un ácido (H2SO4) para que la reacción tenga lugar. Esta reacción también es conocida como hidratación de alquenos y genera alcoholes. Adición de halógenos El cloro y el bromo se adicionan a alquenos para dar 1,2-dihaloalcanos. Por ejemplo, el 1,2dicloroetano es sintetizado por la adición de cloro a eteno. Formación de Halohidrinas Los alquenos reaccionan con halógenos en medio acuoso para formar halohidrinas, compuestos que contienen un halógeno y un grupo hidroxilo en posiciones vecinas. Oximercuriación - Desmercuriación Los alquenos pueden hidratarse con acetato de mercurio acuoso seguido de reducción con borohidruro de sodio. Esta reacción produce alcoholes y sigue la regla de Markovnikov. Hidroboración de Alquenos La hidroboración es una reacción en la cual un hidruro de boro [2] reacciona con un alqueno [1] para dar un organoborano [3]. Dihidroxilación de alquenos La dihidroxilación de un alqueno consiste en añadir un grupo -OH a cada carbono para formar dioles vecinales. Esta reacción se puede realizar con tetraóxido de osmio en agua oxigenada, o bien con permanganato de potasio en agua. Epoxidación de Alquenos Los alquenos reaccionan con perácidos (peroxiácidos) para formar epóxidos. Los epóxidos son ciclos de tres miembros que contienen oxígeno. Ozonólisis de Alquenos Los alquenos reaccionan con ozono para formar aldehídos, cetonas o mezclas de ambos después de una etapa de reducción. Adición de HBr con peróxidos En 1929, el profesor S. Kharasch de la Universidad de Chicago observó la adición antiMarkovnikov de HBr a un alqueno debida a la presencia de peróxidos en el medio de reacción. Polimerización de Alquenos Los alquenos, en presencia de ácido sulfúrico concentrado, condensan formado cadenas llamadas polímeros. Alquinos Adición de hidrógeno Con el empleo de catalizadores como platino, paladio o niquel, los alquinos se adicionan a hidrógenos produciendo un alqueno. Adición de halógenos El cloro o el bromo se adicionan a un triple enlace, pudiendo obtenerse un dihaloalqueno o un tetrahaloalcano. Adición de halogenuros de hidrógeno El HCl, HBr o HI se pueden adicionar a un triple enlace, produciendo un haloalqueno o un dihaloalcano. Adición de agua La adición directa de agua al acetileno, en presencia de sulfato mercúrico y H2SO4 acuoso, es un método industrial para la obtención de etanal. Polimerización El acetileno se puede polimerizar dando benceno, esto se logra a 70°C y 15 atm., en presencia de catalizadores especiales. Métodos de obtención-------------------------------------------Alcanos El principal método para la obtención de alcanos es la hidrogenación de alquenos. Los alcanos pueden obtenerse de fuentes naturales o de fuentes sintéticas. Como fuentes naturales de hidrocarburos se tiene el petróleo, el gas natural y el gas de hulla. El gas natural está constituido principalmente por metano y etano. El petróleo es una mezcla muy compleja de hidrocarburos sólidos, líquidos y gaseosos. Aunque los alcanos pocas veces se sintetizan, pueden obtenerse en el laboratorio por métodos químicos. Alquenos En general, los alquenos pueden obtenerse a partir de reacciones de eliminación sin embargo, todos los alquenos de importancia industrial se producen por el cracking o craqueo del petróleo. Deshidratación de alcoholes: Los alcoholes en presencia de ácido sulfúrico a 160° producen alquenos y como subproducto agua. Deshidrohalogenación de halogenoros de alquilo: Los halogenoros reaccionan con bases fuertes (KOH) (NaoH) en presencia de alcohol para producir alquenos y como subproducto halo ácidos y agua. Polienos o alcalienos: Los alquenos se clasifican en conjugados y no conjugados, lo que depende de la posición de los dobles enlaces en el compuesto. * Alquenos conjugados: se caracterizan por que presentan varios dobles enlaces alternos con sencillos. * Alquenos no conjugados: Se caracterizan por que presentan varios dobles enlaces no secuenciales ni alternos, lo que hace que el doble enlace actúe de forma independiente. Alquinos Existen varios métodos químicos para obtener los alquinos, entre ellos: Deshidrohalogenación de halogenuros de alquilo vecinales -Los halogenuros de alquilo son compuestos que contienen una cadena de carbonos en la que se han sustituido uno o más átomos de hidrógeno por un átomo de halógeno (F, Cl, Br, I) -Por su parte, los vecinales, se caracterizan por tener átomos de halógeno en carbonos contiguos -En la deshidrohalogenación se hace reaccionar el halogenuro de alquilo con una base -Como resultado se obtiene un producto de la reacción, el alquino Hidrolisis del carburo de calcio -En este método se agrega agua al carburo de calcio -Como producto de la reacción se obtiene el acetileno (etino): Pirólisis (crakeo) de naftas -También se le llama craking (rompimiento) -En este método se calienta a altas temperaturas la mezcla de hidrocarburos con el objeto de romper las cadenas grandes y obtener hidrocarburos de baja masa molar -Entre Ios productos de la pirolisis se obtienen algunos compuestos volátiles, entre ellos: -Acetileno (etino) -Propino -Butino