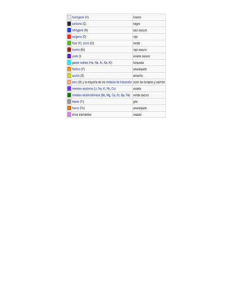
1. Indica que enlace formaran los siguientes compuestos: a) BaCl2 b) Mg c) NF3 d) CS 2. Completa la tabla: Sustancia Enlace Estado de agregación(20C) Conductividad eléctrica Solubilidad en agua Cu HCl Li2O NaBr H2 CaH2 H2O 3. Explique porqué la temperatura de ebullición del CH3F es -78,4 C mientras que la del CH2F2 es de -51,6C. 4. Indique quien propuso los siguientes enunciados: a) Los electrones giran alrededor a grandes distancias: b) Los compuestos están formados por átomos diferentes: c) Los átomos están formados por una parte positiva incrustada en el electrón: d) Los electrones giran a determinadas distancias sin emitir energía: 5. Complete: 6. Escriba la estructura de Lewis del selenio (Se, Z=34) 7. Señala los electrones de valencia de los átomos A y B, indica el tipo de enlace que previsiblemente se formará entre ellos y escribe la fórmula del compuesto. A: 1s2 2s2 2p6 3s2 3p6 4s2 B: 1s2 2s2 2p5 8. Explica qué tipo de enlace formarán las siguientes parejas de elementos: a) bromo y sodio, b) flúor y azufre, c) oxígeno y rubidio, d) oxígeno y nitrógeno. 9. Cita algún ejemplo de estos tipos de sustancia: a) Conductora de la electricidad en estado sólido. b) Conductora de la electricidad en disolución acuosa. c) Con punto de fusión muy bajo. ¿Qué tipo de enlace forma cada una de ellas? 10. ¿Qué clase de sustancias tienen muy bajo punto de fusión y no son solubles enagua, pero sí en benceno?. ¿serán conductoras de la electricidad? 11. Ordena razonadamente los siguientes compuestos de menor a mayor punto de fusión: I2, Ne, Na, NaCl 12. Razona si las siguientes afirmaciones son verdaderas o falsas: a) Los enlaces covalentes moleculares son buenos conductores de la electricidad b) Los enlaces metálicos pueden ser gas, líquido o sólido c) Los enlaces iónicos conducen la electricidad en sólidos d) Las redes cristalinas tienen temperaturas de fusión y ebullición bajas e) Los enlaces metálicos son líquidos y malos conductores de la electricidad