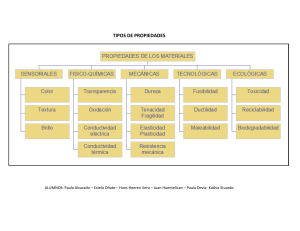
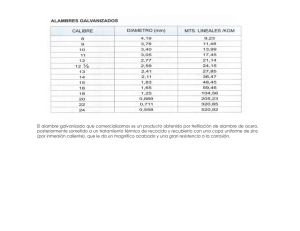
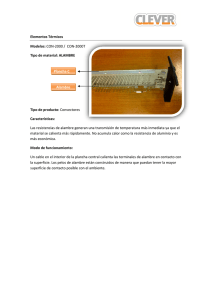
Científicos en acción Comprueba los espectros de energía Aproxímate al problema Durante mucho tiempo, el color que producían diferentes materiales cuando eran expuestos al fuego se explicaba como manifestaciones metafísicas de espíritus. ¿Por qué las llamas de la imagen presentan diferentes colores? Zinc Estroncio Potasio Cobre Sodio Elabora una hipótesis Plantea una hipótesis para el problema propuesto. Sigue el procedimiento Mediante esta prueba experimental observarás los diferentes colores que se producen al colocar distintos materiales a la llama. Materiales • Mechero o estufa de gas •P inzas y agua •S eis tubos de ensayo Reactivos •5 – 10 cm de alambre de cobre Paso 1 Toma una sección de alambre de cobre sin aislante, de no menos de 5 cm y no más de 10 cm. Paso 2 Con ayuda de las pinzas, acerca el alambre de cobre a la llama del mechero o de la estufa; en caso de generar algún color, espera a que este se disipe y deja enfriar (el color puede ser causado por las sustancias que recubren al cable). Paso 3 Etiqueta 6 tubos de ensayo. Coloca una cucharada (5 mL) de Isodine en el primer tubo, y ¼ de agua en los restantes (5 a 6 mL); agrégales una cucharadita de cada sal (5 g) (excepto al que contiene Isodine) y agítalos bien. Paso 4 Con las pinzas, toma el alambre de cobre y sumérgelo en el primer tubo; acércalo a la llama y observa si cambia sutil o fuertemente de color. Repite el ejercicio con cada tubo teniendo cuidado de lavar y dejar enfriar el alambre entre cada prueba. Escribe tus observaciones. Paso 5 Con las pinzas, toma un trozo de la cinta de magnesio y colócala directamente a la llama; registra tus observaciones. Paso 6 Toma el alambre y, a manera de cucharilla, coloca un poco de azufre directamente a la llama; anota tus observaciones. • 5 g de Isodine en solución, cloruro de sodio, cloruro de potasio, bicarbonato de sodio, sulfato de cobre II, permanganato de potasio, cinta de magnesio, azufre Registra tus datos 1 Anota las observaciones respecto a cada una de las sustancias con las que traba- jaste en el laboratorio. Muestra Observaciones de cambio de color en la llama Yodo (Isodine) Cloro (cloruro de sodio) Potasio (cloruro de potasio) Cobre (sulfato de cobre II) Cinta de magnesio Azufre Relaciona y concluye 2 ¿Con cuál de las sustancias el color fue más llamativo? 3 ¿Por qué se dan diferentes coloraciones en la llama del mechero? 4 ¿Comprobaste tu hipótesis? ¿Por qué? Usa el conocimiento 5 Lee el siguiente texto y de acuerdo con la práctica de laboratorio responde. La espectroscopia es el método químico analítico que permite identificar los elementos que componen una sustancia. En los laboratorios más avanzados del mundo se tienen dispositivos que permiten la identificación de cualquier sustancia con el solo hecho de colocar una muestra dentro del espectrofotómetro. Durante este análisis, las muestras son evaporadas y supercalentadas y luego un lector identifica el color característico de los elementos y lo registra; después lo compara con una base de datos que posee la computadora del espectrofotómetro. El registro aparece como una lectura de picos y longitudes. a. ¿Cuáles son las ventajas de esta técnica en el análisis de muestras? b. ¿Qué usos puede darse a la espectroscopia en investigaciones médicas y forenses?