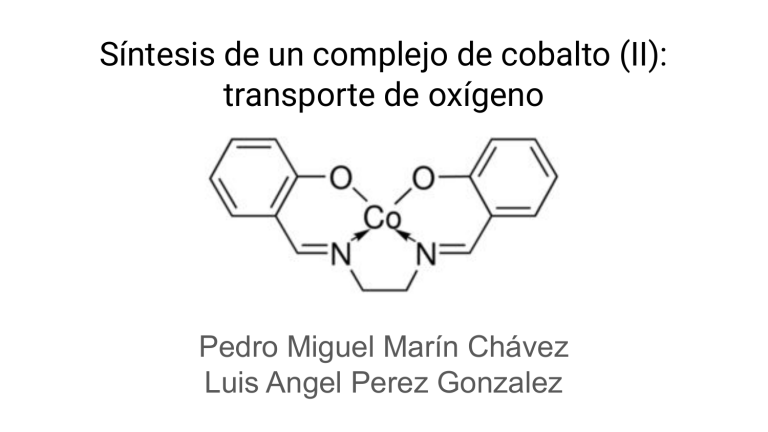
Síntesis de un complejo de cobalto (II): transporte de oxígeno Pedro Miguel Marín Chávez Luis Angel Perez Gonzalez Introducción Forma activa del [Co(salen)] Forma inactiva del [Co(salen)] Complejos con oxígeno molecular Orbital molecular del oxígeno molecular Reacción ● Los dos centros de cobalto pierden un electrón cada uno. ● Los oxígenos ganan dos electrones, formando un peróxido. Parte experimental N2 en condensador . 1.- Cargar matraz de 3 bocas de 250 mL, con un agitador magnético y 95% de etanol. 6.- En un matraz de fondo redondo con agitador magnético añadir 8,7 mmol de Co(OAc)2. 4H2O (2,17 g). 2.- Añadir 18 mmol de salicilaldehido. (0,192 mL). 5.- Añadir 8,7 mmol de etilendiamina ( 0,58 mL). 3.- Ajustar un condensador cuello central, otro cuello con un matraz de adicción y otro con un tapón de goma o septum. 4.- Remover la reacción en un baño de agua (~80° C) con atmósfera inerte. 7.- Añada 15 mL de agua destilada y disuelva. 12.- Filtrar al vacío y lavar los sólidos con etanol frío. 8.- Una vez disuelto, agregar al embudo de adición y desgasificar con N2 por 10 min 9.- Agregar la solución de cobalto lentamente y agitando vigorosamente. 11.- Una vez concluido el tiempo, desmontar y meter en un baño de hielo para ayudar a precipitar. 10.- Concluida la adición, dejar a reflujo durante 60 min. MEDICIÓN DE O2 Conecte la aguja mediante un tubo tygon, 13.- Secar los sólidos. 15 min. 14.- Pesar los sólidos y calcular el rendimiento porcentual. 16.- Añadir 5 ml de DMSO y burbujear con O2 durante 10 min .- Decantar una vez que salió de la centrífuga con ayuda de una pipeta pasteur. .- Lentamente gotear 1 mL de cloroformo. .- Observe el cambio físico que ocurre. Video parte experimental Análisis de resultados Análisis de resultados Aplicaciones - - Estudio de las metaloproteínas. - Catalisis para resolución cinética de epoxidacion. Usado como catalizador para separar una mezcla racémica.