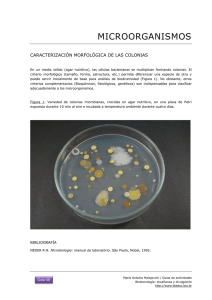
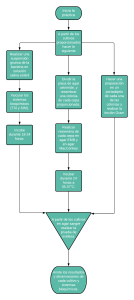
LABORATORIO 05 TÉCNICAS PARA EL AISLAMIENTO Y EL CULTIVO DE MICROORGANISMOS Contenidos Objetivo y definición Materiales Procedimiento Conclusiones Indicador de logro Al finalizar la sesión serás capaz de: • Adquirir conocimientos sobre la separación de microorganismos como colonias individuales a partir de mezclas microbianas mediante técnicas de aislamiento. • Propagar cepas microbianas mediante técnicas de trasplante y conocer las características coloniales de los microorganismos. ¿Dónde se cultiva a los microorganismos? ¿cómo ? Medio de cultivo • Son soluciones nutritivas (líquida o gelatinosa) que se utilizan en el laboratorio para el cultivo y crecimiento de los microorganismos https://www.youtube.com/watch?v=YGoPu0cn9ms https://www.youtube.com/watch?v=miga09gVMyY AISLAMIENTO Es la separación de un microorganismo del resto que lo acompañan. Se aislan para obtener un cultivo puro. TÉCNICAS PARA EL AISLAMIENTO ESTRÍAS DILUCIONES Por su función SELECTIVOS Promueve el crecimiento de ciertos microorganismos o inhibe el crecimiento de otros COMUNES Permite el crecimiento de la mayor parte de los Microorganismos. ENRIQUECIDOS Se le agrega exceso de nutrientes, sangre, suero Agar nutritivo Ejm: Agar Manitol salado Agar Sabouraud Ejm: Agar nutritivo Ejm: Agar sangre “La siembra es superficial” TECNICAS DE SIEMBRA Aislamiento por estrías Flamear 1 2 1 2 Flamear 1 2 Flamear Flamear 3 3 4 https://www.youtube.com/watch?v=6NckVGCobwY 3 II. MATERIALES • Guardapolvo blanco y limpio Láminas porta y cubre objetos Gradilla Asa Drigralsky y aguja de Kolle Mecheros Bunsen Placas petri CEPAS BACTERIANAS Escherichia coli Salmonella Bacillus Staphylococcus MEDIOS DE CULTIVO EN PLACA PETRI Placas Petri con: • Agar MacConkey • Agar Manitol Salado • Agar Nutritivo Agar EMB Agar nutritivo Agar manitol salado •3 tubos con 12 ml de agar nutritivo licuado y mantenido a 50°C. •3 placas Petri estériles. •2 tubos con cuñas de agar nutritivo. •2 tubos con caldo nutritivo III. PROCEDIMIENTO • Limpiar las superficies con un paño con alcohol (70 o 96°) • Encender el mechero • Ponerse los guantes, • Mascarilla III. PROCEDIMIENTO Técnicas de aislamiento 1. Por estrías a. EN CONDICIONES DE ESTERILIDAD/ROTULAR LAS PLACAS b. TOMAR UNA ASADA DE LAS CEPAS c. REALIZAR UN ESTRIADO EN LA SUPERFICIE https://www.youtube.com/watch?v=W6xpPJZIb1E https://www.youtube.com/watch?v=-TnHCd4sY24 Rotular placas: Medio, bacteria, nombre y fecha E. coli Agar MacConkey Agar nutritivo Agar manitol salado A.N Medio de cultivo Bacteria • Fecha Hora Nombre del grupo (siglas) Aislamiento por estrías Flamear 1 2 1 2 Flamear 1 2 Flamear Flamear 3 3 4 3 “Tenga cuidado de no producir roturas en el agar” Incube las placas a 37°C por 24-48 h. 2.Por diluciones 1= DILUCIÓN1 1. ROTULAR 3 PLACAS Y 3 TUBOS ( Cepa a emplear) 2=DILUCIÓN 2 3=DlLUCIÓN 3 1 2 3 1 2 3 Tiene 9mL de caldo nutritivo TÉCNICA DE AISLAMIENTO POR DILUCIONES (Por vertido en placa) 1ml 1ml 1ml 1 2 Tubo 1 con 9mL de caldo 1ml Dilución 1 3 Tubo 2 con 9mL de caldo Tubo 3 con 9mL de caldo 1ml Dilución 2 1ml Dilución 3 1ml Inocular la placa Añadir el agar nutritivo Girar la placa Colonias creciendo en el agar “ A 40°C se solidifica el agar” 3 cepas por grupo Técnicas de transplante “SIEMBRA SOBRE LA SUPERFICIE INCLINADA” Técnicas de transplante ( Caldo a Caldo) ROTULE LOS TUBOS Incubar a 37°C 24-48 horas. CALDO NUTRITIVO (CON INÓCULO) CALDO NUTRITIVO (SIN INÓCULO) EVALUACIÓN DE LOS TUBOS SEMBRADOS EN CALDO (CALDO A CALDO) • Después de la incubación, evalúe los tubos con caldo nutritivo considerando: Cantidad(escasa, moderada, abundante) Apariencia (turbidez, floculación, sedimentación, película completa, anillo superficial, mucosidad). Incubar las placas y tubos a 37°C por 24 a 48 horas …LUEGO DE LA INCUBACIÓN OBSERVAR LAS CARACTERISTICAS DE LAS COLONIAS Observe el desarrollo de las colonias aisladas y describa sus características de forma, bordes, elevación y consistencia (butiroso, viscoso, fibroso) según la figura siguiente: • • • • Forma, Bordes, Elevación Consistencia Colonias REGISTRAR CAMBIOS DE COLOR DE LOS MEDIOS DE CULTIVO Anote los resultados y preste particular atención a los cambios que se producen en los medios selectivo/diferenciales. Explique los resultados en el informe. OBSERVACIONES DE LAS PLACAS MEDIO DE CULTIVO MICROORGANISMO COLOR DEL MEDIO DE CULTIVO CAMBIOS Agar EMB E. coli ROJO COLONIAS NEGRAS CON BRILLO METALICO Agar Manitol Salado Staphylococcus ROSADO AMARILLO (Por rojo de fenol) https://www.youtube.com/watch?v=6hfS1XbPfQk Colonias de Staphylococcus aureus en el medio de cultivo Agar Manitol Salado Colonias de E. coli en el medio EMB IMPORTANTE EVALUACIÓN DE LOS RESULTADOS A LAS 24H • Observar si hay presencia de colonias en el medio de cultivo, forma, elevación y margen • Tomar fotografías a cada microorganismo como se desarrolla en los diferentes medios de cultivo • Apreciar los cambios de coloración • Nota: Investigar la composición química de los medio de cultivo y contrastar con los resultados obtenidos CONCLUSIONES • Las microorganismos se aislan en medios de cultivo con el propósito de obtenerlos puros. • El medio MacConkey es específico para E.coli, sus colonias serán rosadas, el medio Manitol Salado es específico para Staphylococcus. • Las técnica de aislamiento por estrías y la técnica de dilución en placa permite la obtención de colonias aisladas Fuentes de información • Madigan M., John M. Martinko & Jack Parker. Brock: Biología de los microorganismos, 14va. edición, Pearson Educación, S.A., Madrid. 2015. • Agar Manitol Salado. Disponible en: http://www.ucv.ve/fileadmin/user_upload/facultad_farmacia/c atedraMicro/10_AgarManitolSal.pdf • Juan Juscamaita (2006).Guía de Microbiología. UNALM