diapositivas de la presentación
Anuncio

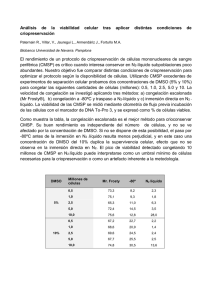
Recuperación de litio por método electroquímico Electrodo Batería Estudios de Cátodos Litio-Oxígeno 14 Terawatts consumo mundial de energía 34% Petróleo y 40% emisiones CO2 Gasolina 13.000 Wh/kg (1700 Wh/kg) a) Automóviles Híbridos (HEV) b) Vehículo Hibrido Eléctrico Enchufable c) Totalmente Eléctricos (EV) Capacidad 125 kWh para 250 Wh/millas 500 millas/800 kilómetros 2Li+O2 = Li2O2 11.680 Wh/kg CANTIDADES A CONSIDERAR • ENERGIA Carga x voltaje (Wh) • CAPACIDAD Carga (Ah = 3600 coul) • POTENCIA (kW) • DENSIDAD ESPECIFICA DE ENERGIA (masa) • (kW.h/kg) • DENSIDAD DE ENERGIA (volumetrica) • (kW.h/l) • TIEMPO DE VIDA DE LA BATERIA (ciclos de carga/descarga) El almacenamiento de energía es crítico para la utilización de energías renovables, para alimentar dispositivos electrónicos y para vehículos eléctricos (EV y HEV) Baterías de Li-ion para: Celular 1 Ah 1 A.h 3,6 V Laptop 4-5 A.h 11 V Vehículo Eléctrico 100 A.h Tecnologias disponibles hoy Energy & Environmental Science Cite this: Energy Environ. Sci., 2011, 4, 3243 Ejemplo: Salar de Cauchari (Jujuy) 8,1 millones de toneladas equivalentes a 50.000 millones de dólares 1 kg Li2CO3 6 $us, 1 kg Li 100 $us pero 1 batería con 5 kg Li para automóvil 25.000 $us!!! (83 toneladas de soja) Mercado 2020 de baterías EV (20% autos) 60.000.000.000 $us!!! Extracción de Litio 1. Metodo Evaporítico 2. Intercambio iónico 3. Extracción por intercambio en óxidos • Minera del Altiplano (FMC). Salar del Hombre Muerto (Catamarca) Catamarca/Salta. Factura 260 millones de dolares con 25 millones de inversión. Por cada ton Li2CO3 (6000 dólares) extraídos a 4000 metros de altura, se evaporan 10 millones de litros de H2O de la salmuera pudiendo afectar el acuifero, y deben llevarse 1,5 ton de soda solway, dejando un residuo de 900 kg de NaCl (en el salar). Método y dispositivo electroquímico para recuperación de litio de soluciones acuosas con bajo impacto ambiental Cambio de estrategia BASF Recuperación de litio por inserción en MnO2 → LiMn III Mniv O4 Li + + Mn2IV O4 + e ← → Li + + Mn2IV O4 ( MnO2 ) + e LiMn III Mn IV O4 ← + E /V vs. Li/Li (3.1 1 vs. vs. Ag/AgC l 3 ,2 3,4 3,6 3,8 4 ,0 4 ,2 4,4 4,6 4 3 2 i /m A 1 0 -1 -2 -3 -4 0,0 0,2 0,4 0,6 0,8 E /V vs. Ag/A gC l 1 ,0 1 ,2 1 ,4 i /m A CAPTURA DE LITIO → LiMn III Mniv O4 Li + + Mn2IV O4 + e ← → Li + + Mn2IV O4 ( MnO2 ) + e LiMn III Mn IV O4 ← 40 35 30 25 20 15 10 5 0 0 50 1 00 1 50 200 t /s 250 300 350 400 CAPTURA DE CLORURO Cristales de LiMn2O4 sobre fibras de fieltros de carbono Prueba de Concepto 10 Transitorios de carga y descarga del electrodo. Carbon felt recubierto con LiMn2O4 en KNO3 50 mM vs Ag/AgCl 8 6 Corriente (mA) 4 step 2 2 0 step 2 step 1 step 1 -2 Step 1: 0 V (150s) Step 2: 1,3 V (150 s) -4 -6 -8 -10 -12 0 100 200 300 Tiempo (s) 400 500 600 Celda filtro prensa tipo FM01 + C elda de flujo para recuperacion de L i Primer ciclo de carga y descarga 1 ,4 1 ,2 vs A g/AgC l (K C l 3M ) P o tenc ial (V ) 1 ,0 C arg a 0,8 Liberación de Li en KNO 3 50mM 0,6 + 0,4 0,2 0,0 D es carg a -0,2 + Captura de Li a partir de salmuera -0,4 -0,6 0 2000 4000 6000 8000 Tiempo (s) 1 0000 1 2000 1 4000 C elda de flujo - Trabajo eléctrico 1 ,0 0,9 C arg a 0,8 Liberacion de Li 0,7 + E (V ) vs A g/A gC l, K C l 3M 0,6 0,5 0,4 0,3 0,2 W = − ∫ Edq = 178,1 J 0,1 0,0 -0,1 D es carg a -0,2 Captura de Li -0,3 -0,4 -300 -250 -200 + -1 50 -1 00 -50 0 C arg a (C ) 0,2 Wh/Kg SELECTIVIDAD Li/Na Algunos números • Para extraer 7 g de litio necesitamos: • 96500 coul/3600 s.h-1= 26,8 A.h (26 h a 1 A o 1 h a 26 A). • 126 g LiMn2O4 ó 174 g de MnO2 para retener 7 g de Li. • Aprox. 7 litros de salmuera contienen 7 g de Li • O sea 7 millones de litros de salmuera para extraer una tonelada de litio COSTO ENERGETICO • • • • 200 Kwh/tonelada de Li Paneles solares 2000 $us/ kW 50 kW →200 kWh/día→1 Ton Li/día Inversión 100.000 $us →800 m2 → 30 años vida útil→11.000 Ton • 10 $us/tonelada!! Pureza de sales de litio Valores de FMC Grado industrial Grado Técnico energía Grado Tecnico Vidrio y cerámic o Grado Batería Li2CO3, masa% min. 99,0 99,3 99,3 99,5 H2O, masa% max. 0,6 0,6 0,6 0,5 Na2O, masa% max. 0,2 0,01 0,01 Na 0,050 CaO, masa% max. 0,05 0,1 0,1 Ca 0,04 SO4, masa% max. 0,1 0,003 0,003 0,1 Fe2O3, masa% max. 0,003 0,05 0,05 F e 5 ppm A l 10 C u 5 N i 6 Z n 5 Cl, masa% max. 0,01 0,2 0,2 0,01 Insol. Acido, m% max. 0,02 0,02 0,02 0,02 Ventajas del Método Propuesto • Limpio,no consume agua, Ca(OH)2, Na2CO3 • • • • Tiene bajo costo energético (200 kWh/ton). Es rápido (horas vs. meses de evaporación) Es selectivo (interferencias de sodio, magnesio) Produce LiCl de alta pureza grado batería en una sola etapa. Funcionamiento de una batería de litio oxigeno en solvente no acuoso EL OBJETIVO PARA AUTOS ELECTRICOS A Critical Review of Li/Air Batteries J. Christensen, P. Albertus, R.S. Sanchez-Carrera, T. Lohmann, B. Kozinsky, R. Liedtke, J. Ahmed, A. Kojica Journal of The Electrochemical Society, 159 (2) R1-R30 (2012) Para trabajar con litio y soluciones no acuosas el control de humedad y ppm de agua es critico! O2 + TEA+ + e → [O2− TEA+ ] [O2− TEA+ ] + TEA+ + e → [O22− TEA2+ ] 80 70 60 IR / µ A 50 O2 + TEA+ + e → [O2− ]DMSO [TEA+ ]DMSO 40 30 20 [O2− TEA+ ] + TEA+ + e → [O22− TEA2+ ] 10 0 2,4 2,6 2,8 3,0 3,2 3,4 3,6 + ED / V Li/Li 0 ID / µ A -100 2 -200 4 -300 9 -400 2,2 2,4 2,6 2,8 3,0 + ED / V Li/Li 3,2 3,4 3,6 RRDE GC/Au RRDE/DMSO, LiPF6 Au/Au RRDE/ DMSO, LiPF6 6 30 4 20 -10 -4 -20 -6 2,0 2,5 3,0 3,5 4,0 4,5 -30 -8 2,0 400 2,5 3,0 3,5 4,0 4,5 600 300 400 200 200 ID / µ A 0 I D /µA 100 -100 0 -200 -200 -400 -300 2,0 2,5 3,0 3,5 4,0 E / V (vs . L i/L i 0.1 M ) + 4,5 -600 2,0 2,5 3,0 3,5 E / V (vs. Li/Li+) 4,0 4,5 R 0 -2 I 10 IR / µ A 0 /µA 2 Transitorios potenciostaticos en electrodo de Anillo, disco Au D 20 0 0 -200 10 2,3 V -400 -600 -5 IR / µA ID / µA -200 ID / µ A 2,5 V 0 0 -400 -600 -10 -800 -800 -20 -1000 -10 0 5 10 15 20 25 -1000 30 -30 E/V 0 5 10 15 20 25 30 t / sec 15 0 5 0 10 0 5 -200 -200 0 -10 -15 -800 -20 -1000 -25 0 5 10 15 t / sec 20 25 2,0 V -400 -5 -600 -10 -800 -15 -1000 30 -20 0 5 10 15 E/V 20 25 30 IR / µ A -600 ID / µ A -5 IR / µ A 2,2 V ID / µ A -400 Mecanismos de Reducción de Oxigeno O2 + Li + + e → [O2 Li ] [O2 Li ] + [O2 Li ] → Li2O2↓ + O2 [O2 Li ] + Li + + e → Li2O2↓ O2 + Li + + e → [O2 Li ]ads → [O2 Li ]ads + [O2 Li ]ads → Li2O2↓ + O2 [O2 Li ]DMSO bimolecular [O2 Li ]DMSO + [O2 Li ]DMSO → Li2O2↓ + O2 Descomposición DMSO O O -2e S H3 C H3 C CH3 CH3 +2 H+ O Au/DMSO 20 0.1 LiPF6 in DMSO, O2 saturated 0.1 LiPF6 in DMSO, deoxygenated 115 0.1 TBAPF6 in DMSO, O2 saturated Transmittance 10 0 I/A S + H2O 4.7 V 4.5 V 4.2 V 3.8 V 3.0 V 1.9 V 110 105 2.3 V 2.8 V -10 100 3.2 V 95 1500 -20 1400 1300 1200 1100 1000 900 -1 Wavenumber, cm 2,0 2,5 3,0 3,5 4,0 4,5 Pt/DMSO + E vs. Li /Li / V 125 4.7 V 4.6 V 4.5 V 4.4 V 4.3 V 120 O O H 3C O 4.3 V 3.5 V S S CH3 -e H3C CH3 +H 20 -e Transmittance 115 + 2H + S H 3C CH3 O 110 4.1 V 105 3.9 V 100 95 3.7 V 3.5 V 3.3 V 90 3.1 V 85 1500 1400 1300 1200 1100 -1 Wavenumber, cm 1000 900