Metabolismo del N-acetil-L-aspartato: valor
Anuncio

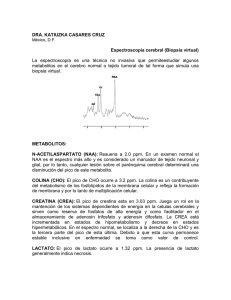
rEVISIÓN Metabolismo del N-acetil-L-aspartato: valor diagnóstico y pronóstico Manuel A. Martínez, Néstor V. Florenzano, Esteban A. Macchia Objetivos. Analizar la implicación clínica del aminoácido N-acetil-L-aspartato (NAA) y el péptido N-acetil-aspartil-glutamato (NAAG) en relación con su valoración diagnóstica y pronóstica mediante espectroscopia de resonancia magnética. Realizar una revisión del metabolismo del NAA y del NAAG, considerando su estructura química y fisiología, en relación con las variaciones de su concentración y en correlación con la clínica. Desarrollo. La revisión se divide en dos partes: en una se comprobó que el único sitio de síntesis del NAA es la mitocondria neuronal, y del NAAG, el citoplasma neuronal; la segunda parte aborda las técnicas de resonancia magnética y, particularmente, la espectroscopia. Se analizan diversas patologías en busca de criterios que posibiliten obtener pautas diagnósticas y pronósticas. Instituto de Morfología J.J. Naón. Facultad de Medicina. Universidad de Buenos Aires. Buenos Aires, Argentina. Correspondencia: Dr. Manuel Alberto Martínez. Instituto de Morfología J.J. Naón. Facultad de Medicina. Universidad de Buenos Aires. J.E. Uriburu, 950, 1.er piso. Buenos Aires, Argentina. Conclusiones. El estudio del aminoácido más abundante del sistema nervioso central (NAA) junto con un producto de su metabolismo, el NAAG, permite en patologías de diversos orígenes su diagnóstico y seguimiento y facilita la obtención de datos de densidad de la población celular y vitalidad de ésta, de manera que se accede, además, al estado funcional de las sinapsis. E-mail: ma12martinez@gmail. com Palabras clave. Espectroscopia de resonancia magnética. Integridad sinaptodendrítica. NAA. NAAG. Vitalidad celular. Cómo citar este artículo: Martínez MA, Florenzano NV, Macchia EA. Metabolismo del N-acetil-L-aspartato: valor diagnóstico y pronóstico. Rev Neurol 2016; 62: 361-70. Introducción Reseña histórica Las primeras observaciones y descripciones del Nacetil-L-aspartato (NAA) se inician en la década de los cincuenta, en ensayos experimentales con animales realizados por Harris Tallan y Bruce Jacobson. En 1954 Tallan lleva a cabo un trabajo con gatos en busca de aminoácidos y sustancias afines e indaga, en concreto, su concentración en varios órganos abdominales y en el cerebro. En el resumen relata un hallazgo que llama su atención: el cerebro es el único lugar donde se encuentra un nivel elevado de ácido aspártico. En 1956, al comprender su hallazgo, declara que se trata de un aminoácido libre debido a la unión del aspartato y la acetil coenzima A (acetil-CoA); al descomponer su estructura lo denomina ‘N-acetil-Laspartato’. Otro dato que revela es que su concentración es elevada y que, además, está presente en roedores, en los que también observa un incremento simultáneo con su maduración. En 1957, al estudiar su distribución, comprueba que en los seres humanos el cerebro es el único órgano en el que se puede hallar; lo descubre también en múltiples especies: reptiles, anfibios, cangrejos, www.neurologia.com Rev Neurol 2016; 62 (8): 361-370 langostas y aves, o sea, vertebrados e invertebrados. Su descubrimiento trasciende lo médico al observar que no es exclusivo de la especie humana; entonces adquiere relevancia biológica y antropológica [1-3]. Jacobson, en 1959, al estudiar el rol del NAA en los mamíferos, confirma que su concentración es elevada y que es común a varias especies. Constata su incremento gradual en ratas durante su maduración. En el cerebro de los humanos realiza dos observaciones: coteja el nivel de NAA en muestras de cerebros de jóvenes y adultos normales y comprueba que las variaciones de concentración se relacionan con la edad, además de advertir que es menor en los adultos. También confronta el nivel de NAA de sujetos normales con enfermos mentales y verifica que es menor en estos últimos; en el mismo ensayo menciona a un autor que sugiere que para lograr la acetilación del ácido aspártico es necesaria la presencia de una enzima que identifica con el nombre de ‘L-aspartato N-acetiltransferasa’. Este relato resistió durante mucho tiempo y 10 años después se pudo confirmar que estaba en lo cierto [4,5]. En los años sesenta, estudios experimentales también realizados en animales permiten comenzar a interpretar e integrar la información obtenida en la década anterior; de todos ellos, los más trascenden- Aceptado tras revisión externa: 15.02.16. © 2016 Revista de Neurología 361 M.A. Martínez, et al Figura 1. Espectroscopia press de eco corto. Barras: azul: sector donde se ubican los compuestos N-acetilados; azul punteada, se ubica el α-glu­ tamato-glutamina-fosfocreatina; verde, sector de las macromoléculas láctico o artificio. Flechas punteadas: roja, glutamato; verde, glutamina; amarilla: sector donde se puede hallar aspartato. CO: componentes de colina; CRE: creatina; GLN: glutamina; GLU: glutamato; MI: mioinositol; TAU: taurina. tes son los siguientes: en 1965 Curatolo et al descubren un péptido derivado del NAA, al cual atribuyen funciones de neurotransmisor, y lo denominan ‘N-acetil-aspartil-glutamato’ (NAAG) [6]; en otro ensayo, Fred Goldstein (el autor mencionado en el trabajo de Jacobson) confirma la existencia de la enzima responsable de su síntesis [7]. Nuestro objetivo es realizar una revisión del metabolismo del NAA. Para lograr que el ensayo sea completo es imprescindible incorporar el análisis del único producto químico derivado de su metabolismo, el NAAG, estudiando en ambos su estructura química y su fisiología, y en el NAA, además, la relación de las variaciones de su concentración y su correlación con la clínica. Una particularidad de ambos metabolitos es que, además de ser los más cuantiosos del sistema nervioso central (SNC), comparten el sitio de su síntesis, pero difieren en el lugar de su catabolismo. Con respecto al NAA, aspiramos con toda esta información a revelar el mecanismo por el cual es esencial para la síntesis de lípidos/mielina, argumentar su relación con la producción de energía y esclarecer el mecanismo por el cual interviene en la correcta distribución de las moléculas del agua. Con el NAAG esperamos exponer con claridad su importancia en el funcionamiento de las sinapsis, la relación con los astrocitos fibrilares y su idoneidad para protegernos del efec- 362 to tóxico del glutamato, así como explicar por qué se los considera la unidad estructural y funcional indispensable para el correcto funcionamiento del cerebro de los vertebrados. Espectroscopia de resonancia magnética Mediante las técnicas de espectroscopia steam y press, en 2.0.1 ppm se ubican los dos metabolitos más copiosos del SNC. En el pico en este sector de la abscisa, el 90% corresponde al NAA y el 10% restante al NAAG; en este sitio sustancias con la misma estructura química comparten el mismo lugar. Todas estas sustancias tienen en común en su estructura química el denominado grupo etilo CH-3(N-acetilados). Entre 2.0.1 y 3.0.2 ppm se detectan sustancias producidas en el ciclo de Krebs. Nos referimos al β y γ-glutamato y derivados del glutamato como, por ejemplo, la glutamina y el ácido γ-aminobutírico. La presencia de estos metabolitos en este lugar confirma que el ciclo de Krebs se halla vigente y es eficaz. Es un sector donde también se pueden encontrar residuos de otros productos químicos debido al denominado desplazamiento químico, por ejemplo, del aspartato. La concentración del NAA puede estimarse en valores absolutos o relativos. Estos últimos se obtienen de la relación con la fosfocreatina, valor normal: 1,8-2,2 ppm (en la práctica clínica se considera descendido por debajo de 1,6 ppm) (Fig. 1). Metabolismo del N-acetil-L-aspartato Compartimento anabólico En la mitocondria de la neurona, la enzima L-aspartato-N-acetiltransferasa asocia aspartato con acetilCoA y produce NAA [8]. Tras su síntesis se desplaza al citoplasma, en donde otra enzima le agrega glutamato, con lo que se produce el NAAG [9]. Los aminoácidos mencionados para su síntesis se originan a partir del ciclo de Krebs, el aspartato se obtiene del ácido oxalacético y el glutamato se elabora gracias al α-cetoglutarato. En cuanto a la acetil-CoA, su mayor proveedor es la glucosa [10], la cual también se puede elaborar mediante la biosíntesis o degradación de ácidos grasos o de aminoácidos. Para el inicio del ciclo de Krebs y la síntesis de ambos metabolitos es esencial la presencia del ácido cítrico, el cual se obtiene cuando se condensa el ácido oxalacético con la acetil-CoA [11] (Fig. 2). www.neurologia.com Rev Neurol 2016; 62 (8): 361-370 Metabolismo del N-acetil-L-aspartato Figura 2. Síntesis del N-acetil-L-aspartato (NAA) y del N-acetil-aspartilglutamato (NAAG). La síntesis del NAA es mitocondrial y la del NAAG citoplasmática. Círculos: A, citrato; B, α-cetoglutarato; C, ácido-oxalacético. Enzimas: 1, L-aspartato-N-acetiltransferasa; 2, sintetasa del glutamato; 3, citrato-sintetasa; 4, piruvato-deshidrogenasa. Figura 3. Regreso del aspartato y del acetato a la neurona. El aspartato (amarillo 5) muestra su conversión en ácido oxalacético y el aporte para la síntesis del N-acetil-L-aspartato. El acetato (rojo 6) muestra su conversión en acetil coenzima A. Compartimento catabólico y fisiología del N-acetil-L-aspartato esa causa lo proponen como un marcador de normalidad del metabolismo mitocondrial [16]. Ello permite corroborar que la síntesis del NAA debe poseer como requisito primordial la normalidad de la fosforilación oxidativa mitocondrial. Por este motivo sólo se detecta en células con niveles adecuados de ATP y acetil-CoA, y se considera un marcador indirecto del estado energético cerebral [17]. La concentración de NAA es variable. Fuera de la membrana plasmática neuronal, su proporción en las neuronas es elevada y más estable: es 100-200 veces superior a la del espacio extracelular y cons­ tituye el 3-4% de la osmolaridad cerebral y el 7% de la neuronal. El gradiente descrito es una condición esencial que le permite desarrollar su circuito metabólico [18]. La ubicación y cantidad de agua en el cerebro depende de diversos factores como, por ejemplo, la concentración de sodio circulante [19] o la ingesta y pérdida controlada por el hipotálamo. Otro de gran importancia es el funcionamiento de la bomba de sodio-potasio ATPasa [20]. También es fundamental la presencia intracelular de sustancias de bajo peso molecular, denominadas osmoles idiogénicos [21]. El más abundante de todos ellos es el NAA. Con respecto a la cantidad de agua extracelular, hay que tener en cuenta en este compartimento, además de todo lo comentado, la presencia de sustancias químicas, algunas de ellas hidrofílicas; por ejemplo, el ácido hialurónico y las glucoproteínas, que al atraer agua aumentan el tamaño y tur- El NAA se desdobla en el oligodendrocito debido a la actividad de la enzima aspartoasilasa, de manera que se produce acetato y aspartato, y su entrada en la célula se debe a la presencia de receptores específicos para células gliales [12]. Otra enzima, la acetilCoA sintetasa con el acetato produce acetil-CoA, con la cual se elaboran lípidos y esteroides necesarios para la síntesis de la mielina en la etapa neonatal: galactocerebrósidos, sulfátidos y colesterol. El aspartato se difunde al espacio extracelular y, al regresar a las neuronas, se consume para sintetizar NAA y ácido oxalacético; la porción de acetato que no se emplea para elaborar mielina también regresa a las neuronas y se utiliza para producir acetil-CoA. El regreso del aspartato y el acetato es trascendente para colaborar con la elaboración del NAA y, en particular, para poder obtener ácido cítrico, que permite al ciclo de Krebs reanudar o proseguir su actividad. Por esta causa se considera que la síntesis de NAA es una manifestación de normalidad del metabolismo energético cerebral [13,14] (Fig. 3). Este concepto se halla confirmado por un trabajo que expone que la emanación de NAA disminuye si se utilizan productos químicos que alteran el funcionamiento de la cadena respiratoria [15]. Además, otro ensayo define que la elaboración del NAA tiene relación directa con el consumo de oxígeno y la producción de trifosfato de adenosina (ATP); por www.neurologia.com Rev Neurol 2016; 62 (8): 361-370 363 M.A. Martínez, et al gencia del espacio extracelular (el denominado tercer espacio) e influyen incluso en la difusión de las moléculas de agua [22,23]. La superficie de las neuronas es impermeable al agua [24]. La diferencia de concentración descrita permite a las moléculas de agua y al aminoácido acceder desde las neuronas por difusión al intersticio y a los astrocitos fibrilares. Su entrada en estos últimos se ve favorecida por los receptores ya mencionados y comunes a toda célula glial, para llegar finalmente a la circulación general a la altura de la barrera hematoencefálica. La presencia de las proteínas acuaporina 4 en la superficie de los astrocitos y en sus prolongaciones, los denominados pies ‘chupadores’ (barrera hematoencefálica), facilita el movimiento de las moléculas de agua; por este motivo el NAA se considera un osmorregulador [25-27]. Por extraer moléculas de agua en exceso dentro de las neuronas en condiciones fisiológicas y patológicas preservando su integridad osmótica y estructural, un autor lo calificó como la bomba del agua [28]. El tema de la osmorregulación merece un debate profundo. Lo descrito expone con claridad la existencia de un gradiente de concentración del NAA entre las neuronas con el espacio extracelular y los astrocitos fibrilares. También revelamos la importancia de los receptores Na+ DC3 y, por supuesto, la utilidad de la presencia de las proteínas acuaporina 4. El NAA y el NAAG son aniones, y el agua no se encuentra en estado neutro todo el tiempo. Se trata de un equilibrio dinámico que mantiene el pH neutro. Constantemente hay una transformación de las moléculas de agua que las descompone en una porción aniónica y otra catiónica: H2O = H+ más OH–. La cuestión por definir es saber qué mecanismo le permite al NAA cubrirse con las moléculas de agua y poder desplazarse juntos, si sólo se debe a la interacción del anión que emite la mitocondria, el NAA y la porción con carga opuesta del agua en estado de descomposición. Algunos autores proponen la existencia entre ambos de la denominada interfaz coloidal, que permite el transporte del agua [29,30], empleada actualmente por la industria farmacéutica para facilitar la circulación y el acceso de los medicamentos al tejido u órgano afectado [31]. Compartimento catabólico y fisiología del N-acetil-aspartil-glutamato El NAAG se cataboliza en la hendidura sináptica mediante la enzima carboxipeptidasa del glutamato II [32], ubicada en la superficie de los astrocitos fi- 364 brilares, que lo desdobla en glutamato y NAA: el glutamato se desplaza a las neuronas y el NAA se difunde al intersticio y a la circulación general [33]. El NAAG es el péptido coneurotransmisor de mayor concentración en el SNC que modula el funcionamiento de varias sinapsis; por ejemplo, del ácido γ-aminobutírico y la acetilcolina, y las glutamatérgicas en la corteza, la amígdala, el hipocampo, el cuerpo estriado, el tronco del encéfalo y la médula espinal, motivo por el cual se relaciona dicho péptido con atención/concentración y memoria (cognición). En la hendidura sináptica de las glutamatérgicas desarrolla su actividad; en ella influye en receptores metabolotrópicos e ionotrópicos del glutamato. Los metabolotrópicos se ubican en la región presináptica y en la membrana de los astrocitos fibrilares. Se trata de los receptores tipo 3 del glutamato, que se denominan GLUR3; sólo actúa sobre uno de los inotrópicos, el denominado N-metil-D-aspartato. Cuando activa el metabolotrópico presináptico reduce la liberación de glutamato; al excitar el situado en los astrocitos fibrilares, libera un factor protector de las sinapsis llamado factor de crecimiento β. Postsinápticamente, desensibiliza y bloquea el Nmetil-D-aspartato [34] (Fig. 4). Por su efecto pre y postsináptico, reduce la concentración y actividad del glutamato; por este motivo se convierte, junto con los astrocitos fibrilares, en otro mecanismo para evitar sus efectos tóxicos. Debido a lo expuesto, el NAAG también se considera esencial para el progreso de la interacción neuronal denominada plasticidad sináptica. Su metabolismo permite que pueda ser sostenida y eficiente; para lograrlo es esencial conciliar la presencia de las células gliales [35,36]. Respecto al NAA que se origina del catabolismo del NAAG, la porción que se ubica en el espacio extracelular al entrar en el oligodendrocito producirá acetato y aspartato, que al regresar a las neuronas nuevamente elaboran ácido cítrico y permiten al ciclo de Krebs continuar produciendo energía. Durante el desarrollo del ciclo se elabora α-ceto­ glutarato, que produce gutamato. Éste es el motivo por el cual algunos autores consideran el NAA reservorio del glutamato [37]. El glutamato que se origina del catabolismo del NAAG al abordar las neuronas producirá α-ceto­ glutarato, que al incorporarse al ciclo de Krebs, además de sintetizar glutamato, continúa con el ciclo. Se trata de una forma alternativa de obtener ATP y NAA sin la necesidad de elaborar ácido cítrico denominada el miniciclo de Krebs [38]. Lo expresado hasta aquí es una manifestación de la importancia del NAAG en la interacción glioneu- www.neurologia.com Rev Neurol 2016; 62 (8): 361-370 Metabolismo del N-acetil-L-aspartato ral, pero la integridad sinaptodendrítica también depende de la presencia de una proteína: la sinaptofisina. Es una proteína sintetizada en la mitocondria neuronal que es responsable de la cinética de las sinapsis, además de recubrir las vesículas de secreción ubicadas en los terminales sinápticos [39]. Estudios realizados en simios infectados con el virus de la inmunodeficiencia humana (VIH) revelaron la reducción del NAA y de la sinaptofisina. En los medicados, además de su mejoría clínica, se observó el incremento simultáneo de ambos. Las oscilaciones descritas de esta proteína y del aminoácido expresan que el NAA es también un marcador de integridad sinaptodendrítica [40]. Las células que participan del metabolismo del NAA y NAAG son las neuronas, los astrocitos fibrilares y los oligodendrocitos, por lo que recibe el nombre de metabolismo tricelular [41]. Las células endoteliales, al contribuir con la actividad del NAAG, se pueden considerar la cuarta célula, pero no pertenecen al circuito metabólico descrito. Son únicamente las efectoras de su influencia en el astrocito fibrilar, que permite adaptar el flujo sanguíneo en relación con el requerimiento de la actividad neuronal. El 99% de la circulación arteriolocapilar se halla cubierta por proyecciones de los astrocitos fibrilares; esta unidad astrocitocapilar permite regular el flujo de acuerdo a los requerimientos fisiológicos [42,43]. Fluctuaciones fisiológicas de concentración del N-acetil-L-aspartato Durante el período de maduración de la corteza y sustancia blanca hay un incremento gradual en la concentración del NAA [44]. En niños y en adultos se describen variaciones de concentración relacionadas con la histología de la corteza examinada. Ésta puede tener seis o tres capas (iso o allocorteza), las cuales, además de por la población de astrocitos, también se diferencian por la cantidad/calidad de neuronas. En la espectroscopia de resonancia magnética que se realiza en áreas del cerebro con iso/neocorteza, el nivel de NAA será mayor al confrontarlo con el de aquellas que por su estructura son más primitivas (allocorteza). Esto se observa al comparar la corteza prefrontal con el giro parahipocámpico y el hipocampo [45]. Fluctuaciones patológicas de concentración del N-acetil-L-aspartato Las alteraciones de su concentración se pueden reflejar por su disminución, la cual puede ser perma- www.neurologia.com Rev Neurol 2016; 62 (8): 361-370 Figura 4. Hendidura sináptica. Sitio de actividad y catabolismo del N-acetil-aspartil-glutamato (NAAG). Rectángulo superior, arriba a la derecha: el nombre y símbolo de cada componente. A: terminal presináptico; B: terminal postsináptico; C: astrocito fibrilar. En A, círculos: verde, NAAG; violeta, glutamato; amarillo, membrana neuronal presináptica y del astrocito, que corresponden al receptor metabolotrópico del glutamato; rojo, membrana neuronal postsináptica, receptor ionotrópico del glutamato, el Nmetil-D-aspartato. Rectángulo marrón: membrana del astrocito, enzima que desdobla el NAAG. Las flechas indican el sitio donde actúa el NAAG: A (barra amarilla), se observa el bloqueo de la secreción del glutamato; C, el destino de los productos del desdoblamiento del NAAG: el glutamato a las neuronas y el N-acetil-L-aspartato a la circulación general e intersticio. nente y, en algunos casos, reversible. En otras ocasiones se observa su incremento, que también puede ser transitorio o permanente. Las variaciones de su concentración en ambas circunstancias, su disminución o incremento, suelen ser patológicas. Las causas de reducción de NAA se pueden dividir en primarias o secundarias. Las afecciones genómicas nuclear y mitocondrial son una causa de origen primario. Se trata de patologías que tienen en común inconvenientes en producir energía, y se denominan citopatías mitocondriales [46]. Las secundarias se producen con frecuencia por exceso de glutamato en el intersticio, lo que al activar receptores en las membranas de las neuronas provoca la entrada de gran cantidad de calcio. El efecto tóxico del calcio se debe a la síntesis de radicales libres de oxígeno, los responsables de afectar a las mitocondrias y al resto de las estructuras neuronales, incluso al ADN. Éstas son alteraciones bioquímicas que pueden provocar muerte celular y, en ocasiones, alteraciones en el correcto funcionamiento de las mitocondrias, que configuran una de las causas de neurotoxicidad, llamada en este caso en particular excitotoxicidad [47,48]. La excitotoxicidad reduce el NAA debido al descenso de población neuronal o a la disminución de la actividad mitocondrial [49]. 365 M.A. Martínez, et al Lipton y Rosenberg describen las patologías agudas y crónicas con niveles intersticiales elevados de glutamato que perjudican el funcionamiento del cerebro en la denominada por ellos vía final común [50]. En todas estas patologías agudas y crónicas durante su evolución se observan alteraciones en los niveles de NAA. En algunas patologías las fluctuaciones pueden ser transitorias y en otras permanentes. En todos los casos depende de su etiología y de su evolución natural, y en algunas circunstancias, de la respuesta a la terapia empleada. Una de ellas es el complejo demencia-VIH, en el cual la excitotoxicidad y la reducción de NAA es en un primer momento reversible y luego permanente. Se produce debido a la colonización del SNC por un retrovirus responsable de una anormalidad histoquímica que recibe el nombre de neuroinflamación y que provoca muerte celular o disfunción mitocondrial. En pacientes sin hallazgos por imágenes, algunos de ellos con síntomas e incluso en asintomáticos, accedemos a la neuroinfección utilizando espectroscopia y, según los niveles de NAA (en concreto por sus variaciones), se puede reconocer si el virus está presente y si responde a la terapia instaurada [51-54]. En la corteza de pacientes VIH positivos, la reducción de NAA también puede deberse a la asociación con alcoholismo [55]. Las patologías neuropsiquiátricas son otra causa, en pacientes sin hallazgos por imágenes, de daño estructural que, además de la clínica, suelen tener co­ mo única expresión las variaciones del nivel de NAA. La región explorada en pacientes psiquiátricos es la corteza frontal/prefrontal y la zona del cíngulo en su región anterior o posterior. Suelen ser pacientes con esquizofrenia y trastorno bipolar [56-60]. Lo importante en los pacientes con sida y psiquiátricos es que, previamente a la presencia en la resonancia de una lesión estructural, la reducción del NAA indica que una enfermedad está causando daño. En estos pacientes, además de la mejoría clínica, se observa simultáneamente a la normalización de los niveles de NAA. El problema en estos pacientes infectados y psiquiátricos es la comorbilidad entre ambas afecciones, con el agravante del consumo de otras drogas o alcohol. En la enfermedad de Alzheimer, la alteración en la producción de energía se describe como un factor relacionado con la etiología de los síntomas y como el origen primario de disminución o ausencia de conexiones lobares [61]. Se observa reducción del NAA en aquellos sectores con menor población de neuronas o viabilidad de las presentes [62]. Bartha analizó exhaustivamente exámenes de espectroscopia de resonancia magnética realizados por 366 diversos autores que demostraban que la reducción de NAA en algunas regiones puede llevar al diagnóstico e incluso predecir (en casos de deterioro cognitivo leve) la aparición de la enfermedad (en algunos trabajos llegaban a cerca del 80%) [63]. La bibliografía consultada expone con suma claridad que el traumatismo es una de las causas más frecuentes de vulnerabilidad metabólica o inestabilidad energética cerebral [64]. Incluso algunos autores utilizan el término ‘crisis energética cerebral’ y lo relacionan con el origen del daño axonal difuso [65]. En los leves, y especialmente en los graves, las variaciones en la concentración de NAA pueden ser unas veces permanentes y otras reversibles, con valor diagnóstico y pronóstico. En el traumatismo grave, si observamos reducción en los primeros 7-10 días y el paciente no mejora en controles a los 4-12 meses, es muy probable el diagnóstico de daño axonal difuso. Por el contrario, si los niveles de NAA mejoran, es de buen pronóstico. Lo mencionado es importante, en especial porque las microhemorragias descritas que sugieren, por su presencia y topografía, el diagnóstico de daño axonal difuso se observan en un 20-30%. Por este motivo, en un paciente con traumatismo de cráneo, el examen bioquímico (en particular, el seguimiento de las fluctuaciones del NAA) tiene un valor indiscutible para el diagnóstico e incluso su pronóstico. Por ejemplo, en la bibliografía consultada, la reducción de NAA en sitios alejados de un foco de contusión ya es de mal pronóstico incluso en los primeros 7-10 días. En cuanto al restablecimiento de los valores de NAA a niveles normales o cercanos a ellos, algunos autores proponen que se puede deber a la remielinización [66], mientras que otros se inclinan por neurogénesis en el hipocampo y en la neocorteza [67]. La reducción del NAA en la epilepsia es uno de los ejemplos de aumento del glutamato sin excitotoxicidad; suele ser reversible en el sitio de la descarga y, simultáneamente, se puede observar en sectores distantes del SNC. En pacientes con esclerosis temporal mesial, la reducción del NAA no depende de la merma de la población neuronal, sino que es un típico caso de disfunción mitocondrial, y en aquellos casos refractarios y quirúrgicos, si se observa su disminución en el lóbulo contralateral, es de mal pronóstico, con una recuperación de menor magnitud a la esperada. La ausencia de relación con la densidad neuronal y disminución del NAA provocada por disfunción mitocondrial suele suceder en otras patologías (por ejemplo, en displasias corticales y polimicrogiria). En conclusión, toda lesión epileptógena cortical es independiente del número de www.neurologia.com Rev Neurol 2016; 62 (8): 361-370 Metabolismo del N-acetil-L-aspartato neuronas afectadas, ya que depende de la calidad de las neuronas que habitan dicho sector [68]. La esclerosis múltiple es un ejemplo de reducción reversible y permanente; en las placas agudas es transitoria, y en los sectores de sustancia blanca de aspecto normal, debido al daño axonal, puede ser permanente [69,70]. En pacientes tratados con interferón β-1b se puede observar un aumento de los niveles de NAA que puede expresar remielinización o mejoría energética neuronal; esto último debido a la presencia de placas corticales [71]. Otra causa de variación de concentración reversible se da al actuar el NAA como osmol idiogénico, ya que se trata de múltiples patologías de origen diferente todas ellas con alteraciones de osmolaridad plasmática. En estos casos su nivel desciende y en varias oportunidades se mantiene estable o asciende levemente [72,73]. En isoosmolaridad, su concentración es estable debido al equilibrio entre los compartimentos anabólico y catabólico: en estos casos el valor de NAA es normal, sin riesgo de estrés osmótico. En hipoosmolaridad, el gradiente provoca la entrada de grandes volúmenes de agua para evitar la sobrehidratación celular y el estrés osmótico. Hay un aumento de salida del NAA al espacio extracelular extrayendo el agua que entró en exceso y se produce una reducción en su concentración celular y un descenso al ser medido por espectroscopia. Las causas de menor osmolaridad (es decir, de la natremia) son de origen hepático si se trata de una cirrosis alcohólica. Una vez resuelto el problema de osmolaridad, el retorno a la normalidad puede deberse a su condición de osmol o a la desintoxicación del paciente. En hiperosmolaridad, para evitar la deshidratación celular, el NAA no se moviliza y el agua se difunde por osmosis sin necesidad de movilizar el NAA: valor/nivel similar a la isoosmolaridad. La deshidratación celular ocasiona un incremento relativo de concentración del osmol, que al ser medido por espectroscopia puede dar valores elevados pero de orden relativo (Fig. 5). Otras patologías relacionadas con la concentración del NAA se deben a enfermedades de origen genético, una de ellas por la falta de la enzima responsable de su síntesis y otra por la carencia de la enzima encargada de su catabolismo. Una causa de ausencia del NAA y, simultáneamente, del NAAG se debe a la falta de la enzima responsable de su síntesis (hipoacetilaspartia). Se trata de una enfermedad genética con graves trastornos clínicos en la cual los niños afectados padecen retraso en la mielinización y microcefalia, además de www.neurologia.com Rev Neurol 2016; 62 (8): 361-370 Figura 5. Cambios del caudal del N-acetil-L-aspartato (NAA) relacionados con la osmolaridad medidos por espectroscopia. Se exhiben los valores normales de osmolaridad plasmática y su relación con el sodio. Además, se visualizan las variaciones de concentración de NAA dentro de la neurona. A: condición fisiológica sin cambios del nivel de NAA. Se observa el traslado de las moléculas de agua desde la neurona hasta la circulación general, en espectroscopia con valores normales. B y C: condiciones patológicas y la respuesta del NAA. B: por osmosis el ingreso de agua es mayor y el NAA para sacarla también debe ser mayor (en espectroscopia se observa su descenso). C: por osmosis el agua sale y el NAA se concentra y la retiene (en espectroscopia los valores son normal o levemente elevados). una amplia y compleja variedad de síntomas: trastornos del lenguaje, motores, de carácter cognitivo y episodios de estado epiléptico [74]. La ausencia de la enzima aspartoacilasa es responsable de una leucodistrofia en la que la carencia del catabolismo del NAA provoca su incremento en los axones en niveles superiores al promedio normal. Esto posibilita la entrada excesiva de moléculas de agua, lo que daña la sustancia blanca y el resto del parénquima cerebral. El efecto mecánico del agua es el responsable de la muerte de los niños, de ahí el nombre de leucodistrofia espongiforme, y es la causa de la macrocefalia. Por este motivo en algunas circunstancias su incremento se considera tóxico (nos referimos a la enfermedad de Canavan) [75]. Lo descrito es una muestra de la condición de osmol idiogénico del NAA y su capacidad de trasladar moléculas de agua. En este caso no beneficia al organismo, sino todo lo contrario: daña el parénquima cerebral. Discusión El NAA es el aminoácido libre/metabolito más abundante del SNC, con una concentración en valores absolutos de 10-16 mmol/kg y un recambio del 100% 367 M.A. Martínez, et al a las 14-16 h. Su alta concentración y rápido recambio definen una sustancia metabólicamente muy activa. Habitualmente, tiene una migración cuantiosa de la mitocondria y una emanación cerebral continua pero de escasa magnitud; sólo en la enfermedad de Canavan su nivel en orina es muy elevado [76]. Su fisiología se inicia en la neurona cuando se traslada desde la mitocondria hasta el citoplasma y se convierte en NAAG. Continúa al desplazarse al exterior de las mitocondrias llegando al espacio extracelular y a las células gliales y abordando también diversos órganos periféricos. Al desdoblarse en el resto del organismo, puede ser útil abasteciendo de productos químicos para el correcto funcionamiento de órganos ubicados fuera del SNC (por ejemplo, en el riñón, el hígado, el corazón y la mama) [77]. Las funciones del NAA son esenciales para el correcto funcionamiento del SNC y en todas ellas su trascendencia se relaciona con su estructura y su alta concentración. Participa en mantener adecuadamente los compartimentos del agua y, por esta razón, se define como un osmorregulador. Cuando hay incremento de consumo de glucosa en condiciones fisiológicas (por ejemplo, en una población neuronal que acrecienta su actividad), se observa un aumento de la cantidad de agua dentro de las neuronas que puede desorganizar su estructura interna y alterar su función. Simultáneamente, se incrementa su síntesis y, debido a su alta concentración, puede extraer el agua en exceso y permitir que las neuronas funcionen correctamente. Según lo expuesto, su función más valiosa como osmorregulador es proteger la integridad osmótica y estructural de las neuronas. En algunas circunstancias, en un traumatismo con focos de contusión hemorrágica se puede complicar con la presencia de un síndrome de secreción inadecuada de hormona antidiurética; por la pérdida de sal e hiponatremia observada en estas ocasiones, la reducción de su concentración y el restablecimiento a su nivel normal puede deberse a su cualidad de osmol idiogénico [78]. Lo descrito en la cita previa es una observación en niños maltratados o golpeados. Los autores no poseemos evidencia propia ni bibliográfica que excluya a los adultos. El NAAG es un péptido que modula el funcionamiento de las sinapsis de varios neurotransmisores; el péptido y las células gliales son responsables de la denominada plasticidad sináptica, que permite que la relación entre neuronas sea fluida y eficiente. Es la principal reserva de acetato y glutamato del organismo. El acetato es esencial para la síntesis de mielina en la etapa neonatal e incluso puede colaborar con la elaboración de los lípidos responsables 368 de la síntesis de mielina en los adultos. Esto último es de gran importancia, especialmente en el traumatismo y la esclerosis múltiple. Un trabajo experimental en ratas del año 2011 argumenta que la enzima aspartoacilasa tipo II no sólo se encuentra en el oligodendrocito [79]. Se detectó en diferentes tipos de cortezas, por ejemplo, en la iso/neocorteza y también en la allocorteza. Asimismo, se la identificó en la sustancia blanca, en la microglía, en células endoteliales y también en células piales, además de las ubicadas en el plexo coroideo. En la sustancia blanca se la detectó en el axoplasma/axones supra e infratentorial. Este hallazgo es lógico si tenemos en cuenta su alta concentración celular y extracelular, y en particular por su relación directa con la mielinogénesis neonatal y la producción de energía. El mismo ensayo menciona que el gen que codifica la enzima responsable de la síntesis del NAA se halló fuera del SNC en el bazo y el timo. Esto plantea que se pueda sintetizar, probablemente, en células relacionadas con tareas vinculadas con la inmunidad. En conclusión, no dudamos de que el NAA y NAAG son la unidad estructural y funcional indispensable para el correcto funcionamiento del cerebro de los vertebrados [80]. El NAA es un metabolito estudiado mediante espectroscopia, un método no invasivo que permite analizar la bioquímica cerebral en sujetos vivos. Esto nos permite acceder al estado de salud neuronal y de su integridad sinaptodendrítica. Con el mismo método y analizando el mismo metabolito, podemos discernir el funcionamiento de las mitocondrias y acceder al estado en que se encuentra el cerebro para producir energía. El trabajo nos permitió también saber que no sólo la glucosa es esencial para elaborar energía, ya que, junto con ella, el glutamato y el acetato son también de gran ayuda en los momentos en que se requiere ATP. Uno de los derivados del acetato es también indispensable para cubrir de mielina los axones y favorecer, junto con la producción de energía, la conexión entre los lóbulos de un hemisferio y lograr la integración obligatoria e imprescindible para unir la información almacenada en ambos hemisferios. Además, al ser el aminoácido libre de mayor concentración cerebral y tener la facultad de migrar, puede colaborar con la subsistencia/conservación de órganos ubicados fuera del SNC. En la introducción mencionamos que se halla en otras especies de vertebrados, por ejemplo, aves y reptiles. Sin el NAA, el edema en sus neuronas no permitiría a las aves volar miles de kilómetros durante su migración o a los reptiles (como se ha descubierto) aprender por imitación. Al resto de los www.neurologia.com Rev Neurol 2016; 62 (8): 361-370 Metabolismo del N-acetil-L-aspartato vertebrados les impediría utilizar sus reflejos de ataque y defensa, lo que los expondría a su extinción. Bibliografía 1. Tallan H, Moore S, Stein W. Studies on the free amino acids and related compounds in the tissues of the cat. J Biol Chem 1954; 211: 927-39. 2. Tallan H, Moore S, Stein W. N-acetyl-L-aspartic acid in brain. J Biol Chem 1956; 219: 257-64. 3. Tallan H. Studies on the distribution of N-acetyl-L-aspartic acid in brain. J Biol Chem 1957; 224: 41-5. 4. Jacobson BK. Studies on the role of N-acetylaspartic acid in mammalian brain. J Gen Physiol 1959; 43: 323-33. 5. Goldstein FB. Biosynthesis of N-acetyl-L-aspartic acid. Biochim Biophys Acta 1959; 33: 583-4. 6. Curatolo A, D’Arcangelo P, Lino A, Brancati A. Distribution of N-acetyl-aspartic and N-acetyl-aspartyl-glutamic acids in nervous tissue. J Neurochem 1965; 12: 339-42. 7. Goldstein FB. The enzymatic synthesis of N-acetyl-L-aspartic acid by subcellular preparations of rat brain. J Biol Chem 1969; 244: 4257-60. 8. Truckenmiller ME, Namboodiri MA, Brownstein MJ, Neale JH. N-acetylation of L-aspartate in the nervous system: differential distribution of a specific enzyme. J Neurochem 1985; 45: 1658-62. 9. Becker I, Lodder J, Gieselmann V, Eckhardt M. Molecular characterization of N-acetylaspartylglutamate synthetase. J Biol Chem 2010; 285: 29156-64. 10. Moreno A, Ross B, Bluml S. Direct determination of the N-acetyll-aspartate synthesis rate in the human brain by 13C MRS and [1-13C] glucose infusion. J Neurochem 2001; 77: 347-50. 11. Mathews CK, Van Holde KE. Bioquímica. 2 ed. Madrid: McGraw Hill-Interamericana; 1999. 12. Huang W, Wang H, Kekuda R, Fei YJ, Friedrich A, Wang J, et al. Transport of N-acetylaspartate by the Na1-dependent high-affinity dicarboxylate transporter NaDC3 and its relevance to the expression of the transporter in the brain. J Pharmacol Exp Ther 2000; 295: 392-403. 13. Moffett JR, Ross B, Arun P, Madhavarao CN, Namboodiri AM. N-acetylaspartate in the CNS: from neurodiagnostic to neurobiology. Prog Neurobiol. 2007; 81: 89-131. 14. Patel TB, Clark JB. Synthesis of N-acetyl-L-aspartate by rat brain mitochondria and its involvement in mitochondrial/ cytosolic carbon transport. Biochem J 1979; 184: 539-46. 15. Bates TE, Strangward M, Keelan J, Davey GP, Munro PM, Clark JB. Inhibition of N-acetylaspartate production: implications for 1H MRS studies in vivo. Neuroreport 1996; 7: 1397. 16. Benarroch EE. N-acetylaspartate and N-acetylaspartylglutamate, neurobiology and clinical significance. Neurology 2008; 70: 1353-7. 17. Vagnozzi R, Signoretti S, Cristofori L, Alessandrini F, Floris R. Assessment of metabolic brain damage and recovery following mild traumatic brain injury: a multicentre, proton magnetic resonance spectroscopic study in concussed patients. Brain 2010; 133: 3232-42. 18. Baslow M. N-acetylaspartate in the vertebrate brain: metabolism and function. Neurochem Res 2003; 28: 941-53. 19. Czerkiewicz I. Trastornos de la osmolaridad. Interpretación y diagnóstico etiológico. Servicio Acta Bioquímica Clínica Latinoamericana 2004; 38: 203-20. 20. Benarroch EE. NA+ K+ ATPase: functions in the nervous system and involvement in neurologic disease. Neurology 2011; 76: 287-93. 21. Peralta JG. Homeostasis del agua cerebral. Separata Línea Montpellier 2009; 17: 1-28. 22. Naranjo TA, Noguera-Salvá R, Fariñas Guerrero F. La matriz extracelular: morfología, función y biotensegridad (parte I). Rev Esp Patol 2009; 42: 249-61. 23. Nicholson CH. Modeling brain extracellular space from diffusion data. Diffusion Fundamentals 2007; 6: 1-15. 24. Andrew RD, Labron MW, Boehnke SE, Carnduff L, Kirov SA. Physiological evidence that pyramidal neurons lack functional water channels. Cereb Cortex 2007; 17: 787-802. www.neurologia.com Rev Neurol 2016; 62 (8): 361-370 25. Symon L. Investigation into the role of N-acetylaspartate in cerebral osmoregulation. J Neurochem 2007; 65: 275-81. 26. Taylor DL, Davies SEC, Obrenovitch TP, Doheny MH, Patsalos PN, Clark JB, et al. Investigation into the role of N-acetylaspartate in cerebral osmoregulation. J Neurochem 1995; 65: 275-81. 27. Agre P, King LS, Yasui M, Guggino WB, Ottersen OP, Fujiyoshi Y, et al. Aquaporin water channels-from atomic structure to clinical medicine. J Physiol 2002; 542: 3-16. 28. Baslow MH. Evidence supporting a role for N-acetyl-L-aspartate as a molecular water pump in myelinated neurons in the central nervous system. An analytical review. Neurochem Int 2002; 40: 295-300. 29. Baslow MH, Guilfoyle DN. Effect of N-acetylaspartic acid on the diffusion coefficient of water: a proton magnetic resonance phantom method for measurement of osmolyte-obligated water. Anal Biochem 2002; 311: 133-8. 30. Mehta SK, Kaur K, Sharma S, Bhasin KK. Behavior of acetyl modified amino acids in reverse micelles: a non-invasive and physiochemical approach. J Colloid Interface Sci 2007; 314: 689-98. 31. Plumridge TH, Waigh RD. Water structure theory and some implications for drug design. J Pharm Pharmacol 2002; 54: 1155-79. 32. Sácha P, Zámecnik J, Barinka C, Hlouchová K, Vícha A, Mlcochová P, et al. Expression of glutamate carboxypeptidase II in human brain. Neuroscience 2007; 144: 1361-72. 33. Neale JH, Bzdega T, Wroblewska B. N-acetylaspartylglutamate: the most abundant peptide neurotransmitter in the mammalian central nervous system. J Neurochem 2000; 75: 443-52. 34. Blakely RD, Coyle JT. The neurobiology of N-acetylaspartylglutamate. Int Rev Neurobiol 1988; 30: 39-100. 35. Baslow MH. The languages of neurons; an analysis of coding mechanisms by which neurons communicate, learn and store information. Entropy 2009; 11: 782-97. 36. Baslow MH. Functions of N-acetyl-L-aspartate and N-acetylL-aspartylglutamate in the vertebrate brain. Role in glial cellspecific signaling. J Neurochem 2000; 75: 453-9. 37. Clark JF, Doepke A, Filosa JA, Wardle RL, Lu A, Meeker TJ, et al. N-acetylaspartate as a reservoir for glutamate. Med Hypotheses 2006; 67: 506-12. 38. Yudkoff M, Nelson D, Daikhin Y, Erecinska M. Tricarboxylic acid cycle in rat brain synaptosomes. Fluxes and interactions with aspartate aminotransferase and malate/aspartate shuttle. J Biol Chem 1994; 269: 27414-20. 39. Kwon SE, Chapman ER. Synaptophysin regulates the kinetics of synaptic vesicle endocytosis in central neurons. Neuron 2011; 70: 847-54. 40. Lentz MR, Kim JP, Westmoreland SV, Greco JB, Fuller RA, Ratai EM, et al. Quantitative neuropathologic correlates of changes in ratio of N-acetylaspartate to creatine in macaque brain. Radiology 2005; 235: 461-8. 41. Baslow M. Evidence that the tri-cellular metabolism of N-acetylaspartate functions as the brain’s ‘operating system’: how NAA metabolism supports meaningful intercellular frequencyencoded communications. Amino Acids 2010; 39: 1139-45. 42. Xu HL, Mao L, Ye S, Paisansathan C, Vetri F. Astrocytes are a key conduit for upstream signaling of vasodilation during cerebral cortical neuronal activation in vivo. Am J Physiol Heart Circ Physiol 2008; 294: 622-32. 43. Attwell D, Buchan AM, Charpak S, Lauritzen M, Macvicar BA. Glial and neuronal control of brain blood flow. Nature 2010; 468: 232-43. 44. Barkovich AJ, Mukherjee P. Normal development of the neonatal and infant brain, skull, and spine. In Barkovich AJ, Raybaud CH, eds. Pediatric neuroimaging. 5 ed. Philadelphia: Lippincott Williams & Wilkins; 2012. p. 20-79. 45. Choi C, Sung Ko T, Lee H, Lee J, Suh D. Localized proton MR spectroscopy of the allocortex and isocortex in healthy children. AJNR Am J Neuroradiol 2000; 21: 1354-8. 46. Bianchi MC, Tosetti M, Battini R, Manca ML, Mancuso M, Cioni G, et al. Proton MR spectroscopy of mitochondrial diseases: analysis of brain metabolic abnormalities and their possible diagnostic relevance. AJNR Am J Neuroradiol 2003; 24: 1958-66. 369 M.A. Martínez, et al 47. Hugon J, Vallat JM, Dumas M. Role of glutamate and excitotoxicity in neurologic diseases. Rev Neurol (Paris) 1996; 152: 239-48. 48. Leighton P, Mark R, Prost W, Johnl U. Pictorial review of glutamate excitotoxicity. Fundamental concepts for neuroimaging. AJNR Am J Neuroradiol 2001; 22: 1813-24. 49. Clark JB. N-acetyl aspartate: a marker for neuronal loss or mitochondrial dysfunction. Dev Neurosci 1998; 20: 271-6. 50. Lipton SA, Rosenberg PA. Excitatory amino acids as final common pathway for neurologic disorders. N Engl J Med 1994; 330: 613-22. 51. Berria MI. Neuropatogenia de HIV en la era HAART. Actualizaciones en Sida 2012; 20: 97-103. 52. Lentz MR, Kim WK, Lee V, Bazner S, Halpern EF, Venna N. Changes in MRS neural markers and cell phenotypes observed during early HIV infection. Neurology 2009; 72: 1465-72. 53. Patel SH, Inglese M, Glosser G, Kolson DL, Grossman RI, Gonen O. Whole-brain N-acetylaspartate level and cognitive performance in HIV infection. AJNR Am J Neuroradiol 2003; 24: 1587-91. 54. Patel SH, Inglese M, Glosser G, Kolson DL, Grossman RI. Whole-brain N-acetylaspartate level and cognitive performance in HIV infection. AJNR Am J Neuroradiol 2003; 24: 1587-91. 55. Pfefferbaum A, Adalsteinsson E, Sullivans EV. Cortical NAA deficits in HIV infection without dementia: influence of alcoholism comorbidity. Neuropsychopharmacology 2005; 30: 1392-9. 56. Jessen F, Fingerhut N, Sprinkart AM, Ku KU, Petrovsky N, Maier W, et al. N-acetylaspartylglutamate (NAAG) and N-acetylaspartate (NAA) in patients with schizophrenia. Schizophr Bull 2013; 39: 197-205. 57. Bertolino A, Callicott JH, Mattay VS, Weidenhammer KM, Rakow R, Egan MF, et al. The effect of treatment with antipsychotic drugs on brain N-acetylaspartate measures in patients with schizophrenia. Biol Psychiatry 2001; 49: 39-46. 58. Bertolino A, Esposito G, Callicott JH, Mattay VS, Van Horn JD, Frank JA, et al. Specific relationship between prefrontal neuronal N-acetylaspartate and activation of the working memory cortical network in schizophrenia. Am J Psychiatry 2000; 157: 26-33. 59. Cecil KM, Del Bello MP, Morey R, Strakowski SM. Frontal lobe differences in bipolar disorder as determined by proton MR spectroscopy. Bipolar Disord 2002; 4: 357-65. 60. Kondo DG, Hellem TL, Shi XF, Sung YH, Prescot AP, Kim TS, et al. A review of MR spectroscopy studies of pediatric bipolar disorder. AJNR Am J Neuroradiol 2014; 35 (Suppl 6): S64-80. 61. Kapogiannis D, Mattson MP. Disrupted energy metabolism and neuronal circuit dysfunction in cognitive impairment and Alzheimer’s disease. Lancet Neurol 2011; 10: 187-98. 62. Gao F, Barker PB. Various MRS application tools for Alzheimer disease and mild cognitive impairment. AJNR Am J Neuroradiol 2014; 35 (Suppl 6): S4-11. 63. Bartha R. Magnetic resonance spectroscopy in the diagnosis of Alzheimer disease. London, Canada: University of Western Ontario. URL: http://www.cccdtd.ca/pdfs/MRSpectroscopy_ RBartha.pdf. 64. Moffett JR, Arun P, Ariyannur PS, Namboodiri AM. N-acetylaspartate reductions in brain injury: impact on post-injury, lipid synthesis and protein acetylation. Front Neuroenergetics 2013; 5: 11. 65. Signoretti S, Marmarou A, Aygok GA. Assessment of mitochondrial impairment in traumatic brain injury using high-resolution-proton-magnetic-resonance-spectroscopy. J Neurosurg 2008; 108: 42-52. 66. Holshouser BA, Tong KA, Ashwal S. Proton MR spectroscopic imaging depicts diffuse axonal injury in children with traumatic brain injury. AJNR Am J Neuroradiol 2005; 26: 1276-85. 67. Richardson M, Sun D, Bulloc MR. Neurogenesis after traumatic brain injury. Neurosurg Clin N Am 2007; 18: 169-181. 68. Kuzniecky R. Clinical applications of MR spectroscopy in epilepsy. Neuroimaging Clin N Am 2004; 14: 507-16. 69. Sarchielli P, Greco L, Floridi A, Floridi A, Gallai V. Excitatory amino acids and multiple sclerosis evidence from cerebrospinal fluid. Arch Neurol 2003; 60: 1082-8. 70. Dutta R, Trapp BD. Pathogenesis of axonal and neuronal damage in multiple sclerosis. Neurology 2007; 68 (Suppl 3): S22-31 [discussion: S43-54]. 71. Narayanan S, De Stefano N, Francis GS, Arnaoutelis R, Caramanos Z, Collins DL, et al. Axonal metabolic recovery in multiple sclerosis patients treated with interferon beta-1b. J Neurol 2001; 248: 979-86. 72. Videen JS, Michaelis T, Pinto P, Ross BD. Human cerebral osmolytes during chronic hyponatremia –a proton magnetic resonance spectroscopy study. J Clin Invest 1995; 95: 788-93. 73. Lee JH, Arcinue E, Ross BD. Organic osmolytes in the brain of an infant with hypernatremia. N Engl J Med 1994; 331: 439-42. 74. Boltshauser E, Schmitt B, Wevers RA, Engelke U, Burlina AB, Burlina AP. Follow-up of a child with hypoacetylaspartia. Neuropediatrics 2004; 35: 255-8. 75. Baslow MH. Brain N-acetylaspartate as a molecular water pump and its role in the etiology of Canavan disease: a mechanistic explanation. J Mol Neurosci 2003; 21: 185-90. 76. Kelley RI, Stamas JN. Quantification of N-acetyl-L-aspartic acid in urine by isotope dilution gas chromatography-mass spectrometry. J Inherit Metab Dis 1992; 15: 97-104. 77. D’Adamo AF Jr, Yatsu FM. Acetate metabolism in the nervous system. N-acetyl-L-aspartic acid and the biosynthesis of brain lipids. J Neurochem 1966; 13: 961-5. 78. Ross BD, Ernst T, Kreis R, Haseler LJ, Bayer S, Danielsen E, et al. 1H MRS in acute traumatic brain injury. J Magn Reson Imaging 1998; 8: 829-40. 79. Moffett JR, Arun P, Ariyannur PS, Garbern JY, Jacobowitz DM, Namboodiri AM. Extensive aspartoacylase expression in the rat central nervous system. Glia 2011; 59: 1414-34. 80. Baslow MH, Burlina AP. N-acetylaspartate metabolism underlays the structural and functional units of the vertebrate brain: a bioenergetic rationale for clinical observations of changes in the neuronal biomarker ‘NAA’ in many human brain disorders. Bioenerg Open Access 2012; 1: 2-10. Metabolism of N-acetyl-L-aspartate: its diagnostic and prognostic value Aims. To analyse the clinical involvement of the amino acid N-acetyl-L-aspartate (NAA) and the peptide N-acetyl-aspartylglutamate (NAAG) regarding their diagnostic and prognostic value by means of magnetic resonance spectroscopy. To conduct a review of the metabolism of NAA and NAAG, bearing in mind their chemical structure and physiology, in terms of the variations in their concentration and the correlation with the clinical features. Development. The review is divided into two parts: in one it was found that the only site where NAA synthesis takes place is in the neuronal mitochondria, while the second part addresses magnetic resonance and, especially, spectroscopic techniques. An array of pathologies were analysed in search of criteria that allow diagnostic and prognostic guidelines. Conclusions. The study of the most abundant amino acid in the central nervous system (NAA) together with a product of its metabolism, NAAG, allows the diagnosis and follow-up of a variety of pathologies. At the same time, it makes it easier to obtain data about the density of the cell population and its vitality, thus also providing access to the functional status of the synapses. Key words. Cell vitality. Magnetic resonance spectroscopy. NAA. NAAG. Synaptodendritic integrity. 370 www.neurologia.com Rev Neurol 2016; 62 (8): 361-370