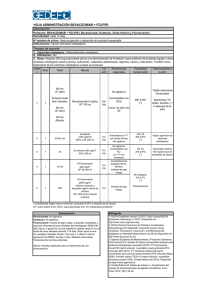
Bevacizumab (Avastin) - Farmacología Clínica
Anuncio

Bevacizumab (Avastin) Concentrado para solución para infusión. Uso en oftalmología Fecha 06/2010 1. AUTORES DEL INFORME DE CONSENSO Autores: Comité de Farmacia y Terapéutica del hospital El Cruce Alta Complejidad en Red. Florencio Varela Este informe de consenso se ha realizado tomando como base los informes técnicos internos de diferentes servicios del hospital. Dichos informes se pueden consultar a través de los siguientes links. 2. INFORMACION DEL SERVICIO SOLICITANTE Servicio: Oftalmología Facultativo que efectuó la solicitud: Rosendi Esequiel Indicación/es clínica/s solicitada/s: Tratamiento de la maculopatía exudativa, maculopatía diabética y edema macular de diferente etiología Declaración Conflicto de Intereses: No se pronunció al respecto Fecha recepción de la solicitud: marzo de 2010 Petición a título: Consenso c/aprobación Jefe Servicio 1.- CARACTERISTICAS GENERALES DEL MEDICAMENTO/GRUPO FARMACOLOGICO Denominación común internacional (DCI): Bevacizumab Nombre comercial: Avastin ® Laboratorio: Roche Código ATC: L01XC07 Grupo farmacológico: Anticuerpo monoclonal Forma farmacéutica, presentación, unidades por tratamiento. Según tabla adjunta DCI Marca Comercial Bevacizumab Avastin FF y potencia (concentración de la unidad) Amp 100 mg/4 ml Amp 400 mg/16 ml Presentación envase 1 vial 1 vial Costo (Precio estimado de compra) $3092 $11262 Mecanismo de acción: Anticuerpo monoclonal recombinante humanizado que se une al factor de crecimiento del endotelio vascular (VEGF), factor clave de la vasculogénesis y la angiogénesis, inhibiendo así la unión de éste a sus receptores Flt1 (VEGFR-1) y KDR (VEGFR-2), situados en la superficie de las células endoteliales. La neutralización de la acti vidad biológica del VEGF produce una regresión de la vascularización de los tumores, normaliza la vasculatura residual del mismo e inhibe la neovascularización, inhibiendo así el crecimiento del tumor. Dentro de este grupo farmacológico se encuentran 2 fármacos más: el ranibizumab (diseñado para ser administrado por vía intraocular) y el pegaptanib (que inhibe de forma específica la isoforma intraocular del VEGF) 2.- CRITERIOS DE SELECCIÓN DE MEDICAMENTOS 2.1. Resumen de la eficacia comparada en diversos entornos clínicos: El bevacizumab no ha sido desarrollado para ser utilizado en la degeneración macular asociada a la edad (DMAE) por tal motivo se dispone de muy pocos y pequeños ensayos clínicos con bevacizumab en la DMAE, a su vez no ha sido comparado con ranibizumab que sí está aprobado para esta indicación tanto en EEUU, la Unión Europea como en Argentina. El estudio CATT patrocinado por The National Eye Institute comenzó a incorporar pacientes en unos 40 centros en enero de 2008. Se prevé la incorporación de 1.200 pacientes con un seguimiento de 2 años. El estudio está diseñado para comparar los tratamientos de la DMAE y se realizará una asignación aleatorizada de los pacientes (300 en cada grupo) a ranibizumab mensual, bevacizumab mensual o a inyección única de bevacizumab o ranibizumab. Ambos productos son fabricados y comercializados por Genentech. Los criterios de inclusión serán menos estrictos (agudeza visual 20/25 o peor) que los de estudios previos sobre tratamiento de la DMAE para reproducir con más fidelidad el tratamiento real de los pacientes que no participan en estudios clínicos. El criterio principal de valoración del CATT será el cambio medio de la agudeza visual en 1 año. Los criterios secundarios de valoración son: número de tratamiento, cambio de tres líneas en la agudeza visual, cambio del líquido subrretiniano e intrarretiniano en TCO (tomografía de coherencia óptica), cambio de tamaño de la lesión en la angiografía con fluoresceína, Incidencia de endoftalmitis, desprendimiento de retina, cataratas y uveítis, Incidencia de complicaciones, costos de los tratamientos. Este estudio es el único que tendrá poder suficiente para demostrar una pequeña diferencia entre ambos fármacos. Los resultados de series de casos con bevacizumab intravítreo han mostrado beneficios: Una serie de casos en 60 pacientes con DMAE húmeda donde recibieron bevacizumab intravítreo (2,5 mg, repetir la inyección al mes o dos meses si la (TCO) o los resultados de la agudeza visual indican actividad de la enfermedad). Tuvieron una mejoría significativa en la agudeza visual media a los 12 meses y una mejora anatómica de la retina, no se observaron efectos secundarios oculares o sistémicos 1. Resultados preliminares de un ensayo randomizado comparando bevacizumab intravítreo y ranibizumab no encuentran diferencias en la eficacia para el tratamiento de la neovascularización coroidea en la DMAE. Sólo 20 pacientes completaron seis meses de seguimiento. La diferencia entre los dos grupos no fue estadísticamente significativa para la agudeza visual2. 2.2. Resumen de la evidencia comparada respecto al riesgo: En un registro de efectos adversos sobre 7.113 inyecciones intravítreas en 5.228 pacientes, la frecuencia de efectos adversos descrita es del 0,21%. Se ha descrito aumento de la presión arterial en un 0,21% (máximo 200mm Hg de sistólica), abrasiones corneales en un 0,15%, y uveítis en un 0,14%. Dada su prolongada semivida de eliminación, se ha sugerido que la frecuencia de efectos sistémicos podría ser superior, el número de complicaciones sistémicas registradas es de 9 (una trombosis venosa, un TIA (accidente isquémico transitorio) 5 accidentes cerebro vascular y dos muertes). De todas formas, la notificación en el registro es voluntaria y se puede estar infraestimando la frecuencia de efectos adversos. El uso de bevacizumab se desaconseja en hipertensos mal controlados y en pacientes con riesgo de acontecimientos tromboembólicos arteriales 3. Se citan a continuación algunos estudios descriptivos: Estudio con 53 pacientes, realizado para informar sobre la aparición de hemorragias submacular luego de la administración de bevacizumab intravítreo en la neovascularización coroidea (NVC) oculta en la degeneración macular relacionada con la edad (DMAE). Las conclusiones a la que llegan los autores son: Las hemorragias submacular parecen ser un acontecimiento adverso significativo tras la inyección intravítrea de bevacizumab en la neovascularización coroidea oculta grande, pudiendo afectar los resultados visuales. Se requieren estudios prospectivos para establecer la dosis óptima de bevacizumab para las lesiones cutáneas grandes o para identificar el agente anti-VEGF más adecuada en grandes NVC oculta 4 Estudio PACORES5, serie de casos, retrospectivo, multicéntrico, abierto, no controlado, informó sobre eventos adversos sistémicos acumulativos y anatomopatológicos de bevacizumab intravítreo durante 12 meses de seguimiento. Los 1.173 pacientes fueron inyectados con bevacizumab para enfermedades como la retinopatía diabética proliferativa, edema macular diabético, oclusión venosa retiniana, y la NVC de diversas etiologías como la DMAE en 8 instituciones de América Latina a partir de 1 septiembre 2005 a 31 enero 2006. Resultados: un total de 4.303 inyecciones intravítreas de bevacizumab en 1310 ojos. Se reportaron eventos adversos sistémicos en 18 (1,5%) pacientes. Estos incluyeron siete (0,59%) casos de elevación aguda de la presión arterial sistémica, seis (0,5%) ACV, cinco (0,4%) infartos de miocardio, dos (0,17%) aneurismas arteria ilíaca, dos (0,17%) amputaciones del dedo del pie y cinco (0,4%) defunciones. Las complicaciones oculares incluyen siete (0,16%) endoftalmitis bacteriana, siete (0,16%) desprendimientos de retina, cuatro (0,09%) uveítis, y un caso (0,02%) de desprendimiento regmatógeno de retina y hemorragia vítrea. Conclusión: A pesar del escaso seguimiento, repetidas inyecciones intravítreas de 1,25 mg o 2,5 mg de bevacizumab parece ser seguro y bien tolerado durante el primer año. Porcentaje de efectos adversos reportados en regimenes antineoplásicos, como único fármaco quimioterápico6 > 10%: Cardiovascular: hipertensión (23% a 67%), evento tromboembólico (≤ 21%;); Sistema nervioso central: dolor (31% a 62%), cefalea (24% a 37%), mareos (19% a 26%), fatiga (≤ 45%) Dermatológicas: Alopecia (6% al 32%), sequedad de la piel (7% a 20%), dermatitis exfoliativa (3% a 19%), decoloración de la piel (2% a 16%) Endocrinos y metabólicos: hipopotasemia (12% a 16%) Gastrointestinales: dolor abdominal (50% a 61%), vómitos (47% a 52%), anorexia (35% a 43%), estreñimiento (29% a 40%), estomatitis (25% a 32%), hemorragia gastrointestinal (19% a 24%), dispepsia (17% a 24%), trastorno del gusto (14% a 21%), flatulencia (11% a 19%), pérdida de peso (9% a 20%) Hematológicas: Hemorragia (≤ 40%), leucopenia (37%), neutropenia ( 6% a 27%) Neuromuscular y esquelético: Debilidad (57% a 74%), dolor mialgia (8% a 19%), espalda (≤ 12%) Renales: proteinuria (4% a 36%) Aparato respiratorio: infección del tracto respiratorio superior (40% a 47%), epistaxis (16% a 35%), disnea (25% a 26%) 2.3. Resumen de la evidencia respecto a la conveniencia: (aspectos cinéticos, contraindicaciones/ precauciones e interacciones de relevancia clínica): La frecuencia óptima para inyección de inhibidores de VEGF no se conoce. La frecuencia de tratamiento para los inhibidores de VEGF, caso puntual ranibizumab, ha sido evaluada en los ensayos MARINA y ANCHOR como inyecciones intravítreas mensuales. En un estudio observacional con bevacizumab mensual durante 3 meses encontró engrosamiento foveal que fue mejorando durante el curso del tratamiento, observándose un empeoramiento durante los siguientes tres meses sin tratamiento7 Un diseño de estudio similar con bevacizumab mostraron una mejoría equivalente en la agudeza visual en dos años, pero menos inyecciones (promedio 4,9) se requiere, posiblemente relacionados con los criterios más estrictos para re-inyección y / o una vida media más larga de bevacizumab 8 2.4. Resumen de los datos disponibles sobre el costo y costo-eficacia comparativos dentro de la clase farmacológica o grupo terapéutico en cuestión: El tratamiento con bevacizumab intravítreo es mucho menos costoso que el tratamiento con ranibizumab intravítreo (50 dólares en comparación con 1950 dólares por cada inyección) 9 10 11. En espera de resultados de grandes ensayos aleatorios, los clínicos han utilizado inyecciones intravítreas de bevacizumab para el tratamiento de la DMAE. Comparación con la terapia de referencia a dosis usuales. Costo tratamiento y comparación terapia de referencia Medicamento Precio unitario (P. estimado de compra) $7295 Posología Costo/ dosis Nº sesiones estimadas mínimas/año Costo tratamiento 6 sesiones Ahorro incremental/ paciente 0.5 mg/ mes $ 7295 6 $43770 --- Ranicizumab FA 10 mg/ml x 0.23 ml (a) $7295 0.5 mg/ mes $ 2431 6 $14586 $29184 Bevacizumab jeringas mg/0.1ml (b) $340 1.25 mg/ mes $ 340 6 $2040 $41730 $3092 1.25 mg/ mes $ 77 6 $463 $43307 Ranicizumab FA 10 mg/ml x 0.23 ml 2.5 Bevacizumab FA 100 mg/4ml (c) (a) Servicio de Farmacia del Hospital El Cruce podría realizar el fraccionamiento del Rn en tres jeringas, una vez instalada la campana de flujo laminar (b) Jeringas compradas a Farmacia que realizan el fraccionamiento bajo campana de flujo laminar del Bz (c) Servicio de Farmacia del Hospital El Cruce podría realizar el fraccionamiento del Bz en jeringas de 2.5 mg/0.1 ml, una vez instalada la campana de flujo laminar Impacto económico en el escenario del HEC: Suponiendo que se traten un promedio de 5 (cinco) pacientes el primer mes; el segundo mes 5 (cinco) nuevos + los 5 primeros (total 10); el tercer mes 5 nuevos + 10 (total 15); el cuarto mes 5 nuevos + 15 (total 20); el 5 mes 5 nuevos + 20 (total 25) y el sexto mes 5 nuevos + 25 (total 30). Total de pacientes tratados en un período de 6 meses: 105 pacientes = 105 dosis Por lo tanto, en un período inicial de 6 meses el impacto en el hospital es el siguiente: Estimación del impacto en el hospital El Cruce Período inicial de 6 meses = 105 dosis Costo Ahorro según las diferentes opciones --$765975 Ranicizumab FA 10 mg/ml x 0.23 ml Dosificando Ranicizumab en 3 jeringas Reemplazo por Bevacizumab fraccionado comprado Reemplazo por Bevacizumab fraccionado en la Farmacia del Hospital $255255 $510720 $35700 $730275 $8116 $757859 3.- CONCLUSIONES Son necesarios estudios con muestras más grandes de pacientes para establecer la significación estadística ya que los pocos estudios encontrados transmiten los resultados de un pequeño número de pacientes Algunas de las claves que afectan el análisis de bevacizumab en la terapéutica de la DMAE exudativa: Ausencia de ensayos clínicos controlados randomizados con ranibizumab Frecuencia de las inyecciones que serían necesarias para mantener la respuesta en la práctica clínica Extrapolación del tratamiento beneficioso asociado con anti-VEGF más allá de la duración de los ECC Por lo tanto, siempre que sea posible, los pacientes expuestos a nuevos fármacos donde las evidencias disponibles corresponden a grados de recomendación C y/o D, deberían ser alentados a inscribirse en ensayos clínicos. El bevacizumab, a diferencia de ranibizumab, no tiene la indicación aprobada para DMAE no dispone de ensayos clínicos controlados y no ha sido desarrollado para ser administrado por vía intravítrea. No obstante, el ranibizumab presenta un costo muy superior al del bevacizumab, una alternativa para la que se dispone de la experiencia de uso en unos miles de pacientes en series de casos con resultados que parecen similares. El Comité concluye que frente a la existencia de gran incertidumbre en la evaluación de la validez para las extrapolaciones de eficacia y seguridad, se debe incluir al bevacizumab para los pacientes con DMAE, en el marco de un protocolo de investigación analizado y aprobado por los comités correspondientes. 4.-RECOMENDACIONES El Comité de Farmacia y Terapéutica considera que nuevas investigaciones sobre bevacizumab para la terapéutica de la degeneración macular asociada a la edad (DMAE) exudativa, son perentorias, incluyendo algunos estudios como: los efectos a largo plazo de los fármacos anti-VEGF en pacientes con DMAE, incluyendo los efectos sobre la agudeza visual, daño anatómico de la mácula, la calidad de vida y eventos adversos. la rentabilidad de bevacizumab (sin aprobación hasta la fecha para la DMAE exudativa) como: costos de instalación y personal adecuado para la inyección intravítrea establecer la duración adecuada y un régimen de tratamiento óptimo en términos de frecuencia de las inyecciones 5.- BIBLIOGRAFIA 1 Bashshur, ZF, Haddad, ZA, Schakal, A, et al. Intravitreal Bevacizumab for Treatment of Neovascular Agerelated Macular Degeneration: A One-year Prospective Study. Am J Ophthalmol 2008; 145:249. 2 Subramanian, ML, Ness, S, Abedi, G, et al. Bevacizumab vs ranibizumab for age-related macular degeneration: early results of a prospective double-masked, randomized clinical trial. Am J Ophthalmol 2009; 148:875. 3 Hospital de Vall d” Hebron. Servei de farmacología Clinica. Monografia sobre ranibizumab. Octubre 2007 4 Goverdhan, SV, Lochhead, J. Submacular haemorrhages after intravitreal bevacizumab for large occult choroidal neovascularisation in age-related macular degeneration. Br J Ophthalmol 2008; 92:210. 5 Wu L, Martínez-CastellanosMA, Quiroz-Mercado H, et al. Twelve-month safety of intravitreal injections of bevacizumab (Avastin®): results of the Pan-American Collaborative Retina Study Group (PACORES). Arch Clin Exp Ophthalmol 2008; 246(1): 81–87. 6 Update 7 Melamud, A, Stinnett, S, Fekrat, S. Treatment of neovascular age-related macular degeneration with intravitreal bevacizumab: efficacy of three consecutive monthly injections. Am J Ophthalmol 2008; 146:91 8 Bashshur, ZF, Haddad, ZA, Schakal, AR, et al. Intravitreal bevacizumab for treatment of neovascular agerelated macular degeneration: the second year of a prospective study. Am J Ophthalmol 2009; 148:59. 9 Rosenfeld, PJ. Intravitreal avastin: the low cost alternative to lucentis?. Am J Ophthalmol 2006; 142:141. 10 Epstein, P. Trials that matter: two faces of progress in the treatment of age-related macular degeneration. Ann Intern Med 2007; 146:532. 11 Chen, CY, Wong, TY, Heriot, WJ. Intravitreal bevacizumab (Avastin) for neovascular age-related macular degeneration: a short-term study. Am J Ophthalmol 2007; 143:510.