efecto de la oxidación de los contaminantes orgánicos
Anuncio

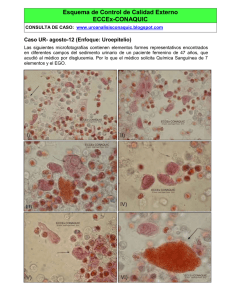
EFECTO DE LA OXIDACIÓN DE LOS CONTAMINANTES ORGÁNICOS SOBRE LAS ASOCIACIONES METAL/SEDIMENTO EN UNA PRESA MEXICANA CONTAMINADA Anne-Laure S. Bussy Beaurain (*) Universidad Autónoma Metropolitana. Doctora en Ciencias y Técnicas del Medio Ambiente, Profesor investigador asociado de la UAM-Azcapotzalco. Ha dirigido tesis de licenciatura. Ha presentado ponencias nacionales e internacionales. Ha publicado en memorias de congresos nacionales e internacionales, coautora de artículos en revistas especializadas nacionales. Candidata en el SNI. Icela D. Barceló Quintal Universidad Autónoma Metropolitana- Unidad Azcapotzalco Hugo E. Solís Correa Universidad Autónoma Metropolitana- Unidad Azcapotzalco Pedro Ávila Pérez Instituto Nacional de Investigaciones Nucleares (*): Av. San Pablo, No. 180, Col. Reynosa-Tamaulipas, Del. Azcapotzalco, C.P. 02200, México D.F. Tel y Fax: (52) 55-5318.9360, Email: ibarcelo@att.net.mx RESUMEN En este trabajo, se pretende verificar, mediante un experimento al nivel banco de laboratorio, si los sedimentos de la presa José Antonio Alzate, embalse que recibe agua del río Lerma, contaminada por descargas industriales y domésticas, entrampan a los metales de manera definitiva cuando no existen cambios externos en las condiciones fisicoquímicas del medio. Para ello, se construyeron tres columnas agua/sedimento que se dejaron madurar durante tiempos diferentes: 5, 23 y 27 semanas. Al final de cada experimento, se cortó la columna de sedimentos en varios estratos. Se midieron la humedad, la perdida de masa a 550 °C y las concentraciones de Cd y Fe. La degradación microbiológica de la materia orgánica en los sedimentos de la presa J.A. Alzate liberó biogases que formaron nuevos y grandes poros en las columnas de sedimento. Estos poros se llenaron parcialmente con agua. Después, se pudo observar el fenómeno de compactación, acompañado de una convección del agua. Se notó una degradación de materia orgánica durante todo el experimento, con reasociaciones de las especies orgánicas disueltas con los sedimentos. Se observó un efecto notable sobre los movimientos de los metales asociados a la fase sólida. Para Cd y Fe, el comportamiento general parece ser una asociación secundaria en la zona superior de la columna de sedimentos, con una posibilidad tanto de redisolución del metal como el de reasociación aún más arriba, dando la impresión del ascenso de un “frente metálico”. El hierro queda asociado a la capa superficial del sedimento, cuando el cadmio parece mantenerse en gran parte en la fase disuelta. Palabras clave: sedimentos, metales, materia orgánica, actividad microbiológica INTRODUCCION En un cuerpo acuático, el sedimento es receptor final de la mayoría de los contaminantes, incluyendo metales y compuestos orgánicos (Barceló, 2000). La parte biodegradable de este último grupo de compuestos es eliminada mediante la actividad de ciertos micro-organismos presentes en el medio. En general, los microbiólogos consideran la existencia de seis tipos de reacción, que clasifican en función de su aporte energético al micro-organismo, como se ilustra en la tabla 1 (Reeburgh, 1983). Es importante notar que el tipo de agua interviene también en el orden de preponderancia de estas reacciones. Por ejemplo, en medio marino, la reducción de los sulfatos, encontrados en concentraciones altas, será la principal responsable de la degradación de la materia orgánica después del agotamiento del oxígeno disuelto, mientras que en las aguas dulces, están favorecidas la respiración, la metanogénesis y la desnitrificación (en este orden, Jones, 1982). Este orden puede variar cuando la concentración de uno de los sustratos oxidados es preponderante o insignificante, como en el caso de un subsuelo rico en óxidos metálicos (por ejemplo, en una zona volcánica) o cuando se encuentra una contaminación específica del agua (por materia orgánica, sulfatos o nitratos, etc.). Tabla 1: Secuencia de las reacciones acopladas a la oxidación de la materia orgánica Reacción reducción de O2 desnitrificación reducción de Mn reducción de Fe -reducción de SO4 metanogénesis O2 H2O NO3 N2 Mn(IV) Mn(II) Fe(III) Fe(II) -SO4 HS CH2O CH4 Energía (kJ/mol de CH2O degradado) - 475 - 448 -349 -114 -77 -58 Desde un punto de vista químico, esta degradación es producida por varios agentes oxidantes. Las diferentes reacciones implicadas se suceden en un orden determinado por la desaparición de los reactivos oxidados necesarios (ecuaciones 1 a 6). (CH2O)x(NH3)y + (x+2y)O2 xCO2 + (x+y)H2O + yHNO3 - Ecuación 1 - 5(CH2O)x(NH3)y + 4xNO3 xCO2 + 3xH2O + 4xHCO3 + 2xN2 + 5yNH3 2+ - Ecuación 2 (CH2O)x(NH3)y + 2xMnO2 + 3xCO2 + xH2O 4xHCO3 + 2xMn (CH2O)x(NH3)y + 4xFe(OH)3 + 7xCO2 + xH2O 8xHCO3 + 3xH2O + 4xFe 2- - 2(CH2O)x(NH3)y + xSO4 2(CH2O)x(NH3)y - 2xHCO3 + xH2S + 2yNH3 xCO2 + xCH4 + 2yNH3 + yNH3 2+ Ecuación 3 + yNH3 Ecuación 4 Ecuación 5 Ecuación 6 La oxidación de la materia orgánica biodegradable se realiza siguiendo esta misma secuencia, desde la superficie hasta el fondo de la columna de sedimento, generando la desaparición o la aparición de ciertas especies químicas en el agua intersticial de los sedimentos (Figura 1, Tebo et al., 1984). Concentración Profundidad O2 NO3- Reacción Respiración Denitrificación Mn 2+ Reducción del Mn(II) y del Mn(IV) Fe 2+ Reducción del Fe(III) HS- SO42- Reducción De los sulfatos Figura 1: Representación esquemática de los perfiles de las especies redox disueltas en las aguas intersticiales de un sedimento Las reacciones implicadas generan protones y moléculas reducidas, lo que provoca una acidificación y una reducción general del medio, que pueden modificar los equilibrios de disolución/precipitación de los compuestos inorgánicos presentes en el sedimento y liberar una parte de los metales asociados a los diversos constituyentes del mismo (Benoit y Hemond, 1990). Este fenómeno puede existir en los cuerpos acuáticos contaminados tanto por descargas industriales y domésticas, donde se encuentran metales y materia orgánica antropogénica fácilmente biodegradable. En este caso, la actividad microbiológica natural del sedimento podría generar cambios en las condiciones fisicoquímicas suficientemente importantes para movilizar ciertas cantidades de éstos metales asociados al sedimento y generar su liberación como etapa secundaria hacia la columna de agua. OBJETIVO En este trabajo, se pretende verificar, mediante un experimento al nivel banco de laboratorio, si los sedimentos de un embalse que recibe agua de un río contaminado, por descargas industriales, domésticas y agrícolas, sufren un proceso de oxidación de la materia orgánica lo suficientemente notable para movilizar los metales asociados al sedimento y determinar si estos cambios son significativos al nivel de las concentraciones particuladas. METODOLOGÍA En el Estado de México, el curso alto del río Lerma esta canalizado desde su nacimiento hasta la presa J.A. Alzate y recibe descargas de aguas negras tanto domésticas, como industriales o agrícolas (CNA, 1998; Peña et al., 2000). Por lo tanto, este embalse artificial, construido para el control de avenidas y el almacenamiento de agua de riego (CNA, 1990), funciona como un receptor de todos los contaminantes introducidos aguas arriba. En particular, la presa entrampa cantidades importantes de sedimentos altamente contaminados (Avila et al., 1999). Los sedimentos superficiales y el agua se recolectaron en la zona de mayor sedimentación de la presa J.A. Alzate (Figura 2, Barceló, 2000), mediante una draga Ekman y un muestreador van Dorn, respectivamente. Posteriormente los sedimentos fueron homogeneizados. Los reactores se conformaron de una columna de vidrio con una extremidad cerrada. Se llenó cada reactor de sedimento y se cubrió el sedimento con agua. La parte del reactor ocupada por el sedimento se protegió para impedir el paso de luz, mientras que la capa de agua quedó en contacto con la luz y el aire, reproduciendo las condiciones encontradas in situ. Se construyeron tres columnas agua/sedimento que se dejaron madurar durante tiempos diferentes: 5, 23 y 27 semanas. R ío L e rm a s a lid a 1000 m S itio d e m u e s tre o R ío L e rm a e n tr a d a A S itio d e m u e s tre o P o b la d o s Figura 2: Sitios de muestreo Durante el experimento, se siguió la evolución de los volúmenes de agua y sedimento en los reactores en función del tiempo. Después se cortaron las columnas de sedimentos en diferentes estratos que se caracterizaron como los sedimentos originales: 1. humedad, 2. pérdida de materia a 550°C, 3. concentraciones metálicas analizadas por absorción atómica (flama u horno, Varian SpectrAA20 plus y GTA-96 Plus) después de una digestión ácida en un digestor de microondas (CEM Mars 5) con 10 mL de una mezcla 1:1 de ácido nítrico y fluorhídrico concentrados. La extracción se hizo por triplicado con una desviación experimental promedio de 5% para los tres metales, y una desviación analítica promedio de 4%. Este procedimiento se resume en la figura 3. RECOLECCIÓN AGUA RECOLECCIÓN SEDIMENTO SUPERFICIAL HOMOGENEIZACIÓN 5 semanas CARACTERIZACIÓN CORTADO SECADO Figura 3:Tratamiento del sedimento RESULTADOS Caracterización de los sedimentos colectados El sedimento empleado presenta una textura arcillosa (Tabla 2), diferente de lo que se encontró en el río Lerma (Bussy et al., 2004). Tabla 2: Caracterización de los sedimentos colectados Arena (%) Limo (%) Arcilla (%) Clasificación humedad (%) 18.3±0.6 17.7±0.7 64.0±0.2 Arcilloso mat. Orga. (%) Cd(mg/kg) Fe (g/kg) 65.8±1.5 12.4±0.5 0.78±0.02 36.3±0.6 Evolución en los reactores La evolución global del volumen de las columnas de agua en función del tiempo transcurrido parece ser relativamente lineal, aunque de pendiente diferente en cada reactor (Figura 4). Esta evolución es la consecuencia de dos fenómenos: la compactación del sedimento que rechaza el agua hacia arriba y la evaporación que disminuye el volumen de agua. Como se observa en la figura 4, la evaporación es la manifestación dominante en los tres reactores. La diferencia de pendiente proviene de los diámetros 2 diferentes de los reactores. Para cada caso, la evaluación de la evaporación es de 0.16 mL/d/cm (5 2 2 sem.), 0.28 mL/d/cm (23 sem.) y 0.24 mL/d/cm (27 sem.), después de corregir la tendencia general por la compactación. A pesar de que fue poco notable en la evolución de la columna de agua, la compactación existe, como lo demuestra la evolución de la columna de sedimento, y sobre todo, la variación de humedad. Al igual que lo que se observó para las columnas de agua, la evolución de la columna de sedimento sigue el mismo patrón en los tres reactores (Figura 5), con amplitudes diferentes. Las relaciones que existen entre las diferentes amplitudes son: 1.64±0.03 (11 puntos, 5/23 sem.), 1.12±0.01 (11 puntos, 5/27 sem.) y 1.44 ±0.03 (27 puntos, 27/23 sem.), y parecen depender del diámetro de los reactores (5 sem.>27 sem.>23 sem.). El proceso inicia con un aumento del volumen en las tres columnas de sedimento que termina el día 25, seguido de un decrecimiento rápido (hasta el día 41), y termina por una disminución más lenta. Este comportamiento describe una actividad microbiológica semejante en los tres reactores. En particular, la producción máxima de biogás ocurre en los 25 primeros días; después los poros creados por los gases se colapsan rápidamente, finalmente las columnas experimentan una compactación más lenta. En un lapso de cinco semanas, la primera columna cortada no logró obtener un volumen inferior al valor original (Figura 5). 5 sem. 23 sem. 27 sem. 0.8 2 vol. de agua (mL) r = 0.9923 0.6 0.4 2 r = 0.9873 0.2 2 r = 0.9532 0.0 0 30 60 90 120 Tiempo (días) 150 180 Figura 4: Evolución global de las columnas de agua vol. de sedimento (mL) 27 sem. 1.17 1.70 1.12 1.60 1.07 1.50 1.40 vol. de sedimento (mL) 5 sem. /1.12 23 sem. 1.80 1.02 0 30 60 90 120 Tiempo (días) 150 180 Figura 5: Evolución global de las columnas de sedimento Evolución de la humedad y del contenido en materia orgánica La figura 6 describe las variaciones en el contenido de materia orgánica (6a) y en la humedad (6b), en función de la profundidad, expresados como porcentaje de la masa del sedimento (seco en el primer caso y húmedo en el segundo). A la profundidad 0 (cero) se encuentra la interfase agua/sedimento. Al igual que la evolución en el tiempo del volumen de la columna de sedimento, el contenido en materia orgánica presenta puntos comunes a los tres reactores. En particular, se observan tendencias comunes: 1. una concentración baja en el fondo, reflejando un consumo de materia orgánica 2. tres zonas de concentración alta que pueden exceder a la concentración original, correspondiendo a una reasociación de la materia orgánica con el sedimento, de 47 a 36 cm, de 24 a 11 cm y en la capa superficial delgada. Los perfiles obtenidos para este parámetro permiten notar que, a pesar de obtener la mayor producción de biogás en los primeros días, la degradación de la materia orgánica sigue a lo largo de todo el experimento, ya que las concentraciones son notablemente más bajas después de 27 semanas, mientras que los resultados encontrados en los dos otros reactores son del mismo orden y no muy diferentes del valor original. Los perfiles de humedad (6b) presentan una pérdida de agua por parte del sedimento, lo que demuestra la existencia de un fenómeno de compactación. En particular, se puede observar que la humedad es mayor en la mitad superior de las columnas que en la mitad inferior. Sin embargo, los porcentajes generales siguen el orden 23 sem.>5 sem.>27 sem., difícil de explicar, pero se justifican por la masa diferente de sedimento contenida el los estratos heterogéneos. 50 Humedad (% ) 60 70 80 0 15 Profundidad (cm) Profundidad (cm) Mat. orgánica (% ) 11.5 12.1 12.7 13.3 0 30 45 60 15 30 45 60 (a) (b) 75 75 Figura 6: Evolución del contenido en materia orgánica (a) y de la humedad (b) T0 5sem. 23sem. 27sem. Si se consideran los volúmenes de agua presentes en las columnas de sedimento (Figura 7), se obtienen perfiles más lógicos de los que se observan en la figura 6b, donde el contenido en agua del sedimento presenta poca diferencia entre 23 y 27 semanas. Con los volúmenes de agua iniciales y finales en los sedimentos, se pueden calcular las siguientes velocidades de compactación para 23 y 27 semanas: 0.7 y 0.3 mm/d, respectivamente. Sin embargo, considerando los volúmenes de la columna entera de sedimento, la variación de volumen es diferente, lo que podría implicar que queda gas en los sedimentos. Además, el primer reactor presenta más agua y más volumen de sedimento al final del experimento, lo que significa que en una etapa intermedia, los poros nuevamente formados por la circulación del biogás se llenan de agua. Por fin, esta nueva presentación permite observar zonas de coincidencia entre los máximos y mínimos de los perfiles de humedad y los de materia orgánica. Humedad (mL) 60 120 180 0 Humedad (mL) 25 50 75 100 0 15 15 15 45 60 30 45 60 (a) 75 23 sem. 75 (b) Profundidad (cm) 0 30 Humedad (mL) 35 55 75 15 0 Profundidad (cm) Profundidad (cm) 0 27 sem. 30 45 60 75 (c) Figura 7: Evolución del contenido en agua del sedimento (a), acercamiento para 23 (b) y 27 (c) semanas. La línea continua = resultado final, línea quebrada = T0 5sem. 23sem. 27sem. Movimientos de los metales asociados al sedimento Los resultados se ilustran en las figuras 8 y 9. Las superficies representan el intervalo de concentración obtenido con triplicados (desviación experimental) para cada estrato. La línea vertical indica la concentración inicial de Cd en el sedimento (T0). Para el cadmio (Figura 8), se pueden observar movimientos amplios del metal a través de la columna de sedimento, que se caracterizan por una pérdida general del Cd en éste. El fenómeno de liberación parece más importante cuando los sedimentos son todavía jóvenes, mientras que después de 27 semanas, aparece un déficit menor, lo que indica un regreso parcial del metal al sedimento. Los perfiles describen la presencia de varias zonas de solubilización (con concentración menor a la concentración inicial), así como de asociación secundaria con el sedimento (con concentración mayor a la concentración inicial). En particular, la superficie parece ser zona de precipitación en un sedimento joven y de solubilización posteriormente, mientras que en el fondo se encuentran condiciones favorables a la solubilización. Se notó un movilización del Cd dentro de la columna con un desplazamiento hacia la superficie. [Cd] (mg/kg) 1 2 0 15 30 45 (a) 60 20 40 60 (b) 1 2 0 0 Profundidad (cm) Profundidad (cm) 0 0 2 Profundidad (cm) 0 [Cd] (mg/kg) [Cd] (m g/kg) 1 20 40 60 (c) 80 80 Figura 8: Cd a t = 5 sem. (a), t = 23 sem. (b), t = 27 sem. (c) [Fe] (g/kg) 35 45 25 15 30 45 (a) 60 25 45 [Fe] (g/kg) 35 45 0 0 Profundidad (cm) Profundidad (cm) 0 [Fe] (g/kg) 35 20 40 60 (b) 80 Profundidad (cm) 25 20 40 60 80 (c) Figura 9: Fe a t = 5 sem. (a), t = 23 sem. (b), t = 27 sem. (c) Para el hierro (Figura 9), los movimientos fueron poco amplios. La heterogeneidad del sedimento joven (5 sem.) permite suponer que el fenómeno de solubilización (reducción de los oxihidróxidos férricos a 2+ Fe disuelto) no es un comportamiento de carácter local, que ocurre en ocasiones diferentes en un mismo estrato. Con el tiempo, el comportamiento se generalizó, y se pudo notar en el fondo de la columna una disminución de las concentraciones del Fe asociado a los sedimentos, mientras que se observó lo contrario en la mitad superior del perfil. Al final del experimento, se observó una acumulación del metal, nuevamente en forma sólida, exactamente en la interfase agua/sedimento, que se había notado visualmente desde el décimo día, con la aparición de un color naranja. El hierro al ser un componente importante de la matriz de los sedimentos, su solubilización puede generar la liberación de los metales asociados con su fase (ya que comúnmente, se encuentra como oxihidróxido férrico, aún en los sedimentos reducidos). Esto se confirma con la semejanza que existe en la parte baja de los perfiles obtenidos para Fe y Cd, los dos metales presentaron una disminución en las concentraciones de la fase sólida. CONCLUSIONES Durante este experimento, la degradación microbiológica de la materia orgánica en los sedimentos de la presa J.A. Alzate, contaminados por descargas domésticas e industriales, se pudo dividir en tres grandes fases. La primera fase es una liberación precoz de biogás, que formó nuevos y grandes poros en las columnas de sedimento. Estos poros se llenaron parcialmente con agua y se colapsó rápidamente parte de los poros (fase 2). Después, se pudo observar el fenómeno de compactación, más lento, acompañado de una convección del agua (fase 3). Se notó una degradación de materia orgánica durante todo el experimento, con reasociaciones de las especies orgánicas disueltas con los sedimentos, con movimientos de difusión hacia la superficie. La degradación microbiológica de la materia orgánica tiene un efecto notable sobre los movimientos de los metales asociados a la fase sólida. Para Cd y Fe, el comportamiento general parece ser una asociación secundaria en la zona superior de la columna de sedimentos, con una posibilidad tanto de redisolución del metal como el de volverse a asociar aún más arriba, dando la impresión de ascenso de un “frente metálico”. Sin embargo, el hierro queda asociado a la capa superficial del sedimento, mientras que el cadmio parece mantenerse en gran parte en la fase disuelta y pasa a la columna de agua. BIBLIOGRAFÍA Avila P., Balcázar G., Zarazúa G., Barceló I., Díaz C. (1999) Heavy metal concentrations in water and bottom sediments of a Mexican reservoir, The Science of the Total Environment, vol 234, 185-196. Barceló I.D. (2000) Estudio de la movilidad de Ca, Cd, Fe, Mn, Pb y Zn en sedimentos de la presa J.A. Alzate en el Estado de México, tesis de doctorado en Ingeniería en Ciencias del Agua, CIRA, Facultad de Ingeniería, Universidad Autónoma del Estado de México. 210 210 Benoit G. and Hemond H.F. (1990) Po and Pb remobilization from lake sediments in relation to iron and manganese cycling, Environmental Science and Technology, vol. 24, 1224-1234. Bussy A.L., Barceló I.D. y Solís H.E. (2004) Transporte de Fe, Cd y Zn en los sedimentos del río Lerma: influencia de la presa J.A. Alzate, Edo. de México, Memorias Técnicas del XVI Congreso Nacional de Ingeniería Sanitaria y Ciencias Ambientales FEMISCA A.C., 12-14 de mayo, Mazatlán Sin., CD-Rom. CNA, Comisión Nacional del Agua (1990) Plan para la recuperación de la cuenca del alta del Río Lerma, México, Reporte de la Comisión Estadal para la Recuperación de la Cuenca del Alta del Río Lerma, Secretaría de Recursos Hidráulicos. CNA, Comisión Nacional del Agua del Edo. de México (1998) Inventario de descargas de aguas residuales en el Estado de México, Departamento de Saneamiento y Calidad del Agua. Jones J.G. (1982) Activities of aerobic and anaerobic bacteria in lake sediments and their effect on the water column, en Sediment Microbiology, Nedwell D.B. & Brown C.M. Editores., Academic Press, 107-145. Peña M.V., Orozco H.M., Olivera M.C., Franco P.R., Castaños M.C., Infante S.J. y Gutierriez C.J. (2000) Atlas ecológico de la cuenca hidrográfica del río Lerma, Comité Editorial del Estado de México, Tomo 5. Reeburgh W.S. (1983). Rates of biogeochemical processes in anoxic sediments, Ann. Rev. Earth Planet. Sci., vol. 11, 269-298. Tebo B.M., Nealson K.H., Emerson S. and Jacobs L. (1984) Microbial mediation of Mn(II) et Co(II) precipitation at the O2/H2S interfaces in two anoxic fjords, Limnology & Oceanography, vol 29, 1247-1258.