estructura tridimensional de las proteinas
Anuncio

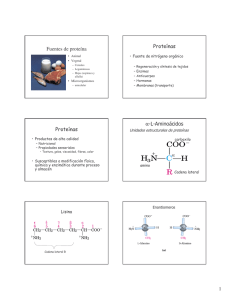
PROTEINAS COMPOSICIÓN ESTRUCTURA CLASIFICACIÓN AMINOÁCIDOS NO POLARES POLARES S/CARGA POLARES C/CARGA áá ESENCIAL PROPIEDADES ENLACE PEPTÍDICO PÉPTIDOS ESTRUCTURA ESTRUCTURA 1ª ESTRUCTURA 2ª Secuencia de áá Alfa-hélice Beta-laminar Estructura supersecundaria Dominio estructural ESTRUCTURA 3ª Fibrosa Globular ESTRUCTURA 4ª Protómero PROPIEDADES SOLUBILIDAD DESNATURALIZACIÓN ESPECIFICIDAD CAPACIDAD TAMPON OPTICAS ACIDO-BASE (Anfóteras) SOLUBILIDAD PUNTO DE FUSIÓN CLASIFICACION DE LAS PROTEINAS HOLOPROTEÍNAS: FIBROSAS Insolubles en agua INTERMEDIAS Estructura fibrosa pero son solubles GLOBULARES Son solubles HETEROPROTEÍNAS: CROMOPROTEÍNAS Metal porfirina GLUCOPROTEÍNAS Glúcido FOSFOPROTEÍNAS Su hidrólisis solo proporciona áá COLÁGENO ELASTINA QUERATINA ACTINA MIOSINA FIBRINÓGENO ALBÚMINAS GLOBULINAS HISTONAS Su hidrólisis proporciona áá y otros compuestos No proteicos HEMOGLOBINA MIOGLOBINA HEMOCIANINA CITOCROMOS INMUNOGLOBULINAS MUCOPROTEINAS PEPTIDOGLICANOS DE MEMBRANA CASEINÓGENO Ac. Fosofórico LIPOPROTEÍNAS Lipidos NUCLEOPROTEINAS Ac. Nucleicos QUILOMICRONES VLDL LDL HDL CROMOSOMAS (con ADN) RIBOSOMAS (con ARN) ESTRUCTURA TRIDIMENSIONAL DE LAS PROTEINAS1 La estructura tridimensional de las proteínas viene determinada por su secuencia de áá. La función de una proteína depende de su estructura tridimensional La estructura tridimensional de una proteína es única Las fuerzas más importantes que estabilizan la estructura tridimensional son interacciones no covalentes. La relación existente entre la secuencia de áá y la estructura de la proteína constituye aún una incógnita en algunos casos. Hay secuencias d áá muy diferentes que adoptan estructura similares, mientras que secuencias parecidas dan a veces estructuras diferentes. La disposición espacial de los átomos de una proteína se denomina conformación. El término conformación se refiere a un estado estructural que puede interconvertirse con otros estados estructurales sin romper enlaces covalentes. Un cambio de conformación puede ser el resultado de la rotación de los enlaces sencillos. De entre las innumerables conformaciones posibles, siempre hay una que predomina, es la más estable. Esquemáticamente se puede considerar que hay cuatro niveles estructurales: Estructura primaria: incluye la secuencia de áá unidos por enlaces covalentes (peptídicos) Estructura secundaria: corresponde a interacciones entre áá adyacentes. A menudo proteínas de tamaño grande tienen varios tipos de estructura secundaria Estructura terciaria: corresponde a las interacciones de todos los áá No siempre esta clara la frontera entre la secundaria y la terciaria. Estructura cuaternaria implica relación entre varias cadenas polipeptídicas. Los continuos avances en el estudio de las proteínas han hecho necesaria la definición de dos niveles estructurales adicionales a medio camino entre la estructura secundaria y la terciaria La estructura supersecundaria son estructuras estables que se observan en muchas proteínas e incluso se repiten varias veces en una misma proteína. El dominio son regiones mas compactas con funciones específicas. Enlaces que estabilizan las conformaciones: Covalentes: Puentes disulfuro No covalentes: Interacciones hidrófobas, fuerzas de van der Waals, puentes de hidrógeno, interacciones iónicas. A pesar de ser los enlaces covalentes mucho más fuertes son las interacciones débiles las que tienen más importancia como fuerza estabilizadora de la estructura de las proteínas gracias al gran nº en que se encuentra presentes. La conformación de la proteína es más estable cuando tiene mayor número de enlaces débiles. La mayor parte de las estructuras obedecen a dos reglas: 1. los restos hidrófobos deben encontrarse enterrados en el interior de la proteína, lejos del contacto del agua 2. Debe formarse el mayor nº de puentes de hidrógeno Las proteínas insolubles y aquellas que se localizan en la membrana siguen reglas diferentes a causa de la función que realizan y del entorno en que se encuentran. ESTRUCTURA SECUNDARIA Al considerar la estructura secundaria resulta de utilidad clasificar las proteínas en dos grupos principales: fibrosas cuyas cadenas se ordenan formando largos filamentos y globulares cuyas cadenas se pliegan de forma globular o esférica. Las fibrosas llevan a cabo importantes funciones estructurales y suelen estar formadas por un solo tipo de estructura secundaria. La mayor parte de los enzimas y hormonas son proteínas globulares son más complejas estructuralmente y suelen contener varios tipos de estructura secundaria. 1 Principios de Bioquímica.Lehninger. Nelson. Cox. Ed. Omega 2ª Edición. Barcelona 1995 Hélice alfa. El esqueleto se encuentra enrollado alrededor de un eje. Cada 3,6 áá se da una vuelta. Los restos quedan hacia fuera. Dextrógira. Está estabilizada por puentes de Hidrógeno cada 4 áá. Es la estructura predominante de las alfa queratinas. Las globulares tienen una cuarta parte en esta estructura. No todos los polipéptidos pueden formar una hélice alfa estable. Las interacciones de las cadenas laterales de los áá pueden estabilizar o desestabilizar, depende del tamaño y la carga. La presencia de PROLINA es incompatible Beta laminar beta queratinas Existen otras estructuras secundarias, pero están presentes en pocas proteínas e incluso en una sola como la hélice de colágeno: hélice levógira de tres residuos por vuelta. Se asocia con dos cadenas mas de forma dextrógira. Las alfa queratinas y el colágeno son ejemplos claros de la relación entre estructura y función en proteínas ESTRUCTURA TERCIARIA áá que están alejados y que pueden encontrarse en estructuras 2ª diferentes, pueden interaccionar entre sí cuando la proteína está plegada. La formación de giros en la cadena durante el plegamiento, la dirección y el ángulo de estos giros están determinados por el nº y localización de áá específicos, PRO. GLY entre otros. La GLY proporciona mucha flexibilidad estructural al tener en el carbono alfa dos hidrógenos. Una manera de demostrar la relación entre estructura y función consiste en alterar la estructura y comprobar que se altera la función. Cuando la desnaturalización es extrema se llama desnaturalización. Las estructuras 3ª no son rígidas sino que presentan cambios conformacionales de pequeño alcance o también estos cambios se producen durante su actividad biológica, en este caso los cambios están asociados a ligandos específicos o incluso a los propios sustratos. Caso de la Hb El plegamiento se va produciendo de una forma espontánea a medida que tiene lugar la síntesis o ayudados por proteínas colaboradoras o fijadoras de la cadena polipeptídica. ESTRUCTURA CUATERNARIA Asociación de varias cadenas. Las interacciones no covalentes también van a estabilizar este nivel estructural. Son proteínas de función reguladora. Subunidades diferentes pueden realizar funciones diferentes aunque relacionadas. Rutas metabólicas enteras se organizan mediante la asociación de enzimas en complejos supramoleculares que aumentan la eficacia de los procesos. Otros tienen función estructural P.Ej. las cápsides de los virus o las histonas del nucleosoma, o el propio ribosoma. Los cambios conformacionales de la Hb alteran su capacidad de unirse al Ox. La Hb capta oxigeno en pulmón y lo cede en los tejidos…. FUNCIONES DE LAS PROTEINAS PROTEÍNAS DE MEMBRANA Recepción de señales químicas y transporte activo de sustancias PROTEÍNAS TUBULARES COLAGENO ELASTINA QUERATINA Citoesqueleto INSULINA, GLUCAGÓN, ADRENALINA HORMONAS DE LA HIPÓFISIS Control del metabolismo de los glúcidos GLOBULINAS Anticuerpos HEMOGLOBINA MIOGLOBINA CITOCROMOS ALBÚMINAS LIPOPROTEINAS Transporte de oxígeno en la sangre ENZIMAS Acción Biocatalizadora Tej. Conjuntivo y óseo Vasos sanguíneos (arterias) Pelo, uñas Control glandular Transporte de oxígeno en el músculo Transporte de electrones transporte de lípidos y reserva de áá transporte de lípidos Mantienen el equilibrio osmótico, el ph y la temperatura HISTONAS Control de la expresión del ADN FIBRINÓGENO Factor de coagulación sanguínea ACTINA Y MIOSINA Responsables de los procesos de movimiento