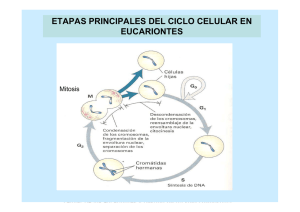
Regulación del ciclo celular
Anuncio

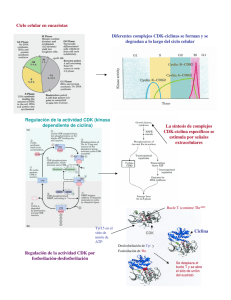
Regulación del ciclo celular Esquema global de los elementos más relevantes implicados en la regulación del ciclo celular. La regulación del ciclo celular, explicada en el año 2001 en organismos eucariotas,5 puede contemplarse desde la perspectiva de la toma de decisiones en puntos críticos, especialmente en la mitosis.6 De este modo, se plantean algunas preguntas:1 • ¿Cómo se replica el ADN una única vez? Una pregunta interesante es cómo se mantiene la euploidía celular. Sucede que, en la fase G1, la Cdk(ciclina) promueve la adición al complejo de reconocimiento del origen de replicación del ADN de unos reguladores llamados Cdc6, los cuales reclutan a Mcm, formando un complejo prerreplicativo del ADN, que recluta a la maquinaria de replicación genética. Una vez que se inicia la fase S, la Cdk-S produce la disociación de Cdc6 y su posterior proteólisis, así como la exportación al citosol de Mcm, con lo que el origen de replicación no puede, hasta el ciclo siguiente, reclutar un complejo prerreplicativo (las degradaciones proteolíticas siempren conllevan irreversibilidad, hasta que el ciclo gire). Durante G2 y M se mantiene la unicidad de la estructura de prerreplicación, hasta que, tras la mitosis, el nivel de actividad Cdk caiga y se permita la adición de Cdc6 y Mdm para el ciclo siguiente. • ¿Cómo se entra en mitosis? La ciclina B, típica en la Cdk-M, existe en todo el ciclo celular. Sucede que la Cdk(ciclina) está habitualmente inhibida por fosforilación mediante la proteína Wee, pero, a finales de G2, se activa una fosfatasa llamada Cdc25 que elimina el fosfato inhibidor y permite el aumento de su actividad. Cdk-M inhibe a Wee y activa a Cdc25, lo que produce una retroalimentación positiva que permite la acumulación de Cdk-M. • ¿Cómo se separan las cromátidas hermanas? Ya en mitosis, tras la formación del huso acromático y superación del punto de restricción de unión a cinetocoros, las cromátidas han de eliminar su esqueleto de cohesinas, que las unen. Para ello, Cdk-M favorece la activación de APC, una ligasa de ubiquitina, por unión a Cdc20. Esta APC ubiquitiniza y favorece la ulterior degradación en el proteasoma de la segurina, inhibidor del enzima separasa que debe escindir las cohesinas. Metafase tardía: placa metafásica previa a la separación de las cromátidas. • ¿Cómo se sale de mitosis? Una vez que los niveles de Cdk-M son altos, parece difícil detener la dinámica de mitosis y entrar en citocinesis: pues bien, esto ocurre porque la APC activada por la Cdk-M, y tras un lapso cuyo mecanismo de control es aún desconocido, ubiquitiniza a la ciclina B, produciendo el cese absoluto de actividad Cdk-M. • ¿Como se mantiene el estado G1? En la fase G1, la actividad Cdk está muy disminuida porque: APC-Hct1 (Cdc20 sólo actúa en mitosis) elimina toda ciclina B; se acumulan inhibidores de Cdk; la transcripción de ciclinas se ve disminuida. Para escapar de este reposo, se deben acumular ciclinas de G1. Esto se controla mediante factores de proliferación celular, señales externas. Los mecanismos moleculares de activación de transcripción de genes de las fases S y G2 necesarios para proseguir el ciclo son apasionantes: éstos genes están regulados por la proteína reguladora E2F, la cual se une a promotores de ciclinas G1/S y S. E2F está controlada por la proteína del retinoblastoma (Rb), la cual, en ausencia de factores tróficos, inhibe la actividad promotora de la transcripción de E2F. Cuando existen señales de proliferación, Cdk-G1 fosforila Rb, que pierde afinidad por E2F, se disocia de éste y permite que se expresen los genes de la fase S. Además, como E2F acelera la transcripción de su propio gen, las Cdk-S y G1/S fosforilan también a Rb y a Hct1 (activador de APC, que degradaría estas ciclinas), se produce una retroalimentación positiva. Componentes reguladores El ciclo celular es controlado por un sistema que vigila cada paso realizado. En regiones concretas del ciclo, la célula comprueba que se cumplan las condiciones para pasar a la etapa siguiente: de este modo, si no se cumplen estas condiciones, el ciclo se detiene.1 Existen cuatro transiciones principales: • • • • Paso de G0 a G1: comienzo de la proliferación. Transición de G1 a S: iniciación de la replicación. Paso de G2 a M: iniciación de la mitosis. Avance de metafase a anafase Los genes que regulan el ciclo celular se dividen en tres grandes grupos:7 1. Genes que codifican proteínas para el ciclo: enzimas y precursores de la síntesis de ADN, enzimas para la síntesis y ensamblaje de tubulina, etc. 2. Genes que codifican proteínas que regulan positivamente el ciclo: también llamados protooncogenes.8 Las proteínas que codifican activan la proliferación celular, para que células quiescentes pasen a la fase S y entren en división. Algunos de estos genes codifican las proteínas del sistema de ciclinas y quinasas dependientes de ciclina. Pueden ser: o Genes de respuesta temprana, inducidos a los 15 minutos del tratamiento con factores de crecimiento, sin necesidad de síntesis proteica; o Genes de respuesta tardía, inducidos más de una hora después del tratamiento con factores de crecimiento, su inducción parece estar causada por las proteínas producidas por los genes de respuesta temprana. 3. Genes que codifican proteínas que regulan negativamente el ciclo:También llamados genes supresores tumorales. Las ciclinas y las quinasas dependientes de ciclina (CDK), son sintetizadas a partir de protooncogenes y trabajan en cooperación para regular el ciclo positivamente. Fosforilan serinas y treoninas de proteínas diana para desencadenar procesos celulares. Los protooncogenes son genes cuya presencia o activación a oncogenes pueden estimular el desarrollo de cancer. cuando se activan exageradamente en las celulas normales provocan que ellas pierdan el control de la division y se mantengan proliferando sin control. Expresión diferencial de ciclinas en las distintas fases del ciclo. Las ciclinas son un grupo heterogéneo de proteínas con una masa de 36 a 87 kDa. Se distinguen según el momento del ciclo en el que actúan.1 Las ciclinas son proteínas de vida muy corta: tras disociarse de sus kinasas asociadas, se degradan con extrema rapidez. Las kinasas dependientes de ciclinas (CDK por sus siglas en inglés) son moléculas de mediano peso molecular que presentan una estructura proteica característica, consistente en dos lóbulos entre los cuales está el centro catalítico, donde se inserta el ATP (que será el donador de grupos fosfato.9 En el canal de entrada al centro catalítico existe una treonina que debe estar fosforilada para que la quinasa actúe. No obstante, en el propio centro hay dos treoninas que, al ser fosforiladas, inhiben a la quinasa y una región de unión a la ciclina llamada PSTAIRE.4 Existe una tercera región en las CDK, alejada del centro catalítico, a la que se une la proteína CKS, que regula la actividad kinasa de la CDK. Relación del algunas ciclinas de vertebrados y levaduras1 Vertebrados Levaduras Complejo Cdk/ciclina Ciclina Cdk asociada Ciclina Cdk asociada Cdk-G1 ciclina D Cdk 4,6 Cln3 Cdk1 Cdk-G1/S ciclina E Cdk2 Cln1,2 Cdk1 Cdk-S ciclina A Cdk2 Clb5,6 Cdk1 Cdk-M ciclina B Cdk1 Clb1,2,3,4 Cdk1 Regulación de los complejos ciclina/CDK Existen multitud de proteínas que modulan la actividad del complejo ciclina/CDK.4 Como vías de activación, se conoce que el complejo ciclina A/CDK2 activa la proteína CAK, quinasa activadora de CDK, y la proteína CAK fosforila a la CDK, activándola. En cambio, la fosfatasa PP2a desfosforila a la CDK, inactivándola. A su vez, hay descritos complejos inhibidores CKI como la p27 y p21 que se unen a la ciclina y a la CDK al mismo tiempo bloqueando el sitio activo. Las enzimas ligasas de ubiquitina conducen a la ubiquitinación de las ciclinas, lo que las marca para su degradación en el proteasoma y, por tanto, destruye la funcionalidad del complejo con la CDK. Una enzima ligasa de ubiquitina implicada en este proceso de regulación del ciclo celular es el complejo SCF, que actúa sobre las ciclinas G1/S. Otro complejo denominado APC (del inglés anaphase promoting complex) actúa sobre ciclinas M.1 • Ciclinas G1 y G1/S: Durante G1,la proteína Rb (retinoblastoma) está unida a la proteína E2F, que a su vez está unida al ADN promotor de genes necesarios para la entrada en S. Al acumularse ciclinas de G1, los complejos ciclina G1/CDK fosforilan a Rb, que se inactiva y deja de inactivar a E2F. La actividad de E2F permite la transcripción de genes para la fase S. Se forman entonces complejos ciclina G1S/CDK y ciclina S/CDK, que inactivan más unidades de Rb, favoreciendo todavía más la actividad de E2F. • Ciclinas S: El complejo ciclina S/CDK promueve la actividad de la ADN polimerasa y de otras proteínas de la replicación. EL complejo multiproteico ORC (del inglés origin recognition complex) está asociado al origen de replicación del ADN. En G1 forma el complejo prerreplicativo al asociarse a la proteína CDC6 y al anillo proteico MCM. Las MCM actúan como helicasas promoviendo la replicación. El complejo ciclina S/CDK también fosforila la CDC6, dejándola accesible para la ubiquitinación por SCF. Así evita una nueva replicación. • Ciclinas M: El complejo ciclina M/CDK activado por CAK está presente en todo el ciclo, pero está inhibido por la quinasa WEE1, que la fosforila. Al final de G2 la fosfatasa CDC25 desfosforila la CDK y activa el complejo ciclina M/CDK.El complejo ciclina M/CDK fosforila varias proteínas durante la mitosis: o proteína lámina nuclear al final de la profase para desestructurar la envoltura nuclear o proteína condensina que condensa los cromosomas o proteínas reguladoras del huso mitótico o complejo APC que separa las cromátidas hermanas El complejo CDC20/APC ubiquitina las ciclinas M para salir de la fase M. • Genes supresores de tumores: Los genes supresores de tumores regulan negativamente el ciclo. Se encargan de que la mitosis no continúe si se ha producido una alteración del proceso normal. Entre estos genes, también llamados 'de verificación', se encuentran los que codifican: o productos que evitan mutaciones de genes reguladores del ciclo o proteínas que inactivan las CDK por fosforilación/desfosforilación (ej. quinasa WEE1, fosfatasa CDC25) 10 o proteínas CKI inhibidoras del ciclo (por ejemplo, p53, p21, p16) o proteína Rb (proteína del retinoblastoma), cuya alteración génica recesiva causa el cáncer de retina con ese nombre. o proteínas que inducen la salida del ciclo hacia un estado celular diferenciado o hacia apoptosis (ej. Bad, Bax, Bak, receptor de ligando de Fas) La verificación se lleva a cabo en los puntos de control y asegura la fidelidad de la replicación y segregación del genoma. Algunos componentes, además de detectar fallos, pueden poner en marcha la reparación. El proceso de síntesis y ensamblaje de ciclinas/CDK está regulado por tres tipos de factores: mitógenos, que estimulan la división celular; factores de crecimiento (GFs), que producen un aumento de tamaño al estimular la síntesis proteica; y factores de supervivencia, que suprimen la apoptosis. Puntos de control Existen unos puntos de control en el ciclo que aseguran la progresión sin fallos de éste, evaluando el correcto avance de procesos críticos en el ciclo, como son la replicación del ADN o la segregación de cromosomas.11 Estas rutas de verificación presentan dos características, y es que son transitorias (desaparecen una vez resuelto el problema que las puso en marcha) y que pueden caducar si el problema no es resuelto al cabo de un tiempo. Dichos puntos de control son:1 • • • Punto de control de ADN no replicado, en la entrada de fase M. Actúa inhibiendo a Cdc25, el cual es un activador de la Ciclina A/B Cdk1. Punto de control de ensamblaje del huso (checkpoint de mitosis), antes de la anafase. Se activa una proteína Mad2 que impide la degradación de la segurina, lo que impide la segregación de las cromátidas hermanas hasta que todas se hayan unido al huso. Es pues el punto de control de la separación de cromosomas, al final de la mitosis. En caso de que fuera incorrecto, se impediría la degradación de la ciclina B por parte de APC. Punto de control del daño del ADN, en G1, S o G2. El daño celular activa a p53, proteína que favorece la reparación el ADN, detiene el ciclo promoviendo la transcripción de p21, inhibidor de Cdk, y, en el caso de que todo falle, estimula la apoptosis.10 Ciclo celular y cáncer Cuando las células normales se lesionan o envejecen, mueren por apoptosis, pero las células cancerosas la evitan. Se cree que muchos tumores son el resultado de una multitud de pasos, de los que una alteración mutagénica no reparada del ADN podría ser el primer paso. Las alteraciones resultantes hacen que las células inicien un proceso de proliferación descontrolada e invadan tejidos normales. El desarrollo de un tumor maligno requiere de muchas transformaciones genéticas. La alteración genética progresa, reduciendo cada vez más la capacidad de respuesta de las células al mecanismo normal regulador del ciclo.8 Los genes que participan de la carcinogénesis resultan de la transformación de los genes normalmente implicados en el control del ciclo celular, la reparación de daños en el ADN y la adherencia entre células vecinas. Para que la célula se transforme en neoplásica se requieren, al menos, 2 mutaciones: una en un gen supresor de tumores y otra en un protooncogén, que dé lugar, entonces, a un oncogén. Bibliografía • • Lodish et al. (2005). Biología celular y molecular. Buenos Aires: Médica Panamericana. ISBN 950-06-1974-3. Alberts et al (2004). Biología molecular de la célula. Barcelona: Omega. ISBN 54-282-1351-8. Citas 1. ↑ a b c d e f g h Lodish et al. (2005). Biología celular y molecular. Buenos Aires: Médica Panamericana. ISBN 950-06-1974-3. 2. ↑ Tavassoli (1980). The cell theory: a foundation to the edifice of biology. American Journal of Patholology January; 98(1): 44..[1] 3. ↑ Paniagua, R.; Nistal, M.; Sesma, P.; Álvarez-Uría, M.; Fraile, B.; Anadón, R. y José Sáez, F. (2002). Citología e histología vegetal y animal. McGraw-Hill Interamericana de España, S.A.U.. ISBN 84-486-0436-9. 4. ↑ a b c Alberts et al (2004). Biología molecular de la célula. Barcelona: Omega. ISBN 54-282-1351-8. 5. ↑ Nobelprize.org: search ”Hunt” 6. ↑ L. H. Hartwell Twenty-Five Years of Cell Cycle Genetics Genetics, 1991 7. ↑ Graña X, Reddy EP. Cell cycle control in mammalian cells: role of cyclins, cyclin dependent kinases (CDKs), growth suppressor genes and cyclindependent kinase inhibitors (CKIs). Oncogene. 1995 Jul 20;11(2):211-9. 8. ↑ a b Bartek, J.; Lukas, J.; Bartkova, J. (1999), "Perspective: Defects in cell cycle control and cancer", Journal of pathology 187 (1): 95–99, doi:10.1002/(SICI)1096-9896(199901)187:1<95::AID-PATH249>3.0.CO;2-#, http://cat.inist.fr/?aModele=afficheN 9. ↑ Mathews, C. K.; Van Holde, K.E et Ahern, K.G (2003). «6», Bioquímica, 3 edición, pp. 204 y ss. ISBN 84-7892-053-2. 10. ↑ a b Soussi, T.; Legros, Y.; Lubin, R.; Ory, K.; Schlichtholz, B. (1994), "Multifactorial analysis of p53 alteration in human cancer: a review", Int J Cancer 57 (1): 1–9, doi:10.1002/ijc.2910570102, http://www.ncbi.nlm.nih.gov/pubmed/8150526 11. ↑ Stephen J. Elledge Cell Cycle Checkpoints: Preventing an Identity Crisis Science 6 December 1996: Vol. 274. no. 5293, pp. 1664 - 1672; DOI: 10.1126/science.274.5293.1664 12. ↑ M, Bruno; Sheen, Jen (2008), "Cytokinin and auxin interaction in root stemcell specification during early embryogenesis", Nature 453 (7198): 1094, doi:10.1038/nature06943, http://www.nature.com/nature/journal/vaop/ncurrent/full/nature06943.html 13. ↑ Dinneny, J.R.; Benfey, P.N. (2008), "Plant Stem Cell Niches: Standing the Test of Time", Cell 132 (4): 553–557, doi:10.1016/j.cell.2008.02.001, http://linkinghub.elsevier.com/retrieve/pii/S0092867408002006 14. ↑ Simillion, Cedric; Vandepoele, Klaas; Van Montagu, Marc C. E.; Zabeau, Marc; Van De Peer, Yves (2002), "The hidden duplication past of Arabidopsisthaliana" (w), Proceedings of the National Academy of Sciences of the United States of America 99 (21): 13627, doi:10.1073/pnas.212522399, PMID 12374856, http://www.pnas.org/cgi/content/full/pnas;99/21/13627 15. ↑ Stals, H.; Inzé, D. (2001), "When plant cells decide to divide" (w), Trends in Plant Science 6 (8): 359–364, doi:10.1016/S1360-1385(01)02016-7, http://www2.unil.ch/lpc/images/docu04/gene/celldivision.pdf 16. ↑ Criqui, M.C.; Parmentier, Y.; Derevier, A.; Shen, W.H.; Dong, A.; Genschik, P. (2000), "Cell cycle-dependent proteolysis and ectopic overexpression of cyclin B1 in tobacco BY2 cells", The Plant Journal 24 (6): 763–773, doi:10.1111/j.1365-313X.2000.t01-1-.x 17. ↑ Khadaroo, B.; Robbens, S.; Ferraz, C.; Derelle, E.; Eychenie, S.; Cooke, R.; Peaucellier, G.; Delseny, M.; et al. (2004), "The first green lineage cdc25 dualspecificity phosphatase" (w), Cell Cycle 3 (4): 513–8, http://www.ncbi.nlm.nih.gov/pubmed/15004533 18. ↑ De Veylder, L.; Beeckman, T.; Beemster, G.T.S.; Krols, L.; Terras, F.; Landrieu, I.; Van Der Schueren, E.; Maes, S.; et al. (2001), "Functional Analysis of Cyclin-Dependent Kinase Inhibitors of Arabidopsis", The Plant Cell 13 (7): 1653, http://plancellalainsun.freetcp.com/cgi/content/full/13/7/1653 19. ↑ Heisler, M.G.; Ohno, C.; Das, P.; Sieber, P.; Reddy, G.V.; Long, J.A.; Meyerowitz, E.M. (2005), "Patterns of Auxin Transport and Gene Expression during Primordium Development Revealed by Live …", Current Biology 15 (21): 1899–1911, doi:10.1016/j.cub.2005.09.052, http://plantlab.caltech.edu/publications/Heisler2005CurrBiol.pdf 20. ↑ Umen, J.G.; Goodenough, U.W. (2001), "Control of cell division by a retinoblastoma protein homolog in Chlamydomonas" (w), Genes & Development 15 (13): 1652–1661, doi:10.1101/gad.892101, http://www.genesdev.org/cgi/content/abstract/15/13/1652 21. ↑ Dewitte, Walter; Scofield, Simon; Alcasabas, Annette A.; Maughan, Spencer C.; Menges, Margit; Braun, Nils; Collins, Carl; Nieuwland, Jeroen; et al. (2007), "Arabidopsis CYCD3 D-type cyclins link cell proliferation and endocycles and are rate-limiting for cytokinin responses" (w), Proceedings of the National Academy of Sciences 104 (36): 14537, doi:10.1073/pnas.0704166104, PMID 17726100, http://www.pnas.org/cgi/content/full/104/36/14537 22. ↑ Leiva-neto, J.T.; Grafi, G.; Sabelli, P.A.; Dante, R.A.; Woo, Y.; Maddock, S.; Gordon-kamm, W.J.; Larkins, B.A. (2004), "A Dominant Negative Mutant of Cyclin-Dependent Kinase a Reduces Endoreduplication but Not Cell Size …", The Plant Cell 16 (7): 1854, http://plancellalainsun.freetcp.com/cgi/content/full/16/7/1854 Obtenido de "http://es.wikipedia.org/wiki/Ciclo_celular" Categorías: Wikipedia:Artículos buenos | Fisiología celular | Ciclo celular


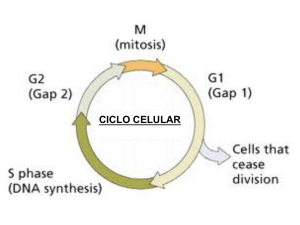
![Fases del ciclo celular [editar]](http://s2.studylib.es/store/data/000868083_1-52ef23802007c746803ce4391df6cab8-300x300.png)