Tratamiento clínico para la muerte fetal temprana (menos de 24
Anuncio

Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
(Revisión)
Neilson JP, Hickey M, Vazquez J
Reproducción de una revisión Cochrane, publicada en The Cochrane Library Número 4, 2007, y traducida.
http://www.thecochranelibrary.com
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
1
TA B L A D E C O N T E N I D O S
RESUMEN. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
RESUMEN EN LENGUAJE SENCILLO. . . . . . . . . . . . . . . . . . .
ANTECEDENTES. . . . . . . . . . . . . . . . . . . . . . . . . . . .
OBJETIVOS. . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
CRITERIOS PARA LA VALORACIÓN DE LOS ESTUDIOS DE ESTA REVISIÓN.
MÉTODOS DE BÚSQUEDA PARA LA IDENTIFICACIÓN DE LOS ESTUDIOS. .
MÉTODOS DE LA REVISIÓN. . . . . . . . . . . . . . . . . . . . . . .
DESCRIPCIÓN DE LOS ESTUDIOS. . . . . . . . . . . . . . . . . . . .
CALIDAD METODOLÓGICA. . . . . . . . . . . . . . . . . . . . . . .
RESULTADOS. . . . . . . . . . . . . . . . . . . . . . . . . . . . .
DISCUSIÓN. . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
IMPLICACIONES DE LOS AUTORES. . . . . . . . . . . . . . . . . . .
POTENCIAL CONFLICTO DE INTERESES. . . . . . . . . . . . . . . . .
AGRADECIMIENTOS. . . . . . . . . . . . . . . . . . . . . . . . . .
FUENTES DE FINANCIACIÓN. . . . . . . . . . . . . . . . . . . . . .
REFERENCIAS. . . . . . . . . . . . . . . . . . . . . . . . . . . . .
TABLAS. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . .
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
5
6
6
6
6
7
7
7
8
8
8
8
9
9
9
9
. . . . . . . . . . . . . . . . . . . . . 18
Características de los estudios incluidos. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 18
Características de los estudios excluidos. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 24
Características de los estudios en curso. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 26
ANÁLISIS. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 27
Comparison 01 Misoprostol vaginal versus placebo. . . . . . . . . . . . . . . . . . . . . .
Comparison 02 Misoprostol vaginal versus evacuación quirúrgica del útero. . . . . . . . . . . . .
Comparison 03 Misoprostol vaginal versus gemeprost vaginal. . . . . . . . . . . . . . . . . .
Comparison 04 Misoprostol vaginal versus prostaglandina E1/2 vaginal. . . . . . . . . . . . . .
Comparison 05 Esquemas de tratamiento con misoprostol vaginal en dosis más bajas versus dosis más altas.
Comparison 06 Preparación húmeda versus seca de misoprostol vaginal. . . . . . . . . . . . . .
Comparison 07 Misoprostol vaginal + metotrexato versus misoprostol vaginal solo. . . . . . . . . .
Comparison 08 Misoprostol vaginal más tapones de laminaria versus misoprostol vaginal solo. . . . . .
Comparison 09 Misoprostol oral versus misoprostol vaginal. . . . . . . . . . . . . . . . . .
Comparison 10 Misoprostol oral + mifepristona versus conducta expectante. . . . . . . . . . . .
Comparison 11 Misoprostol sublingual versus misoprostol vaginal. . . . . . . . . . . . . . . .
Comparison 12 Mifepristona versus placebo. . . . . . . . . . . . . . . . . . . . . . . .
Comparison 13 Gemeprost vaginal versus evacuación quirúrgica del útero. . . . . . . . . . . . .
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
27
28
28
28
28
29
29
29
29
30
30
30
30
INDICE DE TÉRMINOS. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 31
CARÁTULA. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 31
GRÁFICOS Y OTRAS TABLAS. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 33
Análisis 01.01 Comparación 01 Misoprostol vaginal versus placebo, Resultado 01 Aborto espontáneo completo < 24 horas después del tratamiento. 33
Análisis 01.02 Comparación 01 Misoprostol vaginal versus placebo, Resultado 02 Aborto espontáneo completo < 48 horas. . . . . . . . . . 33
Análisis 01.03 Comparación 01 Misoprostol vaginal versus placebo, Resultado 03 Aborto espontáneo sin evacuación de los restos ovulares retenidos el
día 7. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 33
Análisis 01.04 Comparación 01 Misoprostol vaginal versus placebo, Resultado 04 Legrado uterino. . . . . . . . . . . . . . . . . . . 34
Análisis 01.05 Comparación 01 Misoprostol vaginal versus placebo, Resultado 05 Opiáceos para el alivio del dolor. . . . . . . . . . . . . 34
Análisis 01.06 Comparación 01 Misoprostol vaginal versus placebo, Resultado 06 Transfusión de sangre. . . . . . . . . . . . . . . . . 34
Análisis 01.07 Comparación 01 Misoprostol vaginal versus placebo, Resultado 07 Diferencia en la hemoglobina > 10 g/l. . . . . . . . . . . 34
Análisis 01.08 Comparación 01 Misoprostol vaginal versus placebo, Resultado 08 Náuseas. . . . . . . . . . . . . . . . . . . . . . 35
Análisis 01.09 Comparación 01 Misoprostol vaginal versus placebo, Resultado 09 Diarrea. . . . . . . . . . . . . . . . . . . . . . 35
Análisis 01.10 Comparación 01 Misoprostol vaginal versus placebo, Resultado 10 Fiebre. . . . . . . . . . . . . . . . . . . . . . 35
Análisis 01.11 Comparación 01 Misoprostol vaginal versus placebo, Resultado 11 Perforación uterina. . . . . . . . . . . . . . . . . . 35
Análisis 01.12 Comparación 01 Misoprostol vaginal versus placebo, Resultado 12 Hemorragia vaginal 2 semanas después del tratamiento. . . . 36
Análisis 01.13 Comparación 01 Misoprostol vaginal versus placebo, Resultado 13 Satisfacción con el tratamiento. . . . . . . . . . . . . 36
Análisis 02.01 Comparación 02 Misoprostol vaginal versus evacuación quirúrgica del útero, Resultado 01 Evacuación quirúrgica del útero. . . . 36
Análisis 02.02 Comparación 02 Misoprostol vaginal versus evacuación quirúrgica del útero, Resultado 02 Hematócrito postratamiento (%). . . . 37
Análisis 02.03 Comparación 02 Misoprostol vaginal versus evacuación quirúrgica del útero, Resultado 03 Náuseas. . . . . . . . . . . . . 37
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
2
Análisis 02.04 Comparación 02 Misoprostol vaginal versus evacuación quirúrgica del útero, Resultado 04 Alivio del dolor. . . . . . . . . . 37
Análisis 02.05 Comparación 02 Misoprostol vaginal versus evacuación quirúrgica del útero, Resultado 05 Diarrea. . . . . . . . . . . . . 37
Análisis 02.06 Comparación 02 Misoprostol vaginal versus evacuación quirúrgica del útero, Resultado 06 Perforación uterina. . . . . . . . . 38
Análisis 02.07 Comparación 02 Misoprostol vaginal versus evacuación quirúrgica del útero, Resultado 07 Síndrome de Asherman. . . . . . . 38
Análisis 03.01 Comparación 03 Misoprostol vaginal versus gemeprost vaginal, Resultado 01 Aborto espontáneo < 24 horas. . . . . . . . . . 38
Análisis 03.02 Comparación 03 Misoprostol vaginal versus gemeprost vaginal, Resultado 02 Temperatura > 38 º C. . . . . . . . . . . . . 38
Análisis 03.03 Comparación 03 Misoprostol vaginal versus gemeprost vaginal, Resultado 03 Vómitos. . . . . . . . . . . . . . . . . . 39
Análisis 03.04 Comparación 03 Misoprostol vaginal versus gemeprost vaginal, Resultado 03 Vómitos. . . . . . . . . . . . . . . . . . 39
Análisis 03.05 Comparación 03 Misoprostol vaginal versus gemeprost vaginal, Resultado 03 Analgesia con opiáceos. . . . . . . . . . . . 39
Análisis 04.01 Comparación 04 Misoprostol vaginal versus prostaglandina E1/2 vaginal, Resultado 01 Evacuación quirúrgica. . . . . . . . . 39
Análisis 04.02 Comparación 04 Misoprostol vaginal versus prostaglandina E1/2 vaginal, Resultado 02 Transfusión de sangre. . . . . . . . . 40
Análisis 04.03 Comparación 04 Misoprostol vaginal versus prostaglandina E1/2 vaginal, Resultado 03 Hospitalización (días). . . . . . . . . 40
Análisis 04.04 Comparación 04 Misoprostol vaginal versus prostaglandina E1/2 vaginal, Resultado 04 Aborto espontáneo completo. . . . . . 40
Análisis 04.05 Comparación 04 Misoprostol vaginal versus prostaglandina E1/2 vaginal, Resultado 05 Náuseas. . . . . . . . . . . . . . 40
Análisis 05.01 Comparación 05 Esquemas de misoprostol vaginal en dosis más bajas versus dosis más altas, Resultado 01 Aborto espontáneo. . . 41
Análisis 05.02 Comparación 05 Esquemas de misoprostol vaginal en dosis más bajas versus dosis más altas, Resultado 02 Fiebre. . . . . . . 41
Análisis 05.03 Comparación 05 Esquemas de misoprostol vaginal en dosis más bajas versus dosis más altas, Resultado 03 Náuseas. . . . . . . 41
Análisis 05.04 Comparación 05 Esquemas de misoprostol vaginal en dosis más bajas versus dosis más altas, Resultado 04 Diarrea. . . . . . . 42
Análisis 06.01 Comparación 06 Preparación húmeda versus seca de misoprostol vaginal, Resultado 01 Aborto espontáneo < 3 días. . . . . . . 42
Análisis 06.02 Comparación 06 Preparación húmeda versus seca de misoprostol vaginal, Resultado 02 Aborto espontáneo < 8 días. . . . . . . 42
Análisis 06.03 Comparación 06 Preparación húmeda versus seca de misoprostol vaginal, Resultado 03 Aborto espontáneo < 15 días. . . . . . 43
Análisis 06.04 Comparación 06 Preparación húmeda versus seca de misoprostol vaginal, Resultado 04 Aborto espontáneo < 30 días. . . . . . 43
Análisis 06.05 Comparación 06 Preparación húmeda versus seca de misoprostol vaginal, Resultado 05 Diarrea < 48 horas después del tratamiento. 43
Análisis 06.06 Comparación 06 Preparación húmeda versus seca de misoprostol vaginal, Resultado 06 Escalofríos < 48 horas de tratamiento. . . 44
Análisis 06.07 Comparación 06 Preparación húmeda versus seca de misoprostol vaginal, Resultado 07 Vómitos < 48 horas de tratamiento. . . . 44
Análisis 06.08 Comparación 06 Preparación húmeda versus seca de misoprostol vaginal, Resultado 08 Desearía/probablemente desearía el mismo tratamiento
para un futuro embarazo no viable. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 44
Análisis 07.01 Comparación 07 Misoprostol vaginal + metotrexato versus misoprostol vaginal solo, Resultado 01 Aborto espontáneo incompleto. . 45
Análisis 07.04 Comparación 07 Misoprostol vaginal + metotrexato versus misoprostol vaginal solo, Resultado 04 Evacuación quirúrgica adicional. 45
Análisis 07.05 Comparación 07 Misoprostol vaginal + metotrexato versus misoprostol vaginal solo, Resultado 05 Hemorragia. . . . . . . . . 45
Análisis 07.06 Comparación 07 Misoprostol vaginal + metotrexato versus misoprostol vaginal solo, Resultado 06 Alivio del dolor. . . . . . . 46
Análisis 08.01 Comparación 08 Misoprostol vaginal más tapones de laminaria versus misoprostol vaginal solo, Resultado 01 Aborto espontáneo < 24
horas. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 46
Análisis 08.02 Comparación 08 Misoprostol vaginal más tapones de laminaria versus misoprostol vaginal solo, Resultado 02 Aborto espontáneo < 48
horas. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 46
Análisis 09.01 Comparación 09 Misoprostol oral versus misoprostol vaginal, Resultado 01 Aborto espontáneo completo. . . . . . . . . . . 47
Análisis 09.02 Comparación 09 Misoprostol oral versus misoprostol vaginal, Resultado 02 Vómitos. . . . . . . . . . . . . . . . . . . 47
Análisis 09.09 Comparación 09 Misoprostol oral versus misoprostol vaginal, Resultado 09 Náuseas. . . . . . . . . . . . . . . . . . 47
Análisis 09.10 Comparación 09 Misoprostol oral versus misoprostol vaginal, Resultado 10 Diarrea. . . . . . . . . . . . . . . . . . . 48
Análisis 09.12 Comparación 09 Misoprostol oral versus misoprostol vaginal, Resultado 12 Dolor (escala análoga visual). . . . . . . . . . . 48
Análisis 09.13 Comparación 09 Misoprostol oral versus misoprostol vaginal, Resultado 13 Fiebre. . . . . . . . . . . . . . . . . . . 48
Análisis 09.14 Comparación 09 Misoprostol oral versus misoprostol vaginal, Resultado 14 Satisfacción de las mujeres con el tratamiento. . . . 48
Análisis 09.15 Comparación 09 Misoprostol oral versus misoprostol vaginal, Resultado 15 Tiempo hasta el parto (horas). . . . . . . . . . . 49
Análisis 09.16 Comparación 09 Misoprostol oral versus misoprostol vaginal, Resultado 16 Infusión de ocitocina. . . . . . . . . . . . . . 49
Análisis 09.17 Comparación 09 Misoprostol oral versus misoprostol vaginal, Resultado 17 Alumbramiento manual. . . . . . . . . . . . . 49
Análisis 10.01 Comparación 10 Misoprostol oral + mifepristona versus conducta expectante, Resultado 01 Cavidad uterina vacía el día 5. . . . . 49
Análisis 10.02 Comparación 10 Misoprostol oral + mifepristona versus conducta expectante, Resultado 02 Evacuación quirúrgica de urgencia por
hemorragia. . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 50
Análisis 10.03 Comparación 10 Misoprostol oral + mifepristona versus conducta expectante, Resultado 03 Enfermedad pélvica inflamatoria. . . 50
Análisis 10.04 Comparación 10 Misoprostol oral + mifepristona versus conducta expectante, Resultado 04 Dolor (escala análoga visual día 5). . . 50
Análisis 10.05 Comparación 10 Misoprostol oral + mifepristona versus conducta expectante, Resultado 05 Licencia por enfermedad (días). . . . 51
Análisis 10.06 Comparación 10 Misoprostol oral + mifepristona versus conducta expectante, Resultado 06 Hemorragia (días). . . . . . . . . 51
Análisis 10.07 Comparación 10 Misoprostol oral + mifepristona versus conducta expectante, Resultado 07 Satisfacción con el tratamiento (escala análoga
visual día 14). . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 51
Análisis 11.01 Comparación 11 Misoprostol sublingual versus misoprostol vaginal, Resultado 01 Aborto espontáneo completo. . . . . . . . 52
Análisis 11.02 Comparación 11 Misoprostol sublingual versus misoprostol vaginal, Resultado 02 Náuseas. . . . . . . . . . . . . . . . 52
Análisis 11.03 Comparación 11 Misoprostol sublingual versus misoprostol vaginal, Resultado 03 Vómitos. . . . . . . . . . . . . . . . 52
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
3
Análisis 11.04 Comparación 11 Misoprostol sublingual versus misoprostol vaginal, Resultado 04 Diarrea. . . . . . . . .
Análisis 11.05 Comparación 11 Misoprostol sublingual versus misoprostol vaginal, Resultado 05 Hemoglobina día 43. . . . .
Análisis 11.06 Comparación 11 Misoprostol sublingual versus misoprostol vaginal, Resultado 06 Dolor insoportable. . . . .
Análisis 11.07 Comparación 11 Misoprostol sublingual versus misoprostol vaginal, Resultado 07 Satisfecha con el tratamiento.
Análisis 12.01 Comparación 12 Mifepristona versus placebo, Resultado 01 Aborto espontáneo < 48 horas. . . . . . . . .
Análisis 12.02 Comparación 12 Mifepristona versus placebo, Resultado 02 Aborto espontáneo < 3 días. . . . . . . . . .
Análisis 12.03 Comparación 12 Mifepristona versus placebo, Resultado 03 Aborto espontáneo < 4 días. . . . . . . . . .
Análisis 12.04 Comparación 12 Mifepristona versus placebo, Resultado 04 Aborto espontáneo < 5 días. . . . . . . . . .
Análisis 12.05 Comparación 12 Mifepristona versus placebo, Resultado 05 Hemorragia vaginal antes del día 5. . . . . . .
Análisis 12.06 Comparación 12 Mifepristona versus placebo, Resultado 06 Dolor antes del día 5. . . . . . . . . . . . .
Análisis 13.01 Comparación 13 Gemeprost vaginal versus evacuación quirúrgica del útero, Resultado 01 Evacuación quirúrgica .
Análisis 13.02 Comparación 13 Gemeprost vaginal versus evacuación quirúrgica del útero, Resultado 02 Perforación del útero.
Análisis 13.03 Comparación 13 Gemeprost vaginal versus evacuación quirúrgica del útero, Resultado 03 Náuseas. . . . . .
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
.
52
53
53
53
53
54
54
54
54
55
55
55
55
4
Tratamiento clínico para la muerte fetal temprana (menos de 24
semanas) (revisión)
Neilson JP, Hickey M, Vazquez J
Esta revisión debería citarse como:
Neilson JP, Hickey M, Vazquez J. Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas). Base de Datos Cochrane de Revisiones Sistemáticas
(Cochrane Database of Systematic Reviews) 2006, Issue 3. No.: CD002253. DOI: 10.1002/14651858.CD002253.pub3.
Esta versión publicada por primera vez en línea : 19 Julio 2006 in Issue 3, 2006
Fecha de la enmienda significativa más reciente : 24 Abril 2006
ABSTRACT
Antecedentes
En la mayoría de los embarazos que no prosperan, el desarrollo embrionario o fetal se detiene en algún momento, a veces semanas, antes de que ocurra el
aborto espontáneo. El examen ecográfico puede revelar hallazgos anormales durante esta fase demostrando la presencia de embarazos anembrionados o muerte
embrionaria o fetal. Tradicionalmente, el tratamiento antes de las 14 semanas ha sido el quirúrgico, pero los tratamientos clínicos pueden ser efectivos, seguros
y aceptables tal como esperar hasta que ocurra un aborto espontáneo.
Objetivos
Evaluar la efectividad, seguridad y aceptabilidad de cualquier tratamiento clínico de la falla precoz de embarazo (embarazos anembrionados o muerte
embrionaria o fetal antes de las 24 semanas).
Estrategia De Búsqueda
Se realizó una búsqueda en el Registro de Estudios Clínicos del Grupo Cochrane de Embarazo y Parto (Cochrane Pregnancy and Childbirth Group Trials
Register) (30 de noviembre de 2005).
Criterios De Selección
Estudios clínicos aleatorizados que comparan el tratamiento clínico con otro tratamiento (por ejemplo, la evacuación quirúrgica) o con un grupo placebo o
con ningún tratamiento para la falla precoz de embarazo. Se excluyeron los diseños cuasi aleatorizados.
Recolección Y Análisis De Datos
Se extrajeron los datos sin cegamiento.
Resultados Principales
Se incluyeron veinticuatro estudios clínicos (1888 mujeres).
El misoprostol vaginal acelera el aborto (completo o incompleto) en comparación con el placebo: por ejemplo, aborto espontáneo en menos de 24 horas (dos
estudios clínicos, 138 mujeres, riesgo relativo (RR) 4.73, intervalo de confianza del 95% (IC 95%) 2.70 a 8.28), con menor necesidad de realizar un legrado
uterino (dos estudios clínicos, 104 mujeres, RR 0.40, IC 95% 0.26 a 0.60) y sin un aumento significativo en náuseas o diarrea. Los tratamientos con dosis
inferiores de misoprostol vaginal tienden a ser menos efectivos en producir un aborto (tres estudios clínicos, 247 mujeres, RR 0.85, IC 95% 0.72 a 1.00) y la
incidencia de náuseas es similar. Aparentemente no existe una ventaja clara al administrar el preparado húmedo de misoprostol vaginal, agregar metotrexato,
o usar tapones de laminaria después de las 14 semanas. El misoprostol vaginal es más efectivo que la prostaglandina E vaginal para evitar la evacuación
quirúrgica. El misoprostol oral fue menos efectivo que el misoprostol vaginal para producir el aborto completo (2 estudios, 218 mujeres, RR 0.90, IC 95%
0.82 a 0.99). El misoprostol sublingual tuvo una eficacia equivalente al misoprostol vaginal para la inducción del aborto completo pero se asoció con diarreas
más frecuentes. Los dos estudios sobre el tratamiento con mifepristona arrojaron resultados conflictivos. No hubo una diferencia estadísticamente significativa
entre el misoprostol vaginal y el gemeprost en la inducción del aborto por muerte fetal luego de las 13 semanas.
Conclusiones De Los Autores
La evidencia disponible de los estudios aleatorizados favorece el uso de misoprostol vaginal como tratamiento clínico para la interrupción de embarazos no
viables antes de las 24 semanas. Es necesario realizar investigaciones adicionales para evaluar la efectividad y la seguridad, la vía de administración y las
dosis óptimas. Se debe realizar un estudio adicional para resolver los resultados conflictivos sobre el valor de la mifepristona.
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
5
RESUMEN EN LENGUAJE SENCILLO
Tratamientos clínicos para el aborto espontáneo inevitable
Los embarazos que no prosperan a veces pueden ser identificados más precozmente durante el estudio ecográfico si la pérdida se debe a la muerte del feto o
a que el feto no se desarrolló. En el pasado, el tratamiento antes de las 14 semanas generalmente era quirúrgico (legrado) pero los fármacos que se han
desarrollado en la actualidad pueden ser útiles o esperar hasta que acontezca el aborto espontáneo puede ser una mejor alternativa. La revisión de los estudios
clínicos evaluó diferentes tratamientos farmacológicos probables en los que se usaron diferentes vías de administración y dosis, en comparación con la conducta
expectante del aborto espontáneo. Esta revisión identificó 24 estudios en los que se incluyeron 1888 mujeres de menos de 24 semanas de gestación, en donde
el feto sufrió muerte intrauterina o no se había formado en el útero. La mayoría de los estudios fueron de buena calidad. El misoprostol vaginal aceleró el
aborto, no obstante, los estudios eran demasiado pequeños como para evaluar adecuadamente los efectos adversos potenciales, inclusive la fertilidad futura.
Aparentemente, el misoprostol oral fue menos efectivo que por vía vaginal y las mujeres pidieron más días de licencia por enfermedad cuando recibieron el
medicamento oral. Algunas mujeres desean acelerar el aborto inevitable, mientras que otras no lo prefieren. Las mujeres pueden tener acceso a ambas
modalidades de tratamiento. Las mujeres que están amamantando pueden preferir esperar en lugar de recibir el tratamiento farmacológico. Se deben realizar
investigaciones adicionales sobre las dosis, vías de administración y efectos adversos potenciales del medicamento, incluida la fertilidad futura y también se
deben contemplar las opiniones de las mujeres sobre el tratamiento farmacológico, la cirugía y la conducta expectante del aborto.
ANTECEDENTES
Se considera que la incidencia de abortos espontáneos clínicamente obvios
varía entre el 10% y el 15% de todos los embarazos aunque la incidencia
real puede ser considerablemente superior (Grudzinskas 1995; Howie 1995;
Simpson 1991).
El uso generalizado de la ecografía en los primeros meses de embarazo por
razones específicas (por ejemplo, sangrado vaginal) o para un examen de
rutina (Neilson 1998) revela "embarazos no viables" inevitablemente
destinados al aborto espontáneo en su debido momento. Se llaman "embarazos
anembrionados", anteriormente llamados "huevos hueros", si no se ha
desarrollado un embrión dentro de la bolsa gestacional, o "abortos retenidos"
si está presente un embrión o feto pero sin vida.
El protocolo para esta revisión tuvo como objetivo combinar los estudios de
los tratamientos clínicos de embarazos no viables y de abortos espontáneos
incompletos, pero considerándolo mejor, este objetivo era ilógico. Los
embarazos no viables contienen tejido (placentario) trofoblástico viable que
produce hormonas las cuales, en teoría, hacen a estos embarazos más
susceptibles al tratamiento antihormonal y más resistentes al tratamiento
uterotónico (que estimula las contracciones uterinas) que los embarazos que
ya sufrieron un aborto espontáneo (incompleto). Por lo tanto, esta revisión
se concentrará exclusivamente en los embarazos no viables, antes de un
aborto espontáneo. En otra revisión se evaluarán los estudios clínicos sobre
los tratamientos médicos posteriores al aborto espontáneo (Vazquez 2000).
Una revisión adicional compara la conducta expectante con el tratamiento
quirúrgico para el aborto espontáneo (Nanda 2002).
Tradicionalmente, la interrupción de los embarazos no viables en los primeros
meses de gestación (menos de 14 semanas) se realizaba por evacuación
quirúrgica. La interrupción de embarazos de 14 a 24 semanas de gestación
se realizaba con la inducción clínica del aborto.
Diferentes tipos de tratamientos clínicos podrían ser alternativas adecuadas
al tratamiento quirúrgico: el misoprostol es un análogo de la prostaglandina
E1, comercializada para la prevención y el tratamiento de las úlceras pépticas.
Reconocido como un potente método para la interrupción de embarazos
viables no deseados (Costa 1993; Norman 1991), es un medicamento de bajo
costo, estable a temperatura ambiente y con pocas reacciones sistémicas,
aunque se han publicado reacciones adversas como vómitos, diarrea,
hipertensión y hasta teratogenicidad potencial cuando el misoprostol fracasa
en la inducción del aborto (Fonseca 1991). Se demostró que el misoprostol
es un estimulante miometrial efectivo del útero grávido, ya que se une de
manera selectiva a los receptores de los prostanoides EP 2/EP 3 (Senior
1993). Se absorbe con rapidez por vía oral y vaginal. Los niveles séricos de
absorción vaginal son más prolongados y el misoprostol vaginal puede tener
efectos mediados de forma local (Zieman 1997).
El misoprostol puede ser especialmente útil en los países en desarrollo en
los que el transporte y las instalaciones para el almacenamiento de los
medicamentos son inadecuadas, y la disponibilidad de agentes uterotónicos
y de sangre es limitada. Se estudió su uso en la obstetricia y ginecología,
especialmente para inducir el aborto en el primer y segundo trimestre (Ashok
1998; Bugalho 1996), para la inducción del trabajo de parto (Alfirevic 2001;
Hofmeyr 2003) y para la prevención de la hemorragia postparto (Gulmezoglu
2004) a pesar de no estar registrado para este uso.
Entre otros fármacos uterotónicos que podrían desempeñar una función se
incluyen la ergometrina, la ocitocina y la prostaglandina F2alfa.
El antagonista de la progesterona, la mifepristona, tiene valor en la
interrupción de embarazos no deseados de pocas semanas de gestación y
puede ser útil en embarazos no viables y abortos espontáneos (Baulieu 1986;
Kovacs 1984), como único agente o en combinación con la prostaglandina
(Cameron 1986).
El metotrexato puede ser útil para el tratamiento clínico de los embarazos
ectópicos y, por lo tanto, también podría tener un lugar en el tratamiento de
embarazos intrauterinos no viables. Además, se ha utilizado para la
interrupción temprana de embarazos no deseados, seguido por la
administración de un agente uterotónico como el misoprostol.
Aunque a veces se observan problemas de coagulación en mujeres con
retención prolongada de un feto muerto, este efecto es poco frecuente y
generalmente no ocurre dentro del primer mes posterior a la muerte fetal.
Por lo tanto, no existen razones clínicas que obliguen a interrumpir los
embarazos no viables. Aunque de manera anecdótica muchas mujeres
favorecen la interrupción temprana, el "manejo o conducta expectante" (es
decir, esperar a que acontezca el aborto espontáneo) es una alternativa
legítima y esta política debería tenerse en cuenta en la asistencia clínica y
en la planificación de los estudios clínicos.
OBJETIVOS
Evaluar, de los estudios clínicos, la efectividad y la seguridad de los diferentes
tratamientos clínicos para la interrupción de embarazos no viables, con
referencia a la muerte o a complicaciones graves, evacuación quirúrgica
adicional, transfusión de sangre, hemorragia, pérdida de sangre, anemia, con
sangrado, alivio del dolor, infección pélvica, lesión cervical, duración de la
hospitalización, efectos psicológicos, fertilidad posterior, satisfacción de las
mujeres y costos.
C R I T E R I O S PA R A L A VA L O R A C I Ó N D E
L O S E S T U D I O S D E E S TA R E V I S I Ó N
Tipos De Estudios
Los estudios clínicos aleatorizados que comparan el tratamiento clínico con
otro tratamiento, por ejemplo, la evacuación quirúrgica, o con placebo, o
con ningún tratamiento para interrumpir embarazos no viables, la asignación
aleatoria a un grupo de tratamiento o a uno de comparación, las medidas
razonables para garantizar el ocultamiento de la asignación y el
incumplimiento de la conducta asignada no fueron suficientes para afectar
los resultados de forma considerable. Se excluyeron los diseños cuasi
aleatorizados.
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
6
Tipos De Participantes
Mujeres con embarazos no viables (es decir, cuando el embrión o el feto
habían muerto en el útero, y cuando el aborto espontáneo hubiera ocurrido
inevitablemente en su debido momento) si tienen menos de 24 semanas de
edad gestacional estimada. Si es posible, se deben realizar análisis de
subgrupos para las mujeres con embarazos de menos de 14 semanas y para
aquéllas cuya edad gestacional estimada es entre 14 y 23 semanas.
Los estudios clínicos identificados a través de las actividades de búsqueda
descritas reciben un código (o códigos), según el tema. Los códigos se
vinculan a los temas de las revisiones. El Coordinador de Búsqueda de
Ensayos realiza la búsqueda a través de estos códigos, en lugar de usar
palabras clave.
No se establecieron restricciones sobre el idioma.
MÉTODOS DE LA REVISIÓN
Tipos De Intervención
Se tuvieron en cuenta los estudios clínicos si comparaban el tratamiento
clínico con otros métodos; por ejemplo, conducta expectante, placebo o
cualquier otra intervención, entre ellas la evacuación quirúrgica. Si existían
datos, también se incluyeron las comparaciones entre las diferentes vías de
administración del tratamiento clínico, por ejemplo, oral versus vaginal, o
entre diferentes fármacos o dosis de un fármaco, o la duración de un
tratamiento o el momento oportuno para administrarlo.
Tipos De Medidas De Resultado
Se tuvieron en cuenta los estudios clínicos que reportaban alguno de los
siguientes resultados.
Resultados primarios
(1) Aborto espontáneo completo (es decir, sin restos de tejidos de embarazo
en el útero, según los hallazgos clínicos en la cirugía o el examen ecográfico
después de un período determinado).
(2) Muerte o complicaciones serias (por ejemplo; rotura uterina, perforación
uterina, histerectomía, fallo orgánico, ingreso a la unidad de cuidados
intensivos).
Resultados secundarios
(1) Evacuación quirúrgica adicional
(2) Transfusión de sangre
(3) Hemorragia
(4) Pérdida de sangre
(5) Anemia
(6) Días con sangrado
(7) Alivio del dolor
(8) Infección pélvica
(9) Lesión cervical
(10) Trastornos digestivos (náuseas o vómitos o diarrea)
(11) Trastornos hipertensivos
(12) Duración de la hospitalización
(13) Efectos psicológicos
(14) Fertilidad posterior
(15) Satisfacción o aceptabilidad del método por parte de la mujer
(16) Costos
M É T O D O S D E B Ú S Q U E D A PA R A L A
IDENTIFICACIÓN DE LOS ESTUDIOS
Ver: métodos utilizados en las revisiones:
Se realizaron búsquedas en el registro de ensayos del Grupo Cochrane de
Embarazo y Parto mediante contacto con el Coordinador de Búsqueda de
Ensayos (30 de noviembre de 2005).
El Coordinador de Búsqueda de Estudios Clínicos realiza el mantenimiento
del Registro de Estudios Clínicos del Grupo Cochrane de Embarazo y Parto,
que contiene los estudios clínicos identificados de:
(1) búsquedas trimestrales del Registro Central Cochrane de Estudios Clínicos
Controlados (Cochrane Central Register of Controlled Trials, CENTRAL);
(2) búsquedas mensuales en MEDLINE;
(3) búsquedas manuales en 30 revistas y en los resúmenes de congresos
importantes;
(4) búsqueda semanal de concienciación actual de otras 37 revistas científicas.
Los detalles de las estrategias de búsqueda correspondientes a CENTRAL
y MEDLINE, la lista de revistas y actas de congresos en los que se realizó
una búsqueda manual y la lista de revistas científicas examinadas mediante
el servicio de concientización actualizada pueden encontrarse en la sección
"Estrategias de búsqueda para la identificación de estudios", en la información
editorial sobre el Grupo Cochrane de Embarazo y Parto.
Se seleccionaron todos los estudios clínicos potenciales de acuerdo con los
criterios especificados en el protocolo. Un único autor extrajo los datos de
cada publicación y los coautores los verificaron. Se resolvieron las
discrepancias mediante sesiones de discusión. Además de las principales
medidas de resultado enumeradas antes, se recopiló información sobre el
lugar donde se realizó el estudio (país, tipo de población, nivel
socioeconómico), el método de aleatorización, una descripción detallada del
régimen antibiótico utilizado (fármacos, vía de administración, dosis,
frecuencia), definiciones de los resultados (si estaban disponibles), y si los
clínicos y los participantes desconocían la asignación del tratamiento. Siempre
que fue posible se realizó el análisis por intención de tratar. También se
recolectó cualquier tipo de información sobre la culminación del seguimiento.
La calidad metodológica de los estudios clínicos se evaluó con los criterios
Cochrane estándar de ocultamiento de la asignación:
(A) adecuado;
(B) poco claro;
(C) inadecuado;
(D) no se utilizó ocultamiento de la asignación.
Se obtuvo información sobre el cegamiento de la evaluación de los resultados
y las pérdidas al seguimiento.
Se realizaron comparaciones por separado de los diferentes regímenes de
tratamiento, agrupados, según correspondiera, por la cantidad de dosis
administradas y la vía de administración. Para calcular los riesgos relativos
combinados se utilizó un modelo de efectos fijos (siempre que no hubiera
una heterogeneidad significativa entre los estudios clínicos, definida como
1 cuadrado superior al 50%). Debido al escaso número de estudios clínicos
y comparaciones, fue imposible realizar el análisis de sensibilidad usando
la calidad del estudio (A versus B, C, D).
DESCRIPCIÓN DE LOS ESTUDIOS
Esta revisión incluyó 24 estudios que compararon el misoprostol vaginal
con la conducta expectante (Bagratee 2004), placebo (Herabutya 1997;
Kovavisarach 2002; Lister 2005; Wood 2002), evacuación quirúrgica
(Demetroulis 2001; Graziosi 2004; Muffley 2002), misoprostol oral o
sublingual (Creinin 1997; Ngoc 2004; Tang 2003), otros tipos de preparación
de prostaglandina vaginal o intracervical (Al Inizi 2003; Eng 1997**; Fadalla
2004**; Kara 1999**); diferentes dosis (Heard 2002; Kovavisarach 2005;
Niromanesh 2005**) y preparaciones (Gilles 2004) de misoprostol vaginal;
la adición de metotrexato al misoprostol vaginal (Autry 1999) o tapones de
laminaria (Jain 1996**); mifepristona versus placebo (Lelaidier 1993);
mifepristona y misoprostol oral versus conducta expectante (Nielsen 1999),
y gemeprost vaginal versus evacuación quirúrgica (Egarter 1995).
En el estudio clínico de Bagratee 2004 se comparó el misoprostol vaginal
versus placebo para estudiar las comparaciones con la conducta expectante
(hasta siete días) y, por lo tanto, difirieron en concepto con respecto a los
estudios de Herabutya 1997 y Wood 2002 en los que la intervención
quirúrgica temprana se realizó después, a las 24 y 48 horas, respectivamente.
De los 24 estudios incluidos, cinco se refirieron el tratamiento clínico de los
embarazos no viables después de las 14 semanas (Eng 1997**; Fadalla
2004**; Jain 1996**; Kara 1999**; Niromanesh 2005**). Estos estudios
están marcados con un asterisco para facilitar la interpretación.
Hay estudios clínicos adicionales que incluyeron datos sobre mujeres con
embarazos no viables y abortos incompletos (por ejemplo, Ngai 2001). Si
los investigadores pudieran separarlos, es probable que estos datos se incluyan
en actualizaciones futuras.
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
7
CALIDAD METODOLÓGICA
Trece estudios usaron métodos sólidos de ocultamiento de la asignación
(Autry 1999; Bagratee 2004; Creinin 1997; Demetroulis 2001; Gilles 2004;
Graziosi 2004; Kovavisarach 2005; Lelaidier 1993; Lister 2005; Muffley
2002; Ngoc 2004; Tang 2003; Wood 2002). Nueve informes no describieron
el proceso de aleatorización (Al Inizi 2003; Egarter 1995; Fadalla 2004*;
Herabutya 1997; Jain 1996*; Kara 1999*; Kovavisarach 2002; Nielsen 1999;
Niromanesh 2005*). Un estudio se publicó sólo en forma de resumen, sin
detalles sobre la aleatorización (Heard 2002). En un estudio, la asignación
se realizó mediante la elección de un sobre no numerado; método que se
reconoce como menos sólido (Eng 1997**).
En la mayoría de los estudios, se realizó un análisis por intención de tratar.
Fue imposible que los médicos desconocieran el método de tratamiento en
algunos estudios, si el tratamiento consistía en la evacuación quirúrgica del
útero, vías alternativas de administración del fármaco (oral versus vaginal)
o una política de conducta expectante. Sin embargo, es posible ocultar el
método de tratamiento al personal responsable de evaluar las complicaciones
durante las visitas de seguimiento, pero ningún estudio lo menciona.
Hubo una variación entre los estudios en la determinación del momento
oportuno para las visitas de seguimiento programadas.
R E S U LTA D O S
Se incluyeron 24 estudios con 1888 mujeres en total. De estos estudios, 19
se refirieron a la interrupción de los embarazos no viables antes de las 14
semanas.
El tratamiento con misoprostol vaginal acelera el aborto (pasaje de los restos
ovulares, ya sea completo o incompleto) en comparación con placebo: aborto
espontáneo en menos de 24 horas (dos estudios clínicos, 138 mujeres, riesgo
relativo (RR) 4.73, intervalo de confianza (IC) del 95% 2.70 a 8.28), aborto
espontáneo en menos de 48 horas (otros dos estudios clínicos, 84 mujeres,
RR 5.74, IC 95% 2.70 a 12.19, aborto espontáneo completo sin necesidad
de recurrir a una intervención quirúrgica a los siete días (un estudio clínico,
83 mujeres, RR 2.99, IC 95% 1.80 a 4.99). Hubo una menor necesidad de
realizar un legrado uterino (dos estudios clínicos, 104 mujeres, RR 0.40, IC
95% 0.26 a 0.60) y no se observó un aumento estadísticamente significativo
de los efectos adversos: náuseas (dos estudios, 88 mujeres, RR 1.38, IC 95%
0.43 a 4.40), diarrea (dos estudios clínicos, 88 mujeres, RR 2.21, IC 95%
0.35 a 14.06). En un estudio se demostró una reducción en los costos en
relación con una estrategia de iniciar el tratamiento con misoprostol en
comparación con el legrado inmediato (diferencia media EUR192, IC 95%
33 a 351), sin diferencia obvia en la fertilidad posterior y con cantidades
similares de mujeres (58%) que elegirían la misma estrategia de tratamiento
en el futuro (Graziosi 2004); aunque más mujeres que tuvieron un aborto
espontáneo completo después del misoprostol (76%) elegirían este tratamiento
que quienes posteriormente requirieron un legrado (38%).
Compatible con estas observaciones, el tratamiento con misoprostol vaginal
disminuye la necesidad de una evacuación quirúrgica del útero en
comparación con la política de realizar una evacuación quirúrgica inmediata
(tres estudios clínicos, 254 mujeres, RR 0.42, IC 95% 0.34 a 0.52) a costa
de más náuseas (un estudio clínico, 154 mujeres, RR 21.85, IC 95% 1.31 a
364.37) y diarrea (un estudio clínico, 154 mujeres, RR 40.85, IC 95% 2.52
a 662.57).
El misoprostol vaginal se administró en dosis de 400 mcg, 600 mcg y 800
mcg en los estudios: los tratamientos con dosis inferiores tienden a ser menos
efectivos en producir un aborto (tres estudios clínicos, 247 mujeres, (RR)
0.85, IC 95% 0.72 a 1.00) y la incidencia de náuseas es similar (dos estudios
clínicos, 214 mujeres, RR 0.67, IC 95% 0.31 a 1.41). Aparentemente no
existe una ventaja clara en la administración de una preparación "húmeda"
de misoprostol vaginal en comparación con una preparación "seca": aborto
espontáneo en menos de tres días (un estudio clínico, 80 mujeres, RR 1.14,
IC 95% 0.85 a 1.54). La combinación del metotrexato con el misoprostol
vaginal no resultó ser favorable en un pequeño estudio clínico como para
resolver este problema: el aborto espontáneo fue incompleto después del
tratamiento (21 mujeres, RR 0.26, IC 95% 0.01 a 5.65). Los tapones de
laminaria tampoco fueron un complemento útil del misoprostol vaginal
durante el segundo trimestre: aborto espontáneo completo en menos de 24
horas (un estudio clínico, 38 mujeres, RR 0.90, IC 95% 0.65 a 1.25), en
menos de 48 horas (un estudio clínico, 38 mujeres, RR 1.07, IC 95% 0.88 a
1.29). El misoprostol vaginal fue más efectivo que la prostaglandina E vaginal
para evitar la evacuación quirúrgica (un estudio clínico, 80 mujeres, RR
0.39, IC 95% 0.21 a 0.72) y para lograr el aborto completo en el segundo
trimestre (un estudio clínico, 65 mujeres, RR 1.44, IC 95% 1.06 a 1.96).
En general, se observó que el misoprostol oral resultaba menos efectivo que
el misoprostol vaginal para producir un aborto completo (dos estudios
clínicos, 218 mujeres, RR 0.90, IC 95% 0.82 a 0.99), pero esta diferencia se
observó solamente con la dosis oral de 400 mcg (un estudio clínico, 20
mujeres, RR 0.29, IC 95% 0.10 a 0.79) y no se observó con la dosis oral de
800 mcg (un estudio clínico, 198 mujeres, RR 0.96, IC 95% 0.88 a 1.05).
Con el tratamiento oral hubo menos vómitos (un estudio clínico, 190 mujeres,
RR 0.29, IC 95% 0.10 a 0.84), pero una incidencia similar de diarrea (dos
estudios clínicos, 210 mujeres, RR 1.05, IC 95% 0.67 a 1.66). Los niveles
de satisfacción con respecto al tratamiento fueron altos (y similares) (un
estudio clínico, 198 mujeres, RR 0.96, IC 95% 0.86 a 1.06). El misoprostol
oral indujo el aborto de manera más lenta que el misoprostol vaginal en un
único estudio clínico en el que se incluyeron mujeres con muerte fetal en el
segundo trimestre (diferencia de medias ponderada 4 horas y 10 minutos,
IC 95% 2.64 a 5.56).
El misoprostol sublingual tuvo una eficacia equivalente al misoprostol vaginal
en inducir el aborto completo (un estudio clínico, 80 mujeres, RR 1.00, IC
95% 0.85 a 1.18), pero se asoció con diarreas más frecuentes (RR 2.65, IC
95% 1.48 a 4.38), pero sin otros efectos secundarios.
Los dos estudios sobre el tratamiento con mifepristona arrojaron resultados
conflictivos. Un estudio descubrió que la mifepristona era mucho más efectiva
que el placebo: el aborto espontáneo fue completo después del tratamiento
(46 mujeres, RR 9.50, IC 95% 2.49 a 36.19). El otro estudio comparó el
tratamiento con mifepristona y misoprostol oral con una política de conducta
expectante (sin tratamiento); pero no hubo una diferencia estadísticamente
significativa en el aborto completo hasta el día cinco (122 mujeres, RR 1.08,
IC 95% 0.90 a 1.30).
No hubo una diferencia estadísticamente significativa entre el misoprostol
vaginal y el gemeprost en la inducción del aborto en menos de 24 horas para
la muerte fetal después de las 13 semanas (un estudio clínico, 50 mujeres,
RR 1.24, IC 95% 0.90 a 1.70).
En los estudios clínicos publicados son pocos los informes sobre efectos
adversos serios, pero en una mujer se debió practicar una resección intestinal
después de una perforación uterina durante la evacuación del útero (Egarter
1995).
DISCUSIÓN
La gran mayoría de los estudios incluidos (21/24) abordaron el uso del
misoprostol (principalmente por administración vaginal). Existe gran interés
en el uso del misoprostol como agente abortivo porque aparentemente es un
método potente para la interrupción del embarazo además de tener un costo
bajo y ser estable a temperatura ambiente, y por ende, probablemente sea
útil en los países en desarrollo donde el transporte y las instalaciones para
el almacenamiento es inadecuado, y la disponibilidad de los agentes
uterotónicos y de sangre es limitada. Sin embargo, es necesario recurrir a la
ecografía para diagnosticar embarazos no viables y en muchos países en
desarrollo los ecógrafos son escasos. Otras revisiones Cochrane describen
el uso del misoprostol para indicaciones que incluyen la interrupción de
embarazos no deseados (Kulier 2004; Say 2002), inducción del trabajo de
parto (Alfirevic 2001; Hofmeyr 2003; Muzonzini 2004) y prevención y
tratamiento de la hemorragia postparto (Gulmezoglu 2004; Mousa 2003).
IMPLICACIONES DE LOS AUTORES
Implicaciones para la práctica
La evidencia disponible de los estudios aleatorizados favorece el uso de
misoprostol vaginal como una opción posible para el tratamiento de
embarazos no viables antes de las 24 semanas.
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
8
Implicaciones para la investigación
La demostración ecográfica de la falla precoz de un embarazo antes de las
14 semanas es un problema frecuente que amerita un mayor esfuerzo de
investigación que el que se ha dedicado hasta el momento. Es necesario
realizar investigaciones adicionales para evaluar la efectividad, seguridad y
efectos secundarios del misoprostol, incluida la vía de administración y dosis
óptimas. Se debe realizar un estudio adicional para resolver los resultados
conflictivos sobre el valor de la mifepristona. Las opiniones de las mujeres
acerca de la aceptabilidad del tratamiento clínico, el tratamiento quirúrgico
y la conducta expectante debe ser parte integral de los futuros protocolos de
investigación, tal como deben serlo los análisis económicos. El resultado a
largo plazo, especialmente la fertilidad ulterior, merece un estudio adicional
en estudios clínicos controlados aleatorizados de una potencia estadística
apropiada.
Se agradece a Sonja Henderson y a Lynn Hampson del Grupo Cochrane de
Embarazo y Parto (Cochrane Pregnancy and Childbirth Group), Hospital de
la Mujer de Liverpool (Liverpool Women's Hospital), Reino Unido.
Como parte del proceso editorial previo a la publicación, dos revisores pares
(un editor y un evaluador externo que no pertenecían al equipo editorial),
uno o más miembros del panel internacional de consumidores del Grupo
Cochrane de Embarazo y Parto y el Asesor estadístico del Grupo hicieron
el comentario de esta revisión.
FUENTES DE FINANCIACIÓN
Fuentes Externas De Financiación
• Programa de Reproducción Humana/OMS, Ginebra, SUIZA
POTENCIAL CONFLICTO DE INTERESES
Fuentes Internas De Financiación
Ninguno del que se tenga conocimiento.
• Hospital America Arias, Havana, CUBA
AGRADECIMIENTOS
• Universidad de Liverpool, REINO UNIDO
REFERENCIAS
Referencias de los estudios incluidos en esta revisión
Al Inizi 2003 {sólo datos publicados}
Al Inizi SA, Ezimokhai M. Vaginal misoprostol versus dinoprostone for the
management of missed abortion. International Journal of Gynecology &
Obstetrics 2003;83:73 4.
Autry 1999 {sólo datos publicados}
Autry A, Jacobson G, Sandhu R, Isbill K. Medical management of non viable
early first trimester pregnancy. International Journal of Gynecology &
Obstetrics 1999;67(1):9 13.
Bagratee 2004 {sólo datos publicados}
Bagratee JS, Khullar V, Regan L, Moodley J, Kagoro H. A randomized
controlled trial comparing medical and expectant management of first trimester
miscarriage. Human Reproduction 2004;19:266 71.
Creinin 1997 {sólo datos publicados}
Creinin MD, Moyer R, Guido R. Misoprostol for medical evacuation of early
pregnancy failure. Obstetrics & Gynecology 1997;89:768 72.
Demetroulis 2001 {sólo datos publicados}
* Demetroulis C, Saridogan E, Kunde D, Naftalin AA. A prospective
randomized control trial comparing medical and surgical treatment for early
pregnancy failure. Human Reproduction 2001;16:365 9.
Demetroulis C, Saridogan E, Kunde D, Naftalin AA. A prospective randomized
control trial comparing medical and surgical treatment for early pregnancy
failure. XVI FIGO World Congress of Obstetrics and Gynecology; 2000 Sept
3 8; Washington DC, USA. 2000.
Egarter 1995 {sólo datos publicados}
Egarter C, Lederhilger J, Kurz C, Karas H, Reisenberger K. Gemeprost for
first trimester missed abortion. Archives of Gynecology and Obstetrics
1995;256:29 32.
Eng 1997* {sólo datos publicados}
Eng NS, Guan AC. Comparative study of intravaginal misoprostol with
gemeprost as an abortifacient in second trimester missed abortion. Australian
and New Zealand Journal of Obstetrics and Gynaecology 1997;37:331 4.
Fadalla 2004* {sólo datos publicados}
Fadalla FA, Mirghani OA, Adam I. Oral misoprostol vs vaginal misoprostol
for termination of pregnancy with intrauterine fetal demise in the
second trimester. International Journal of Gynecology & Obstetrics
2004;86:52 3.
Gilles 2004 {sólo datos publicados}
Barnhart KT, Bader T, Huang X, Frederick MM, Timbers KA, Zhang JJ.
Hormone pattern after misoprostol administration for a nonviable first trimester
gestation. Fertility and Sterility 2004;81:1099 105.
Creinin MD, Harwood B, Guido RS, Fox MC, Zhang J, NICHD Early
Pregnancy Failure Trial. Endometrial thickness after misoprostol use for early
pregnancy failure. International Journal of Gynecology & Obstetrics
2004;86:22 6.
Davis AR, Robilotto CM, Westhoff CL, Forman S, Zhang J, NICHD
Management of Early Pregnancy Failure Trial. Bleeding patterns after vaginal
misoprostol for treatment of early pregnancy failure. Human Reproduction
2004;19:1655 8.
Gilles J, Creinin MM, Barnhart KT, Westhoff C, Frederick MM, Zang J, et
al. Wet versus dry misoprostol application for treatment of early pregnancy
failure. Fertility and Sterility 2002;78:S64 S65.
* Gilles JM, Creinin MD, Barnhart K, Westhoff C, Frederick MM, Zhang J.
A randomized trial of saline solution moistened misoprostol versus dry
misoprostol for the first trimester pregnancy failure. American Journal of
Obstetrics and Gynecology 2004;190:389 94.
Graziosi 2004 {sólo datos publicados}
Graziosi GCM, Bruinse HW, Reuwer PJH, Teteringen O, Mol BWJ. Fertility
outcome after a randomized trial comparing curettage with misoprostol for
treatment of early pregnancy failure. Human Reproduction 2005;20:1749 50.
Graziosi GCM, Bruinse HW, Reuwer PJH, van Kessel PH, Westerweel PE,
Mol BW. Misoprostol versus curettage in women with early pregnancy failure:
impact on women's health related quality of life. A randomized controlled
trial. Human Reproduction 2005;20:2340 7.
* Graziosi GCM, Mol BWJ, Reuwer PJH, Drogtrop A, Bruinse HW.
Misoprostol versus curettage in women with early pregnancy failure after
initial expectant management: a randomized trial. Human Reproduction
2004;19:1894 9.
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
9
Graziosi GCM, van der Steeg JW, Reuwer PHW, Drogtrop AP, Bruinse HW,
Mol BWJ. Economic evaluation of misoprostol in the treatment of early
pregnancy failure compared to curettage after an expectant management.
Human Reproduction 2005;20:1067 71.
Heard 2002 {sólo datos publicados}
Heard MJ, Stewart GM, Buster JE, Carson SA, Miller HJ. Outpatient
management of missed abortion with vaginal misoprostol [abstract]. Obstetrics
& Gynecology 2002;99(4 Suppl):20S.
Herabutya 1997 {sólo datos publicados}
Herabutya Y, O Prasertsawat P. Misoprostol in the management of missed
abortion. International Journal of Gynecology & Obstetrics 1997;56:263 6.
Jain 1996* {sólo datos publicados}
Jain JK, Mishell DR. A comparison of misoprostol with and without laminaria
tents for induction of second trimester abortion. American Journal of Obstetrics
and Gynecology 1996;175:173 7.
Kara 1999* {sólo datos publicados}
Kara M, Ozden S, Eroglu M, Cetin A, Arioglu P. Comparison of misoprostol
and dinoproston administration for the induction of labour in second trimester
pregnancies in cases of intrauterine fetal loss. Italian Journal of Gynecology
and Obstetrics 1999;1:13 6.
Kovavisarach 2002 {sólo datos publicados}
Kovavisarach E, Sathapanachai U. Intravaginal 400 micrograms misoprostol
for pregnancy termination in cases of blighted ovum: a randomised controlled
trial. Australian and New Zealand Journal of Obstetrics and Gynaecology
2002;42:161 3.
Tang 2003 {sólo datos publicados}
Tang OS, Lau WNT, Ng EHY, Lee SWH, Ho PC. A prospective randomized
study to compare the use of repeated doses of vaginal with sublingual
misoprostol in the management of first trimester silent miscarriage. Human
Reproduction 2003;18:176 81.
Wood 2002 {sólo datos publicados}
Wood SL, Brain PH. Medical management of missed abortion: a randomized
clinical trial. Obstetrics & Gynecology 2002;99:563 6.
References to studies excluded from this review
Abdel Fattah 1997
Abdel Fattah IH. PGE1 analogue for the induction of midtrimester abortion
in cases of intrauterine fetal death. Acta Obstetricia et Gynecologica
Scandinavica Supplement 1997;76(167:2):26.
Almog 2005
Almog B, Levin I, Winkler N, Fainaru O, Pauzner D, Lessing JB, et al. The
contribution of laminaria placement for cervical ripening in second trimester
termination of pregnancy induced by intra amniotic injection of prostaglandin
F2alpha followed by concentrated oxytocin infusion. European Journal of
Obstetrics & Gynecology and Reproductive Biology 2005;118:32 5.
Anderman 2000
Anderman S, Jaschevatzky OE, Ballas S. Comparison between a double balloon
device and the foley catheter in extraamniotic prostaglandin F2a infusion for
termination of midtrimester missed abortion. XVI FIGO World Congress of
Obstetrics & Gynecology; 2000 Sept 3 8; Washington DC, USA. 2000:162.
Kovavisarach 2005 {sólo datos publicados}
Kovavisarach E, Jamnansiri C. Intravaginal misoprostol 600mcg and 800mcg
for the treatment of early pregnancy failure. International Journal of
Gynecology & Obstetrics 2005;90:208 12.
Avila Vergara 1997
Avila Vergara MA, Morgan Ortiz F, Fragoza Sosa O, Haro Garcia L. Cervical
labor induction with prostaglandin E2 in patients with fetal death [Maduracion
cervical con prostaglandina E2 en pacientes con feto muerto]. Ginecologia y
Obstetricia de Mexico 1997;65:155 8.
Lelaidier 1993 {sólo datos publicados}
Lelaidier C, Baton Saint Mleux C, Fernandez H, Bourget P, Frydman R.
Mifepristone (RU 486) induces embryo expulsion in first trimester
non developing pregnancies: a prospective randomized trial. Human
Reproduction 1993;8:492 5.
Bebbington 2002
Bebbington MW, Kent N, Lim K, Gagnon A, Delisle MF, Tessier F, et al. A
randomized controlled trial comparing two protocols for the use of misoprostol
in midtrimester pregnancy termination. American Journal of Obstetrics and
Gynecology 2002;187:853 7.
Lister 2005 {sólo datos publicados}
Lister MS, Shaffer LET, Bell JG, Lutter KQ, Moorma KH. Randomized,
double blind, placebo controlled trial of vaginal misoprostol for management
of early pregnancy failures. American Journal of Obstetrics and Gynecology
2005;193:1338 43.
Cabrol 1990
Cabrol D, Dubois C, Cronje H, Gonnet JM, Guillot M, Maria B, et al. Induction
of labour with mifepristone (RU 486) in intrauterine fetal death. American
Journal of Obstetrics and Gynecology 1990;163:540 2.
Muffley 2002 {sólo datos publicados}
Muffley PE, Stitely ML, Gherman RB. Early intrauterine pregnancy failure:
a randomized trial of medical versus surgical treatment. American Journal of
Obstetrics and Gynecology 2002;187:321 6.
Ngoc 2004 {sólo datos publicados}
Ngoc NTN, Blum J, Westheimer E, Quan TTV, Winikoff B. Medical treatment
of missed abortion using misoprostol. International Journal of Gynecology &
Obstetrics 2004;87:138 42.
Nielsen 1999 {sólo datos publicados}
Nielsen S, Hahlin M, Platz Christensen J. Expectant management or
pharmacological treatment for first trimester spontaneous abortion: a
randomised trial. Acta Obstetricia et Gynecologica Scandinavica
1997;76(167:2):77.
* Nielsen S, Hahlin M, Platz Christensen J. Randomised trial comparing
expectant with medical management for first trimester miscarriages. British
Journal of Obstetrics and Gynaecology 1999;106:804 7.
Niromanesh 2005* {sólo datos publicados}
Niromanesh S, Hashemi Feasharaki M, Mosavi Jarrahi A. Second trimester
abortion using intravaginal misoprostol. International Journal of Gynecology
& Obstetrics 2005;89:276 7.
Clevin 2001
Clevin L, Munk T, Hansen TR. Spontaneous abortion. Drug treatment versus
surgery [Spontan abort. Medicinsk versus kirurgisk behandling]. Ugeskrift for
Laeger 2001;163(15):2136 9.
David 2003
David M, Chen FCK, Lichtenegger W. NO donor nitroglycerin versus the
prostaglandin gemeprost for cervical ripening in first trimester missed abortion.
International Journal of Gynecology & Obstetrics 2003;83:71 2.
Dickinson 1998
Dickinson JE, Godfrey M, Evans SF. Efficacy of intravaginal misoprostol in
second trimester pregnancy termination: a randomized controlled trial. Journal
of Maternal Fetal Medicine 1998;7:115 9.
Dickinson 2002
Dickinson JE, Evans SF. The optimization of intravaginal misoprostol dosing
schedules in second trimester pregnancy termination. American Journal of
Obstetrics and Gynecology 2002;186:470 4.
Dickinson 2003
Dickinson JE, Evans SF. A comparison of oral misoprostol with vaginal
misoprostol administration in second trimester pregnancy termination for fetal
abnormality. Obstetrics & Gynecology 2003;101:1294 9.
Eppel 2005
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
10
Eppel W, Facchinetti F, Schleussner E, Piccinini F, Pizzi C, Gruber DM, et
al. Second trimester abortion using isosorbide mononitrate in addition to
gemeprost compared with gemeprost alone: a double blind randomized,
placebo controlled multicenter trial. American Journal of Obstetrics and
Gynecology 2005;192:856 61.
Feldman 2003
Feldman DM, Borgida AF, Rodis JF, Leo MV, Campbell WA. A randomized
comparison of two regimens of misoprostol for second trimester pregnancy
termination. American Journal of Obstetrics and Gynecology 2003;189:710 3.
Ghorab 1998
Ghorab MNM, El Helw BA. Second trimester termination of pregnancy by
extra amniotic prostaglandin F2alpha or endocervical misoprostol. Acta
Obstetricia et Gynecologica Scandinavica 1998;77:429 32.
Gonzalez 2001
Gonzalez JA, Carlan SJ, Alverson MW. Outpatient second trimester pregnancy
termination. Contraception 2001;63:89 93.
Grimes 2004
Grimes DA, Smith MS, Witham AD. Mifepristone and misoprostol versus
dilatation and evacuation for midtrimester abortion: a pilot randomised
controlled trial. BJOG: an international journal of obstetrics and gynaecology
2004;111:148 53.
Gronland 2002
Gronland A, Gronland L, Clevin L, Andersen B, Palmegren N, Lidegaard O.
Management of missed abortion: comparison of medical treatment with either
mifepristone + misoprostol or misoprostol alone with surgical evacuation. A
multi center trial in Copenhagen county, Denmark. Acta Obstetricia et
Gynecologica Scandinavica 2002;81:1060 5.
Hausler 1997
Häusler MCH, Koroschetz F, Tamussino K, Walcher W. Is a curettage after
spontaneous abortion still relevant. A prospective randomised study [Ist eine
Curettage nach Abortus completus noch zeitgemäb?. Eine prospektiv
randomisierte Studie]. Geburtshilfe und Frauenheilkunde 1997;57:396 9.
Herabutya 2005
Herabutya Y, Chanrachakul B, Punyavachira P. A randomised controlled trial
of 6 and 12 hourly administration of vaginal misoprostol for second trimester
pregnancy termination. BJOG: an international journal of obstetrics and
gynaecology 2005;112:1297 301.
Hidar 2001
Hidar S, Fekih M, Chaieb A, Bibi M, Mellouli R, Khairi H. Oxytocin and
misoprostol administered intravaginally for termination of pregnancy at 13 29
weeks of amenorrhea. A prospective randomized trial [Apport de l'association
d'ocytocine au misoprostol administre en intravaginal au cours des interruptions
de grossesses entre 13 et 29 semaines d'amenorrhee. Essai clinique prospectif
randomise]. Journal de Gynecologie, Obstetrique et Biologie de la
Reproduction 2001;30:439 43.
Hill 1991
Hill NCW, Selinger M, Ferguson J, MacKenzie IZ. Management of intra uterine
fetal death with vaginal administration of gemeprost or prostaglandin E2: a
random allocation controlled trial. Journal of Obstetrics and Gynaecology
1991;11:422 6.
Hogg 2000
Hogg B, Owen J. Laminaria versus extraamniotic saline infusion (EASI) for
cervical ripening and mid trimester labor induction. American Journal of
Obstetrics and Gynecology 2000;182(1 Pt 2):S135.
Jain 1994
Jain JK, Mishell DR. A comparison of intravaginal misoprostol with
prostaglandin E2 for termination of second trimester pregnancy. New England
Journal of Medicine 1994;331:290 3.
Jain 1999
Jain JK, Kuo J, Mishell DR. A comparison of two dosing regimens of
intravaginal misoprostol for second trimester pregnancy termination. Obstetrics
& Gynecology 1999;93:571 5.
Johnson 1997
Johnson N, Priestnall M, Marsay T, Ballard P, Watters J. A randomised trial
evaluating pain and bleeding after a first trimester miscarriage treated surgically
or medically. European Journal of Obstetrics & Gynecology and Reproductive
Biology 1997;72(2):213 5.
Kanhai 1989
* Kanhai HHH, Keirse MJNC. Induction of labour after fetal death: a
randomized controlled trial of two prostaglandin regimens. British Journal of
Obstetrics and Gynaecology 1989;96:1400 4.
Kanhai HHH, Keirse MJNC. Intravenous administration of sulfprostone for
the induction of labour after fetal death: a randomised comparison of two dose
schedules. Proceedings of 1st European Congress on Prostaglandins in
Reproduction; 1988 July 6 9; Vienna, Austria. 1988:45.
Kanhai HHH, Keirse MJNC. Intravenous administration of sulfprostone for
the induction of labour after fetal death: a randomised comparison of two dose
schedules. World Congress of Gynecology and Obstetrics; 1988 October 23 28;
Brazil. 1988:201 2.
Lippert 1978
Lippert TH, Luthi A. Induction of labour with prostaglandin E2 gel in cases
of intrauterine fetal death. Prostaglandins 1978;15:533 42.
Machtinger 2002
Machtinger R, Stockheim D, Goldenberg M, Soriano D, Atlas M, Seidman
DS. A randomized prospective study of misoprostol alone or combined with
mifepristone for treatment of first trimester spontaneous abortion. Fertility
and Sterility 2002;78(3 Suppl 1):S64.
Machtinger 2004
Machtinger R, Stockheim D, Shulman A, Dulitzki M, Schiff E, Seidman DS.
A randomized prospective study comparing the effectiveness of four protocols
for treatment of first trimester spontaneous abortion. Fertility and Sterility
2004;82 Suppl 2:S80.
Makhlouf 2003
Makhlouf AM, Al Hussaini TK, Habib DM, Makarem MH. Second trimester
pregnancy termination: comparison of three different methods. Journal of
Obstetrics and Gynaecology 2003;23:407 11.
Martin 1965
Martin RH, Menzies DN. Oestrogen therapy in missed abortion and labour.
Journal of Obstetrics and Gynaecology of the British Commonwealth
1965;62:256 8.
Nakintu 2001
Nakintu N. A comparative study of vaginal misoprostol and intravenous
oxytocin for induction of labour in women with intrauterine fetal death in
Mulago Hospital, Uganda. African Health Sciences 2001;1:55 9.
Ngai 2001
Ngai SW, Chan YM, Tang OS, Ho PC. Vaginal misoprostol as medical
treatment for first trimester spontaneous miscarriage. Human Reproduction
2001;16(7):1493 6.
Nuthalapaty 2004
Nuthalapaty F, Ramsey P, Biggio J, Owen J. Comparative efficacy of high
dose vaginal misoprostol versus concentrated oxytocin + low dose vaginal
misoprostol for mid trimester labor induction. American Journal of Obstetrics
and Gynecology 2004;191(6 Suppl 1):S73.
Nuutila 1997
Nuutila M, Toivonen J, Ylikorkala O, Halmesmaki E. A comparison between
two doses of intravaginal misoprostol and gemeprost for induction of
second trimester abortion. Obstetrics & Gynecology 1997;90:896 900.
Owen 1999
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
11
Owen J, Hauth JC. Vaginal misoprostol vs concentrated oxytocin plus low dose
prostaglandin E2 for second trimester pregnancy termination. Journal of
Maternal Fetal Medicine 1999;8:48 50.
Paraskevaides 1992
Paraskevaides E, Prendiville W, Stuart B, Scanaill SN, Walsh D, McGuinness
N, et al. Medical evacuation of first trimester (twelve weeks gestation)
incomplete abortion and missed abortion. Journal of Gynecologic Surgery
1992;8:159 63.
* Zhang J, Gilles JM, Barnhart K, Creinin MD, Westhoff C, Frederick MM,
et al. A comparison of medical management with misoprostol and surgical
management for early pregnancy failure. New England Journal of Medicine
2005;353:761 9.
Zhang J, Gilles K, Barnhart K, Creinin M, Westhoff C, Frederick M. Medical
management with misoprostol for early pregnancy failure: a multicenter,
randomized equivalence trial. Fertility and Sterility 2004;82 Suppl 2:S53 S54.
Referencias de los estudios pendientes de evaluación
Perry 1999
Perry KG, Rinehart BK, Terrone DA, Martin RW, May WL, Roberts WE.
Second trimester uterine evacuation: a comparison of intra amniotic
(15S) 15 methyl prostaglandin F2alpha and intravaginal misoprostol. American
Journal of Obstetrics and Gynecology 1999;181:1057 61.
Piotrowski 1979
Piotrowski J, Basta A, Klimczyk K, Malolepazy A, Dluzniewska M, Splawinski
JA. Indomethacin increases abortifacient effect of PGE2 in man. Prostaglandins
1979;17:451 9.
Pongsatha 2004
Pongsatha S, Tongsong T. Intravaginal misoprostol for pregnancy termination.
International Journal of Gynecology & Obstetrics 2004;87:176 7.
Ramsey 2004
Ramsey PS, Savage K, Lincoln T, Owen J. Vaginal misoprostol versus
concentrated oxytocin and vaginal PGE2 for second trimester labor induction.
Obstetrics & Gynecology 2004;104:138 45.
Roy 2003
Roy G, Ferreira E, Hudon L, Marquette G. The efficacy of oral versus vaginal
misoprostol for second trimester termination of pregnancy: a double blind,
randomized placebo controlled trial. American Journal of Obstetrics and
Gynecology 2003;189(6):S70.
Salamalekis 1990
Salamalekis E, Loghis C, Kassanos D, Traka A, Zourlas PA. Comparison of
extra amniotic prostaglandin F2alpha and dinoprostone use for labor induction
after second trimester intrauterine fetal death. Proceedings of 12th European
Congress of Perinatal Medicine; 1990; Lyon, France. 1990:228.
Su 2005
Su LL, Biswas A, Choolani M, Kalaichelvan V, Singh K. A prospective
randomized comparison of vaginal misoprostol versus intra amniotic
prostaglandins for midtrimester termination of pregnancy. American Journal
of Obstetrics and Gynecology 2005;193:1410 4.
Surita 1997
Surita FGC, Cecatti JG, Pinto e Silva JL. Misoprostol versus laminaria for
cervical ripening in intrauterine fetal death. Acta Obstetricia et Gynecologica
Scandinavica Supplement 1997;76(167:2):32.
Thavarasah 1986
Thavarasah AS, Almohdzar SA. Prostaglandin (F2alpha) in missed abortion.
Intravenous extra amniotic and intramuscular administration a randomized
study. Biological Research in Pregnancy 1986;7:106 10.
Toppozada 1994
Toppozada MK, Shaala SA, Anwar MY, Haiba NA, Abdrabbo S, El Absy
HM. Termination of pregnancy with fetal death in the second and third
trimesters the double balloon versus extra amniotic prostaglandin.
International Journal of Gynecology & Obstetrics 1994;45:269 73.
Aberdeen 1993
Henshaw RC, Hinshaw K, Smith NC, Templeton AA. The medical management
of miscarriage. Fertility Society of Australia / Australian Gynaecological
Endoscopy Society; 1995 November 19 25; Melbourne, Australia. 1995:FSA
75.
* Hinshaw K, Rispin N, Smith N, Templeton A. Medical versus surgical
management in first trimester miscarriage: a prospective, pragmatic random
allocation trial. Journal of Obstetrics and Gynaecology 1993;13:404 5.
Hinshaw K, Rispin R, Henshaw R, Smith N, Templeton A. Medical versus
surgical uterine evacuation in first trimester miscarriage: a prospective,
pragmatic randomised trial. 27th British Congress of Obstetrics and
Gynaecology; 1995 July 4 7; Dublin. 1995:4.
Hughes J, Ryan M, Hinshaw K, Henshaw R, Rispin R, Templeton A. The
costs of treating miscarriage: a comparison of medical and surgical
management. British Journal of Obstetrics and Gynaecology 1996;103:1217 21.
Rispin R, Hinshaw K, Henshaw R, Smith N, Templeton A. New aspects of
care in the management of miscarriage. Proceedings of Research in Midwifery
Conference; 1993 September 14; Birmingham, UK. 1993.
Bangkok 2003
Chittacharoen A, Herabutya Y, Punyavachira P. A randomized trial of oral
and vaginal misoprostol to manage delivery in cases of fetal death. Obstetrics
& Gynecology 2003;101:70 3.
Lahore 1999
Amjad T, Akhtar S. Termination of pregnancy with foetal death in second
trimester: Foley's catheter versus extra amniotic prostaglandins. Journal of
College of Physicians & Surgeons Pakistan 1999;9:403 5.
Rivero Lopez 1998
Rivero Lopez E, Marquez Maraver F, Duenas Diez JL, Cabezas Sanchez B.
Deferred miscarriage: effectiveness of intravaginal misoprostol versus laminaria
alone [Aborto diferido: eficacia del misoprostol intravaginal versus la aplicacion
de tallos de laminaria]. Progresos de Obstetricia y Ginecologia 1998;41:579 81.
Referencias de estudios en curso
Australia 2000
Louey K. Misoprostol for the medical management of miscarriage (RCT).
Personal communication 2000.
UK 1999
Trinder J. Miscarriage Treatment Study (MIST). National Research Register
www.nrr.nhs.uk (accessed 1999).
Referencias adicionales
Alfirevic 2001
Alfirevic Z. Oral misoprostol for induction of labour. Cochrane Database of
Systematic Reviews 2001, Issue 2. Art. No.: CD001338. DOI:
10.1002/14651858.CD001338.pub2.
Yapar 1996
Yapar EG, Senoz S, Urkutur M, Batioglu S, Gokmen O. Second trimester
pregnancy termination including fetal death: comparison of five different
methods. European Journal of Obstetrics & Gynecology and Reproductive
Biology 1996;69:97 102.
Ashok 1998
Ashok PW, Penney GC, Flett GM, Templeton A. An effective regimen for
early medical abortion: a report of 2000 consecutive cases. Human
Reproduction 1998;13:2962 5.
Zhang 2005
Baulieu 1986
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
12
Baulieu E, Ulmann A. Antiprogesterone activity of RU 486 and its
contragestive and other applications. Human Reproduction 1986;1:107 10.
Bugalho 1996
Bugalho A, Faundes A, Jamisse L, Usfa M, Maria E, Bique C. Evaluation of
the effectiveness of vaginal misoprostol to induce first trimester abortion.
Contraception 1996;53:244 6.
Cameron 1986
Cameron IT, Michie AF, Baird DT. Therapeutic abortion in early pregnancy
with antiprogestogen RU486 alone or in combination with prostaglandin
analogue (gemeprost). Contraception 1986;34(5):459 68.
Costa 1993
Costa SH, Vessey MP. Misoprostol and illegal abortion in Rio de Janeiro,
Brazil. Lancet 1993;341:1258 61.
Fonseca 1991
Fonseca W, Alencar AJC, Mota FSB, Coelho HLL. Misoprostol and congenital
malformations. Lancet 1991;338:56.
Grudzinskas 1995
Grudzinskas JG. Endocrinological and metabolical assessment of early
pregnancy. In: Chamberlain G editor(s). Turnbull's obstetrics. London: Pearson
Professional Ltd, 1995:185 93.
Gulmezoglu 2004
Gulmezoglu AM, Forna F, Villar J, Hofmeyr GJ. Prostaglandins for prevention
of postpartum haemorrhage. Cochrane Database of Systematic Reviews 2004,
Issue 1.
Hofmeyr 2003
Hofmeyr GJ, Gulmezoglu AM. Vaginal misoprostol for cervical ripening and
induction of labour. Cochrane Database of Systematic Reviews 2003, Issue 1.
Art. No.: CD000941. DOI: 10.1002/14651858.CD000941.
Howie 1995
Howie PG. Abortion and ectopic pregnancy. In: Whitfield CR editor(s).
Dewhurst's textbook of obstetrics and gynecology for postgraduates. Oxford:
Blackwell Science Ltd, 1995:140 63.
Kovacs 1984
Kovacs L, Sas M, Resch BA, Ugocsai G, Swahn ML, Bygdeman, et al.
Termination of very early pregnancy by RU 486 an antiprogestational
compound. Contraception 1984;29(5):399 410.
Kulier 2004
Kulier R, Gulmezoglu AM, Hofmeyr GJ, Cheng LN, Campana A. Medical
methods for first trimester abortion. Cochrane Database of Systematic Reviews
2004, Issue 1. Art. No.: CD002855. DOI: 10.1002/14651858.CD002855.pub3.
Mousa 2003
Mousa HA, Alfirevic Z. Treatment for primary postpartum haemorrhage.
Cochrane Database of Systematic Reviews 2003, Issue 1. Art. No.: CD003249.
DOI: 10.1002/14651858.CD003249.pub2.
Muzonzini 2004
Muzonzini G, Hofmeyr GJ. Buccal or sublingual misoprostol for cervical
ripening and induction of labour. Cochrane Database of Systematic Reviews
2004, Issue 4. Art. No.: CD004221. DOI: 10.1002/14651858.CD004221.pub2.
Nanda 2002
Nanda K, Peloggia A, Nanda G, Grimes D. Expectant care versus surgical
treatment for miscarriage. Cochrane Database of Systematic Reviews 2002,
Issue 1. Art. No.: CD003518. DOI: 10.1002/14651858.CD003518.pub2.
Neilson 1998
Neilson JP. Ultrasound for fetal assessment in early pregnancy. Cochrane
Database of Systematic Reviews 1998, Issue 4. Art. No.: CD000182. DOI:
10.1002/14651858.CD000182.
Norman 1991
Norman JE, Thong KJ, Baird DT. Uterine contractility and induction of
abortion in early pregnancy by misoprostol and mifepristone. Lancet
1991;338:1233 6.
Say 2002
Say L, Kulier R, Gulmezoglu AM, Campana A. Medical versus surgical
methods for first trimester termination of pregnancy. Cochrane Database of
Systematic Reviews 2002, Issue 4. Art. No.: CD003037. DOI:
10.1002/14651858.CD003037.pub2.
Senior 1993
Senior J, Marshall K, Sangha R, Clayton JK. In vitro characterisation of
prostanoid receptors on human myometrium at term pregnancy. British Journal
of Pharmacology 1993;108:501 6.
Simpson 1991
Simpson JL. Fetal wastage. In: Gabe SG, Simpson JL editor(s). Obsterics.
Normal and problem pregnancies. New York: Churchill Livingstone Inc,
1991:783 807.
Vazquez 2000
Vazquez JC, Hickey M, Neilson JP. Medical treatment for miscarriage.
Cochrane Database of Systematic Reviews 2000, Issue 3.
Zieman 1997
Zieman M, Fong SK, Benowitz NL, Bankster D, Darney PD. Absorption
kinetics of misoprostol with oral or vaginal administration. Obstetrics &
Gynecology 1997;90:88 92.
Referencias de los estudios incluidos en esta revisión
Al Inizi 2003 {sólo datos publicados}
Al Inizi SA, Ezimokhai M. Vaginal misoprostol versus dinoprostone for the
management of missed abortion. International Journal of Gynecology &
Obstetrics 2003;83:73 4.
Autry 1999 {sólo datos publicados}
Autry A, Jacobson G, Sandhu R, Isbill K. Medical management of non viable
early first trimester pregnancy. International Journal of Gynecology &
Obstetrics 1999;67(1):9 13.
Bagratee 2004 {sólo datos publicados}
Bagratee JS, Khullar V, Regan L, Moodley J, Kagoro H. A randomized
controlled trial comparing medical and expectant management of first trimester
miscarriage. Human Reproduction 2004;19:266 71.
Creinin 1997 {sólo datos publicados}
Creinin MD, Moyer R, Guido R. Misoprostol for medical evacuation of early
pregnancy failure. Obstetrics & Gynecology 1997;89:768 72.
Demetroulis 2001 {sólo datos publicados}
* Demetroulis C, Saridogan E, Kunde D, Naftalin AA. A prospective
randomized control trial comparing medical and surgical treatment for early
pregnancy failure. Human Reproduction 2001;16:365 9.
Demetroulis C, Saridogan E, Kunde D, Naftalin AA. A prospective randomized
control trial comparing medical and surgical treatment for early pregnancy
failure. XVI FIGO World Congress of Obstetrics and Gynecology; 2000 Sept
3 8; Washington DC, USA. 2000.
Egarter 1995 {sólo datos publicados}
Egarter C, Lederhilger J, Kurz C, Karas H, Reisenberger K. Gemeprost for
first trimester missed abortion. Archives of Gynecology and Obstetrics
1995;256:29 32.
Eng 1997* {sólo datos publicados}
Eng NS, Guan AC. Comparative study of intravaginal misoprostol with
gemeprost as an abortifacient in second trimester missed abortion. Australian
and New Zealand Journal of Obstetrics and Gynaecology 1997;37:331 4.
Fadalla 2004* {sólo datos publicados}
Fadalla FA, Mirghani OA, Adam I. Oral misoprostol vs vaginal misoprostol
for termination of pregnancy with intrauterine fetal demise in the
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
13
second trimester. International Journal of Gynecology & Obstetrics
2004;86:52 3.
Gilles 2004 {sólo datos publicados}
Barnhart KT, Bader T, Huang X, Frederick MM, Timbers KA, Zhang JJ.
Hormone pattern after misoprostol administration for a nonviable first trimester
gestation. Fertility and Sterility 2004;81:1099 105.
Creinin MD, Harwood B, Guido RS, Fox MC, Zhang J, NICHD Early
Pregnancy Failure Trial. Endometrial thickness after misoprostol use for early
pregnancy failure. International Journal of Gynecology & Obstetrics
2004;86:22 6.
Davis AR, Robilotto CM, Westhoff CL, Forman S, Zhang J, NICHD
Management of Early Pregnancy Failure Trial. Bleeding patterns after vaginal
misoprostol for treatment of early pregnancy failure. Human Reproduction
2004;19:1655 8.
Gilles J, Creinin MM, Barnhart KT, Westhoff C, Frederick MM, Zang J, et
al. Wet versus dry misoprostol application for treatment of early pregnancy
failure. Fertility and Sterility 2002;78:S64 S65.
* Gilles JM, Creinin MD, Barnhart K, Westhoff C, Frederick MM, Zhang J.
A randomized trial of saline solution moistened misoprostol versus dry
misoprostol for the first trimester pregnancy failure. American Journal of
Obstetrics and Gynecology 2004;190:389 94.
Kovavisarach E, Jamnansiri C. Intravaginal misoprostol 600mcg and 800mcg
for the treatment of early pregnancy failure. International Journal of
Gynecology & Obstetrics 2005;90:208 12.
Lelaidier 1993 {sólo datos publicados}
Lelaidier C, Baton Saint Mleux C, Fernandez H, Bourget P, Frydman R.
Mifepristone (RU 486) induces embryo expulsion in first trimester
non developing pregnancies: a prospective randomized trial. Human
Reproduction 1993;8:492 5.
Lister 2005 {sólo datos publicados}
Lister MS, Shaffer LET, Bell JG, Lutter KQ, Moorma KH. Randomized,
double blind, placebo controlled trial of vaginal misoprostol for management
of early pregnancy failures. American Journal of Obstetrics and Gynecology
2005;193:1338 43.
Muffley 2002 {sólo datos publicados}
Muffley PE, Stitely ML, Gherman RB. Early intrauterine pregnancy failure:
a randomized trial of medical versus surgical treatment. American Journal of
Obstetrics and Gynecology 2002;187:321 6.
Ngoc 2004 {sólo datos publicados}
Ngoc NTN, Blum J, Westheimer E, Quan TTV, Winikoff B. Medical treatment
of missed abortion using misoprostol. International Journal of Gynecology &
Obstetrics 2004;87:138 42.
Graziosi 2004 {sólo datos publicados}
Graziosi GCM, Bruinse HW, Reuwer PJH, Teteringen O, Mol BWJ. Fertility
outcome after a randomized trial comparing curettage with misoprostol for
treatment of early pregnancy failure. Human Reproduction 2005;20:1749 50.
Nielsen 1999 {sólo datos publicados}
Nielsen S, Hahlin M, Platz Christensen J. Expectant management or
pharmacological treatment for first trimester spontaneous abortion: a
randomised trial. Acta Obstetricia et Gynecologica Scandinavica
1997;76(167:2):77.
Graziosi GCM, Bruinse HW, Reuwer PJH, van Kessel PH, Westerweel PE,
Mol BW. Misoprostol versus curettage in women with early pregnancy failure:
impact on women's health related quality of life. A randomized controlled
trial. Human Reproduction 2005;20:2340 7.
* Nielsen S, Hahlin M, Platz Christensen J. Randomised trial comparing
expectant with medical management for first trimester miscarriages. British
Journal of Obstetrics and Gynaecology 1999;106:804 7.
* Graziosi GCM, Mol BWJ, Reuwer PJH, Drogtrop A, Bruinse HW.
Misoprostol versus curettage in women with early pregnancy failure after
initial expectant management: a randomized trial. Human Reproduction
2004;19:1894 9.
Niromanesh 2005* {sólo datos publicados}
Niromanesh S, Hashemi Feasharaki M, Mosavi Jarrahi A. Second trimester
abortion using intravaginal misoprostol. International Journal of Gynecology
& Obstetrics 2005;89:276 7.
Graziosi GCM, van der Steeg JW, Reuwer PHW, Drogtrop AP, Bruinse HW,
Mol BWJ. Economic evaluation of misoprostol in the treatment of early
pregnancy failure compared to curettage after an expectant management.
Human Reproduction 2005;20:1067 71.
Tang 2003 {sólo datos publicados}
Tang OS, Lau WNT, Ng EHY, Lee SWH, Ho PC. A prospective randomized
study to compare the use of repeated doses of vaginal with sublingual
misoprostol in the management of first trimester silent miscarriage. Human
Reproduction 2003;18:176 81.
Heard 2002 {sólo datos publicados}
Heard MJ, Stewart GM, Buster JE, Carson SA, Miller HJ. Outpatient
management of missed abortion with vaginal misoprostol [abstract]. Obstetrics
& Gynecology 2002;99(4 Suppl):20S.
Herabutya 1997 {sólo datos publicados}
Herabutya Y, O Prasertsawat P. Misoprostol in the management of missed
abortion. International Journal of Gynecology & Obstetrics 1997;56:263 6.
Jain 1996* {sólo datos publicados}
Jain JK, Mishell DR. A comparison of misoprostol with and without laminaria
tents for induction of second trimester abortion. American Journal of Obstetrics
and Gynecology 1996;175:173 7.
Kara 1999* {sólo datos publicados}
Kara M, Ozden S, Eroglu M, Cetin A, Arioglu P. Comparison of misoprostol
and dinoproston administration for the induction of labour in second trimester
pregnancies in cases of intrauterine fetal loss. Italian Journal of Gynecology
and Obstetrics 1999;1:13 6.
Kovavisarach 2002 {sólo datos publicados}
Kovavisarach E, Sathapanachai U. Intravaginal 400 micrograms misoprostol
for pregnancy termination in cases of blighted ovum: a randomised controlled
trial. Australian and New Zealand Journal of Obstetrics and Gynaecology
2002;42:161 3.
Wood 2002 {sólo datos publicados}
Wood SL, Brain PH. Medical management of missed abortion: a randomized
clinical trial. Obstetrics & Gynecology 2002;99:563 6.
References to studies excluded from this review
Abdel Fattah 1997
Abdel Fattah IH. PGE1 analogue for the induction of midtrimester abortion
in cases of intrauterine fetal death. Acta Obstetricia et Gynecologica
Scandinavica Supplement 1997;76(167:2):26.
Almog 2005
Almog B, Levin I, Winkler N, Fainaru O, Pauzner D, Lessing JB, et al. The
contribution of laminaria placement for cervical ripening in second trimester
termination of pregnancy induced by intra amniotic injection of prostaglandin
F2alpha followed by concentrated oxytocin infusion. European Journal of
Obstetrics & Gynecology and Reproductive Biology 2005;118:32 5.
Anderman 2000
Anderman S, Jaschevatzky OE, Ballas S. Comparison between a double balloon
device and the foley catheter in extraamniotic prostaglandin F2a infusion for
termination of midtrimester missed abortion. XVI FIGO World Congress of
Obstetrics & Gynecology; 2000 Sept 3 8; Washington DC, USA. 2000:162.
Avila Vergara 1997
Kovavisarach 2005 {sólo datos publicados}
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
14
Avila Vergara MA, Morgan Ortiz F, Fragoza Sosa O, Haro Garcia L. Cervical
labor induction with prostaglandin E2 in patients with fetal death [Maduracion
cervical con prostaglandina E2 en pacientes con feto muerto]. Ginecologia y
Obstetricia de Mexico 1997;65:155 8.
Bebbington 2002
Bebbington MW, Kent N, Lim K, Gagnon A, Delisle MF, Tessier F, et al. A
randomized controlled trial comparing two protocols for the use of misoprostol
in midtrimester pregnancy termination. American Journal of Obstetrics and
Gynecology 2002;187:853 7.
Cabrol 1990
Cabrol D, Dubois C, Cronje H, Gonnet JM, Guillot M, Maria B, et al. Induction
of labour with mifepristone (RU 486) in intrauterine fetal death. American
Journal of Obstetrics and Gynecology 1990;163:540 2.
Clevin 2001
Clevin L, Munk T, Hansen TR. Spontaneous abortion. Drug treatment versus
surgery [Spontan abort. Medicinsk versus kirurgisk behandling]. Ugeskrift for
Laeger 2001;163(15):2136 9.
David 2003
David M, Chen FCK, Lichtenegger W. NO donor nitroglycerin versus the
prostaglandin gemeprost for cervical ripening in first trimester missed abortion.
International Journal of Gynecology & Obstetrics 2003;83:71 2.
Dickinson 1998
Dickinson JE, Godfrey M, Evans SF. Efficacy of intravaginal misoprostol in
second trimester pregnancy termination: a randomized controlled trial. Journal
of Maternal Fetal Medicine 1998;7:115 9.
Dickinson 2002
Dickinson JE, Evans SF. The optimization of intravaginal misoprostol dosing
schedules in second trimester pregnancy termination. American Journal of
Obstetrics and Gynecology 2002;186:470 4.
Dickinson 2003
Dickinson JE, Evans SF. A comparison of oral misoprostol with vaginal
misoprostol administration in second trimester pregnancy termination for fetal
abnormality. Obstetrics & Gynecology 2003;101:1294 9.
Eppel 2005
Eppel W, Facchinetti F, Schleussner E, Piccinini F, Pizzi C, Gruber DM, et
al. Second trimester abortion using isosorbide mononitrate in addition to
gemeprost compared with gemeprost alone: a double blind randomized,
placebo controlled multicenter trial. American Journal of Obstetrics and
Gynecology 2005;192:856 61.
Feldman 2003
Feldman DM, Borgida AF, Rodis JF, Leo MV, Campbell WA. A randomized
comparison of two regimens of misoprostol for second trimester pregnancy
termination. American Journal of Obstetrics and Gynecology 2003;189:710 3.
Ghorab 1998
Ghorab MNM, El Helw BA. Second trimester termination of pregnancy by
extra amniotic prostaglandin F2alpha or endocervical misoprostol. Acta
Obstetricia et Gynecologica Scandinavica 1998;77:429 32.
Gonzalez 2001
Gonzalez JA, Carlan SJ, Alverson MW. Outpatient second trimester pregnancy
termination. Contraception 2001;63:89 93.
Grimes 2004
Grimes DA, Smith MS, Witham AD. Mifepristone and misoprostol versus
dilatation and evacuation for midtrimester abortion: a pilot randomised
controlled trial. BJOG: an international journal of obstetrics and gynaecology
2004;111:148 53.
Gronland 2002
Gronland A, Gronland L, Clevin L, Andersen B, Palmegren N, Lidegaard O.
Management of missed abortion: comparison of medical treatment with either
mifepristone + misoprostol or misoprostol alone with surgical evacuation. A
multi center trial in Copenhagen county, Denmark. Acta Obstetricia et
Gynecologica Scandinavica 2002;81:1060 5.
Hausler 1997
Häusler MCH, Koroschetz F, Tamussino K, Walcher W. Is a curettage after
spontaneous abortion still relevant. A prospective randomised study [Ist eine
Curettage nach Abortus completus noch zeitgemäb?. Eine prospektiv
randomisierte Studie]. Geburtshilfe und Frauenheilkunde 1997;57:396 9.
Herabutya 2005
Herabutya Y, Chanrachakul B, Punyavachira P. A randomised controlled trial
of 6 and 12 hourly administration of vaginal misoprostol for second trimester
pregnancy termination. BJOG: an international journal of obstetrics and
gynaecology 2005;112:1297 301.
Hidar 2001
Hidar S, Fekih M, Chaieb A, Bibi M, Mellouli R, Khairi H. Oxytocin and
misoprostol administered intravaginally for termination of pregnancy at 13 29
weeks of amenorrhea. A prospective randomized trial [Apport de l'association
d'ocytocine au misoprostol administre en intravaginal au cours des interruptions
de grossesses entre 13 et 29 semaines d'amenorrhee. Essai clinique prospectif
randomise]. Journal de Gynecologie, Obstetrique et Biologie de la
Reproduction 2001;30:439 43.
Hill 1991
Hill NCW, Selinger M, Ferguson J, MacKenzie IZ. Management of intra uterine
fetal death with vaginal administration of gemeprost or prostaglandin E2: a
random allocation controlled trial. Journal of Obstetrics and Gynaecology
1991;11:422 6.
Hogg 2000
Hogg B, Owen J. Laminaria versus extraamniotic saline infusion (EASI) for
cervical ripening and mid trimester labor induction. American Journal of
Obstetrics and Gynecology 2000;182(1 Pt 2):S135.
Jain 1994
Jain JK, Mishell DR. A comparison of intravaginal misoprostol with
prostaglandin E2 for termination of second trimester pregnancy. New England
Journal of Medicine 1994;331:290 3.
Jain 1999
Jain JK, Kuo J, Mishell DR. A comparison of two dosing regimens of
intravaginal misoprostol for second trimester pregnancy termination. Obstetrics
& Gynecology 1999;93:571 5.
Johnson 1997
Johnson N, Priestnall M, Marsay T, Ballard P, Watters J. A randomised trial
evaluating pain and bleeding after a first trimester miscarriage treated surgically
or medically. European Journal of Obstetrics & Gynecology and Reproductive
Biology 1997;72(2):213 5.
Kanhai 1989
* Kanhai HHH, Keirse MJNC. Induction of labour after fetal death: a
randomized controlled trial of two prostaglandin regimens. British Journal of
Obstetrics and Gynaecology 1989;96:1400 4.
Kanhai HHH, Keirse MJNC. Intravenous administration of sulfprostone for
the induction of labour after fetal death: a randomised comparison of two dose
schedules. Proceedings of 1st European Congress on Prostaglandins in
Reproduction; 1988 July 6 9; Vienna, Austria. 1988:45.
Kanhai HHH, Keirse MJNC. Intravenous administration of sulfprostone for
the induction of labour after fetal death: a randomised comparison of two dose
schedules. World Congress of Gynecology and Obstetrics; 1988 October 23 28;
Brazil. 1988:201 2.
Lippert 1978
Lippert TH, Luthi A. Induction of labour with prostaglandin E2 gel in cases
of intrauterine fetal death. Prostaglandins 1978;15:533 42.
Machtinger 2002
Machtinger R, Stockheim D, Goldenberg M, Soriano D, Atlas M, Seidman
DS. A randomized prospective study of misoprostol alone or combined with
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
15
mifepristone for treatment of first trimester spontaneous abortion. Fertility
and Sterility 2002;78(3 Suppl 1):S64.
Machtinger 2004
Machtinger R, Stockheim D, Shulman A, Dulitzki M, Schiff E, Seidman DS.
A randomized prospective study comparing the effectiveness of four protocols
for treatment of first trimester spontaneous abortion. Fertility and Sterility
2004;82 Suppl 2:S80.
Makhlouf 2003
Makhlouf AM, Al Hussaini TK, Habib DM, Makarem MH. Second trimester
pregnancy termination: comparison of three different methods. Journal of
Obstetrics and Gynaecology 2003;23:407 11.
Martin 1965
Martin RH, Menzies DN. Oestrogen therapy in missed abortion and labour.
Journal of Obstetrics and Gynaecology of the British Commonwealth
1965;62:256 8.
Nakintu 2001
Nakintu N. A comparative study of vaginal misoprostol and intravenous
oxytocin for induction of labour in women with intrauterine fetal death in
Mulago Hospital, Uganda. African Health Sciences 2001;1:55 9.
Ngai 2001
Ngai SW, Chan YM, Tang OS, Ho PC. Vaginal misoprostol as medical
treatment for first trimester spontaneous miscarriage. Human Reproduction
2001;16(7):1493 6.
Nuthalapaty 2004
Nuthalapaty F, Ramsey P, Biggio J, Owen J. Comparative efficacy of high
dose vaginal misoprostol versus concentrated oxytocin + low dose vaginal
misoprostol for mid trimester labor induction. American Journal of Obstetrics
and Gynecology 2004;191(6 Suppl 1):S73.
Nuutila 1997
Nuutila M, Toivonen J, Ylikorkala O, Halmesmaki E. A comparison between
two doses of intravaginal misoprostol and gemeprost for induction of
second trimester abortion. Obstetrics & Gynecology 1997;90:896 900.
Owen 1999
Owen J, Hauth JC. Vaginal misoprostol vs concentrated oxytocin plus low dose
prostaglandin E2 for second trimester pregnancy termination. Journal of
Maternal Fetal Medicine 1999;8:48 50.
Paraskevaides 1992
Paraskevaides E, Prendiville W, Stuart B, Scanaill SN, Walsh D, McGuinness
N, et al. Medical evacuation of first trimester (twelve weeks gestation)
incomplete abortion and missed abortion. Journal of Gynecologic Surgery
1992;8:159 63.
Perry 1999
Perry KG, Rinehart BK, Terrone DA, Martin RW, May WL, Roberts WE.
Second trimester uterine evacuation: a comparison of intra amniotic
(15S) 15 methyl prostaglandin F2alpha and intravaginal misoprostol. American
Journal of Obstetrics and Gynecology 1999;181:1057 61.
Piotrowski 1979
Piotrowski J, Basta A, Klimczyk K, Malolepazy A, Dluzniewska M, Splawinski
JA. Indomethacin increases abortifacient effect of PGE2 in man. Prostaglandins
1979;17:451 9.
Pongsatha 2004
Pongsatha S, Tongsong T. Intravaginal misoprostol for pregnancy termination.
International Journal of Gynecology & Obstetrics 2004;87:176 7.
Ramsey 2004
Ramsey PS, Savage K, Lincoln T, Owen J. Vaginal misoprostol versus
concentrated oxytocin and vaginal PGE2 for second trimester labor induction.
Obstetrics & Gynecology 2004;104:138 45.
Roy 2003
Roy G, Ferreira E, Hudon L, Marquette G. The efficacy of oral versus vaginal
misoprostol for second trimester termination of pregnancy: a double blind,
randomized placebo controlled trial. American Journal of Obstetrics and
Gynecology 2003;189(6):S70.
Salamalekis 1990
Salamalekis E, Loghis C, Kassanos D, Traka A, Zourlas PA. Comparison of
extra amniotic prostaglandin F2alpha and dinoprostone use for labor induction
after second trimester intrauterine fetal death. Proceedings of 12th European
Congress of Perinatal Medicine; 1990; Lyon, France. 1990:228.
Su 2005
Su LL, Biswas A, Choolani M, Kalaichelvan V, Singh K. A prospective
randomized comparison of vaginal misoprostol versus intra amniotic
prostaglandins for midtrimester termination of pregnancy. American Journal
of Obstetrics and Gynecology 2005;193:1410 4.
Surita 1997
Surita FGC, Cecatti JG, Pinto e Silva JL. Misoprostol versus laminaria for
cervical ripening in intrauterine fetal death. Acta Obstetricia et Gynecologica
Scandinavica Supplement 1997;76(167:2):32.
Thavarasah 1986
Thavarasah AS, Almohdzar SA. Prostaglandin (F2alpha) in missed abortion.
Intravenous extra amniotic and intramuscular administration a randomized
study. Biological Research in Pregnancy 1986;7:106 10.
Toppozada 1994
Toppozada MK, Shaala SA, Anwar MY, Haiba NA, Abdrabbo S, El Absy
HM. Termination of pregnancy with fetal death in the second and third
trimesters the double balloon versus extra amniotic prostaglandin.
International Journal of Gynecology & Obstetrics 1994;45:269 73.
Yapar 1996
Yapar EG, Senoz S, Urkutur M, Batioglu S, Gokmen O. Second trimester
pregnancy termination including fetal death: comparison of five different
methods. European Journal of Obstetrics & Gynecology and Reproductive
Biology 1996;69:97 102.
Zhang 2005
* Zhang J, Gilles JM, Barnhart K, Creinin MD, Westhoff C, Frederick MM,
et al. A comparison of medical management with misoprostol and surgical
management for early pregnancy failure. New England Journal of Medicine
2005;353:761 9.
Zhang J, Gilles K, Barnhart K, Creinin M, Westhoff C, Frederick M. Medical
management with misoprostol for early pregnancy failure: a multicenter,
randomized equivalence trial. Fertility and Sterility 2004;82 Suppl 2:S53 S54.
Referencias de los estudios pendientes de evaluación
Aberdeen 1993
Henshaw RC, Hinshaw K, Smith NC, Templeton AA. The medical management
of miscarriage. Fertility Society of Australia / Australian Gynaecological
Endoscopy Society; 1995 November 19 25; Melbourne, Australia. 1995:FSA
75.
* Hinshaw K, Rispin N, Smith N, Templeton A. Medical versus surgical
management in first trimester miscarriage: a prospective, pragmatic random
allocation trial. Journal of Obstetrics and Gynaecology 1993;13:404 5.
Hinshaw K, Rispin R, Henshaw R, Smith N, Templeton A. Medical versus
surgical uterine evacuation in first trimester miscarriage: a prospective,
pragmatic randomised trial. 27th British Congress of Obstetrics and
Gynaecology; 1995 July 4 7; Dublin. 1995:4.
Hughes J, Ryan M, Hinshaw K, Henshaw R, Rispin R, Templeton A. The
costs of treating miscarriage: a comparison of medical and surgical
management. British Journal of Obstetrics and Gynaecology 1996;103:1217 21.
Rispin R, Hinshaw K, Henshaw R, Smith N, Templeton A. New aspects of
care in the management of miscarriage. Proceedings of Research in Midwifery
Conference; 1993 September 14; Birmingham, UK. 1993.
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
16
Bangkok 2003
Chittacharoen A, Herabutya Y, Punyavachira P. A randomized trial of oral
and vaginal misoprostol to manage delivery in cases of fetal death. Obstetrics
& Gynecology 2003;101:70 3.
Hofmeyr 2003
Hofmeyr GJ, Gulmezoglu AM. Vaginal misoprostol for cervical ripening and
induction of labour. Cochrane Database of Systematic Reviews 2003, Issue 1.
Art. No.: CD000941. DOI: 10.1002/14651858.CD000941.
Lahore 1999
Amjad T, Akhtar S. Termination of pregnancy with foetal death in second
trimester: Foley's catheter versus extra amniotic prostaglandins. Journal of
College of Physicians & Surgeons Pakistan 1999;9:403 5.
Howie 1995
Howie PG. Abortion and ectopic pregnancy. In: Whitfield CR editor(s).
Dewhurst's textbook of obstetrics and gynecology for postgraduates. Oxford:
Blackwell Science Ltd, 1995:140 63.
Rivero Lopez 1998
Rivero Lopez E, Marquez Maraver F, Duenas Diez JL, Cabezas Sanchez B.
Deferred miscarriage: effectiveness of intravaginal misoprostol versus laminaria
alone [Aborto diferido: eficacia del misoprostol intravaginal versus la aplicacion
de tallos de laminaria]. Progresos de Obstetricia y Ginecologia 1998;41:579 81.
Kovacs 1984
Kovacs L, Sas M, Resch BA, Ugocsai G, Swahn ML, Bygdeman, et al.
Termination of very early pregnancy by RU 486 an antiprogestational
compound. Contraception 1984;29(5):399 410.
Referencias de estudios en curso
Australia 2000
Louey K. Misoprostol for the medical management of miscarriage (RCT).
Personal communication 2000.
UK 1999
Trinder J. Miscarriage Treatment Study (MIST). National Research Register
www.nrr.nhs.uk (accessed 1999).
Referencias adicionales
Alfirevic 2001
Alfirevic Z. Oral misoprostol for induction of labour. Cochrane Database of
Systematic Reviews 2001, Issue 2. Art. No.: CD001338. DOI:
10.1002/14651858.CD001338.pub2.
Ashok 1998
Ashok PW, Penney GC, Flett GM, Templeton A. An effective regimen for
early medical abortion: a report of 2000 consecutive cases. Human
Reproduction 1998;13:2962 5.
Baulieu 1986
Baulieu E, Ulmann A. Antiprogesterone activity of RU 486 and its
contragestive and other applications. Human Reproduction 1986;1:107 10.
Bugalho 1996
Bugalho A, Faundes A, Jamisse L, Usfa M, Maria E, Bique C. Evaluation of
the effectiveness of vaginal misoprostol to induce first trimester abortion.
Contraception 1996;53:244 6.
Cameron 1986
Cameron IT, Michie AF, Baird DT. Therapeutic abortion in early pregnancy
with antiprogestogen RU486 alone or in combination with prostaglandin
analogue (gemeprost). Contraception 1986;34(5):459 68.
Costa 1993
Costa SH, Vessey MP. Misoprostol and illegal abortion in Rio de Janeiro,
Brazil. Lancet 1993;341:1258 61.
Fonseca 1991
Fonseca W, Alencar AJC, Mota FSB, Coelho HLL. Misoprostol and congenital
malformations. Lancet 1991;338:56.
Grudzinskas 1995
Grudzinskas JG. Endocrinological and metabolical assessment of early
pregnancy. In: Chamberlain G editor(s). Turnbull's obstetrics. London: Pearson
Professional Ltd, 1995:185 93.
Gulmezoglu 2004
Gulmezoglu AM, Forna F, Villar J, Hofmeyr GJ. Prostaglandins for prevention
of postpartum haemorrhage. Cochrane Database of Systematic Reviews 2004,
Issue 1.
Kulier 2004
Kulier R, Gulmezoglu AM, Hofmeyr GJ, Cheng LN, Campana A. Medical
methods for first trimester abortion. Cochrane Database of Systematic Reviews
2004, Issue 1. Art. No.: CD002855. DOI: 10.1002/14651858.CD002855.pub3.
Mousa 2003
Mousa HA, Alfirevic Z. Treatment for primary postpartum haemorrhage.
Cochrane Database of Systematic Reviews 2003, Issue 1. Art. No.: CD003249.
DOI: 10.1002/14651858.CD003249.pub2.
Muzonzini 2004
Muzonzini G, Hofmeyr GJ. Buccal or sublingual misoprostol for cervical
ripening and induction of labour. Cochrane Database of Systematic Reviews
2004, Issue 4. Art. No.: CD004221. DOI: 10.1002/14651858.CD004221.pub2.
Nanda 2002
Nanda K, Peloggia A, Nanda G, Grimes D. Expectant care versus surgical
treatment for miscarriage. Cochrane Database of Systematic Reviews 2002,
Issue 1. Art. No.: CD003518. DOI: 10.1002/14651858.CD003518.pub2.
Neilson 1998
Neilson JP. Ultrasound for fetal assessment in early pregnancy. Cochrane
Database of Systematic Reviews 1998, Issue 4. Art. No.: CD000182. DOI:
10.1002/14651858.CD000182.
Norman 1991
Norman JE, Thong KJ, Baird DT. Uterine contractility and induction of
abortion in early pregnancy by misoprostol and mifepristone. Lancet
1991;338:1233 6.
Say 2002
Say L, Kulier R, Gulmezoglu AM, Campana A. Medical versus surgical
methods for first trimester termination of pregnancy. Cochrane Database of
Systematic Reviews 2002, Issue 4. Art. No.: CD003037. DOI:
10.1002/14651858.CD003037.pub2.
Senior 1993
Senior J, Marshall K, Sangha R, Clayton JK. In vitro characterisation of
prostanoid receptors on human myometrium at term pregnancy. British Journal
of Pharmacology 1993;108:501 6.
Simpson 1991
Simpson JL. Fetal wastage. In: Gabe SG, Simpson JL editor(s). Obsterics.
Normal and problem pregnancies. New York: Churchill Livingstone Inc,
1991:783 807.
Vazquez 2000
Vazquez JC, Hickey M, Neilson JP. Medical treatment for miscarriage.
Cochrane Database of Systematic Reviews 2000, Issue 3.
Zieman 1997
Zieman M, Fong SK, Benowitz NL, Bankster D, Darney PD. Absorption
kinetics of misoprostol with oral or vaginal administration. Obstetrics &
Gynecology 1997;90:88 92.
* Indica la publicación principal para el estudio
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
17
TA B L A S
Características de los estudios incluidos
Estudio
Al Inizi 2003
Métodos
"Asignación aleatoria". Se desconocen los detalles.
Participantes
Sesenta mujeres con embarazos no viables en los primeros meses de gestación, diagnosticados por ecografía.
Intervenciones
Se administró una dosis de 400 mcg de misoprostol vaginal dos veces por día hasta alcanzar un máximo de
1600 mcg (n = 27) versus comprimidos vaginales de dinoprostona (PGE2) administrados cada 6 horas hasta
alcanzar un máximo de 36 mg (n = 33).
Resultados
Aborto espontáneo completo/necesidad de evacuación quirúrgica.
Notas
Se estableció contacto con los autores.
Ocultamiento de la asignación
B – Poco claro
Estudio
Autry 1999
Métodos
Aleatorización mediante tablas de números aleatorios. El ocultamiento de la asignación se logró con el uso de sobres opacos cerrados
numerados secuencialmente, que se entregaron en el momento del reclutamiento en el estudio. Análisis por intención de tratar.
Participantes
Veintiún mujeres con diagnóstico de embarazo intrauterino no viable de hasta 49 días de gestación. La evidencia de no viabilidad
incluyó uno de los siguientes hallazgos en la ecografía transvaginal: 1) diámetro medio del saco gestacional superior a 18 mm y sin
polo embrionario; 2) polo embrionario de 5 10 mm sin actividad cardiaca; 3) saco gestacional intrauterino con títulos anormales de
hCG. Otros criterios de inclusión: 1) 18 años de edad o más; 2) cuello uterino cerrado al realizar el tacto vaginal; 3) sin intolerancia
o alergia conocida al misoprostol o al metotrexato; 4) hemoglobina de 9 g/dl o superior; 5) recuento plaquetario de 100,000/mcl o
superior; 6) sin antecedentes de trastornos de la coagulación; 7) sin enfermedad hepática o renal activa; 8) capacidad o disposición
para cumplir con el cronograma de visitas; 9) hCG inferior a 40 000 UI/l; y 10) fácil acceso a un teléfono o al transporte.
Intervenciones
Grupo combinado (n = 12): una dosis de metotrexato de 50 mg/m2 de superficie corporal por vía intramuscular (día 1) seguida dos
días después (día 3) de 800 mcg de misoprostol vaginal (por introducción vaginal de cuatro comprimidos de 200 mcg de misoprostol).
Si el saco gestacional estaba presente se repetía el misoprostol vaginal. Grupo que recibió misoprostol como único fármaco (n = 9):
cuatro comprimidos de 200 mcg introducidos en la vagina el día 1. El resto del seguimiento fue similar al del grupo combinado.
Resultados
Aborto completo logrado con éxito: metotrexato más misoprostol 12/12 versus misoprostol solo 8/9. No se administraron transfusiones
de sangre ni antibióticos. Prueba de embarazo en orina positiva en la consulta de seguimiento inicial: 2/9 versus 7/7. Alivio del
dolor: 4/12 versus 4/9.
Notas
Wisconsin, Milwaukee, USA. Todas las mujeres recibieron: 1) receta para 10 comprimidos de acetaminofeno con codeína (300
mg/30 mg) y 8 comprimidos de ibuprofeno (600 mg); 2) hoja de instrucciones con el número de teléfono para comunicarse con el
médico las 24 horas/día y una planilla para registrar diariamente los síntomas, efectos secundarios y uso de analgésicos. También
se incluyen los datos sobre los efectos secundarios (cefalea, náuseas y emesis) y el nivel de satisfacción de las mujeres no se incluye
como dato separado. Los autores concluyen que ambos tratamientos son efectivos para la evacuación completa de un embarazo no
viable en los primeros tres meses de gestación y que representan una alternativa razonable para las mujeres que desean evitar la
cirugía.
Ocultamiento de la
asignación
A – Adecuado
Estudio
Bagratee 2004
Métodos
Asignación aleatoria a partir de una lista de números de estudios generada por computadora. Sobres numerados que
contengan misoprostol o placebo.
Participantes
Ciento cuatro mujeres que asistieron a la Early Pregnancy Unit, St Mary's Hospital con aborto espontáneo incompleto o
falla precoz de embarazo en los primeros meses < 13 semanas.
Intervenciones
600 mcg de misoprostol (n = 52) o placebo [conducta expectante] (n = 52). La segunda dosis se administra el día siguiente
a menos que durante ese lapso haya ocurrido un aborto espontáneo completo. Revisar el día 7 y realizar la evacuación
quirúrgica si el aborto no es completo. Revisión adicional el día 14.
Resultados
Primarios: aborto espontáneo completo sin necesidad de una evacuación de los restos ovulares retenidos el día 7. Resultados
secundarios: clínicos, efectos secundarios, satisfacción y elecciones futuras.
Notas
El resultado primario se informó para embarazos no viables y abortos incompletos mientras que no ocurrió lo mismo para
los resultados secundarios. Se agregarán si los autores pueden aportar los datos por separado para embarazos no viables
y abortos espontáneos incompletos.
Ocultamiento de la asignación
A – Adecuado
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
18
Estudio
Creinin 1997
Métodos
Sobres secuenciales numerados, cerrados, que contenían instrucciones basadas en una tabla de números aleatorios
generados por computadora.
Participantes
Veinte mujeres con embarazos no viables diagnosticados por ecografía transvaginal, < 9 semanas, cuello uterino
cerrado, sin contraindicaciones en cuanto al uso del misoprostol, sin hemorragia profusa.
Intervenciones
Dosis de 400 mcg de misoprostol oral, repetida después de 24 horas si no se había expulsado el embarazo (n = 12);
800 mcg de misoprostol vaginal repetida después de 24 horas si era necesario (tal como se describe anteriormente)
(n = 8). Si después de 48 horas el tratamiento no era satisfactorio, se ofrecía evacuación quirúrgica a todas las mujeres
de ambos grupos.
Resultados
Aborto espontáneo, dolor (escala análoga visual), efectos secundarios.
Notas
Estudio piloto.
Ocultamiento de la asignación
A – Adecuado
Estudio
Demetroulis 2001
Métodos
Aleatorización generada por computadora, ocultamiento de la asignación por medio de sobres opacos cerrados. No se
intentó un enmascaramiento dadas las diferencias manifiestas entre la intervención clínica y la quirúrgica.
Participantes
Ochenta mujeres con aborto incompleto o embarazo anembrionado o aborto retenido inferior a 13 semanas, diagnosticado
por ecografía. Los datos en esta revisión se extrajeron sólo del subgrupo de embarazos no viables (n = 50) y no del subgrupo
con abortos incompletos. Las mujeres eran examinadas entre 8 y 10 horas luego del tratamiento clínico; si al hacer la
evaluación ecográfica el útero se encontraba vacío, se les daba de alta, de lo contrario se programaba la evacuación
quirúrgica.
Intervenciones
Una sola dosis de 800 mcg de misoprostol vaginal (n = 26) versus evacuación quirúrgica del útero (n = 24).
Resultados
Necesidad de evacuación quirúrgica, síntomas como dolor y sangrado, "satisfacción".
Notas
Se estableció contacto con los autores para obtener información sobre los resultados según la indicación para el tratamiento.
Sólo los datos utilizables actualmente disponibles se refieren a la incidencia de la evacuación quirúrgica.
Ocultamiento de la asignación
A –adecuado
Estudio
Egarter 1995
Métodos
Asignación aleatoria de las mujeres, sin detalles.
Participantes
Ochenta y siete mujeres en Austria con embarazos no viables entre las 8 y 12 semanas de gestación,
diagnosticados por ecografía.
Intervenciones
Dosis de 1 mg de gemeprost vaginal cada 3 horas hasta alcanzar un máximo de 3 mg diarios por 2 días
(n = 43) versus legrado uterino (n = 44).
Resultados
Necesidad de realizar un legrado quirúrgico. Efectos adversos.
Notas
Ocultamiento de la asignación
B – poco claro
Estudio
Eng 1997*
Métodos
La aleatorización se realizó "extrayendo a ciegas de una caja un sobre cerrado que contenía un número". La asignación
al tratamiento dependió de que el número fuera par o impar.
Participantes
Cincuenta mujeres con muerte fetal intrauterina de 13 a 26 semanas de gestación.
Intervenciones
Una dosis de 200 mcg de misoprostol vaginal cada 3 horas hasta alcanzar una dosis máxima de 1200 mcg (n = 25)
versus 1 mg de gemeprost vaginal cada 3 horas hasta alcanzar una dosis máxima de 5 mg (n = 25).
Resultados
Resultado principal "fracaso de tratamiento" definido como imposibilidad de provocar el aborto dentro de las 24
horas o efectos secundarios lo suficientemente serios como para excluir el uso de una dosis adicional del
medicamento.
Notas
Ocultamiento de la asignación
C – Inadecuado
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
19
Estudio
Fadalla 2004*
Métodos
"Aleatorizado"; sin detalles.
Participantes
Setenta mujeres en el Hospital Escuela Wad Medeni (Wad Medeni Teaching Hospital), Sudán, con diagnóstico
ecográfico de muerte fetal entre las 13 y las 28 semanas de gestación.
Intervenciones
Misoprostol oral (n = 35) versus misoprostol vaginal (n = 35); ambos administrados como comprimidos de
100 mcg cada 4 horas hasta el inicio del trabajo de parto.
Resultados
Tiempo transcurrido hasta el parto, infusión de ocitocina, extracción manual de la placenta.
Notas
Ocultamiento de la asignación
B – Poco clara
Estudio
Gilles 2004
Métodos
Asignación aleatoria mediante el uso de un sistema computarizado de respuestas telefónicas automáticas. Estratificación
por tipo de embarazo. Bloques permutados aleatorios de 4 u 8.
Participantes
Ochenta mujeres con embarazos anembrionados, con un saco gestacional de menos de 46 mm de diámetro o muerte
embrionaria/fetal con una longitud cefalocaudal inferior a 41 mm. Cuatro centros.
Intervenciones
Una dosis de 800 mcg de "misoprostol húmedo" + 2 ml de solución fisiológica por vía vaginal (n = 41) versus
"misoprostol seco" (tal como se menciona, sin solución fisiológica) (n = 39). Si no se producía el aborto se administraba
una segunda dosis el día 3.
Resultados
Resultado primario: aborto sin necesidad de realizar un legrado antes de los 30 días. Resultados secundarios: aborto
espontáneo < 3, < 8 y < 15 días; efectos secundarios, opiniones de las mujeres.
Notas
Ocultamiento de la asignación
A – Adecuado
Estudio
Graziosi 2004
Métodos
El consentimiento se obtuvo en el momento del diagnóstico de falla precoz de embarazo. Asignación aleatoria después
de una semana de conducta expectante, como mínimo. Programa computarizado con secuencia de aleatorización en
bloques. Estratificación según parto vaginal previo; edad gestacional < o > 10 semanas; centro.
Participantes
Ciento cincuenta y cuatro mujeres con diagnóstico ecográfico de falla precoz de embarazo, ya sea embarazo anembrionado
o muerte fetal entre las 6 y las 14 semanas de gestación. Seis centros de estudio en Holanda.
Intervenciones
Una dosis de 800 mcg de misoprostol vaginal, repetida después de 24 horas si la ecografía indicaba presencia de restos
de tejido en el útero. Legrado después de 3 días si no se había inducido el aborto o si era incompleto (n = 79) o legrado
por aspiración dentro de la semana de la aleatorización (n = 75).
Resultados
Primarios: evacuación completa. Secundarios: efectos secundarios, dolor y necesidad de analgesia, intensidad/duración
del sangrado.
Notas
De las 241 mujeres elegibles, 87 (36%) no aceptaron participar y eligieron el legrado.
Ocultamiento de la asignación
A – Adecuado
Estudio
Heard 2002
Métodos
Se describió como "aleatorizado", pero no se proporcionaron detalles.
Participantes
Treinta y tres mujeres con un "aborto retenido".
Intervenciones
Una dosis de 400 mcg de misoprostol vaginal (n = 12) versus 800 mcg (n = 21).
Resultados
El único resultado utilizable que se informó en el resumen fue el aborto.
Notas
Resumen sin explicación sobre el desequilibrio en los números.
Ocultamiento de la asignación
B – Poco clara
Estudio
Herabutya 1997
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
20
Métodos
"Asignación aleatoria" pero en la publicación no se describe el método.
Participantes
Ochenta y cuatro mujeres sin confirmación ecográfica de muerte fetal, con tamaño uterino de menos de 14 semanas,
sin pérdida de sangre y con el cuello uterino no permeable.
Intervenciones
Administración de misoprostol (200 microgramos por vía vaginal) (n = 42) o de placebo vaginal (n = 42) en el
momento del ingreso al hospital.
Resultados
El resultado primario fue el aborto dentro de las 24 horas del tratamiento. Algunos datos disponibles sobre las
complicaciones.
Notas
Gran parte de los datos informados sobre los resultados describen sólo los subgrupos de mujeres que sufrieron un
aborto antes de la evacuación quirúrgica.
Ocultamiento de la asignación
B – Poco clara
Estudio
Jain 1996*
Métodos
"Tabla de números aleatorios".
Participantes
Setenta mujeres en Los Angeles, Estados Unidos, con muerte fetal (n = 40) o indicaciones clínicas o genéticas para
interrumpir el embarazo (n = 30) entre las 12 y las 22 semanas de gestación. Aquí se incluyen sólo los datos de los
embarazos complicados por muerte fetal.
Intervenciones
Dosis de 200 mcg de misoprostol vaginal cada 12 horas más tapones de laminaria (n = 20) versus 200 mcg de
misoprostol vaginal cada 12 horas solamente.
Resultados
Aborto espontáneo.
Notas
Los efectos adversos se describen para los grupos como un todo, por lo tanto no se incluyen en esta revisión. Dos
mujeres fueron excluidas de los análisis; una por violación del protocolo y la otra mujer tenía un embarazo ectópico
intersticial.
Ocultamiento de la asignación
B – Poco claro
Estudio
Kara 1999*
Métodos
"Asignación aleatoria". No se proporcionan detalles.
Participantes
Sesenta y cinco mujeres en Estambul, Turquía, con diagnóstico ecográfico de muerte fetal en el segundo trimestre.
Intervenciones
Una dosis de 200 mcg de misoprostol vaginal (n = 32) versus 0.5 mcg de dinoproston intracervical (n = 33). La
administración intravenosa de ocitocina se iniciaba después de 6 horas si las contracciones no eran "efectivas".
Resultados
Aborto espontáneo completo. Efectos adversos.
Notas
La dosis reportada de misoprostol fue de 200 mg. Se supone que era una dosis de 200 mcg. No se incluyó el
tiempo transcurrido hasta el aborto espontáneo ya que los desvíos estándar parecían incorrectos.
Ocultamiento de la asignación
B – Poco claro
Estudio
Kovavisarach 2002
Métodos
"Asignación aleatoria". Método no especificado.
Participantes
Cincuenta y cuatro mujeres con embarazos anembrionados de menos de 12 semanas diagnosticados por ecografía
transvaginal. Estudio con un único centro, en Bangkok, Tailandia.
Intervenciones
Misoprostol vaginal, 400 mcg (n = 27) o placebo (n = 27). Se las revisaba después de 24 horas y se ofrecía un
legrado si el aborto era incompleto o no había sido inducido. Revisión adicional después de 1 semana.
Resultados
Primarios: aborto espontáneo completo dentro de las 24 horas del tratamiento.
Notas
Ocultamiento de la asignación
Estudio
B – Poco claro
Kovavisarach 2005
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
21
Métodos
Asignación aleatoria en la que se usaron sobres cerrados, secuencialmente numerados, preparados con una tabla
publicada de números aleatorios.
Participantes
Ciento catorce mujeres en Bangkok, Tailandia, con embarazos no viables (anembrionados o muerte fetal) de menos
de 12 semanas, diagnosticados por ecografía transvaginal. Las mujeres con cuellos de útero permeables no cumplieron
con los requisitos para el reclutamiento.
Intervenciones
Una dosis de 600 mcg de misoprostol vaginal (n = 57) u 800 mcg (n = 57) Si el aborto completo no acontecía dentro
de las 24 horas, o si las circunstancias clínicas así lo indicaban (dolor, sangrado), se realizaba el legrado uterino.
Resultados
Primarios: aborto espontáneo completo sin necesidad de hacer un legrado uterino dentro de las 24 horas. Secundarios:
efectos adversos.
Notas
Ocultamiento de la asignación
A – Adecuado
Estudio
Lelaidier 1993
Métodos
Medicamento o placebo idéntico suministrado por la farmacia según una lista de aleatorización en la que se usaron
bloques de permutación de cuatro.
Participantes
Cuarenta y seis mujeres con embarazos no viables diagnosticados ecográficamente por dos exámenes realizados con
un intervalo de una semana. < 14 semanas. Sin sangrado ni dolor.
Intervenciones
Mifepristona 600 mg por vía oral (n = 23) o placebo (n = 23). Todas las mujeres fueron revisadas después de 5 días
y si el aborto no se había producido, ese día se realizaba la evacuación quirúrgica.
Resultados
El resultado primario fue la expulsión del embarazo. También se registraron los síntomas.
Notas
Médicos privados practicaron la evacuación quirúrgica en dos mujeres del grupo placebo antes de la revisión en el día
5. Ambas tenían un aborto en curso y fueron clasificadas como expulsión positiva; sin información disponible sobre
los síntomas.
Ocultamiento de la asignación
A – Adecuado
Estudio
Lister 2005
Métodos
Asignación aleatoria bloqueadas y estratificadas por consultorio del médico y por día de reclutamiento día del
diagnóstico o día posterior al diagnóstico.
Participantes
Treinta y cuatro mujeres en Columbus, Ohio, EE. UU., con diagnóstico por ecografía transvaginal de falla precoz de
embarazo (embarazos anembrionados o muertes fetales tempranas).
Intervenciones
Dosis de 800 mcg de misoprostol vaginal, repetida después de 24 horas si al realizar una ecografía transvaginal el saco
todavía estaba presente (n = 18) o placebo (n = 16).
Resultados
Primarios: aborto espontáneo completo a las 48 horas.
Notas
Tamaño muestral programado de 84, pero el estudio se detuvo después del análisis preliminar de las primeras 36
mujeres. Se excluyeron dos mujeres del análisis, una por violación del protocolo y la segunda porque no satisfacía los
criterios de inclusión. Dos mujeres no regresaron para la evaluación a las 2 semanas del tratamiento inicial.
Ocultamiento de la asignación
A – Adecuado
Estudio
Muffley 2002
Métodos
Tabla de números aleatorios generados por computadora con permutaciones bloqueadas y asignaciones a grupos
registradas en sobres numerados opacos cerrados.
Participantes
Cincuenta mujeres con diagnóstico ecográfico de embarazos no viables (anembrionados o muertes embrionarias o
fetales) < 12 semanas. Exclusiones: sangrado excesivo, anemia, signos vitales inestables, coagulopatía, asma u otra
contraindicación al tratamiento con prostaglandinas, infección, cuello de útero permeable.
Intervenciones
Dosis de 800 mcg de misoprostol vaginal, repetida después de 24 horas si la ecografía mostraba que el tejido todavía
estaba presente en el útero; revisión final después de 24 horas adicionales; si aún había presencia de tejido, se realizaba
la evacuación quirúrgica (n = 25). Legrado por aspiración (n = 25).
Resultados
Resultado primario: aborto espontáneo.
Notas
Análisis por intención de tratar. Los detalles sobre las náuseas, vómitos, diarrea se comunicaron sólo para el grupo
misoprostol.
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
22
Ocultamiento de la asignación
A – Adecuado
Estudio
Ngoc 2004
Métodos
Aleatorizadas tras abrir sobres numerados secuencialmente y preparados en bloques de 10 por un código generado
por computadora.
Participantes
Doscientas mujeres en la ciudad de Ho Chi Minh, Vietnam, con diagnóstico ecográfico de embarazos no viables en
el primer trimestre (anembrionados o muerte fetal temprana); cuello uterino cerrado.
Intervenciones
Dosis de 800 mcg de misoprostol oral (n = 100) versus 800 mcg de misoprostol vaginal (n = 98). Las mujeres fueron
revisadas después de 48 horas; si presentaban restos embrionarios retenidos se les ofrecía la opción de practicarles la
evacuación quirúrgica o una revisión adicional después de otros 5 días (cuando se hacía la evacuación, si todavía
tenían restos ovulares).
Resultados
Primarios: aborto espontáneo completo sin necesidad de evacuación quirúrgica. Secundarios: efectos adversos.
Notas
No fue posible realizar el seguimiento de 2 mujeres.
Ocultamiento de la asignación
A – Adecuado
Estudio
Nielsen 1999
Métodos
En esta publicación no se analiza el método de aleatorización.
Participantes
Ciento veintidós mujeres de menos de 13 semanas de gestación con síntomas de amenaza de aborto (sangrado +/ dolor),
cuello uterino cerrado y demostración ecográfica de la no viabilidad del embarazo (embarazo anembrionado n = 44;
muerte embrionaria/fetal n = 46; "masa compleja con saco gestacional deformado" n = 32). Evacuación quirúrgica el día
5 si la ecografía transvaginal mostraba restos embrionarios retenidos de más de 15 mm de diámetro.
Intervenciones
Mifepristona (400 mg por vía oral) seguida por misoprostol oral (400 microgramos) 48 horas después (n = 60) versus
conducta expectante (n = 62).
Resultados
Eventos clínicos; ecografía transvaginal de rutina a los 5 días para identificar los restos embrionarios retenidos, escala
análoga visual para evaluar el dolor en el día 5; escala análoga visual para evaluar la satisfacción en el día 14.
Notas
Se busca clarificación de los autores si la "masa compleja con saco gestacional deformado" representa un aborto retenido
o incompleto. En el ínterin se incluyeron los datos.
Ocultamiento de la asignación
B – Poco claro
Estudio
Niromanesh 2005*
Métodos
En esta publicación no se analiza el método de aleatorización.
Participantes
Cien mujeres en Teherán, Irán, con muertes fetales entre las 14 y las 25 semanas.
Intervenciones
Misoprostol vaginal: 400 mcg (n = 50) versus 600 mcg (n = 50): ambos cada 12 horas durante 48 horas.
Resultados
Aborto espontáneo; evacuación quirúrgica; efectos adversos.
Notas
Ocultamiento de la asignación
B – Poco claro
Estudio
Tang 2003
Métodos
Aleatorización mediante números aleatorios generados por computadora.
Participantes
Ochenta mujeres con embarazos no viables diagnosticados por ecografía antes de las 13 semanas.
Intervenciones
Grupo 1: 600 mcg de misoprostol sublingual cada 3 horas hasta un máximo de 3 dosis (n = 40); Grupo 2: 600 mcg
de misoprostol vaginal cada 3 horas hasta un máximo de 3 dosis (n = 40). Las mujeres fueron dadas de alta al
terminar el tratamiento y volvieron a ser evaluadas el día 7, fecha en la que se realizaba la evacuación quirúrgica
si el saco gestacional todavía estaba presente o si tenían restos ovulares retenidos y hemorragia profusa.
Resultados
Resultado primario: aborto completo (sin necesidad de evacuación quirúrgica hasta el retorno de la menstruación).
Notas
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
23
Ocultamiento de la asignación
A – Adecuado
Estudio
Wood 2002
Métodos
Lista en bloques de números aleatorios generada por computadora. La farmacia preparó los sobres numerados.
Los comprimidos no eran idénticos por lo tanto la enfermera los colocó en un introductor vaginal opaco para
que el médico los insertara; de esta manera se mantuvo el ocultamiento de la asignación.
Participantes
Cincuenta mujeres con diagnóstico ecográfico de embarazos no viables. Edad gestacional entre 7 17 semanas,
pero las mujeres no se incluían si el tamaño fetal por ecografía era equivalente a > 12 semanas. También se las
excluía del reclutamiento si tenían contracciones uterinas o hemorragia.
Intervenciones
Misoprostol (800 mcg por vía vaginal) (n = 25) o placebo vaginal (n = 25). El tratamiento se repetía si no había
sospechas de un aborto completo después de 24 horas. A las 48 horas, si se consideraba que el aborto era
incompleto o no se había inducido, se les ofrecía un legrado uterino.
Resultados
El tamaño muestral se realizó de acuerdo a la reducción del legrado uterino del 50% al 10%. También se evaluó
la satisfacción de las mujeres, pero esta información no se incluyó en los análisis ya que no se comunicaron
datos del grupo control.
Notas
Análisis por intención de tratar.
Ocultamiento de la asignación
A – Adecuado
ERPC: evacuación de los restos ovulares retenidos
hCG: gonadotropina coriónica humana
IM: intramuscular
UI: unidades internacionales
mcg: microgramos
MTX: metotrexato
POC: restos ovulares
TVS: ecografía transvaginal
vs: versus
Características de los estudios excluidos
Estudio
Motivo de la exclusión
Abdel Fattah 1997
Resumen del congreso. No se aporta información sobre la edad gestacional pero, dado el título, probablemente incluya
embarazos de más de 24 semanas y de menos de 24 semanas.
Almog 2005
Interrupción de embarazos "viables"; principalmente con anomalías fetales.
Anderman 2000
Resumen del congreso. Incluye embarazos de > 24 semanas y de < 24 semanas.
Avila Vergara 1997
Muertes intrauterinas principalmente en el tercer trimestre.
Bebbington 2002
Interrupción de embarazos viables.
Cabrol 1990
Estudio clínico sobre la mifepristona para la inducción del trabajo de parto después de una muerte intrauterina, pero
principalmente embarazos de fines del segundo trimestre y en el tercer trimestre.
Clevin 2001
Resumen en idioma danés. Estudio aleatorizado, prospectivo, que se realizó para esclarecer el efecto de la administración
vaginal de un análogo de la prostaglandina E1 (gemeprost) versus el manejo quirúrgico (legrado) en abortos espontáneos
de hasta 12 semanas de gestación. Tres grupos: 1 (n = 27), 2A (n = 17) y 2B (n = 17), asignadas según el grosor del
endometrio. Los resultados medidos fueron la reducción en el grosor del endometrio, la duración del sangrado vaginal y
el dolor, comunicados en un formato inadecuado para el análisis.
David 2003
Estudio aleatorizado (detalles de la aleatorización poco claros) de dos métodos para ablandar el cuello uterino antes de la
evacuación quirúrgica de embarazos tempranos no viables. Datos clínicos no utilizables, dado el breve plazo entre el
tratamiento y la cirugía.
Dickinson 1998
El estudio incluyó embarazos con malformaciones fetales e indicaciones maternas para la interrupción de embarazos entre
las 14 y las 28 semanas, así como embarazos con muerte fetal. Los datos se incluirán para este último si se pueden obtener
de los autores.
Dickinson 2002
El estudio incluyó embarazos con malformaciones fetales e indicaciones maternas para la interrupción de embarazos entre
las 14 y las 30 semanas, así como embarazos con muerte fetal. Los datos se incluirán para este último si se pueden obtener
de los autores.
hCG: gonadotropina coriónica humana
POC: restos ovulares
RCT: estudio clínico controlado aleatorizado
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
24
Dickinson 2003
Estudio aleatorizado que compara la administración oral con la administración vaginal de misoprostol para interrumpir
embarazos con malformaciones fetales; no se incluyeron embarazos no viables.
Eppel 2005
El estudio incluyó embarazos con malformaciones fetales e indicaciones maternas para la interrupción de embarazos entre
las 14 y las 23 semanas, así como embarazos con muerte fetal. Los datos se incluirán para este último si se pueden obtener
de los autores.
Feldman 2003
El estudio incluyó embarazos con malformaciones fetales e indicaciones maternas para la interrupción de embarazos entre
las 14 y las 23 semanas, así como embarazos con muerte fetal. Los datos se incluirán para este último si se pueden obtener
de los autores.
Ghorab 1998
El estudio incluyó embarazos con malformaciones fetales para la interrupción del embarazo y embarazos con muerte fetal.
Los datos se incluirán para este último si se pueden obtener de los autores.
Gonzalez 2001
El estudio incluyó embarazos con malformaciones fetales e indicaciones maternas para la interrupción de embarazos entre
las 14 y las 23 semanas, así como embarazos con muerte fetal. Los datos se incluirán para este último si se pueden obtener
de los autores.
Grimes 2004
El estudio incluyó mujeres con otras razones para la interrupción del embarazo y embarazos con muerte fetal. Los datos
se incluirán para este último si se pueden obtener de los autores.
Gronland 2002
No es un estudio clínico aleatorizado. Estudio de tres centros sobre mujeres con embarazos no viables que compara tres
tratamientos: misoprostol, mifepristona + misoprostol, evacuación quirúrgica, con tratamiento que cambiaba en cada
hospital cada cuatro meses.
Hausler 1997
Estudio controlado aleatorizado prospectivo que evalúa tres intervenciones para el aborto espontáneo completo. El diagnóstico
se realizó en función de una prueba de embarazo positiva, hemorragia vaginal o evacuación del tejido de la vagina, orificio
uterino cerrado con sólo un sangrado leve al ingresar y un posible diagnóstico ecográfico claro de embarazo en la historia
clínica. Intervenciones: A) n = 15 legrado; B) n = 20 sólo controladas y; C) n = 15 tratadas adicionalmente durante 10 días
con la administración oral de 2 mg de la hormona acetato de noretisterona y de 0.01 mg de etinil estradiol, tres veces por
día. Aleatorización por medio de sobres no marcados cerrados. Sesenta y tres pacientes fueron incluidas en el estudio y
asignadas aleatoriamente a cada grupo. Después de la aleatorización se excluyeron 13 (20.6%) mujeres del estudio: Diez
pacientes no asistieron al control de seguimiento programado, una no se presentó para el legrado, en una mujer el grosor
del endometrio era mayor que 8 mm y en otra se diagnosticó un embarazo ectópico 6 días después de la aleatorización. El
estudio sólo presenta resultados, en un formato no adecuado, con respecto al tiempo de depuración de la hCG y a la duración
de la hemorragia desde el día de la aleatorización.
Herabutya 2005
Estudio controlado aleatorizado de misoprostol para la interrupción de embarazos viables.
Hidar 2001
El estudio incluyó embarazos con malformaciones fetales e indicaciones maternas para la interrupción de embarazos entre
las 13 y las 29 semanas, así como embarazos con muerte fetal. Los datos se incluirán para este último si se pueden obtener
de los autores.
Hill 1991
El estudio incluye muertes fetales en el segundo y tercer trimestre.
Hogg 2000
Resumen. El estudio incluyó mujeres con otras razones para la interrupción del embarazo y embarazos con muerte fetal.
Los datos se incluirán para este último si se pueden obtener de los autores.
Jain 1994
El estudio incluyó embarazos con malformaciones fetales e indicaciones maternas para la interrupción de embarazos entre
las 12 y las 22 semanas, así como embarazos con muerte fetal. Los datos se incluirán para este último si se pueden obtener
de los autores.
Jain 1999
El estudio incluyó embarazos con malformaciones fetales e indicaciones maternas para la interrupción de embarazos entre
las 12 y las 22 semanas, así como embarazos con muerte fetal. Los datos se incluirán para este último si se pueden obtener
de los autores.
Johnson 1997
Estudio controlado aleatorizado que evalúa el dolor y el sangrado, y que compara el tratamiento quirúrgico con el tratamiento
clínico. Rama quirúrgica (n = 12) legrado uterino con anestesia general. Rama clínica (n = 17) incluye tres estados clínicos
diferentes y los tratamientos de las participantes: a) ningún tratamiento si las mujeres tenían un aborto completo y una
ecografía de la cavidad uterina (miometrio miometrio) inferior a 1.5 mm; b) mujeres con aborto incompleto: pesario de 1
mg de Gemeprost (Cervagem, May y Baker) y permanecían hospitalizadas por 4 horas o hasta que habían expulsado los
restos ovulares; y c) mujeres con un saco gestacional intacto (pero con un feto no viable) 200 mg RU 486 (mifepristona)
y luego se les daba el alta y eran rehospitalizadas 36 48 horas después para la administración de 1 mg de Cervagem vaginal.
En la rama clínica, los datos de cada subgrupo no están separados. El tamaño muestral es demasiado pequeño para detectar
cualquier diferencia entre estos números de grupos.
Kanhai 1989
Incluye muertes fetales en el segundo y el tercer trimestre de embarazo.
Lippert 1978
Muertes fetales en el segundo y el tercer trimestre de embarazo. No está aleatorizado de manera evidente.
Machtinger 2002
Resumen Aparentemente se incluyen los embarazos no viables y los abortos espontáneos. Se espera el informe completo.
Machtinger 2004
Resumen. Aparentemente se incluyen los embarazos no viables y los abortos espontáneos. Se espera el informe completo.
Makhlouf 2003
En el artículo no está claro si todos los embarazos estaban complicados por muerte fetal. Se busca la aclaración de los
autores.
Martin 1965
Asignación según la alternancia, no la aleatorización. Se violó la alternancia.
hCG: gonadotropina coriónica humana
POC: restos ovulares
RCT: estudio clínico controlado aleatorizado
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
25
Nakintu 2001
Muertes fetales en el segundo y el tercer trimestre de embarazo. Se buscan datos separados del autor.
Ngai 2001
Incluye datos sobre mujeres con embarazos no viables y abortos espontáneos incompletos. Si los investigadores pudieran
separarlos, es probable que estos datos se incluyan en actualizaciones futuras.
Nuthalapaty 2004
Resumen. No se describen las indicaciones clínicas para la interrupción del embarazo.
Nuutila 1997
El estudio incluyó embarazos con malformaciones fetales e indicaciones maternas para la interrupción de embarazos entre
las 12 y las 24 semanas, así como embarazos con muerte fetal. Los datos se incluirán para este último si se pueden obtener
de los autores.
Owen 1999
El estudio incluyó embarazos con malformaciones fetales e indicaciones maternas para la interrupción de embarazos entre
las 16 y las 24 semanas, así como embarazos con muerte fetal. Los datos se incluirán para este último si se pueden obtener
de los autores.
Paraskevaides 1992
Estudio de escasa magnitud de 16 mujeres "aleatorizadas" a evacuación quirúrgica o a un tratamiento con prostaglandina
F2alfa o Trilostane. No hay detalles sobre la presentación clínica o los hallazgos ecográficos y clínicos pero el resumen
incluye mujeres con embarazos no viables y abortos espontáneos incompletos.
Perry 1999
Excluyó a las mujeres con muertes fetales.
Piotrowski 1979
No está claro si se trataba de un estudio clínico aleatorizado.
Pongsatha 2004
El estudio excluyó a las mujeres con muertes fetales.
Ramsey 2004
El estudio incluyó a mujeres con otras razones para la interrupción del embarazo y embarazos con muerte fetal. Los datos
se incluirán para este último si se pueden obtener de los autores.
Roy 2003
Resumen. No está claro si la muerte fetal esta incluida como indicación para la interrupción.
Salamalekis 1990
Sólo en forma de resumen. La asignación al tratamiento fue por alternancia, no por aleatorización.
Su 2005
Interrupción del embarazo por anomalías fetales, motivos sociales o enfermedad materna, no por embarazos no viables.
Surita 1997
Sólo en forma de resumen. Puede incluir muertes fetales en el tercer trimestre.
Thavarasah 1986
En el artículo no está claro pero la asignación puede haber sido por alternancia. Se buscará la aclaración de los autores.
Toppozada 1994
Incluye muertes fetales en el tercer trimestre.
Yapar 1996
Incluye indicaciones para la interrupción además de muerte fetal. Alto grado de violación del protocolo (60/400). Los
resultados no se presentan como un análisis por intención de tratar.
Zhang 2005
Incluye embarazos no viables y abortos espontáneos. Los datos se incluirán para el primer estudio si se pueden obtener de
los autores.
hCG: gonadotropina coriónica humana
POC: restos ovulares
RCT: estudio clínico controlado aleatorizado
Características de los estudios en curso
Estudio
Australia 2000
Nombre o título del estudio
Misoprostol para el manejo clínico del aborto espontáneo (estudio clínico controlado aleatorizado).
Participantes
Mujeres con aborto espontáneo incompleto o retenido hasta las 12 semanas de gestación inclusive.
Intervenciones
Fármacos y medicamentos; cirugía.
Resultados
Medidas de resultados primarios:
(1) necesidad de evacuar quirúrgicamente los restos ovulares retenidos en el quirófano, dentro del primer mes de la
intervención;
(2) infección que requiere tratamiento con antibióticos;
(3) cambio en la hemoglobina desde la preintervención hasta las 72 horas y 4 semanas después de la intervención.
Resultados secundarios: (1) efectos secundarios; por ejemplo, náuseas, vómitos, diarrea, dolor abdominal;
(2) necesidad de administrar analgesia en el hospital: narcóticos u analgesia oral;
(3) necesidad de administrar antieméticos en el hospital;
(4) duración de la hemorragia;
(5) tasas de complicación basadas en la extracción étnica.
Fecha de inicio
Abril de 1999.
Contacto
Katharine Louey
7 Eagle 11 Bridge Rd
Mackay Qld 4740
Australia
Tel: + 61 7 49531817
Correo electrónico: klouey@mrbean.net.au
Notas
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
26
Estudio
UK 1999
Nombre o título del estudio
Miscarriage Treatment Study (MIST).
Participantes
Mujeres con aborto espontáneo confirmado, retenido o incompleto, que concurren a los consultorios durante los primeros
meses de embarazo, con fechas gestacionales inferiores a 91 días (13 semanas) o con un volumen de la cavidad uterina
menor de 91 días. Otros criterios de inclusión: las mujeres pueden entender el idioma inglés, están dispuestas a ser aleatorizadas
a cualquier grupo de tratamiento y hay incertidumbre sobre el mejor abordaje. Criterios de exclusión: hemorragia severa,
dolor intenso, pirexia superior a 37.5 ºC, asma grave, discrasia sanguínea, diabetes, tratamiento actual con anticoagulantes
o corticosteroides, embarazo gemelar o múltiple de mayor orden, uso contraindicado de prostaglandina, no entiende el
idioma inglés escrito, rechaza el consentimiento por escrito.
Intervenciones
Grupo de conducta expectante: dadas de alta con indicaciones por escrito y analgesia. Grupo clínico: serán hospitalizadas
(inmediatamente si el aborto espontáneo es incompleto, y entre 24 y 48 horas después de la administración oral de la
mifepristona si tienen un aborto retenido) y se les administrará misoprostol vaginal. Grupo quirúrgico: como es la práctica
actual.
Resultados
Medida de resultado primario:
(1) infección ginecológica dentro de los 14 días de la confirmación del aborto espontáneo por ecografía transvaginal. Medidas
de resultado secundario:
(1) tratamiento con antibióticos (dentro de los 14 días y las 6 semanas);
(2) días de dolor, días de sangrado vaginal, días de licencia en el trabajo, regreso a las actividades diarias habituales;
(3) hemoglobina y hematócrito (a los 10 y a los 14 días), evacuación quirúrgica no programada de restos ovulares retenidos
u otro tipo de ingreso (dentro de los 14 días o a las 6 semanas);
(4) evacuación completa del útero por ecografía transvaginal (a los 10 o 14 días);
(5) depresión, ansiedad y estado de salud general (a las 6 semanas).
Fecha de inicio
Contacto
Miss Lohanna Trinder
MIST Study Co ordinating Center
Dept of Women's Health
Cotswold Center
Southmead Hospital
Bristol
BS10 5NB
UK
Tel: 01179595186
FAX 01179595178
e-mail: jo_trinder@msn.com.uk
Notas
ERPC: evacuación de los restos ovulares retenidos
TVS: ecografía transvaginal
ANÁLISIS
Comparison 01. Misoprostol vaginal versus placebo
Título del resultado
N.º de
estudios
N.º de
Método estadístico
participantes
Magnitud del efecto
01 Aborto espontáneo completo < 24 horas
después del tratamiento
2
138
Riesgo relativo (efectos fijos) IC 95%
4.73 [2.70, 8.28]
02 Aborto espontáneo completo < 48 horas
2
84
Riesgo relativo (efectos fijos) IC 95%
5.74 [2.70, 12.19]
03 Aborto espontáneo completo sin
1
evacuación de los productos retenidos, día 7
83
Riesgo relativo (efectos fijos) IC 95%
2.99 [1.80, 4.99]
04 Legrado uterino
2
104
Riesgo relativo (efectos fijos) IC 95%
0.40 [0.26, 0.60]
05 Opiáceos para el alivio del dolor
1
84
Riesgo relativo (efectos fijos) IC 95%
5.00 [0.25, 101.11]
06 Transfusión de sangre
1
84
Riesgo relativo (efectos fijos) IC 95%
0.20 [0.01, 4.04]
07 Diferencias en la hemoglobina > 10 g/l
1
50
Riesgo relativo (efectos fijos) IC 95%
1.25 [0.38, 4.12]
08 Náuseas
2
88
Riesgo relativo (efectos fijos) IC 95%
1.38 [0.43, 4.40]
09 Diarrea
2
88
Riesgo relativo (efectos fijos) IC 95%
2.21 [0.35, 14.06]
10 Fiebre
1
54
Riesgo relativo (efectos fijos) IC 95%
9.00 [0.51, 159.43]
11 Perforación uterina
1
84
Riesgo relativo (efectos fijos) IC 95%
0.33 [0.01, 7.96]
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
27
12 Hemorragia vaginal 2 semanas después del 1
tratamiento
32
Riesgo relativo (efectos fijos) IC 95%
1.00 [0.41, 2.45]
13 Satisfacción con el tratamiento
32
Riesgo relativo (efectos fijos) IC 95%
1.17 [0.83, 1.64]
1
Comparison 02. Misoprostol vaginal versus evacuación quirúrgica del útero
Título del resultado
N.º de
estudios
N.º de
participantes
Método estadístico
Magnitud del efecto
01 Evacuación quirúrgica del útero
3
254
Riesgo relativo (efectos fijos) IC 95%
0.42 [0.34, 0.52]
02 Hematócrito postratamiento (%)
1
50
Diferencia de medias ponderada (efectos fijos)
IC 95%
1.40 [ 3.51, 0.71]
03 Náuseas
1
154
Riesgo relativo (efectos fijos) IC 95%
21.85 [1.31, 364.37]
04 Alivio del dolor
1
154
Riesgo relativo (efectos fijos) IC 95%
1.42 [0.82, 2.46]
05 Diarrea
1
154
Riesgo relativo (efectos fijos) IC 95%
40.85 [2.52, 662.57]
06 Perforación uterina
1
154
Riesgo relativo (efectos fijos) IC 95%
0.32 [0.01, 7.65]
07 Síndrome de Asherman
1
154
Riesgo relativo (efectos fijos) IC 95%
0.32 [0.01, 7.65]
Comparison 03. Misoprostol vaginal versus gemeprost vaginal
Título del resultado
N.º de
estudios
N.º de
participantes
Método estadístico
Magnitud del efecto
01 Aborto espontáneo < 24 horas
1
50
Riesgo relativo (efectos fijos) IC 95%
1.24 [0.90, 1.70]
02 Temperatura > 38 ºC
1
50
Riesgo relativo (efectos fijos) IC 95%
1.50 [0.27, 8.22]
03 Vómitos
1
50
Riesgo relativo (efectos fijos) IC 95%
3.00 [0.13, 70.30]
04 Diarrea
1
50
Riesgo relativo (efectos fijos) IC 95%
0.14 [0.01, 2.63]
05 Analgesia con opiáceos
1
50
Riesgo relativo (efectos fijos) IC 95%
No estimable
Comparison 04. Misoprostol vaginal versus prostaglandina E1/2 vaginal
Título del resultado
N.º de
estudios
N.º de
participantes
Método estadístico
Magnitud del efecto
01 Evacuación quirúrgica
1
60
Riesgo relativo (efectos fijos) IC 95%
0.39 [0.21, 0.72]
02 Transfusión de sangre
1
60
Riesgo relativo (efectos fijos) IC 95%
6.07 [0.30, 121.33]
03 Hospitalización (días)
1
60
Diferencia de medias ponderada (efectos fijos)
IC 95%
2.38 [ 3.36, 1.40]
04 Aborto espontáneo completo
1
65
Riesgo relativo (efectos fijos) IC 95%
1.44 [1.06, 1.96]
05 Náuseas
1
65
Riesgo relativo (efectos fijos) IC 95%
1.03 [0.28, 3.78]
Comparison 05. Esquemas de tratamiento con misoprostol vaginal en dosis más bajas versus dosis más altas
Título del estudio
N.º de estudios N.º de participantes Método estadístico
Magnitud del efecto
01 Aborto espontáneo
3
247
Riesgo relativo (efectos fijos) IC 95%
0.85 [0.72, 1.00]
02 Fiebre
2
214
Riesgo relativo (efectos fijos) IC 95%
0.73 [0.41, 1.30]
03 Náuseas
2
214
Riesgo relativo (efectos fijos) IC 95%
0.67 [0.31, 1.41]
04 Diarrea
2
214
Riesgo relativo (efectos fijos) IC 95%
0.54 [0.15, 1.91]
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
28
Comparison 06. Preparación húmeda versus seca de misoprostol vaginal
Título del resultado
N.º de
estudios
N.º de
Método estadístico
participantes
Magnitud del efecto
01 Aborto espontáneo < 3 días
1
80
Riesgo relativo (efectos fijos) IC 95%
1.14 [0.85, 1.54]
02 Aborto espontáneo < 8 días
1
80
Riesgo relativo (efectos fijos) IC 95%
1.04 [0.84, 1.29]
03 Aborto espontáneo < 15 días
1
80
Riesgo relativo (efectos fijos) IC 95%
0.92 [0.78, 1.10]
04 Aborto espontáneo < 30 días
1
80
Riesgo relativo (efectos fijos) IC 95%
0.95 [0.79, 1.14]
05 Diarrea < 48 horas después del tratamiento
1
77
Riesgo relativo (efectos fijos) IC 95%
1.75 [0.89, 3.42]
06 Escalofríos < 48 horas de tratamiento
1
77
Riesgo relativo (efectos fijos) IC 95%
1.36 [0.94, 1.98]
07 Vómitos < 48 horas de tratamiento
1
77
Riesgo relativo (efectos fijos) IC 95%
0.93 [0.33, 2.62]
08 Desearía/probablemente desearía el mismo 1
tratamiento para un futuro embarazo no viable
73
Riesgo relativo (efectos fijos) IC 95%
1.18 [0.93, 1.49]
Comparison 07. Misoprostol vaginal + metotrexato versus misoprostol vaginal solo
Título del resultado
N.º de
estudios
N.º de
participantes
Método estadístico
Magnitud del efecto
01 Aborto espontáneo incompleto
1
21
Riesgo relativo (efectos fijos) IC 95%
0.26 [0.01, 5.65]
04 Evacuación quirúrgica adicional
1
21
Riesgo relativo (efectos fijos) IC 95%
0.26 [0.01, 5.65]
05 Hemorragia
1
21
Riesgo relativo (efectos fijos) IC 95%
2.31 [0.10, 50.85]
06 Alivio del dolor
1
21
Riesgo relativo (efectos fijos) IC 95%
0.75 [0.25, 2.22]
Comparison 08. Misoprostol vaginal más tapones de laminaria versus misoprostol vaginal solo
Título del resultado
N.º de estudios
N.º de participantes Método estadístico
Magnitud del efecto
01 Aborto espontáneo < 24 horas
1
38
Riesgo relativo (efectos fijos) IC 95%
0.90 [0.65, 1.25]
02 Aborto espontáneo < 48 horas
1
38
Riesgo relativo (efectos fijos) IC 95%
1.07 [0.88, 1.29]
Comparison 09. Misoprostol oral versus misoprostol vaginal
Título del resultado
N.º de
estudios
N.º de
participantes
Método estadístico
Magnitud del efecto
01 Aborto espontáneo completo
2
218
Riesgo relativo (efectos fijos) IC 95%
0.90 [0.82, 0.99]
02 Vómitos
1
190
Riesgo relativo (efectos fijos) IC 95%
0.29 [0.10, 0.84]
09 Náuseas
1
20
Riesgo relativo (efectos fijos) IC 95%
0.80 [0.37, 1.74]
10 Diarrea
2
210
Riesgo relativo (efectos fijos) IC 95%
1.05 [0.67, 1.66]
12 Dolor (escala análoga visual)
1
18
Diferencia de medias ponderada (efectos fijos) IC 1.90 [ 4.82, 1.02]
95%
13 Fiebre
1
190
Riesgo relativo (efectos fijos) IC 95%
1.00 [0.36, 2.74]
14 Satisfacción de las mujeres con el
tratamiento
1
198
Riesgo relativo (efectos fijos) IC 95%
0.96 [0.86, 1.06]
15 Tiempo hasta el parto (horas)
1
70
Diferencia de medias ponderada (efectos fijos) IC 4.10 [2.64, 5.56]
95%
16 Infusión de ocitocina
1
70
Riesgo relativo (efectos fijos) IC 95%
2.75 [0.97, 7.81]
17 Alumbramiento manual
1
70
Riesgo relativo (efectos fijos) IC 95%
4.50 [1.05, 19.35]
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
29
Comparison 10. Misoprostol oral + mifepristona versus conducta expectante
Título del resultado
N.º de
estudios
N.º de
participantes
Método estadístico
Magnitud del efecto
01 Cavidad uterina vacía el día 5
1
122
Riesgo relativo (efectos fijos) IC 95%
1.08 [0.90, 1.30]
02 Evacuación quirúrgica de urgencia por
hemorragia
1
122
Riesgo relativo (efectos fijos) IC 95%
0.34 [0.01, 8.29]
03 Enfermedad pélvica inflamatoria
1
122
Riesgo relativo (efectos fijos) IC 95%
0.52 [0.05, 5.55]
04 Dolor (escala análoga visual día 5)
1
122
Diferencia de medias ponderada (efectos fijos) 4.10 [ 5.92, 14.12]
IC 95%
05 Licencia por enfermedad (días)
1
122
Diferencia de medias ponderada (efectos fijos) 1.80 [0.63, 2.97]
IC 95%
06 Hemorragia (días)
1
122
Diferencia de medias ponderada (efectos fijos) 0.70 [ 0.43, 1.83]
IC 95%
07 Satisfacción con el tratamiento (escala
análoga visual día 14)
1
122
Diferencia de medias ponderada (efectos fijos) 3.40 [ 5.54, 12.34]
IC 95%
Comparison 11. Misoprostol sublingual versus misoprostol vaginal
Título del resultado
N.º de
estudios
N.º de
participantes
Método estadístico
Magnitud del efecto
01 Aborto espontáneo completo
1
80
Riesgo relativo (efectos fijos) IC 95%
1.00 [0.85, 1.18]
02 Náuseas
1
80
Riesgo relativo (efectos fijos) IC 95%
1.20 [0.80, 1.79]
03 Vómitos
1
80
Riesgo relativo (efectos fijos) IC 95%
0.78 [0.32, 1.88]
04 Diarrea
1
80
Riesgo relativo (efectos fijos) IC 95%
2.55 [1.48, 4.38]
05 Hemoglobina día 43
1
80
Diferencia de medias ponderada (efectos fijos) IC 0.10 [ 0.38, 0.58]
95%
06 Dolor insoportable
1
80
Riesgo relativo (efectos fijos) IC 95%
0.75 [0.29, 1.97]
07 Satisfecha con el tratamiento
1
77
Riesgo relativo (efectos fijos) IC 95%
0.99 [0.79, 1.25]
Comparison 12. Mifepristona versus placebo
Título del resultado
N.º de
estudios
N.º de
participantes
Método estadístico
Magnitud del efecto
01 Aborto espontáneo < 48 horas
1
46
Riesgo relativo (efectos fijos) IC 95%
5.00 [0.25, 98.75]
02 Aborto espontáneo < 3 días
1
46
Riesgo relativo (efectos fijos) IC 95%
19.00 [1.17, 308.40]
03 Aborto espontáneo < 4 días
1
46
Riesgo relativo (efectos fijos) IC 95%
14.00 [2.00, 97.88]
04 Aborto espontáneo < 5 días
1
46
Riesgo relativo (efectos fijos) IC 95%
9.50 [2.49, 36.19]
05 Hemorragia vaginal antes del día 5
1
44
Riesgo relativo (efectos fijos) IC 95%
4.20 [1.95, 9.03]
06 Dolor antes del día 5
1
44
Riesgo relativo (efectos fijos) IC 95%
2.19 [0.93, 5.17]
Comparison 13. Gemeprost vaginal versus evacuación quirúrgica del útero
Resultado del título
N.º de estudios N.º de
participantes
Método estadístico
Magnitud del efecto
01 Evacuación quirúrgica
1
87
Riesgo relativo (efectos fijos) IC 95%
0.23 [0.14, 0.40]
02 Perforación del útero
1
87
Riesgo relativo (efectos fijos) IC 95%
0.20 [0.01, 4.14]
03 Náuseas
1
87
Riesgo relativo (efectos fijos) IC 95%
1.79 [0.56, 5.68]
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
30
INDICE DE TÉRMINOS
Títulos de Temas Médicos (MeSH)
Abortifacient Agents [*therapeutic use], Abortion, Induced [*methods], Administration, Intravaginal, Administration, Oral, Fetal Death [ultrasonography],
Mifepristone [*therapeutic use], Misoprostol [*therapeutic use], Randomized Controlled Trials, Ultrasonography, Prenatal
Control de palabras MeSH
Female; Humans; Pregnancy
C A R ÁT U L A
Titulo
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Autor(es)
Neilson JP, Hickey M, Vazquez J
Contribución de los autor(es)
Juan Vazquez: responsable del desarrollo del protocolo y de las correcciones del primer borrador
de la revisión.
Martha Hickey: responsable del desarrollo del protocolo y de las correcciones del primer borrador
de la revisión.
Jim Neilson: responsable de la supervisión del protocolo y del primer borrador de la revisión.
Número de protocolo publicado inicialmente
2000/3
Número de revisión publicada inicialmente
2006/3
Fecha de la enmienda más reciente
17 Mayo 2006
Fecha de la modificación SIGNIFICATIVA más
reciente
24 Abril 2006
Cambios más recientes
El protocolo para esta revisión tuvo como objetivo incluir los dos estudios clínicos sobre el
tratamiento de embarazos no viables y de abortos espontáneos incompletos diagnosticados por
ecografía. Debido a las razones descritas en la revisión, estos temas se abordarán en dos revisiones
diferentes, lo que explica la modificación en el título.
Fecha de búsqueda de nuevos estudios no
localizados
El autor no facilitó la información
Fecha de localización de nuevos estudios aún
no incluidos/excluidos
El autor no facilitó la información
Fecha de localización de nuevos estudios
incluidos/excluidos
30 Noviembre 2005
Fecha de modificación de la sección
conclusiones de los autores
El autor no facilitó la información
Dirección de contacto
Prof James P Neilson
Professor of Obstetrics and Gynaecology/Head of School of Reproductive and Developmental
Medicine
Division of Perinatal and Reproductive Medicine
The University of Liverpool
First Floor
Liverpool Women's NHS Foundation Trust, Crown Street
Liverpool
L8 7SS
UK
E-mail: jneilson@liverpool.ac.uk
Tel: +44 151 7024100
Fax: +44 151 7024024
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
31
DOI
10.1002/14651858.CD002253.pub3
Número de la Cochrane Library
CD002253
Grupo editorial
Grupo Cochrane de Embarazo y Parto (Cochrane Pregnancy and Childbirth Group)
Código del grupo editorial
HM-PREG
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
32
G R Á F I C O S Y O T R A S TA B L A S
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 01 ABORTO ESPONTÁNEO COMPLETO < 24 HORAS
DESPUÉS DEL TRATAMIENTO
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 02 ABORTO ESPONTÁNEO COMPLETO < 48 HORAS
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 03 ABORTO ESPONTÁNEO SIN EVACUACIÓN DE
LOS RESTOS OVULARES RETENIDOS EL DÍA 7
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
33
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 04 LEGRADO UTERINO
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 05 OPIÁCEOS PARA EL ALIVIO DEL DOLOR
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 06 TRANSFUSIÓN DE SANGRE
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 07 DIFERENCIA EN LA HEMOGLOBINA > 10 G/L
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
34
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 08 NÁUSEAS
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 09 DIARREA
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 10 FIEBRE
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 11 PERFORACIÓN UTERINA
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
35
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 12 HEMORRAGIA VAGINAL 2 SEMANAS DESPUÉS
DEL TRATAMIENTO
COMPARACIÓN 01 MISOPROSTOL VAGINAL VERSUS PLACEBO, RESULTADO 13 SATISFACCIÓN CON EL TRATAMIENTO
COMPARACIÓN 02 MISOPROSTOL VAGINAL VERSUS EVACUACIÓN QUIRÚRGICA DEL ÚTERO, RESULTADO 01 EVACUACIÓN
QUIRÚRGICA DEL ÚTERO
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
36
COMPARACIÓN 02 MISOPROSTOL VAGINAL VERSUS EVACUACIÓN QUIRÚRGICA DEL ÚTERO, RESULTADO 02 HEMATÓCRITO
POSTRATAMIENTO (%)
COMPARACIÓN 02 MISOPROSTOL VAGINAL VERSUS EVACUACIÓN QUIRÚRGICA DEL ÚTERO, RESULTADO 03 NÁUSEAS
COMPARACIÓN 02 MISOPROSTOL VAGINAL VERSUS EVACUACIÓN QUIRÚRGICA DEL ÚTERO, RESULTADO 04 ALIVIO DEL DOLOR
COMPARACIÓN 02 MISOPROSTOL VAGINAL VERSUS EVACUACIÓN QUIRÚRGICA DEL ÚTERO, RESULTADO 05 DIARREA
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
37
COMPARACIÓN 02 MISOPROSTOL VAGINAL VERSUS EVACUACIÓN QUIRÚRGICA DEL ÚTERO, RESULTADO 06 PERFORACIÓN
UTERINA
COMPARACIÓN 02 MISOPROSTOL VAGINAL VERSUS EVACUACIÓN QUIRÚRGICA DEL ÚTERO, RESULTADO 07 SÍNDROME DE
ASHERMAN
COMPARACIÓN 03 MISOPROSTOL VAGINAL VERSUS GEMEPROST VAGINAL, RESULTADO 01 ABORTO ESPONTÁNEO < 24 HORAS
COMPARACIÓN 03 MISOPROSTOL VAGINAL VERSUS GEMEPROST VAGINAL, RESULTADO 02 TEMPERATURA > 38 º C
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
38
COMPARACIÓN 03 MISOPROSTOL VAGINAL VERSUS GEMEPROST VAGINAL, RESULTADO 03 VÓMITOS
COMPARACIÓN 03 MISOPROSTOL VAGINAL VERSUS GEMEPROST VAGINAL, RESULTADO 03 VÓMITOS
COMPARACIÓN 03 MISOPROSTOL VAGINAL VERSUS GEMEPROST VAGINAL, RESULTADO 03 ANALGESIA CON OPIÁCEOS
COMPARACIÓN 04 MISOPROSTOL VAGINAL VERSUS PROSTAGLANDINA E1/2 VAGINAL, RESULTADO 01 EVACUACIÓN QUIRÚRGICA
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
39
COMPARACIÓN 04 MISOPROSTOL VAGINAL VERSUS PROSTAGLANDINA E1/2 VAGINAL, RESULTADO 02 TRANSFUSIÓN DE
SANGRE
COMPARACIÓN 04 MISOPROSTOL VAGINAL VERSUS PROSTAGLANDINA E1/2 VAGINAL, RESULTADO 03 HOSPITALIZACIÓN (DÍAS)
COMPARACIÓN 04 MISOPROSTOL VAGINAL VERSUS PROSTAGLANDINA E1/2 VAGINAL, RESULTADO 04 ABORTO ESPONTÁNEO
COMPLETO
COMPARACIÓN 04 MISOPROSTOL VAGINAL VERSUS PROSTAGLANDINA E1/2 VAGINAL, RESULTADO 05 NÁUSEAS
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
40
COMPARACIÓN 05 ESQUEMAS DE MISOPROSTOL VAGINAL EN DOSIS MÁS BAJAS VERSUS DOSIS MÁS ALTAS, RESULTADO 01
ABORTO ESPONTÁNEO
COMPARACIÓN 05 ESQUEMAS DE MISOPROSTOL VAGINAL EN DOSIS MÁS BAJAS VERSUS DOSIS MÁS ALTAS, RESULTADO 02
FIEBRE
COMPARACIÓN 05 ESQUEMAS DE MISOPROSTOL VAGINAL EN DOSIS MÁS BAJAS VERSUS DOSIS MÁS ALTAS, RESULTADO 03
NÁUSEAS
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
41
COMPARACIÓN 05 ESQUEMAS DE MISOPROSTOL VAGINAL EN DOSIS MÁS BAJAS VERSUS DOSIS MÁS ALTAS, RESULTADO 04
DIARREA
COMPARACIÓN 06 PREPARACIÓN HÚMEDA VERSUS SECA DE MISOPROSTOL VAGINAL, RESULTADO 01 ABORTO ESPONTÁNEO
< 3 DÍAS
COMPARACIÓN 06 PREPARACIÓN HÚMEDA VERSUS SECA DE MISOPROSTOL VAGINAL, RESULTADO 02 ABORTO ESPONTÁNEO
< 8 DÍAS
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
42
COMPARACIÓN 06 PREPARACIÓN HÚMEDA VERSUS SECA DE MISOPROSTOL VAGINAL, RESULTADO 03 ABORTO ESPONTÁNEO
< 15 DÍAS
COMPARACIÓN 06 PREPARACIÓN HÚMEDA VERSUS SECA DE MISOPROSTOL VAGINAL, RESULTADO 04 ABORTO ESPONTÁNEO
< 30 DÍAS
COMPARACIÓN 06 PREPARACIÓN HÚMEDA VERSUS SECA DE MISOPROSTOL VAGINAL, RESULTADO 05 DIARREA < 48 HORAS
DESPUÉS DEL TRATAMIENTO
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
43
COMPARACIÓN 06 PREPARACIÓN HÚMEDA VERSUS SECA DE MISOPROSTOL VAGINAL, RESULTADO 06 ESCALOFRÍOS < 48
HORAS DE TRATAMIENTO
COMPARACIÓN 06 PREPARACIÓN HÚMEDA VERSUS SECA DE MISOPROSTOL VAGINAL, RESULTADO 07 VÓMITOS < 48 HORAS
DE TRATAMIENTO
COMPARACIÓN 06 PREPARACIÓN HÚMEDA VERSUS SECA DE MISOPROSTOL VAGINAL, RESULTADO 08
DESEARÍA/PROBABLEMENTE DESEARÍA EL MISMO TRATAMIENTO PARA UN FUTURO EMBARAZO NO VIABLE
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
44
COMPARACIÓN 07 MISOPROSTOL VAGINAL + METOTREXATO VERSUS MISOPROSTOL VAGINAL SOLO, RESULTADO 01 ABORTO
ESPONTÁNEO INCOMPLETO
COMPARACIÓN 07 MISOPROSTOL VAGINAL + METOTREXATO VERSUS MISOPROSTOL VAGINAL SOLO, RESULTADO 04 EVACUACIÓN
QUIRÚRGICA ADICIONAL
COMPARACIÓN 07 MISOPROSTOL VAGINAL + METOTREXATO VERSUS MISOPROSTOL VAGINAL SOLO, RESULTADO 05
HEMORRAGIA
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
45
COMPARACIÓN 07 MISOPROSTOL VAGINAL + METOTREXATO VERSUS MISOPROSTOL VAGINAL SOLO, RESULTADO 06 ALIVIO
DEL DOLOR
COMPARACIÓN 08 MISOPROSTOL VAGINAL MÁS TAPONES DE LAMINARIA VERSUS MISOPROSTOL VAGINAL SOLO, RESULTADO
01 ABORTO ESPONTÁNEO < 24 HORAS
COMPARACIÓN 08 MISOPROSTOL VAGINAL MÁS TAPONES DE LAMINARIA VERSUS MISOPROSTOL VAGINAL SOLO, RESULTADO
02 ABORTO ESPONTÁNEO < 48 HORAS
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
46
COMPARACIÓN 09 MISOPROSTOL ORAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 01 ABORTO ESPONTÁNEO COMPLETO
COMPARACIÓN 09 MISOPROSTOL ORAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 02 VÓMITOS
COMPARACIÓN 09 MISOPROSTOL ORAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 09 NÁUSEAS
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
47
COMPARACIÓN 09 MISOPROSTOL ORAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 10 DIARREA
COMPARACIÓN 09 MISOPROSTOL ORAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 12 DOLOR (ESCALA ANÁLOGA VISUAL)
COMPARACIÓN 09 MISOPROSTOL ORAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 13 FIEBRE
COMPARACIÓN 09 MISOPROSTOL ORAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 14 SATISFACCIÓN DE LAS MUJERES
CON EL TRATAMIENTO
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
48
COMPARACIÓN 09 MISOPROSTOL ORAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 15 TIEMPO HASTA EL PARTO (HORAS)
COMPARACIÓN 09 MISOPROSTOL ORAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 16 INFUSIÓN DE OCITOCINA
COMPARACIÓN 09 MISOPROSTOL ORAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 17 ALUMBRAMIENTO MANUAL
COMPARACIÓN 10 MISOPROSTOL ORAL + MIFEPRISTONA VERSUS CONDUCTA EXPECTANTE, RESULTADO 01 CAVIDAD UTERINA
VACÍA EL DÍA 5
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
49
COMPARACIÓN 10 MISOPROSTOL ORAL + MIFEPRISTONA VERSUS CONDUCTA EXPECTANTE, RESULTADO 02 EVACUACIÓN
QUIRÚRGICA DE URGENCIA POR HEMORRAGIA
COMPARACIÓN 10 MISOPROSTOL ORAL + MIFEPRISTONA VERSUS CONDUCTA EXPECTANTE, RESULTADO 03 ENFERMEDAD
PÉLVICA INFLAMATORIA
COMPARACIÓN 10 MISOPROSTOL ORAL + MIFEPRISTONA VERSUS CONDUCTA EXPECTANTE, RESULTADO 04 DOLOR (ESCALA
ANÁLOGA VISUAL DÍA 5)
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
50
COMPARACIÓN 10 MISOPROSTOL ORAL + MIFEPRISTONA VERSUS CONDUCTA EXPECTANTE, RESULTADO 05 LICENCIA POR
ENFERMEDAD (DÍAS)
COMPARACIÓN 10 MISOPROSTOL ORAL + MIFEPRISTONA VERSUS CONDUCTA EXPECTANTE, RESULTADO 06 HEMORRAGIA
(DÍAS)
COMPARACIÓN 10 MISOPROSTOL ORAL + MIFEPRISTONA VERSUS CONDUCTA EXPECTANTE, RESULTADO 07 SATISFACCIÓN
CON EL TRATAMIENTO (ESCALA ANÁLOGA VISUAL DÍA 14)
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
51
COMPARACIÓN 11 MISOPROSTOL SUBLINGUAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 01 ABORTO ESPONTÁNEO
COMPLETO
COMPARACIÓN 11 MISOPROSTOL SUBLINGUAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 02 NÁUSEAS
COMPARACIÓN 11 MISOPROSTOL SUBLINGUAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 03 VÓMITOS
COMPARACIÓN 11 MISOPROSTOL SUBLINGUAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 04 DIARREA
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
52
COMPARACIÓN 11 MISOPROSTOL SUBLINGUAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 05 HEMOGLOBINA DÍA 43
COMPARACIÓN 11 MISOPROSTOL SUBLINGUAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 06 DOLOR INSOPORTABLE
COMPARACIÓN 11 MISOPROSTOL SUBLINGUAL VERSUS MISOPROSTOL VAGINAL, RESULTADO 07 SATISFECHA CON EL
TRATAMIENTO
COMPARACIÓN 12 MIFEPRISTONA VERSUS PLACEBO, RESULTADO 01 ABORTO ESPONTÁNEO < 48 HORAS
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
53
COMPARACIÓN 12 MIFEPRISTONA VERSUS PLACEBO, RESULTADO 02 ABORTO ESPONTÁNEO < 3 DÍAS
COMPARACIÓN 12 MIFEPRISTONA VERSUS PLACEBO, RESULTADO 03 ABORTO ESPONTÁNEO < 4 DÍAS
COMPARACIÓN 12 MIFEPRISTONA VERSUS PLACEBO, RESULTADO 04 ABORTO ESPONTÁNEO < 5 DÍAS
COMPARACIÓN 12 MIFEPRISTONA VERSUS PLACEBO, RESULTADO 05 HEMORRAGIA VAGINAL ANTES DEL DÍA 5
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
54
COMPARACIÓN 12 MIFEPRISTONA VERSUS PLACEBO, RESULTADO 06 DOLOR ANTES DEL DÍA 5
COMPARACIÓN 13 GEMEPROST VAGINAL VERSUS EVACUACIÓN QUIRÚRGICA DEL ÚTERO, RESULTADO 01 EVACUACIÓN
QUIRÚRGICA
COMPARACIÓN 13 GEMEPROST VAGINAL VERSUS EVACUACIÓN QUIRÚRGICA DEL ÚTERO, RESULTADO 02 PERFORACIÓN DEL
ÚTERO
COMPARACIÓN 13 GEMEPROST VAGINAL VERSUS EVACUACIÓN QUIRÚRGICA DEL ÚTERO, RESULTADO 03 NÁUSEAS
Tratamiento clínico para la muerte fetal temprana (menos de 24 semanas)
Copyright © 2007, La Colaboración Cochrane. Publicado por John Wiley & Sons, Ltd.
XML to PDF by RenderX XEP XSL-FO Formatter, visit us at http://www.renderx.com/
55
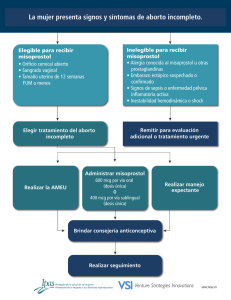




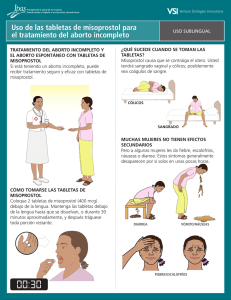
![Finalización de la gestación [Modo de compatibilidad]](http://s2.studylib.es/store/data/006311140_1-9ee2d15dfc724b1d09c32bde78c356bf-300x300.png)