Melody - Medtronic
Anuncio

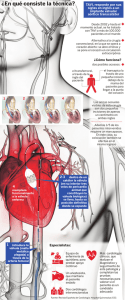
Melody ® TERAPIA CON VÁLVULA PULMONAR TRANSCATÉTER Desempeño comprobado, fácil de realizar Comprometido con los pacientes Con la terapia TVP Melody®, los niños y adultos con conductos disfuncionales de la válvula pulmonar tienen una opción de tratamiento comprobado diseñado para restablecer la función de la válvula pulmonar y retrasar la necesidad de una intervención quirúrgica. Miles de pacientes alrededor del mundo se han beneficiado con esta terapia. Se ha comprobado que el reemplazo de la válvula pulmonar transcatéter con la válvula Melody es un tratamiento seguro y efectivo para los pacientes con disfunción del conducto del tracto de salida del ventrículo derecho (RVOT) después de la operación. Se ha comprobado que la TPV Melody: • Libera la obstrucción del conducto • Restaura la función de la válvula • Retrasa el próximo reemplazo quirúrgico del conducto del paciente Un enfoque menos invasivo para restaurar la función de la válvula Diseño de la válvula pulmonar La válvula Melody está diseñada específicamente para tratar la disfunción de la válvula RVOT. Compuesta por una válvula de vena yugular bovina (BJV) suturada dentro de un marco de iridio de platino: • V alvas de la válvula venosa natural que se abren y cierran bajo presión mínima para una hemodinámica óptima • C oaptación profunda de valvas proporciona competencia de la válvula a través de un rango de medidas y geometrías de conductos • Stent radiopaco para una cómoda visualización Dispensador de la válvula transcatéter El sistema de dispensación Ensemble despliega la válvula Melody, con guía fluoroscópica, a través del sistema cardiovascular del cuerpo: • Simple plegamiento y carga manual de la válvula • F unda integrada que elimina la necesidad de una funda adicional y protege la válvula durante la dispensación • Tecnología balón-en-balón (BIB) para un despliegue controlado de la válvula Evidencia clínica sustancial Experiencia clínica de la TPV Melody Número de centros Número de pacientes Primer implante Último implante Estudio US IDE1,2 5 150 2007 2010 3 años US PAS3 10 100 2010 2012 1 año EU/CA PMSS1 7 63 2007 2009 5 años Experiencia RU4 1 155 2000 2007 5.8 años Estudio alemán5 2 102 2006 2010 1 año Registro italiano6 6 63 2007 2010 1 año Experiencia canadiense7 1 28 2005 2008 3 años Registro francés8 5 64 2008 2010 5 años Estudio Datos reportados 1. M cElhinney DB, Cheatham JP, Jones TK, et al. Stent fracture, valve dysfunction, and right ventricular outflow tract reintervention after transcatheter pulmonary valve implantation: patient-related and procedural risk factors in the US Melody Valve Trial. Circ Cardiovasc Interv. 2011 Dec 1;4(6):602-14. Epub 2011 Nov 9. 2. McElhinney DB, Hellenbrand WE, Zahn EM, et al. Short- and medium-term outcomes after transcatheter pulmonary valve placement in the expanded multicenter US melody valve trial. Circulation. 2010;122:507-16. 3. Armstrong AK, Balzer DT, Cabalka AK, et al. One-year follow-up of the Melody transcatheter pulmonary valve multicenter post-approval study. JACC Cardiovasc Interv. 2014 Nov;7(11):1254-62. 4. Lurz P, Coats L, Khambadkone S, et al. Percutaneous pulmonary valve implantation: impact of evolving technology and learning curve on clinical outcome. Circulation. 2008 Apr 15;117(15):1964-72. Epub 2008 Apr 7. 5. Eicken A, Ewert P, Hager A, et al. Percutaneous pulmonary valve implantation: two-centre experience with more than 100 patients. Eur Heart J. 2011 May;32(10):1260-5. Epub 2011 Jan 27. 6. Butera G, Milanesi O, Spadoni I, et al. Melody transcatheter pulmonary valve implantation. Results from the registry of the Italian Society of Pediatric Cardiology (SICP). Catheter Cardiovasc Interv. 2012 Jun 21. doi: 10.1002/ ccd.24518. [Pub. electrónica antes de impresión]. 7. Vezmar M, Chaturvedi R, Lee KJ, et al. Percutaneous pulmonary valve implantation in the young 2-year follow-up. JACC Cardiovasc Interv. 2010 Apr;3(4):439-48. 8. Fraisse A, Aldebert P, Malekzadeh-Milani S, et al. Melody transcatheter pulmonary valve implantation: Results from a French registry. Arch Cardiovasc Dis. 2014 Nov;107(11):607-14. doi: 10.1016/j.acvd.2014.10.001. Epub 2014 Nov 6. Desde el año 2007, los datos acumulados sobre TPV Melody y el Sistema de dispensación Ensemble han demostrado de manera consistente resultados clínicos excelentes. Los datos presentados en las siguientes páginas provienen de estos tres estudios: Estudio US IDE Estudio de investigación prospectivo, no aleatorio llevado a cabo en cinco centros. 150 sujetos con implante entre enero de 2007 y enero de 2010; se les dará seguimiento a los pacientes durante 10 años. Los datos presentados son resultados provisionales vigentes al 1 de marzo de 2014 (duración media de seguimiento de 4.4 ± 1.3 años). Estudio después de la aprobación EE. UU. (PAS) Estudio de investigación prospectivo, no aleatorio llevado a cabo en 10 centros. 100 sujetos con implante entre julio de 2010 y julio de 2012; se les dará seguimiento a los pacientes durante cinco años. Los datos presentados son resultados provisionales al 1 de marzo de 2014 (duración media de seguimiento de 2.1 ± 0.8 años). Estudio de vigilancia después de comercialización en Europa y Canadá (PMSS) Estudio prospectivo, no aleatorio llevado a cabo en siete centros en Europa y Canadá. 63 sujetos con implante entre octubre de 2007 y abril de 2009; se les dará seguimiento a los pacientes durante cinco años. Los datos presentados son resultados provisionales al 1 de marzo de 2014 (duración media de seguimiento de 4.2 ± 1.1 años). Rendimiento comprobado Demora la próxima intervención quirúrgica del paciente Menores índices de nuevas operaciones quirúrgicas de conductos en cinco años. 99.3% 100% Freedom From Conduit Reoperation 91.7% 98.4% 97.9% 90% 91.7% 80% 70% IDE Study PAS PMSS 60% 50% 40% 30% Number at risk: 20% 149 144 62 58 128 18 56 108 63 62 145 91 60 53 13 0 1 2 3 4 5 10% 99 0% Years Post-Implant No más nuevas intervenciones con catéter No más nuevas intervenciones con catéter en TPV fue más del 80% en cinco años. 100% 100% Freedom From Re-Intervention 90% 80.9% 79.5% 97.3% 91.8% 80% 70% IDE Study PAS PMSS 60% 50% 40% 30% Number at risk: 20% 149 133 63 50 113 17 48 90 50 62 142 91 55 46 11 0 1 2 3 4 5 10% 99 0% Years Post Implant Excelente rendimiento de la válvula Menores gradientes RVOT Después del implante de TPV Melody la media de gradientes RVOT disminuyó y permaneció consistente durante todo el seguimiento en los tres estudios. Media del gradiente RVOT por intervalo de tiempo Visita inicial 1 año 3 años 5 años Estudio IDE (N=149) 32.1 ± 13.9 18.7 ± 9.1 17.5 ± 7.8 17.1 ± 7.5 Estudio después de la aprobación (N=99) 33.4 ± 14.1 15.1 ± 7.1 19.5 ± 15.4 -- Estudio de vigilancia después de la comercialización (N=62) 37.7 ± 12.1 17.9 ± 9.2 17.3 ± 8.4 16.4 ± 8.6 Mean RVOT Gradient (mm Hg) 40 IDE Study PAS PMSS 35 30 25 20 15 10 5 0 Baseline 1 Year 2 Year 3 Year 4 Year 5 Year Regurgitación mínima La mayoría de sujetos en los tres estudios tenía una regurgitación pulmonar moderada o severa al inicio. Durante todo el seguimiento, la mayoría de sujetos no tenía más que trazas de regurgitación pulmonar. 100% None 80% Trace 70% Mild 60% Moderate 50% Severe 40% 30% 20% Baseline 1 Year 3 Years PMSS IDE PMSS PAS IDE PMSS PAS IDE PMSS 0% PAS 10% IDE Pulmonary Regurgitation Rates 90% 5 Years Estudio IDE (N=149) PAS (N=99) PMSS (N=62) Éxito procedimental y perfil de segu Altos índices de éxito en el procedimiento agudo Altos índices de manera consistente en la implantación exitosa de válvulas en los tres estudios, incluyendo fuerte hemodinámica y baja incidencia de eventos adversos de procedimiento. El éxito procedimental es un resultado compuesto definido como: • T PV Melody se administró con éxito en el lugar designado • E l gradiente pico a pico RV-PA (medido en el laboratorio de cateterización) menor a 35 mmHg después del implante •M enos que regurgitación pulmonar leve • S in explantación a las 24 horas después del implante Estudio Sujetos con éxito en el procedimiento Estudio IDE (N=149) 94.7% Estudio después de la aprobación (N=99) 92.1% Estudio de vigilancia después de la comercialización (N=62) 85.7%* *No se evaluó a tres sujetos por una o más de las variables compuestas y fueron considerados como una falla de procedimiento. uridad fortalecido Bajos índices de eventos adversos relacionados con el dispositivo El perfil de seguridad de la válvula Melody permanece por cinco años como lo evidencian los bajos índices de eventos adversos relacionados con el dispositivo en todas las categorías. Estudio IDE PMSS PAS No más eventos en cinco años (SE) (N=149) No más eventos en cuatro años (SE) (N=62) No más eventos en dos años (SE) (N=99) Rotura de stent: mayor 84.3% (4.5%) 91.5% (3.8%) 97.6% (1.9%) Disfunción de la válvula: estenosis 79.9% (4.9%) 86.1% (4.7%) 96.3% (2.3%) Disfunción de la válvula: Regurgitación 99.2% (1.1%) 98.3% (1.8%) 96.7% (2.3%) Endocarditis de la válvula protésica 96.1% (2.4%) 94.9% (3.0%) 92.9% (3.2%) 100.0% (-) 100% (-) 100.0% (-) Evento Embolización de la TPV Mejoras en la calidad de vida Mejora el estado funcional 100% 90% Class I 80% Class II 70% Class III 60% Class IV 50% 40% 30% 20% Baseline 1 Year 3 Years PMSS IDE PMSS PAS IDE PMSS PAS IDE PMSS 0% PAS 10% IDE NYHA Functional Class by Time and Interval Al inicio, la mayoría de sujetos en los tres estudios estaban en NYHA clase II/III. Después del implante de TPV Melody, la mayoría de sujetos estaban en NYHA clase I, lo que permaneció consistente durante el seguimiento. 5 Years Estudio IDE (N=149) PAS (N=99) PMSS (N=62) Mejora la calidad de vida En PMSS, las Evaluaciones de Calidad de vida (QoL) utilizando EQ-5D se obtuvieron al inicio y anualmente durante todo el seguimiento. El Estado de salud EQ-5D demostró mejoras tempranas que se sostuvieron por medio del seguimiento en la mayoría de categorías, incluyendo Dificultades con movilidad, Problemas con actividades usuales, Dolor o molestia, y Ansiedad o depresión. Estado de salud EQ-5D (0-100) Inicial (N=43) Seis meses (N=40) 1 año (N=39) Cuatro años (N=36) 72.3 ± 20.4 83.1 ± 12.2 85.5 ± 12.4 86.7 ± 12.5 EQ-5D es un instrumento estandarizado para utilizarse como una medida de resultado de salud aplicable a un amplio rango de condiciones y tratamientos de salud. Proporciona un perfil descriptivo simple y un valor de índice simple para el estado de la salud. Una mayor calificación del Estado de salud representa una mejora en QoL. Para obtener más información, visite www.Melody-TPV.com Desempeño comprobado, fácil de realizar Válvula pulmonar transcatéter Melody®, Sistema dispensador de la válvula transcatéter Ensemble® Información importante en la etiqueta para Estados Unidos. Indicaciones: el TVP Melody está indicado para utilizarse como un complemento a la cirugía en el manejo de pacientes pediátricos y adultos con las siguientes condiciones clínicas: • E xistencia de un conducto RVOT completo (circunferencial) de diámetro igual o superior a 16 mm en el momento de la implantación original Y • Conductos RVOT disfuncionales con una indicación clínica para intervención, Y -Regurgitación: ≥ regurgitación moderada, O -Estenosis: gradiente RVOT media ≥ 35 mm Hg Contraindicaciones: ninguna conocida. Advertencias/Precauciones/Efectos secundarios: • NO implantar en la posición aórtica o mitral. Las pruebas de simulación preclínicas de la válvula Melody sugieren que la función y durabilidad de la válvula se limitarán extremadamente cuando se utilice en estos lugares. • NO la use si la anatomía del paciente impide la introducción de la válvula, si la anatomía venosa no puede acomodar un introductor con medida de 22-Fr, o si existe una obstrucción significativa de las venas centrales. • NO la use si hay una señal clínica o biológica de infección, incluyendo endocarditis activa. Se debe considerar enfáticamente la atención médica y quirúrgica estándar en estas circunstancias. • Se debe llevar a cabo la evaluación de la anatomía de la arteria coronaria por riesgo de la compresión de dicha arteria en todos los pacientes antes del despliegue de la TPV. • Para minimizar la ruptura del conducto, no utilice un balón con un diámetro mayor al 110% del diámetro nominal (tamaño original del implante) del conducto para la dilatación previa del lugar designado para el despliegue, o para el despliegue de la TPV. • Se debe considerar la posibilidad de rotura del stent en todos los pacientes que se someten a la colocación de la TPV. Deberá incluirse un examen radiográfico del stent mediante fluoroscopia o radiografía de tórax en la evaluación sistemática posterior a la operación de los pacientes que reciban una TPV. • Si se detecta una rotura del stent, deberá realizarse un seguimiento continuado del stent junto con la evaluación hemodinámica clínicamente apropiada. En los pacientes que presenten una rotura del stent y una insuficiencia u obstrucción importantes asociadas del RVOT, deberá considerarse la posibilidad de realizar una nueva intervención conforme a lapráctica clínica habitual. Las posibles complicaciones derivadas del procedimiento que pueden surgir por la implantación del dispositivo Melody incluyen las siguientes: ruptura del conducto RVOT, compresión de un vaso sanguíneo mayor, embolia o migración del dispositivo, perforación de una cámara cardíaca, arritmias, reacción alérgica al medio de contraste, eventos cerebrovasculares (TIA, CVA), infección/sepsis, fiebre, hematoma, eritema inducido por la radiación, ampollas o descamación de la piel, dolor, hinchazón o moretones en el lugar de la cateterización. Los posibles eventos adversos relacionados con el dispositivo que pueden ocurrir después de la implantación del dispositivo incluyen los siguientes: rotura del stent,* rotura del stent lo que provocaría obstrucción recurrente, endocarditis, embolia o migración del dispositivo, disfunción valvular (estenosis o regurgitación), fuga paravalvular, trombosis valvular, tromboembolismo pulmonar, hemólisis. * El término “rotura del stent” se refiere a la rotura de la TPV Melody. Sin embargo, en sujetos con varios stents en la RVOT es difícil atribuir definitivamente roturas del stent al marco de Melody en comparación con otro stent. Para obtener más información, consulte las instrucciones de uso suministradas con el producto. PRECAUCIÓN: Las leyes federales (EE. UU.) restringen la venta de este dispositivo a médicos o bajo su supervisión. Información importante en la etiqueta para geografías fuera de Estados Unidos. Indicaciones: la Válvula Pulmonar Transcatéter Melody® está indicada para utilizarse con pacientes con las siguientes condiciones clínicas: • Pacientes que presentan conductos de tracto de salida del ventrículo derecho (Right Ventricular Outflow Tract, RVOT) protésicos regurgitantes con una indicación clínica para intervención invasiva o quirúrgica, O BIEN • Pacientes con conductos RVOT protésicos estenóticos en los que el riesgo de empeoramiento de la regurgitación es una contraindicación relativa para la dilatación por balón o la colocación de un stent. • E xistencia de un conducto RVOT completo (circunferencial) de diámetro igual o superior a 16 mm en el momento de la implantación original. La vida útil prevista para el dispositivo Melody® es de dos años. Contraindicaciones: • Anatomía venosa incapaz de alojar una funda introductora de tamaño 22 Fr; Implantación en el ventrículo izquierdo; • Tracto de salida del ventrículo derecho no favorable para un correcto anclaje del stent; • Obstrucción del tracto de salida del ventrículo derecho grave que no se puede dilatar mediante un balón; • Obstrucción de las venas centrales; • Signos clínicos o biológicos de infección; • Endocarditis activa; • Alergia conocida a la aspirina o la heparina; • Embarazo. Posibles complicaciones y efectos adversos: las posibles complicaciones derivadas del procedimiento que pueden surgir por la implantación del dispositivo Melody incluyen las siguientes: ruptura del conducto RVOT, compresión de un vaso sanguíneo mayor, embolia o migración del dispositivo, perforación de una cámara cardíaca, arritmias, reacción alérgica al medio de contraste, eventos cerebrovasculares (TIA, CVA), infección/sepsis, fiebre, hematoma, eritema inducido por la radiación, dolor en el lugar de la cateterización. Los posibles eventos adversos relacionados con el dispositivo que pueden ocurrir después de la implantación del dispositivo incluyen los siguientes: rotura del stent lo que provocaría obstrucción recurrente, endocarditis, embolia o migración del dispositivo, disfunción valvular (estenosis o regurgitación), fuga paravalvular, trombosis valvular, tromboembolismo pulmonar, hemólisis. Para obtener más información, consulte las instrucciones de uso suministradas con el producto. La Válvula pulmonar transcatéter Melody® y el Sistema de dispensación de transcatéter Ensemble® han recibido la aprobación de la Marca CE y están disponibles para su distribución en Europa. Adicionalmente, se ha otorgado una Licencia de Dispositivo médico y el sistema está disponible para su distribución en Canadá. melody-tpv.com // medtronic.com Medtronic 710 Medtronic Parkway Minneapolis, MN 55432-5604 USA Tel: (763) 514-4000 Fax: (763) 514-4879 Llamada gratuita: 1 (800) 328-2518 (soporte técnico las 24 horas para médicos y profesionales de la salud) Europa Medtronic International Trading Sàrl Route du Molliau 31 Case postale 84 CH-1131 Tolochenaz Switzerland Tel: 41.21.802.7000 Fax: 41.21.802.7900 Canada Medtronic of Canada Ltd. 99 Hereford Street Brampton, Ontario L6Y 0R3 Canada Tel: (905) 460-3800 Fax: (905) 460-3998 Llamada gratuita: 1 (800) 268-5346 Asia Medtronic International Ltd. 49 Changi South Avenue 2 Nasaco Tech Centre Singapore 486056 Singapore Tel: (65) 6436 5000 Fax: (65) 6776 6335 América Latina Medtronic USA Doral Corporate Center II 3750 NW 87th Avenue Suite 700 Miami, FL 33178 USA Tel: (305) 500-9328 Fax: (786) 709-4244 LifeLine Asistencia técnica de Cardiovascular Tel: (877) 526-7890 Tel: (763) 526-7890 Fax: (763) 526-7888 Correo electrónico: rs.cstechsupport@medtronic.com Melody y Ensemble son marcas comerciales registradas de Medtronic. UC201501804 AS © 2015 Medtronic. Todos los derechos reservados. 01/2015