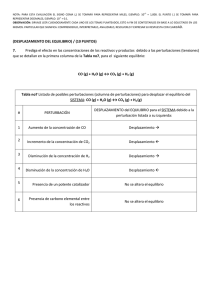
Tabla periódica
Anuncio

Tema 5. REACCIONES QUIMICAS 1.Calcula para la siguiente reacción los valores de x e y A + 4g 10 g B === C 12g 16g x y x = masa de B = 10 g A x 12 g B / 4 g A = 30 g B y = masa de C = 10 g A x 16 g C / 4 g A = 40 g C 2. Ajusta la reacción: C6H12O6 + O2 === CO2 + H2O 1º. Carbono: como hay 6, multiplicamos por 6 el CO2 2º. Hidrógeno: como hay 12, multiplicamos por 6 el H2O 3º. Oxígeno: a la derecha hay 18 y a la izquierda 8. luego necesitamos 10 más, así multiplicamos el oxígeno por 6. C6H12O6 + 6 O2 === 6 CO2 + 6 H2O 3. Ajusta las siguientes reacciones: a) N2 + H2 ==== NH3 b) HCl + Al === AlCl3 + H2 c) SO2 + H2S === S + H2O 4. El magnesio reacciona con el oxígeno dando óxido de magnesio. Si partimos de 5 g de magnesio halla la masa de óxido de magnesio. Datos: Pesos atómicos: Mg=24, O=16. En primer lugar escribimos la reacción y la ajustamos. Luego calculamos las masas moleculares y las ponemos debajo del compuesto correspondiente: 2 Mg + O2 === 2 MgO 2*24 g -------------------- 2*40 g 5 g ---------------------- x . masa de óxido= 5 g Mg x 2x40 g MgO / 2+24 g Mg = 8,3 g MgO 5. El sodio reacciona violentamente con el agua dando el hidróxido y liberando hidrógeno. Halla la masa de sodio que produce 100 g de hidrógeno. (Pesos atómicos: Na=23, O=16, H=1) 2 Na + 2 H2O === 2 NaOH + H2 2*23 g -------------------------------- 2 g x ------------------------------------- 100 g masa de sodio = 100 g H2 x 46 g Na / 2 g H2 = 2300 g Na 6. Escribe la reacción entre el hidrógeno y el oxígeno para formar agua. Y calcula: a) Cuantos gramos de agua se obtendrían a partir de 10 gr de hidrógeno b) Que volumen de hidrógeno medido en C.N. sería necesario para formar 1 g de agua 2 H2 + O2 ==== 2 H2O 2*2 g H2 ---------- 2*18 g H2O 10 g H2 ----------- x masa de agua que se forma = 10 * 2*18 / 2*2 = 90 g H2O 2 H2 + O2 ==== 2 H2O 2*22,4 L H2 ------ 2*18 g H2O V ------------- 1 g H2O V = 2*22,4 / 2*18 = 1,24 L de H2 en C.N. 7. Escribe la reacción del combustión del carbono para formar CO2 y calcular la masa de carbono que reacciona estequiométricamente con 8 litros de oxígeno, medidos a presión normal y 27ºC de temperatura, para formar CO2. En primer lugar vamos a calcular el volumen de CO2 medido en condiciones normales, para eso: Condiciones iniciales P = 1 atm V=8L T = 27ºC+273 = 300 ºK P*V T ------- = --P´*V´ T´ ; Condiciones al final P’ = 1 atm V’ = ? T’ = 0ºC =273 ºK 1*8 300 ------------- = -----1 * V´ 273 Simplificamos y despejamos: V´ = 7,28 L de CO2 en C.N. C + O2 ==== CO2 12 g C ---------- 22,4 L de O2 en CN x -------------- 7,28 L O2 en CN masa de carbono necesaria = 12 * 7,28 / 22,4 = 3,9 g de C