descargar artículo - Revista de Patología Respiratoria
Anuncio

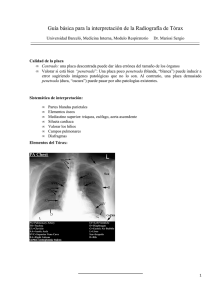
REVISTA DE Patología Respiratoria Volumen 18 • Número 2 • Abril-Junio 2015 nota clínica Infiltrados pulmonares alveolares difusos: un reto diagnóstico para el clínico E. Lozano Rincón, L. Cabeza Osorio, M. Arroyo Gallego, B. Arnalich Jiménez, Á. Casanova Espinosa Hospital Universitario del Henares. Coslada. Madrid. Rev Patol Respir. 2015; 18(2): 82-85 Resumen La presencia de infiltrados pulmonares bilaterales es un hallazgo radiológico frecuente en la práctica clínica habitual. En un varón de edad media no siempre es indicativo de infección y hay que considerar otras entidades diagnósticas (procesos no infecciosos). La sospecha de metástasis pulmonares debe incluirse dentro de estas entidades, aunque se trate de un diagnóstico clínico poco frecuente. La clínica es variable y depende del tumor primario, la edad del paciente, la situación cardiorrespiratoria del mismo y del mecanismo de diseminación tumoral. La linfangitis carcinomatosa es un patrón poco frecuente de metástasis pulmonares y el diagnóstico diferencial se realiza con procesos infecciosos (como neumonías atípicas) e inflamatorios (neumonía intersticial, neumonitis por hipersensibilidad o eosinofilias pulmonares). El paciente que se presenta debutó con clínica respiratoria e infiltrados pulmonares bilaterales y fue diagnosticado de linfangitis carcinomatosa, cuyo origen era un adenocarcinoma gástrico. Palabras clave: Infiltrados pulmonares alveolares difusos; Linfangitis carcinomatosa. Abstract The presence of bilateral pulmonary infiltrates is a frequent radiological finding in routine clinical practice. In a middle-aged man is not always indicative of infection and you need to consider other diagnostic entities (non-infectious processes). Suspected pulmonary metastases should be included in these entities, although it is a rare clinical diagnosis. The clinical course is variable and depends on the primary tumor, the patient’s age, cardiopulmonary status thereof and the mechanism of tumor dissemination . Carcinomatous lymphangitis is a rare radiographic pattern of pulmonary metastases and the differential diagnosis includes infectious processes (such as atypical pneumonia) and inflammatory diseases (interstitial pneumonia, hypersensitivity pneumonitis or pulmonary eosinophilia). We report the case of a man with respiratory symptoms and bilateral pulmonary infiltrates who was diagnosed of carcinomatous lymphangitis, whose origin was a gastric adenocarcinoma. Key words: Diffusse alveolar pulmonary infiltrates; Carcinomatous lymphangitis. Introducción El hallazgo en una radiografía simple de tórax de infiltrados pulmonares bilaterales en un paciente joven con clínica de disnea y tos obliga al clínico a realizar un diagnóstico diferencial exhaustivo que engloba a diferentes entidades que pueden ser el desencadenante de los mismos. A pesar de que las infecciones respiratorias (bacterias, virus, micobacterias) son, a priori, la causa más frecuente de infiltrados pulmonares, hay que considerar otros procesos no infecciosos (cardiogénicos, inflamatorios e inmunológicos) y en ocasiones otros menos frecuentes, que también pueden dar lugar a este patrón radiológico. Para llevar a cabo un buen diagnóstico diferencial es necesario realizar una historia clínica meticulosa, que incluya la historia exposicional y ocupacional del paciente, los factores de riesgo para infecciones oportunistas, los antecedentes familiares, la ingesta de fármacos y sustancias tóxicas y constatar la existencia de enfermedades sistémicas. Correspondencia: Erika Lozano Rincón. Hospital Universitario del Henares. Avda/ Marie Curie s/n 28822. Coslada (Madrid). E-mail: erika.lozano.rincon@gmail Recibido: 11 de agosto de 2014; Aceptado: 11 de septiembre de 2014 82 Revista de Patología Respiratoria Vol. 18 Nº2 - Abril-Junio 2015 Se presenta el caso de un varón de 53 años que acude por disnea y tos de varios meses de evolución con infiltrados alveolares parcheados difusos y derrame pleural izquierdo en la radiografía de tórax convencional. Tras realizar las exploraciones y pruebas complementarias pertinentes, se diagnosticó de una entidad poco frecuente entre los desencadenantes de infiltrados pulmonares. Caso clínico Varón de 53 años de edad, sin alergias medicamentosas ni sensibilización a neumoalérgenos ambientales. Había sido fumador de 10 cigarrillos al día hasta el año 2009 (índice paquetes/año: 15) y ex bebedor, de un litro de vino al día, desde hacía 2 meses. Trabajador durante 33 años y hasta la fecha del ingreso en un almacén frigorífico de pollos, encargándose de recibir, despiezar y empaquetar la mercancía. Además, en su historia exposicional destacaba la presencia en su domicilio de dos jilgueros, un canario y una ninfa. No presentaba antecedentes médico-quirúrgicos de interés, ni había requerido ingresos hospitalarios. No realizaba ningún tratamiento de forma habitual y nunca había presentado síntomas sugestivos de las enfermedades del tejido conectivo (artralgias, mialgias, fenómeno de Raynaud). No vivía en condiciones de hacinamiento y no había contactado, que supiera, con enfermos de tuberculosis. Acude al Servicio de Urgencias por un cuadro de disnea y tos seca de dos meses de evolución, refractario a tratamiento con antitusivos, mucolíticos y antibióticos. Había experimentado pérdida de 20 kilogramos de peso en los últimos meses. No había tenido fiebre, dolor torácico ni hemoptisis. No refería síntomas extratorácicos, digestivos ni urinarios. A la exploración física destacaba una tensión arterial de 175/93, una frecuencia cardiaca de 88 lpm, una temperatura de 36,8°C y una saturación de oxígeno basal con pulsioximetría del 89%. Ligera taquipnea con el esfuerzo, sin disnea de reposo. La auscultación pulmonar mostraba estertores crepitantes bibasales, más acentuados en la base pulmonar derecha con una disminución generalizada del murmullo vesicular. La auscultación cardiaca era normal. No se palpaban adenopatías cervicales, supraclaviculares ni axilares. La exploración neurológica, la exploración abdominal y el resto de la exploración física eran normales. En relación a los parámetros analíticos, el paciente tenía una leucocitosis (11.560 leucocitos/mm3) con neutrofilia (78%). Los eosinófilos eran normales (2,5% del total). La hemoglobina era de 11,4 g/dl, el hematocrito de 34,4% y las plaquetas de 427.000. El estudio de la coagulación (actividad de protrombina 71,1%, I.N.R. 1,19, fibrinógeno >500 mg/ dL), la función renal (urea 16 mg/dl, creatinina 0,62 mg/dl) y los iones (sodio 137 mmol/L, potasio 3,5 mmol/L) dentro de los parámetros de la normalidad. El perfil hepático (GPT 14 U/L, GOT 19 U/L) y los marcadores de daño miocárdico (troponina I <0,017) eran normales. Había una elevación de los reactantes de fase aguda (LDH 216 U/L y proteína c reactiva 121,3 mg/L) y datos de insuficiencia respiratoria aguda con alcalosis respiratoria (pH: Revista de Patología Respiratoria Vol. 18 Nº2 - Abril-Junio 2015 Figuras 1 y 2. Radiografía simple de tórax PA y L donde se aprecian infiltrados alveolares pulmonares bilaterales y pequeño derrame pleural izquierdo. 7,50, PaCO2: 33,6 mmHg, PaO2: 55,8 mmHg, bicarbonato: 25,4 mmol/L) en la gasometría arterial basal realizada a su llegada al Servicio de Urgencias. En la radiografía de tórax presentaba infiltrados alveolares parcheados en ambos hemitórax, con afectación de ambos lóbulos inferiores y del lóbulo superior izquierdo y derrame pleural izquierdo (Figs. 1 y 2). Con el diagnóstico de presunción de posible neumonía bilateral se inició tratamiento empírico con levofloxacino 500 mg cada 24 horas intravenoso, oxigenoterapia con Venturi al 28% (4 litros) y analgesia (paracetamol) a demanda Se completó el estudio de imagen con tomografía axial computarizada de alta resolución (TACAR) torácica para una mejor caracterización de las lesiones. Se identificaron infiltrados alveolares parcheados en lóbulos superiores e inferiores, que oscilaban entre los pocos milímetros y centímetros de 83 Figuras 3, 4 y 5. Cortes de TACAR de tórax (campos pulmonares superiores, medios e inferiores) donde se aprecian infiltrados pulmonares bilaterales difusos de diferentes tamaños, engrosamientos septales interlobulillares y derrame pleural bilateral. tamaño y se acompañaban de patología distal con imágenes en árbol en brote de distribución difusa. En el mediastino se observaron adenopatías de tamaño patológico de localización prevascular, paratraqueal y subcarinal, y derrame pleural bilateral (Figs. 3, 4 y 5). 84 Entre los diagnósticos diferenciales que planteamos en nuestro paciente incluimos las diferentes causas de infiltrados pulmonares bilaterales difusos. Entre ellas el edema pulmonar cardiogénico, las neumonías bacterianas típicas y atípicas, la tuberculosis pulmonar, neumonías por virus y Pneumocistys jirovecii, la neumonía intersticial, la neumonía organizada criptogenética, la neumonitis por hipersensibilidad, la afectación pulmonar de las colagenopatías, las eosinofilias pulmonares, las vasculitis (enfermedad de Wegener), el carcinoma bronquioalveolar, los síndromes linfoproliferativos y la carcinomatosis linfangítica. Se amplió el estudio analítico con inmunología (ANCAs, ANAs, ENAs, ECA, factor reumatoide, inmunoglobulinas), serologías para virus (VIH, VHB, VHC, CMV, EBV y VVZ) y serología de NAC (virus respiratorio sincitial, influenza A y B, Legionella pneumophila, Mycoplasma pneumoniae, Coxiella. burnetii, Chlamydia pneumoniae), siendo todos negativos. Los antígenos en orina para neumococo y Legionella fueron negativos. Se realizó un ecocardiograma sin observarse disfunción ventricular izquierda ni alteraciones valvulares, con una fracción de eyección del ventrículo izquierdo conservada, sin derrame pericárdico. Dado el compromiso respiratorio del paciente con insuficiencia respiratoria aguda, se decidió su ingreso en la UCI para la realización de una fibrobroncoscopia con soporte ventilatorio a través de tubo endotraqueal. Se identificaron alteraciones a nivel de la mucosa del LSI y de la carina de separación con la língula, mostrando un aspecto muy inflamado, granulado y blanquecino, así como una disminución de la luz del culmen. La mucosa del árbol bronquial derecho estaba ligeramente inflamada, sin presentar lesiones endoluminales. Se realizó lavado broncoalveolar en língula con población mayoritariamente macrofágica (90%) y citologías negativas para malignidad. La tinción de auramina, los cultivos para hongos y bacterias y la inmunofluorescencia directa para P. jirovecii fueron negativas. La toracocentesis para el estudio del líquido pleural evidenció un líquido de aspecto seroso con características de exudado pleural línfocítico con ADA normal (LDH 206 U/L, proteínas 3,8 g/dl, glucosa 119 mg/Dl y 325 leucocitos con 89% de linfomononucleares). Tras varios días de hospitalización del paciente, se obtuvieron los resultados de la biopsia bronquial, identificándose una mucosa bronquial infiltrada por una población celular sospechosa de malignidad, con inmunofenotipo sugestivo de adenocarcinoma aunque sin poder establecer un diagnóstico definitivo dado el tamaño pequeño de la muestra. Fue la realización de una segunda fibrobroncoscopia la que estableció el diagnóstico de linfangitis carcinomatosa de adenocarcinoma. Se completó el estudio con la realización de una TAC abdominal y un estudio endoscópico digestivo (gastroscopia y colonoscopia), donde se observó un engrosamiento irregular del cuerpo gástrico con erosión y ulceración. El resultado de las biopsias gástricas permitió establecer el diagnóstico final de adenocarcinoma gástrico, demostrando un origen abdominal de los infiltrados alveolares parcheados y del derrame pleural. Revista de Patología Respiratoria Vol. 18 Nº2 - Abril-Junio 2015 Discusión El pulmón es la segunda localización más frecuente de la enfermedad metastásica, englobando todos los tipos histológicos de tumores (alcanzando casi el 30% de los casos) y supone el único órgano de infiltración metastásica en el 20% de los mismos. Puede observarse una imagen de “suelta de globos” (nódulos pulmonares múltiples) o de linfangitis carcinomatosa con infiltrados difusos y afectación intersticial, como ocurre en el caso clínico que se expone. Anatómicamente, los pulmones son un lecho vascular muy rico, además del primer lecho capilar, que las células tumorales circulantes encuentran después de abandonar el tumor primario y “caer” al sistema de drenaje venoso. De este modo los pulmones actuarían como un filtro inicial y las células tumorales serían atrapadas de forma mecánica al llegar a él, creciendo después para formar la metástasis. Las metástasis por vía linfática son mucho menos frecuentes. Las células tumorales se diseminan por vía retrógrada a través de los ganglios hiliares y mediastínicos. Menos frecuentes son la diseminación linfangítica (sobre todo en los tumores gastrointestinales como el que se presenta en este caso), transbronquial, bronquial y procedente de derrame pleural maligno. La linfangitis carcinomatosa (LC) es un patrón poco frecuente de metástasis pulmonares (6-8% del total). Los principales tumores que originan LC son los de mama (33%), estómago (29%) y pulmón (17%). Histológicamente la mayoría son adenocarcinomas (70-80%). En nuestro caso, el paciente fue diagnosticado de linfangitis carcinomatosa cuyo origen era un adenocarcinoma gástrico. La presentación clínica habitual es disnea crónica y progresiva (similar a la referida por el paciente de nuestro caso clínico), que evoluciona en semanas o meses a insuficiencia respiratoria y muerte. Radiológicamente, lo más habitual es la presencia de infiltrados intersticiales retículo-nodulares, y en la TACAR, un engrosamiento nodular de los septos interlobulares y del intersticio perilobulillar, siendo este último un hallazgo altamente correlacionable con la anatomía patológica. Por consiguiente, el diagnóstico diferencial es muy amplio y se deben considerar varias entidades, tales como la neumonía atípica, la neumonitis por hipersensibilidad (una de nuestras sospechas diagnósticas iniciales al tener el paciente una historia exposicional significativa a antígenos aviares) y la eosinofilia pulmonar (descartada tras la ausencia de eosinofilia en sangre periférica y en el lavado broncoalveolar), las enfermedades relacionadas con el tejido conectivo (ausencia de síntomas y signos de estas entidades y estudio de autoinmunidad negati- Revista de Patología Respiratoria Vol. 18 Nº2 - Abril-Junio 2015 vo) o las neumonías intersticiales (descartadas tras completar el estudio con la TACAR y la fibrobroncoscopia). En el diagnóstico diferencial de los infiltrados pulmonares difusos la fibrobroncoscopia constituye una exploración complementaria fundamental. Permite la visualización directa endobronquial y la toma de muestras representativas del aparato respiratorio, permitiendo conocer la celularidad predominante (neutrófilos, linfocitos, eosinófilos, macrófagos), el estudio microbiológico de las muestras (virus, bacterias, micobacterias, hongos, Pneumocystis) y la toma de biopsias bronquiales y trasnbronquiales. El diagnóstico de certeza de la linfangitis carcinomatosa se establece mediante el estudio de la biopsia bronquial, transbronquial o pulmonar. En nuestro paciente, fue el resultado de la segunda biopsia (obtenida por fibrobroncoscopia) la que identificó células sospechosas de infiltración por adenocarcinoma de probable origen abdominal. La supervivencia de la linfangitis carcinomatosa oscila entre los 2 y los 4 meses tras el diagnóstico, aunque en ocasiones, como en nuestro paciente, la supervivencia no supera los 30 días. Existe evidencia científica sobre el tratamiento de la linfangitis carcinomatosa, como una condición tratable oncológicamente con impacto sobre la progresión de la disnea y las lesiones radiológicas, con cierta mejoría en la supervivencia. Sin embargo, no todos los pacientes son candidatos a este tratamiento puesto que, al igual que en nuestro caso, el diagnóstico es tardío y la evolución del tumor primario es muy avanzada. Nuestro paciente inició tratamiento oncológico paliativo con mala evolución clínica y progresión de la enfermedad. Finalmente, falleció 4 semanas después del diagnóstico. Bibliografía 1. Ré DP, Cazaux A, Cambursano VH, Zaya A, Cortés JR. Pulmonary carcinomatous lymphangitis: presentation as acute pneumopathy. Report of two cases. Revista Facultad de Ciencias Médicas. 2013; 70: 31-3. 2. Dettino A, Pagano T, Jardim C, Takagaki T, Deheinzelin D, Okamoto V, et al. Neoplastic pulmonary lymphangitis: Symptomatic treatment and quality-of-life evaluation in a prospective palliative care series. J Clin Oncology. 2007; 25: 1953-6. 3. Putnam JB Jr, Roth JA, Wesley MN, Johnston MR, Rosenberg SA. Survival following aggressive resection of pulmonary metastases from osteogenic sarcoma: analysis of prognostic factors. Ann Thorac Surg. 1983; 36: 516-23. 4. Jiménez Orozco E, Fernández Cantón I, Gordón Santiago MM, et al. Tumor metastásico pulmonar. En: Soto Campos JG, ed. Manual de diagnóstico y terapéutica en Neumología. Madrid: Ergon; 2005. p. 589-602. 85