4. Introducción a la Física Moderna. 4.1 Radiación de cuerpo negro
Anuncio

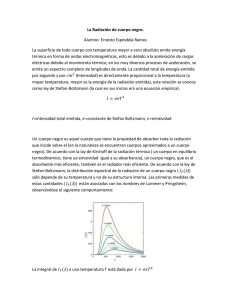
4. Introducción a la Física Moderna. 4.1 Radiación de cuerpo negro. Formula de Planck. 4.2 Efecto fotoeléctrico. 4.3 Naturaleza dual de la luz. Fotones 4.4 Naturaleza dual de los electrones: Ondas de De Broiglie 4.5 Espectro de átomo de hidrógeno. Modelo de Bohr 4.6 Ecuación de Schrödinger. Interpretación probabilística de la función de onda 4.7 Radiación y absorción de ondas electromagnéticas. 4.8 El laser (Light Amplification by Stimulated Emission of Radiation). A finales del siglo 19, los científicos creían que habían desarrollado la mayor parte de leyes de Física que permiten describir el mundo que lo que nos rodea. Leyes de Newton y su teoría de la gravitación universal, la obra teórica de Maxwell en unificador la electricidad y el magnetismo, y las leyes de la termodinámica y la teoría cinética métodos matemáticos empleados para explicar con éxito una amplia variedad de fenómenos. Sin embargo, al pasar al siglo 20, una gran revolución sacudió el mundo de la física. En 1900 Planck proporciona las ideas básicas que llevaron a la teoría cuántica, y en 1905 Einstein formuló su teoría de la relatividad. La emoción producida por estos descubrimientos fue señalada en las propias palabras de Einstein: "Fue una maravillosa tiempo de estar vivo”. Ambas ideas iban a tener un profundo efecto en nuestra comprensión de la naturaleza. En unas pocas décadas, estas teorías inspiraron nueva la evolución y las teorías en el campo de la atómica, nuclear y la teoría materia condenada. Aunque la física moderna ha dado lugar a una multitud de importantes logros tecnológicos, la historia es aún incompleta. Descubrimientos seguirán siendo hechos durante nuestra vida, muchas de las cuales se profundizará o refinar nuestra comprensión de la naturaleza y el mundo que nos rodea. Todavía es un "tiempo maravilloso estar vivo”. El funcionamiento de la mayoría de dispositivos opto y micro-electrónicos solo puede entender teniendo en cuenta algunas ideas de teoría cuántica, la cual como ciencia surgió al inicio del siglo XX. ¿Cuáles son Orígenes de Teoría Cuántica? “Creo que puedo afirmar con toda seguridad que nadie entiende la mecánica cuántica”. Así de tajante fue en una ocasión el Premio Nóbel de física Richard Feynman. Y es que ciertamente, esta teoría fundamental no es una herramienta sencilla para los físicos, y mucho menos para las personas que no han dedicado mucho tiempo a estudiarla. No obstante, cualquiera de nosotros puede hacerse una idea general sobre este tema. Físicos también estaban llegando a estas ideas un poco extraños paso a paso. MAX PLANCK Y LOS CUANTOS Todo comenzó en el año 1900, cuando el físico alemán Max Planck se enfrentaba a enormes dificultades para medir la radiación que emiten los cuerpos negros, los cuales son objetos teóricos que absorben toda la radiación que incide sobre ellos y posteriormente la emiten. Un ejemplo cotidiano aproximado sería un metal al rojo vivo, que tras recibir mucho calor comienza a emitir luz roja. Algo parecido a esta luz roja es lo que intentaba medir Max Planck, pero se encontró con que había demasiadas variaciones a nivel microscópico como para calcular la cantidad total con exactitud. El paso de gigante que dio Planck consistió en considerar que la energía no era emitida como algo continuo, sino que pensó que era mucho más fácil si se imaginaba pequeños paquetes de energía saliendo al exterior. Sería algo así como medir el volumen de un vaso de agua llenándolo de arroz, sabiendo cuanto granos hay y cuanto ocupa cada uno, sabríamos el volumen total más fácilmente que usando el agua para tal fin. Estos pequeños paquetes de energía fueron llamados cuantos, y Planck formuló que el tamaño de ellos contaba con un valor fijo. Este valor se llama ahora Constante de Planck. Es importante tener en cuenta que esto en aquella época se consideró un afortunado artificio teórico, pero que no se correspondía con la realidad física. Nadie consideraba aún que realmente la energía pudiera estar compuesta por pequeños paquetes. ALBERT EINSTEIN Y EL EFECTO FOTOELÉCTRICO Poco después, en 1905, este genio alemán, mientras estudiaba la naturaleza de ciertos metales que emiten electricidad cuando reciben luz, se dio cuenta de que el desarrollo de Planck le servía también a él, llegando a la sorprendente conclusión de que se podía considerar la luz como un conjunto de pequeños paquetes que golpeaban a los electrones y les hacían abandonar el metal. Calculó que la energía de los cuantos de luz (en la actualidad llamados fotones) también se medía a partir de la constante de Planck. Fue gracias a este estudio por el que Einstein recibió el Premio Nobel, por la descripción del llamado efecto fotoeléctrico, el cual ahora utilizamos en aparatos como placas solares o células fotoeléctricas, siendo el silicio el mejor material fotosensible utilizado. NIELS BOHR Y EL ÁTOMO Por su parte, el danés Niels Bohr, en el año 1913, encontró otra interesante “coincidencia” en la naturaleza relacionada con la constante de Planck. Se hallaba estudiando la naturaleza del átomo, concretamente del átomo de hidrógeno, por ser el más simple y tratarse de un campo nuevo en su época. Un átomo de hidrógeno consta de un electrón que gira alrededor de un núcleo compuesto solamente por un protón. Bohr propuso que cada electrón podía orbitar a distintas distancias de su núcleo, dependiendo de lo caliente que se hallara el gas. Pero lo realmente importante era que estas distancias no podían ser cualesquiera, sino que eran proporcionales a múltiplos enteros de la constante de Planck. Una vez más esa constante, que aún se consideraba un artificio matemático, venía ligada a un fenómeno natural a escala minúscula. LOUIS DE BROGLIE Y LA DOBLE NATURALEZA DE LA MATERIA El siguiente avance esencial vino de mano del francés Louis de Broglie, quien en 1924 expuso su tesis doctoral, en la cual propugnaba que el electrón en movimiento tenía una doble naturaleza: por un lado era una partícula, pero también presentaba las características de una onda. Para ello partió de la explicación cuántica de Einstein sobre la luz y vio que se podía aplicar a cualquier tipo de cuerpo, no sólo a los paquetes o cuantos de luz. En 1927 se llevó a cabo un experimento cuyo resultado se ajustaba a esta hipótesis. Se comprobó que los electrones experimentan difracción, una característica de las ondas. Este fue el primer paso para comprender que la materia tiene una doble naturaleza: onda y partícula, así como que las ondas presentan también comportamiento de partículas. Es lo que se llama dualidad onda partícula, y no sólo se da en los electrones y demás partículas subatómicas, se cumple en cualquier cuerpo, desde un balón de fútbol, pasando por una persona o un edificio, y hasta los planetas o el Sol. Lo que ocurre es que la longitud de onda es menor cuanto mayor es el objeto, y por tanto es inapreciable a escala mayor que la de los átomos. 4.1 Radiación de cuerpo negro. Formula de Planck. La radiación de ondas electromagnéticas por los cuerpos (emisión) puede realizarse a cuenta de diferentes tipos de energía. Lo más difundida es la radiación de calor, o sea la emisión de ondas electromagnéticas provocada por la energía interna do los cuerpos. Todas las demás variedades de emisión, estimulada por otros tipos de energía, excepto la interna (calorífica), se unen bajo el nombro común de «luminiscencia». El fósforo que so oxida en el aire resplandece como resultado de la energía que se libera do la transformación química. Esa clase de radiación se denomina quimioluminiscencia. La emisión que surge de diferentes clases de descargas autónomas en un gas lleva el nombre de electroluminiscencia. La luminiscencia de los sólidos, provocada por el bombardeo con electrones, es denominada catodolumlniscencia y provocada por la absorción de radiación electromagnética, fotoluminiscencia. La radiación de calor tiene lugar a cualquier temperatura, sin embargo, a bajas temperaturas se emiten prácticamente sólo ondas electromagnéticas largas (infrarrojas). Rodeemos el cuerpo emisor con una envoltura de superficie reflectora ideal (Fig. 4.1.1). Evacuemos el aire de la envoltura. La radiación que se refleja en la misma, al caer en el cuerpo, se absorbe por esto (completamente o en parte). Por lo tanto ocurre un intercambio ininterrumpido de energía entre el cuerpo y la radiación que llena la envoltura. Si la distribución de la energía entre el cuerpo y la radiación permanece invariable para cada longitud de onda, el estado del sistema cuerporadiación será de equilibrio. La experiencia muestra que el único tipo de radiación que puede encontrarse en equilibrio con los cuerpos emisores es la radiación de calor. Todas las demás variedades de radiación resultan ser desequilibradas. La capacidad de la radiación de calor de encontrarse en equilibrio-con los cuerpos emisores está condicionada por que su intensidad crece con el aumento de la temperatura. Supongamos que el Fig. 4.1.1 Equilibrio entre equilibrio entre el cuerpo y la radiación haya sido alterado y el cuerpo emita más energía que la que absorbe. Entonces la energía interna del cuerpo decrecerá, lo que conllevará a la disminución de la radiación y emisión temperatura. Esto a su vez provocará la reducción de la cantidad de energía emitida por el cuerpo. La temperatura del mismo irá decreciendo hasta que la cantidad de energía emitida no sea igual a la de energía absorbida. Si el equilibrio se altera hacia el otro lado, o sea la cantidad de energía emitida resulta ser menor que la absorbida, la temperatura del cuerpo irá aumentando hasta que se restablezca el equilibrio. De esta manera, la alteración del equilibrio en el sistema cuerpo-radiación provoca el surgimiento de procesos que lo restablecen. De todas las clases de radiación, la única que puede ser equilibrada es la radiación de calor. La intensidad de la radiación de calor se caracteriza mediante la magnitud del flujo de energía medido en vatios. El flujo de energía R emitido por la unidad de superficie del cuerpo emisor en unidad de tiempo en todas las direcciones se denomina luminosidad energética del cuerpo. La luminosidad energética es una función de la temperatura T. La radiación, además, se compone de ondas de diferentes frecuencias (o longitudes de onda λ ). El flujo de energía emitida por la unidad de superficie del cuerpo en el intervalo de frecuencias d entre y d mediante dR es proporcional al ancho de este intervalo: dR , T r , T d (4.1.1) λ La magnitud r se llama el poder emisor del cuerpo. La radiación puede ser caracterizada por la longitud de onda en vez de la ν frecuencia . En este caso la relación (4.1.1) se reemplaza por la siguiente: dR , T r , T d (4.1.2) El intervalo de longitudes de onda dλ corresponderá al sector del espectro d . Las magnitudes dλ y d definen una d c d ; d c d c (c misma región y están vinculadas por una relación simple que se deriva de la fórmula: 8 8 es la velocidad de la luz c 3 10 m / s c 3 10 m / s ). El signo menos en esta expresión no tiene un significado sustancial e indica solamente que con el aumento de una de las magnitudes la otra disminuye. Las magnitudes dR , T y dR ,T deben coincidir y por eso: 2 r , T r , T c r , T 2 2 (4.1.3) c Con ayuda de la fórmula (4.1.3) se puede pasar de r , T a r , T y viceversa. En las investigaciones de la composición espectral del poder emisor más fácil analizar teóricamente un cuerpo negro para el cual se cumple la condición de igualdad entre la energía emitida y energía absorbida. Un cuerpo negro es un objeto ideal que absorbe toda la luz y toda la energía radiante que incide sobre él. Nada de la radiación incidente se refleja o pasa a través del cuerpo negro. A pesar de su nombre, el cuerpo negro emite luz y constituye un modelo ideal físico para el estudio del emisor de radiación 2 electromagnética. El nombre cuerpo negro fue introducido por Gustav Kirchhoff en 1862. La luz emitida por un cuerpo negro se denomina radiación de cuerpo negro. Todo cuerpo emite energía en forma de ondas electromagnéticas, siendo esta radiación, que se emite incluso en el vacío, tanto más intensa cuando más elevada es la temperatura del emisor. La energía radiante emitida por un cuerpo a temperatura ambiente es escasa y corresponde a longitudes de onda superiores a las de la luz visible (es decir, de menor frecuencia). Al elevar la temperatura no sólo aumenta la energía emitida sino que lo hace a longitudes de onda más cortas; a esto se debe el cambio de color de un cuerpo cuando se calienta. Los cuerpos no emiten con igual intensidad a todas las frecuencias o longitudes de onda, sino que siguen la ley de Planck que vamos a discutir más adelante. A igualdad de temperatura, la energía emitida depende también de la naturaleza de la superficie; así, una superficie mate o negra tiene un poder emisor mayor que una superficie brillante. Así, la energía emitida por un filamento de carbón incandescente es mayor que la de un filamento de platino a la misma temperatura. La ley de Kirchhoff establece que un cuerpo que es buen emisor de energía es también buen absorbedor de dicha energía. Así, los cuerpos de color negro son buenos absorbedores y el cuerpo negro es un cuerpo ideal, no existente en la naturaleza, que absorbe toda la energía. En la naturaleza no existen cuerpos absolutamente negros. Sin embargo, pueden crearse artificios que por sus propiedades sean tan próximos como se quiera al cuerpo negro. Ese dispositivo puede ser representado por una cavidad provista de un pequeño orificio (Fig. 4.1.2). La radiación que penetra hacia el interior a través del orificio, antes de salir del mismo, sufre una reflexión repetida. Parte de la energía es absorbida en cada reflexión, como resultado de lo cual toda la radiación de cualquier frecuencia se absorbe en esa cavidad. De acuerdo con la ley de Kirchhoff, el poder emisor de ese dispositivo es muy próximo a la función r , T de un cuerpo negro, significando T la temperatura de las paredes de la cavidad. De esta manera, si mantenemos las paredes de la cavidad a cierta temperatura T, del orificio la o saldrá una radiación bastante cercana por su composición espectral a la del cuerpo negro a esa misma temperatura T. Fig. 4.1.2 Modelo de La explicación teórica de las leyes de la radiación del cuerpo negro tuvo un significado enorme cuerpo negro en la historia do la Física ya que condujo al concepto de los cuantos de energía. Durante mucho tiempo, los intentos por obtener la forma teórica do la función r , T no daban la solución general del problema. Stefan (1879), analizando los dalos experimentales, llegó a la conclusión do que la luminosidad energética R (poder emisor integral) es proporcional a la cuarta potencia de la temperatura absoluta. Sin embargo, mediciones posteriores más exactas mostraron la inexactitud de sus conclusiones. Boltzmann (1884), partiendo do consideraciones termodinámicas obtuvo en forma teórica el siguiente valor para la luminosidad energética del cuerpo negro: R r , T d T 4 (4.1.4) 0 donde es una magnitud constante y T, la temperatura absoluta. De esta forma, la conclusión a la que llegó Stefan para cualquier cuerpo (él no experimentó con cuerpos negros), resultó correcta sólo para los cuerpos negros. La relación (4.1.4) entre la luminosidad energética del cuerpo negro y su temperatura absoluta recibió el nombre de la ley de Stefan — Boltzmann. La constante se denomina constante de Stefan- Boltzmann. Su valor experimental es igual a: 5.7 108 W / m2 K 4 (4.1.5) Ejemplo ¿En cuántas veces se incrementa la radiación de un cuerpo negro al subir la temperatura desde 27°C hasta 327°C ? Solución E1 T14 ; E2 T24 ; E2 E1 T2 T1 24 16 4 Respuesta En 16 veces Más tarde Wien (1893), utilizando las ideas de la termodinámica y de la teoría electromagnética, mostró que las curvas de poder emisor en función de la longitud de onda deben tener una forma de campana que arrancan en origen de las coordenadas pasan por un máximo y después tienden a cero para grandes longitudes de onda, así como lo muestra Fig. 4.1.3. Según la Ley de desplazamiento de Wien hay una relación inversa entre la longitud de onda en la que se produce el máximo de emisión de un cuerpo negro y su temperatura. b max ; b 0.0028976 m K T (4.1.6) donde T es la temperatura del cuerpo negro en Kelvin (K) y λmax es la longitud de onda Fig. 4.1.3 Poder emisor de un cuerpo negro del pico de emisión en metros. Las consecuencias de la ley de Wien es que el máximo en función de la longitud de onda para de la curva de poder emisor con el aumento de temperatura se desplaza hacia diferentes temperaturas longitudes de ondas electromagnéticas más cortas, es decir, cuanta mayor sea la temperatura de un cuerpo negro menor es la longitud de onda en la cual emite. Por ejemplo, la temperatura de la fotosfera solar es de 5780 K y el pico de emisión se produce a 475 nm o 4750 Å. Como el rango visible se extiende desde 4000 Å hasta 7400 Å, esta longitud de onda cae dentro del espectro visible siendo un tono de verde. Sin embargo, debido a la difusión de Rayleigh de la luz azul por la atmósfera la componente azul se separa distribuyéndose por la bóveda celeste y el Sol aparece amarillento. Ejemplo. La longitud de onda corresponde al máximo del poder emisor de un cuerpo negro se desplazó desde 1 500nm hacía 2 400nm . ¿En cuánto se incrementó la temperatura de superficie? Solución 1 0.0028976 T 1 ; 2 0.0028976 T 2 T2 T1 C 2 1 / 21 0.0028976 100 109 500 109 400 109 1449 K El siguiente paso en el estudio de la radiación de un cuerpo negro hicieron Rayleigh y Jeans los en los comienzos del siglo XX , quienes trataron de determinar la densidad do equilibrio de la radiación, partiendo del teorema de la estadística clásica sobro la equípartición de la energía por los grados de libertad. Ellos supusieron que a cada oscilación electromagnética le corresponde, en promedio una energía igual a dos mitades de kT, una mitad corresponde a la energía eléctrica y la otra, a la magnética de la onda (recordamos que según las concepciones clásicas, a cada grado de libertad oscilatorio le corresponde, en promedio, una energía igual a dos mitades de kT). La radiación de equilibrio en la cavidad no es más que un sistema de ondas estacionarias. Sin tener en cuenta las posibles formas de polarización, la cantidad de ondas estacionarias referentes a la unidad de la superficie de la cavidad con las frecuencias entre y d es igual a dn 2 2 c2 d , donde c es la velocidad de la luz. A cada de estas ondas estacionarias Rayleigh y Jeans les atribuyeron una energía kT. Multiplicando esta energía por el número de las ondas estacionarias, obtendremos la fórmula para el poder emisor de un cuerpo negro: r , T 2 2 c2 kT Fig. 4.1.4 Comparación de las curvas experimenta-les del poder emisor de un cuerpo negro en función de longitud de onda con el resultado de la teoría clásica (4.1.7) La expresión (4.1.7) se llama fórmula de Reyleigh-Jeans. La fórmula (4.1.7) puede ser presentada en una forma diferente para el poder emisor en función de longitud de onda usando las relaciones (4.1.3) r , T r , T c 2 2 c 4 kT (4.1.8) Lord Rayleigh obtuvo por primera vez el cuarto grado de la dependencia de la longitud de onda en 1900; una derivación más completa, la cual incluía una constante de proporcionalidad, fue presentada por Rayleigh y Sir James Jeans en 1905. Ésta agregaba unas medidas experimentales para diferentes longitudes de onda que concordaban satisfactoriamente con la formula (4.1.8) sólo para longitudes de onda muy largas y divergen considerablemente con esta fórmula para longitudes de onda cortas (véase Fig. 4.1.4 donde la curva experimental ha sido representada por un trazo continuo, y la curva construida según la fórmula de Rayleigh -Jeans, por una línea de puntos). Además al integrar la expresión (4.1.7) por en los límites desde 0 hasta obtendremos para la densidad de equilibrio de la energía emitida por un cuerpo negro un valor infinitamente grande. Este resultado, que fue denominado catástrofe ultravioleta, también se encuentra en contradicción con el experimento, el cual muestra que el poder emisor se tiende a cero para longitudes de ondas electromagnéticas emitidas muy cortas (ultravioletas), es decir r , T 0 para 0 . En el año 1900, Planck pudo encontrar una forma para la dependencia de poder emisor de un cuerpo negro r , T de la frecuencia y de temperatura que concordaba exactamente con los datos experimentales. Para esto, él se vio obligado a hacer una suposición completamente ajena a los conceptos clásicos, que la radiación electromagnética se emite en forma de porciones aisladas de energía (cuantos) , cuya magnitud es proporcional a la frecuencia de la radiación : (4.1.9) h El factor de proporcionalidad h se denominó posteriormente constante de Planck. Su valor experimental es igual a: (4.1.10) h 6.626 1034 J s Si la radiación se emite en porciones h , su energía n deberá ser múltiplo de esta magnitud n n h , n 0,1, 2,3, (4.1.11) En estado de equilibrio, lo distribución de las oscilaciones por valores do energía deberá cumplir con la ley do Boltzmann según la cual la probabilidad Pn de que la energía de oscilación de frecuencia tenga un valor n se determina por la expresión: Pn exp n kT Nn N exp n kT (4.1.12) n Conociendo la probabilidad de los diferentes valores de la energía de oscilación, podemos hallarse el valor medio de esta energía: n Pn n 0 h exp h kT 1 (4.1.13) Aquí nosotros hemos omitido los cálculos de sumas que después de sustitución de (4.1.10) y (4.1.11) en (4.1.11) conducen a la formula (4.1.13) (no son difíciles, pero un poco largos). Hay que anotar que cuando h 0 (el limite clásico cuando cuantos se hacen muy pequeñitos y la energía se varia en forma continua) la fórmula (4.1.13) se convierto en la expresión clásica kT . Podemos convencernos de esto haciendo exp h kT 1 h kT lo que se cumple más exactamente mientras menor sea h kT . De esta manera, si la energía pudiera tomar una serie continua de valores, su valor medio sería igual a kT . Ahora podemos corregir la fórmula de fórmula de Reyleigh-Jeans (4.1.7) reemplazando la energía promedia de las ondas estacionarias kT por la expresión (4.1.13) 2 2 h (4.1.14) 2 c exp h kT 1 La expresión (4.1.14) se denomina formula de Planck. Esta última concuerda perfectamente con los datos experimentales en todo el intervalo de frecuencias desde 0 hasta . La función (4.1.14), además cumple las leyes de Wien (4.1.6) y de Stefan Boltzmann (4.1.4). De esta manera, la fórmula de Planck da una descripción completa de la radiación de equilibrio do calor. r , T 4.2 Efecto fotoeléctrico. Se denomina efecto fotoeléctrico la emisión de electrones por una sustancia bajo lo acción de la luz. Esto fenómeno fue descubierto por Hertz en el año 1887. El observó que el paso de una chispa entre las esferas de un chispero do electrodos esféricos se facilita considerablemente al iluminar una de ellas con rayos ultravioletas. 10 años después (en 1898), Lenard y Thomson, al medir la carga específica de las partículas emitidas bajo el efecto de la luz, establecieron que las mismas eran electrones. Lenard y otros investigadores perfeccionaron el experimento colocando los electrodos en un balón al vació (Fig. 4.2.1). La luz al pasar a través de una ventanilla de cuarzo ilumina el cátodo C confeccionado con el material a investigar. Los electrones emitidos a consecuencia del fotoefecto se mueven bajo la acción del campo eléctrico hacia el ánodo A. Como resultado, en el circuito del aparato aparece corriente fotoeléctrica que se mide por el galvanómetro C. La tensión entre el ánodo y el cátodo puede variarse con ayuda del potenciómetro P. La característica corriente-tensión obtenida en este aparato (o sea, la Fig. 4.2.1 Aparato para observar dependencia de la corriente fotoeléctrica I de la tensión entre los electrodos V se muestra el efecto fotoeléctrico en la Fig. 4.2.2. Por supuesto, dicha característica se obtiene para un flujo de luz invariable. En el gráfico puede observarse que a cierta tensión no muy alta la corriente fotoeléctrica llega a la saturación, o sea, todos los electrones emitidos por el cátodo caen sobre el ánodo. Por consiguiente, la intensidad de la corriente de saturación I s , se define por la cantidad de electrones emitidos por el cátodo en la unidad de tiempo bajo la acción de la luz. La caída suave do la curva indica que los electrones se arrancan del cátodo a diferentes velocidades. Parte de los electrones que responden a la intensidad de la corriente I 0 poseen velocidades suficientes para llegar al ánodo «por sí mismos», o sea, sin la acción del campo. Para que la intensidad do la corriente alcance el valor cero hay que aplicar un Vr . A este potencial, ninguno de los electrones, incluso aquellos que al salir del cátodo tienen la mayor velocidad v max puede vencer el campo Vr y alcanzar el potencial de frenado Fig.4.2.2 Característica voltioamperica del efecto fotoeléctrico ánodo. Por esta razón puede escribirse que: mvmax 2 eVr . donde m es la masa del electrón. De esta manera, al medir la tensión de retardo Ur, so puedo determinar el valor máximo de la velocidad de los fotoelectrones. Hacia el año 1905 fue establecido que la velocidad máxima de los fotoelectrones no depende de la intensidad do la luz, sino sólo de su frecuencia, o sea el aumento de la frecuencia conlleva al incremento de la velocidad. Estas dependencias, que fueron establecidas experimentalmente, contradicen los conceptos clásicos. Por ejemplo, la velocidad de los fotoelectrones, según las ideas clásicas, debe aumentarse con la amplitud y, por consiguiente, con la intensidad de la onda electromagnética incidente. En el año 1905, A. Einstein mostró que todas las leyes del efecto fotoeléctrico se explican fácilmente, si se supone que la luz se absorbe por las mismas porciones h (cuantos) por las cuales, según Planck, la mismo se emite. Según la idea de Einstein la energía que obtiene el electrón, lo llega en forma de cuanto h que es asimilado completamente por el mismo. Parte de esta energía igual a la función de trabajo (el mínimo de la energía necesaria para la salida del electrón desde el material) se gasta para que el electrón pueda abandonar el cuerpo. Si el electrón se libera por la luz no en la superficie misma, sino a cierto profundidad, parte de la energía, igual a E , puede perderse a consecuencia de los choques casuales en la sustancia. El resto de la energía se convierte en 2 energía cinética Ecin del electrón que abandona la sustancia. La energía Ecin puede sor máxima, si E 0 . En esto caso debe cumplirse la relación: (4.2.1) h mv2max 2 que se llama la ecuación de Einstein. El efecto fotoeléctrico y la función de trabajo dependen en gran medida del estado de la superficie del metal (en particular, de los óxidos y sustancias adsorbidas en ello). Por esta razón, durante mucho tiempo no fue posible comprobar la fórmula de Ein stein con suficiente exactitud. En el año 1916, Millikan creó un aparato, en el cual las superficies investigadas eran sometidas a una purificación al vacío, y luego se medía la función de trabajo y se investigaba la energía cinética máxima de los fotoelectrones en dependencia de la frecuencia de la luz (esta energía era determinada por medio de la medición del potencial de frenado Vr . Los resultados obtenidos estaban en completa concordancia con la fórmula (4.2.1) Millikan determinó además el valor de la constante de Planck h sustituyendo en la fórmula (2.1.15) los valores medidos de 2 y mvmax 2 V (para una dada), el cual coincidió con los valores hallados de la distribución espectral de la radiación de equilibrio de calor. De la fórmula (4.2.1)se deriva que en caso de que la función de trabajo sea mayor que la energía del cuanto h los electrones no pueden salir del metal. Por consiguiente, para que se produzca el efecto fotoeléctrico es necesario que se cumpla la condición h o que: (4.2.2)) 0 h Como c para la longitud de onda se obtiene la condición respectiva: 0 c h (4.2.3) La frecuencia 0 o la longitud de onda 0 se llaman el umbral rojo del efecto fotoeléctrico. El número de electrones liberados a consecuencia del efecto fotoeléctrico debe ser proporcional al número de cuantos de luz que inciden sobre la superficie. AI mismo tiempo, el flujo luminoso se define por la cantidad de cuantos de luz que inciden sobre la superficie en la unidad de tiempo. De acuerdo con esto, la corriente do saturación I s en Fig. 4.2.2, debe ser proporcional al flujo luminoso incidente. Esta relación también se corrobora experimentalmente. Señalemos que sólo una pequeña parte de los cuantos transmite su energía a los fotoelectrones. La energía de los demás cuantos se gasta en el calentamiento del cuerpo que absorbe la luz. Ejemplo. La longitud máxima de onda para cual puede observarse el efecto fotoeléctrico en un metal es 600nm. Encuéntrese: a) la función de trabajo para este material; b) la velocidad de fotoelectrón para la longitud de onda 400nm Solución m V2 c c hc hc hc 6.626 1034 3 108 a) h e h max 3.313 1019 J 2.07eV ; 2 max 6 107 b) 4 107 m; h 4.3 c meV 2 V 2 c 2 h me 6.626 1034 3 108 2 3.313 1019 7 19 4 10 3.32 10 6 105 m / s 31 31 9.1 10 9.1 10 Naturaleza dual de la luz. Fotones Como hemos visto en el párrafo anterior, para explicar la distribución de la energía en el espectro de la radiación de calor de equilibrio es suficiente suponer que la luz se emite sólo en porciones h (hipótesis de Planck). Posteriormente, para esclarecer el efecto fotoeléctrico fue necesario admitir que la luz se absorbe en esas mismas porciones (hipótesis de Einstein). Sin embargo, Einstein no so detuvo en esto. El propuso una tercera hipótesis de que la luz siempre se propaga en forma de partículas discretas, llamadas inicialmente cuantos lumínicos. Posteriormente, en el año 1926 éstos recibieron el nombre de fotones. La demostración de existencia de fotones como las partículas que transfieren las ondas electromagnéticas fue obtenida en el experimento de Bothe. En realidad, esto suena un poco extraño cuando se dice que una onda se transfiere a través de las partículas. Hasta este momento en la historia de Física las partículas y las ondas se consideraron completamente por separado como dos diferentes formas de materia, siempre adscribiendo ondas a los campos. En el caso de ondas electromagnéticas según estos últimos descubrimientos se aclaró que tiene lugar una dualidad, a veces estas se comportan como ondas (interferencia, difracción, polarización, etc.) y a veces como partículas (radiación de cuerpo negro, efecto fotoeléctrico, etc.). Es decir, cuando onda electromagnética se interactúa con objetos (obstáculos) de tamaños macroscópicos ésta se comporta como “buena muchacha” similar a una onda con todos atributos correspondientes a las ondas, pero al interactuar con los objetos microscópicos (en nuestro caso con electrones) se comporta como “mala muchacha” parecida a un flujo de partículas llamadas fotones. Esta dualidad expresamos en forma de un diagrama: ONDA ELECTROMAGNÉTICA FLUJO DE FOTONES Las fórmulas para la energía y momento lineal (impulso) de un fotón son muy importantes para toda física cuántica y les presentamos a continuación: (4.3.1) E h ; 2 ; h 2 ; h 6.262 1034 J s; 1.054 1034 J s p h k; k 2 ; h 2 ; c 3 108 m / s (4.3.2) La primera de estas fórmulas llamada formula de Planck a veces se escribe en forma que expresa la energía de fotón a través de frecuencia y a veces en términos de frecuencia angular . En el segundo caso en lugar de constante de Planck h se utiliza constante de Planck “cruzada” . Para entender como aparece la relación (2.1.19) para el momento lineal, hay que saber dos resultados fundamentales que surgen desde la teoría de relatividad de Einstein. El primer de ellos consiste en la afirmación de que la masa de las partículas se incrementa con el crecimiento de su velocidad v , según la formula m m0 1 v2 c 2 , donde m0 es la masa en el reposo y c 3 108 m / s es la velocidad de la luz en vacío. Según esta fórmula los fotones que se mueven con la velocidad de luz ( v c ) deben tener la masa de reposo m0 m 1 v2 c 2 0 . Es decir, a los fotones no les se puede parar, ellos siempre se mueven con la velocidad de luz. Lo dicho significa que el fotón es una partícula de carácter especial, diferente de tales partículas como el electrón, el protón, etc., que pueden existir moviéndose a velocidades menores que c o incluso en reposo. La segunda afirmación de la teoría de relatividad consiste en que a cada partícula de masa m le corresponde la energía E m c2 . Según esta última formula el momento lineal del fotón debe ser igual a p m c E / c / c k Reducimos todas las características de correspondencia de propiedades de onda electromagnética y de fotón en una tabla: Característica de fotón Energía E Momento lineal p Característica de onda electromagnética Frecuencia angular ω Número de onda k Relación E h h c / p k h En este capítulo hemos estudiado una serie de fenómenos, en los cuales la luz se comporta como un flujo de partículas (fotones). No obstante, no se debe olvidar fenómenos tales como la interferencia y la difracción de la luz, los que pueden ser explicados sólo a base do las concepciones ondulatorias. De esta manera, la luz manifiesta un dualismo corpuscular-ondulatorio: en unos fenómenos se revela su naturaleza ondulatoria y se comporta como una onda electromagnética, mientras que en otros se manifiesta su naturaleza corpuscular y se comporta como un haz de fotones. Más adelante veremos que el dualismo corpuscularondulatorio está presente no sólo en las partículas luminosas, sino que también en las partículas materiales (electrones, protones, átomos, etc). Aclaremos en qué relaciones se encuentran el cuadro corpuscular y el ondulatorio. La respuesta puede obtenerse al estudiar desde ambos puntos de vista la iluminación de una superficie cualquiera. Según los conceptos ondulatorios, la iluminación en cierto punto de la superficie es proporcional al cuadrado de la amplitud de la onda lumínica. Desde el punto de vista corpuscular, la iluminación es proporcional a la densidad del flujo de fotones. Por consiguiente, entre el cuadrado de la amplitud de la onda lumínica y la densidad del haz de fotones existe una proporcionalidad directa. El fotón es el portador del impulso y de la energía. Esta última 2 se desprende en aquel punto de la superficie en el cual cae el fotón. El cuadrado de la amplitud de onda A caracteriza la probabilidad de que el fotón caiga en determinado punto do la superficie. Más exactamente, la probabilidad de que el fotón se encuentre en los límites del volumen dV que incluye en s! el punto examinado del espacio dado, se define por la expresión: dP A2dV , donde es un coeficiente de proporcionalidad y A, la amplitud do la onda lumínica. De lo dicho se infiere quo la distribución de los fotones por la superficie sobre la cual cae la luz debe tener un carácter estadístico. La uniformidad de la iluminación que se observa en la práctica está condicionada por el hecho de que frecuentemente la densidad del flujo de fotones es muy grande. Así, por ejemplo, a una iluminación producida por un bombillo 100w de potencia sobre 18 una pantalla alejada a una distancia 10m para una longitud de onda de 500nm por 1 cm 2 de superficie inciden aproximadamente 10 fotones por segundo (véase el ejemplo a continuación). La fluctuación relativa del número de fotones por unidad de área es inversamente proporcional a la raíz cuadrada del número de partículas. Por esta razón, para el valor señalado del flujo de fotones la fluctuación resulta ser insignificante y la superficie parece estar iluminada uniformemente Ejemplo. Calcúlese el número de fotones que inciden sobre S 2m de tablero en el tiempo t 1seg alejado de un bombillo de P 100w potencia a la distancia R 10m , considerando que la luz de bombillo es monocromática y corresponde a la longitud de onda 500nm Solución: La energía total emitida por el bombillo es igual a E P t . Esta energía se emite en forma isotropíca por partes iguales en todas direcciones. Cuando onda electromagnética llega hasta tablero la energía se distribuye en una forma homogénea sobre una esfera del área 4 R 2 , con la densidad por unidad de área P t / 4 R2 . La energía que cae sobre tablero es producto de esta densidad por el área del tablero, es decir Etab P t S / 4 R2 Por otro lado, la onda electromagnética es un flujo de N fotones y la energía total de los fotones bombardean el tablero es Etab N h N h c / . Debe cumplirse la igualdad 2 P t S / 4 R2 N h c / N P t S / 4 R2 h c 100 1 2 5 107 / 4 3.14 102 6.626 1034 3 108 4 1017 Respuesta 4 10 fotones inciden el tablero 17