MF04818 Nombre del curso: Matemáticas y Físicas integradas IV
Anuncio

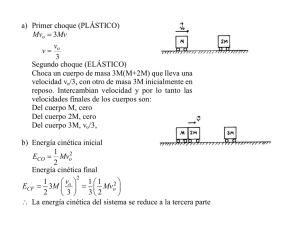
Universidad Tec Milenio: Profesional Clave: MF04818 Nombre del curso: Matemáticas y Físicas integradas IV El calor y los cambios de temperatura Calor: forma de energía que se manifiesta mediante un cambio de estado físico y/o mediante un cambio en la temperatura de una sustancia. MF04818 Matemáticas y Física integradas IV Capacidad calorífica: es la relación que hay entre la cantidad de calor (Q) recibida por el cuerpo y el cambio que experimenta en la temperatura (∆t). Actividad 8. El calor y los cambios de temperatura Calor específico: la cantidad de calor que se necesita agregar a una masa de 1 gramo de una sustancia para elevar su temperatura en 1 °C. 1 2 El calor y los cambios de temperatura El calor y los cambios de temperatura El calor necesario Q para elevar la temperatura de una masa “m” de una sustancia en ∆T °C está dada por: Ejemplo 1: Cuánto calor es necesario agregar a una barra de plomo de 500 gramos para elevar su temperatura desde 20 °C hasta 150 °C. El calor especifico del plomo es 0.031 cal/g°C Q = mCe∆T Datos: Ce = 0.031 cal/g °C m = 500 g T1 = 20 °C T2 = 150 °C donde: Ce es el calor específico de la sustancia. Q = mCe∆T Q = 500 gr(0.031 cal )(150 − 20)°C g °C Q = 2015 cal = 2.015 Kcal. 3 El calor y los cambios de temperatura El calor y los cambios de temperatura Ejemplo 3: Una esfera sólida de acero de 500 gr lleva una velocidad de 10 m/s cuando golpea a otra esfera sólida de acero de 200 g que se encuentra en reposo. Ambas esferas tienen una temperatura de 20 °C antes del choque. Si después del choque la segunda esfera adquiere una velocidad de 12 m/s calcular: a) El calor ganado por las esferas b) La temperatura que tienen las esferas, después del choque Ejemplo 2: Una pieza de 500 gramos de cobre que se encuentra a 200 °C pierde 300 cal. ¿Cuál es la temperatura final de la pieza? El calor especifico del cobre es 0.093 cal/gr°C Datos: Ce = 0.031 cal/g °C Q = - 300 cal m = 500 g T1 = 200 °C T2 = ? Q = mCe ∆T Q - 300cal = mCe (50 gr )(0.093 cal ) gr °C ∆T = −64.5°C ∆T = ∆T = T 2 − T 1 ; T 2 = 135.5°C 4 v10 = 10 m/s v 20 = 0 m/s m1 = 500 g m1 = 200 g v1 f = ? v 2 = 12 m/s f T 2 = ∆T + T 1 5 D.R. © Universidad TecMilenio Lázaro Cárdenas #2610 Col. Del Paseo Residencial Monterrey, N.L., 2006. Antes del choque Después del choque 6 1 Universidad Tec Milenio: Profesional Clave: MF04818 Nombre del curso: Matemáticas y Físicas integradas IV El calor y los cambios de temperatura El calor y los cambios de temperatura Energía cinética antes del choque 1 1 EK 0 = m1 (v10 ) 2 + m 2 (v 20 ) 2 2 2 1 EK 0 = (0.5 Kg )(10m / s ) 2 + 0 = 25 J 2 Energía cinética después del choque 1 1 EK f = m1 (v1 f ) 2 + m 2 (v 2 f ) 2 2 2 1 1 EK f = (0.5Kg )(5.2m / s ) 2 + (0.2 Kg )(12m / s) 2 = 21.16 J 2 2 La energía cinética perdida se transforma en calor Solución: Primero calcular la velocidad de la primera esfera después del choque utilizando la ley de la conservación de la cantidad de movimiento. Cant. de Mov. antes del choque = Cant. de Mov después del choque m1v10 + m2v20 = m1v1f + m2v2f 500(10) + 200(0) = 500v1f + 200(12) v1f = 5000 − 2400 m = 5.2 500 s Q = mCe∆T = −( EKf − EK 0) = −(21.6 − 25) J Cálculo de la energía cinética antes y después del choque: 7 El calor y los cambios de temperatura Q = mCe ∆T = 3.4 J (0.24cal / J ) = 0.816 cal 8 Bibliografía Giancoli, Douglas C. Física para universitarios, Volumen I. México: Pearson Educación, 2000 (ISBN: 9684444842). Q=0.816 cal. es el calor ganado por las dos esferas de acero después del choque. Para el cálculo de el incremento en la temperatura se utiliza la masa de las dos esferas, ya que el calor se transmite a ambas y como son del mismo material y se encuentran a la misma temperatura tenemos que: Q = m1Ce∆T + m 2Ce∆T = ( m1 + m 2)Ce∆T = 0.816cal ∆T = Q 0.816cal = = 0.0103°C (m1 + m 2)Ce (700 g )(0.113cal / g °C ) Tf = T 0 + 0.0103°C = 20°C + 0.0103°C Tf = 20.0103°C 9 10 Créditos Diseño de contenido: Ing. Olegario Pérez González Edición de contenido: Lic. Carolina Ramírez García Diseño Gráfico: Lic. Alejandro Calderas González, MATI 11 D.R. © Universidad TecMilenio Lázaro Cárdenas #2610 Col. Del Paseo Residencial Monterrey, N.L., 2006. 2