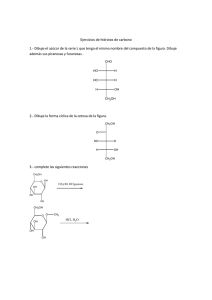
D-glucosa
Anuncio

TEMA 7 HIDRATOS DE CARBONO GLÚCIDOS- MONOSACÁRIDOS GLÚCIDOS Llamados también carbohidratos, azúcares o sacáridos Se definen como polihidroxialdehídos o polihidroxicetonas o compuestos que por hidrólisis dan dichos compuestos. Los azúcares aldehídicos se denominan aldosas Los que tienen una función cetona se denominan cetosas Ejm: 1 CH2OH H-C=O O H 2 HO 3 H H 4 OH H H 5 OH H 6 OH CH2OH D-GLUCOSA pentahidroxihexanal OH H OH OH CH2OH D-FRUCTOSA pentahidroxihexanona 1 Triosas tetrosas pentosas Hexosas Aldosas No Hidrolizables Monosacáridos D- Glucosa D- Manosa D- Galactosa ó Hexosas Cetosas Disacáridos Oligosacáridos (2-10 osas) Hidrolizables Tri,tetra.etc. Holósidos Polisacáridos (más de 10 osas) Por hidrólisis dan osas y compuestos no glucídicos Heterósidos Oligosacáridos D- Fructosa Reductores Maltosa Lactosa Celobiosa No Reductores Sacarosa Disacáridos Tri,tetra,etc Homopolisacáridos Polisacáridos Almidón Glucógeno Celulosa Quitina Mucopolisacáridos Heteropolisacáridos Gomas vegetales Pectinas 2 Configuración D y L del gliceraldehído ESTEROISÓMEROS • Esteroisómeros: compuestos cuyos átomos están enlazados en el mismo orden pero difieren en su posición en el espacio. Pueden ser: – Enantiómeros : pares de compuestos que son imágenes especulares no superponibles. – Diasterómeros : esteroisómeros que no tienen imágenes especulares. 3 Enantiómeros Par de enantiómeros de una hexosa espejo DIASTEROISÓMEROS 1y 3- diasteroisómeros espejo 1 y 2- enantiómeros 2 y 3- epímeros en C 3 4 FORMULA HEMIACETALICA (CICLICA) H FORMULA de HAWORTH (CICLICA) C-OH 6 CH2OH H FORMULA LINEAL 1 O HO H H 2 HO 3 H H 4 OH OH OH OH H H 4 H O 5 H 1 OH OH 2 3 H CHO H OH OH α-D-glucopiranosa H CH2OH α−-D-glucopiranosa OH 6 HO CH2OH D-GLUCOSA H C-H 6 CH2OH H OH 4 O HO OH H H OH OH 1 OH 3 H H O 5 H 2 OH β−D-glucopiranosa H CH2OH β−D-glucopiranosa CH2OH OH H H O HOH2C OH H HO H OH H OH H CH2OH D-FRUCTOSA OH 6 CH2OH O 5 H H 2 4 OH 1 O CH2OH OH 3 2 OH H α-D-fructofuranosa CH2OH α-D-fructofuranosa NOTA: Escribir las formulas hemiacetalica y de Hawort para β-D-fructofuranosa 5 Glucosa: Forma cíclica o piranósica • Anómeros alfa y beta ESPECIFICACIONES DEL NOMBRE SISTEMÁTICOS DE LOS AZÚCARES • EJEMPLOS: α- D(+)-glucopiranosa β- D(+)-glucopiranosa • α y β: posición del OH del C anomérico en la forma hemiacetálica – α: hacia abajo ( axial) se llama anómero alfa – β: hacia arriba (ecuatorial) se llama anómero beta. • D y L: es la configuración de la serie o familia a la que pertenecen los azúcares. D: tienen el grupo OH del último C quiral a la derecha. L: tienen el grupo OH del último C quiral a la izquierda. • + o - : se refiere al sentido de rotación de la luz polarizada. +: en el sentido de las agujas del reloj -: en el sentido contrario al de las agujas del reloj. 6 Esquema del polarímetro ¿PORQUE LA GLUCOSA Y LAS OTRAS ALDOSAS QUE EN SU FORMA HEMIACETÁLICA Ó CÍCLICA, NO TIENEN EL GRUPO CARBONILO LIBRE, DAN (+) ESTAS REACCIONES? Porque en solución acuosa la forma α-D- glucopiranosa (çíclica) se interconvierte en la β -D-glucopiranosa (cíclica), pasando por la forma abierta (0.02%) que es la que reacciona con los reactivos de Fehling ó Tollens. Como las tres formas están en equilibrio, a medida que la forma abierta reacciona y se consume, se forman nuevas cantidades de forma abierta para restablecer el equilibrio y así continua hasta que se oxida toda la glucosa. CH2OH H HO H OH H O H OH OH α-D-glucopiranosa 36% CH2OH H HO H OH H CH2OH OH H C=O H OH Forma abierta 0,02% H HO H OH O OH H H H OH β - D-glucopiranosa 64% 7 Mutarrotación – Definición: es la variación espontánea del valor del ángulo de rotación de la luz polarizada por una sustancia opticamente activa que se encuentra en solución – Ejemplo: – anómero α de glucosa puro = +122º – anómero β de glucosa puro = +18,7º Mezcla en equilibrio de α y β = +52,6º PROPIEDADES QUÍMICAS ● Oxidación suave ● Oxidación fuerte ● Oxidación enzimática 1-Oxidación ● Oxidantes suaves. Oxidan únicamente el C-1. Son: I) Reactivo de Tollens II) Reactivo de Fehling III) Bromo Ecuación General: COOH CHO H HO H H H OH H OH OH CH2OH D-glucosa Oxidantes suaves HO H H OH H OH OH CH2OH Ácido D-glucónico 8 Propiedad reductora de la glucosa Reacción química que se realiza en el laboratorio para identificar azúcares reductores 9 ● Oxidación fuerte. Oxidan el C-1 y el último. Con HNO3 Ecuación General: H HO H H CHO OH H OH OH CH2OH H HO H H HNO3 COOH OH H OH OH COOH D-glucosa Ácido D-glucárico ● Oxidación enzimática. Se realiza con enzimas específicas y selectivas, ya que solo oxidan al C-6 formando los ácidos urónicos. Ejemplo: de galactosa se obtiene ácido galacturónico , de glucosa: ácido glucurónico Ecuación: CHO H HO CHO OH H H Enzimas HO OH H H OH H OH H OH H OH CH2OH D- glucosa COOH Ácido glucurónico 10 2- Reducción Ecuación: CHO H OH HO H + H H OH OH CH 2 O H D- glucosa CH 2 O H H2 H HO H Pt ó P d catalizador OH H OH H OH CH 2 O H G lucitol ó sorbitol Es un producto natural aislado de bayas y frutos y se em plea com o edulcorante 3-Formación de osazonas Los azúcares adicionan fenilhidracina para formar osazonas. Las osazonas son sólidos cristalinos característicos de cada carbohidrato ya que éstos se pueden reconocer por: I) forma de sus cristales, II) tiempo de formación, III) punto de fusión, IV) rotación específica. Ecuación: H CHO H HO H H HO H OH CH2OH D- glucosa N-NH-Ph N-NH-Ph OH OH C + 3 NH2 - NH-Ph Fenilhidracina H H H OH + H2N -Ph + NH3 + H2O Anilina OH CH2OH osazona 11 4-Isomerización Consiste en la interconversión entre glucosa, manosa y fructosa, en medio alcalino suave. Esta reacción explica porqué la fructosa siendo una cetosa da (+) las reacciones de Fehling y Tollens, que ocurren en medio alcalino suave.( Se convierte en aldosa) C HO HO HO C HO H HO OH H H H OH OH C H 2O H D - glu cosa OH- H H H OH H OH C H 2O H D - m a nosa OH- C H 2O H HO H H O H OH OH C H 2O H D - fru cto sa 12