La progesterona que le ayuda a mantener el apego al tratamiento
Anuncio

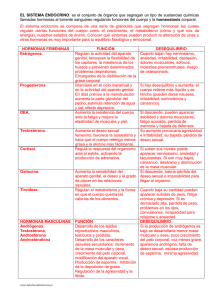
La progesterona que le ayuda a mantener el apego al tratamiento Monografía de Producto Progesterona Natural (Bioidéntica) Microesferas Cristalinas Bioerosionables Suspensión Acuosa Inyectable I.M. Soporte de la Fase Lútea en Reproducción Asistida Amenaza de aborto Amenorrea Secundaria Primer Inyectable de Progesterona de Liberación Prolongada. Único en Monodosis Semanal (cada 7 días) por Vía I.M. 2 Contenido 1 Vista Panorámica Prosphere Pág. 4 2 Introducción 5 3 Información del producto 3.1 Propiedades químicas 3.2 Producto 3.3 Indicaciones 3.4 Posología 7 7 8 8 8 4 Farmacodinamia 4.1 Progestágenos 4.2 Progesterona 9 9 9 5 Farmacocinética 5.1 Absorción 5.2 Distribución 5.3 Metabolismo 5.4 Eliminación 10 10 10 10 10 6 Experiencia Preclínica 6.1 Farmacocinética y Biodisponibilidad 6.2 Tolerabilidad local 12 12 12 7 Experiencia Clínica-EFICACIA 7.1 Suplementación de la Fase Lútea 13 13 8 Experiencia Clínica-SEGURIDAD Y TOLERABILIDAD 8.1 Efectos secundarios 8.2 Tolerabilidad 8.3 Contraindicaciones 8.4 Interacciones medicamentosas 15 15 15 15 15 9 Prosphere® en la Práctica 9.1 Presentación 9.2 Método de aplicación 16 16 16 10 Información para prescribir reducida (IPP-R) 17 11 Referencias Bibliográficas 20 ® 3 1. Vista Panorámica El uso de ProSphere® 200 mg en clínica, ha mostrado efectividad en las técnicas de Reproducción Asistida. (21) Prosphere® 200 mg es el primer inyectable de Progesterona Natural (Bioidéntica) en Microesferas Cristalinas Bioerosionables de Liberación Prolongada, único en Monodosis Semanal (cada 7 días) por vía I.M. que mantiene niveles de Progesterona superiores a 10 ng/mL por siete días. La presentación en jeringa prellenada, permite una administración fácil, rápida y segura. (10,11,12, 21) ProSphere® 200 mg tiene una mejor tolerabilidad local respecto a la solución oleosa de Progesterona. Además presenta una seguridad y tolerabilidad sistémica con un amplio perfil de aceptación y comodidad para las pacientes. (21) Prosphere® 200 mg es una Suspensión Acuosa Inyectable Monodosis de Liberación Prolongada. Está formulada con Microesferas Cristalinas Bioerosionables de Progesterona, libre de polímeros, lo que es posible gracias a una tecnología farmacéutica que ha sido considerada como la máxima innovación en los últimos años desarrollada en México y patentada mundialmente con aplicación como Soporte Lúteo en Procedimientos de Reproducción Asistida y en los casos en los que la Progesterona esté indicada. Prosphere® 200 mg se disuelve lentamente en el músculo, liberando el 100% de Progesterona después de 10-12 días y mantiene niveles promedio de Progesterona mayores a 10 ng/ml semejantes a los de la Fase Lútea. (11) La administración de Prosphere® 200 mg una vez por semana (cada 7 días), evita las molestias locales provocadas por la aplicación diaria de soluciones oleosas inyectables y permite un mejor cumplimiento de la posología indicada para cada tratamiento. (21) La eficacia de Prosphere® 200 mg permite un tratamiento cómodo y seguro durante el procedimiento de Reproducción Asistida y a lo largo del primer trimestre del embarazo y en caso de amenaza de aborto. (21) 4 Primera Progesterona Natural (Bioidéntica) I.M. en Microesferas Cristalinas Bioerosionables de Liberación Prolongada para la Terapia Ginecológica y de la Fertilidad Femenina Patentada mundialmente 5 2. Introducción Prosphere® 200 mg es una alternativa más segura, confiable y eficaz que las otras presentaciones para los casos en que se requiera una terapia hormonal a base de Progesterona por tiempo corto o prolongado. La Progesterona continúa utilizándose en diferentes esquemas terapéuticos, tales como Soporte de la Fase Lútea en Reproducción Asistida, Pérdida Gestacional Recurrente, Amenaza de Aborto y Trastornos Menstruales (Amenorrea Secundaria). (18, 22, 25, 28, 30) Las Microesferas tienen la forma geométrica perfecta: la esfera, las cuales logran por medio de un proceso minucioso obtener el polimorfo alfa de la Progesterona que proporciona características únicas y ventajosas a Prosphere® 200 mg para la terapia con Progesterona Natural (Bioidéntica), con una aplicación I.M. Las Microesferas se disuelven lentamente liberándose en un 100% después de 10-12 días y mantienen niveles promedio de Progesterona semejantes o por encima a los de la Fase Lútea (más de 10 ng/ml) por 7 días. (10, 11) Existen diferentes dosis y presentaciones de Progesterona tales como la inyección intramuscular oleosa, la oral y la transvaginal (gel, perlas, óvulos); no obstante, estas presentaciones se asocian a la dificultad de apego al tratamiento indicado debido a su frecuencia de uso, a la incomodidad en la vía de administración o a mayores problemas de tolerabilidad o dolor local, eritema, rubor y formación de abcesos en el sitio de aplicación. (21, 30). Prosphere® 200 mg supera muchas de estas desventajas: cada jeringa prellenada contiene 200 mg de Microesferas Cristalinas Bioerosionables de Progesterona Natural (Bioidéntica) en una Suspensión Acuosa para administración Intramuscular que garantiza una Liberación Prolongada asegurando niveles plasmáticos constantes de Progesterona por más de 10 ng/ml por un tiempo de 7 días. (10) El control en la liberación por medio de las Microesferas Cristalinas Bioerosionables sin polímeros asegura una cinética de liberación clara y reproducible, libre del efecto de primer paso hepático y de todos aquellos efectos asociados a la vía oral. (10, 11) Esta dosis de Progesterona se puede utilizar fundamentalmente en el Soporte de la Fase Lútea en Reproducción Asistida o bien en casos de pérdidas gestacionales recurrentes asociadas a deficiencias de cuerpo lúteo, por supuesto tiene aplicaciones clínicas en otros tipos de terapia en los que la Progesterona esté indicada. (21) Se ha observado que los productos a base de Progesterona en solución oleosa presentan una serie de incomodidades y dificultades en el apego al tratamiento por su dosis diaria, principalmente por dolor en el sitio de inyección y posibles efectos secundarios. Las perlas orales presentan una absorción limitada, incomodidades gastrointestinales y un primer paso hepático que reduce sus niveles de biodisponibilidad. Otras presentaciones farmacéuticas en gel o perlas vaginales presentan incomodidad para las pacientes, bajo perfil de absorción y biodisponibilidad, así como efectos adversos locales. (21, 28, 30) Por las características ventajosas de Prosphere® 200 mg relacionadas con su Liberación Prolongada, gracias a la tecnología de Microesferas en Suspensión Acuosa, permite asegurar la concentración requerida, se logra un mayor apego al tratamiento por la frecuencia de su administración y mejor tolerabilidad en el sitio de aplicación. (11, 21) 6 3. Información del Producto Prosphere® 200 mg 3.1 Propiedades Químicas Es el Primer Inyectable de Progesterona Natural (Bioidéntica) I.M. en Microesferas Cristalinas Bioerosionables de Liberación Prolongada que mantiene niveles semejantes a los de la Fase Lútea con una administración semanal (cada 7 días). (10, 11, 21) La Progesterona (Δ4-pregnen-3,20-diona), es la sustancia activa de Prosphere® 200 mg . La síntesis inicia a partir de material vegetal el cual es modificado hasta obtener una molécula que es bioidéntica a la Progesterona endógena. Esta Progesterona Natural (Bioidéntica) es transformada de acuerdo a una tecnología propia patentada a nivel mundial para formar Microesferas de Liberación Prolongada sin la adición de polímeros. Figura No.1: Estructura Química de la Progesterona 7 Figura No. 2: Fotografía Microscópica de Prosphere® Microesferas Cristalinas Bioerosionables de Progesterona. 3.2 Producto 3.4 Posología Prosphere® 200 mg se presenta en jeringa prellenada con 2 mL de una Suspensión Acuosa de Microesferas Cristalinas Bioerosionables de Progesterona. Suplementación de Fase Lútea en Procedimientos de Reproducción Asistida: Aplicar una inyección monodosis semanal (cada 7 días) a partir del día del procedimiento hasta la semana 12 en caso de vitalidad embrionaria. Suspender su aplicación cuando la prueba de embarazo sea negativa. (21) 3.3 Indicaciones Suplementación de Fase Lútea en Procedimientos de Reproducción Asistida. (18, 21, 22, 30) Prosphere® 200 mg Amenaza de Aborto o Prevención de Aborto de Repetición por Insuficiencia Lútea: Aplicar una inyección monodosis semanal (cada 7 días). (21) Amenaza de Aborto o Prevención de Aborto Recurrente por Insuficiencia Lútea. (21, 30) Parto Prematuro Aplicar una inyección monodosis semanal (cada 7 días). (21) Parto Prematuro. (21, 30) Amenorrea Secundaria. (21, 30) Amenorrea Secundaria Aplicar una sola inyección. (21) Otras indicaciones (30) Otras Indicaciones (30) Hemorragia Uterina Disfuncional Endometriosis Síndrome Premenstrual Hirsutismo Hiperplasia Endometrial Hemorragia Uterina Disfuncional Endometriosis Síndrome Premenstrual Hirsutismo Hiperplasia Endometrial La dosis se establecerá según el efecto deseado y el caso individual a criterio del Médico. 8 4. Farmacodinamia 4.1 Progestágenos Los progestágenos de manera característica son lipofílicos y se difunden con libertad hacia las células, donde se unen al receptor de la Progesterona. Al igual que otros miembros de la superfamilia de receptores de esteroides/tiroides, el receptor de la Progesterona es un factor de transcripción nuclear activado por ligando el cual interactúa con un elemento de reacción a Progesterona en genes blanco para regular su expresión. trual normal. Los niveles de estradiol que alcanzan su concentración máxima inmediatamente antes de la ovulación, disminuyen con los aumentos de los niveles de hormona luteinizante (LH), hormona folículo estimulante (FSH) y el incremento de los niveles de Progesterona. El aumento del espesor del endometrio se asocia con el incremento de los niveles de estrógenos en la primera mitad del ciclo. La transformación del endometrio estimulado con estrógenos en un endotelio secretor, se asocia con el aumento de los niveles de Progesterona en la segunda mitad del ciclo. Ante la ausencia de embarazo, la menstruación tiene lugar una vez finalizada la producción de Progesterona. El receptor de la Progesterona se expresa en vías reproductoras femeninas, glándulas mamarias, Sistema Nervioso Central (incluso en la región del generador de impulsos en el hipotálamo) e hipófisis, pero por lo general tiene una distribución en los tejidos más limitada que los receptores de estrógenos u otras hormonas esteroides. Se puede corregir el desequilibrio hormonal que puede producir hemorragias uterinas disfuncionales mediante la administración de Progesterona exógena. El cuerpo lúteo representa la fuente principal de este progestágeno natural, la placenta sigue secretando Progesterona a fin de mantener el embarazo. La Progesterona estimula el desarrollo de los componentes glandulares de las mamas, aumenta el espesor del moco cervical e incrementa la temperatura corporal. Asimismo, es antagonista de los efectos de retención de sodio de los mineralocorticoides, lo que conduce a un aumento de la secreción de aldosterona. En muchas células, los estrógenos inducen la expresión de los receptores de Progesterona, cuya presencia es un marcador frecuente de efectos de estrógenos en situaciones tanto de investigación como clínicas. En muchos sistemas biológicos, los progestágenos aumentan la diferenciación y se oponen a las acciones de los estrógenos para estimular la proliferación de células. Este efecto de los progestágenos puede incluir decrementos de las concentraciones de receptores de estrógenos, aumento del metabolismo local de estrógenos hacia metabolitos menos activos o la inducción de productos de genes que disminuyen las respuestas celulares a compuestos estrogénicos. (16) Afinidad a Receptores La afinidad de unión relativa es aquella que cada molécula de Progesterona o progestina tienen por determinado Receptor Esteroidal Humano y por lo tanto se manifiesta por una respuesta dependiendo del grado de afinidad. 4.2 Progesterona La Progesterona tiene mayor afinidad por los receptores progestacionales y por lo tanto se convierte en un protector o estimulador del endometrio. Tiene poca afinidad de unión relativa androgénica, y mayor afinidad mineralocorticoide y glucocorticoide. (4) La Progesterona influye determinantemente en la conservación del embarazo, suprime la menstruación y la contractilidad uterina, motivo por el cual y de manera histórica se utiliza para evitar la amenaza de aborto. La Progesterona endógena se produce por el cuerpo lúteo durante la segunda mitad del ciclo mens- 9 5. Farmacocinética 5.3 Metabolismo El objetivo de la terapia con Progesterona para el Soporte de la Fase Lútea es mantener las concentraciones plasmáticas semejantes a las de la Fase Lútea (5-20 ng/mL). Las características farmacocinéticas de las Microesferas Cristalinas Bioerosionables de Prosphere® 200 mg permiten alcanzar estas concentraciones plasmáticas durante no menos de 7 días, lo cual conduce a poder administrar el producto semanalmente, y que se traduce en una posología más cómoda y segura para la paciente, a diferencia de las otras formas farmacéuticas que requieren administraciones diarias. (10, 11, 12) La biotransformación de la Progesterona se realiza principalmente en el hígado a metabolitos hidroxilados y sus conjugados, sulfato y glucurónido, que se eliminan en la orina. Un metabolito urinario importante específico para el metabolismo de la Progesterona es el pregnen-3α,20α-diol; su medición en orina y plasma se utiliza como un índice de la secreción de la Progesterona endógena. A diferencia de la Progesterona oral. (16) Prosphere® 200 mg evita el metabolismo de primer paso prehepático y hepático, lo que resulta en una mayor biodisponibilidad. (11) 5.1 Absorción 5.4 Eliminación Después de la administración intramuscular de Prosphere® 200 mg en una Suspensión Acuosa de Microesferas Cristalinas Bioerosionables, la concentración plasmática máxima se obtuvo a las 24 horas. La vida media aparente de eliminación después de una dosis semanal (cada 7 días) de Prosphere® 200 mg fue de 8.1 ± 3.9 días y después de la cuarta administración fue de 5.80 ± 2.14 días. La vida media de eliminación promedio es de 7 días. (10, 11). Se realizaron dos estudios de farmacocinética en mujeres posmenopáusicas, uno con una sola administración y otro con cuatro administraciones semanales de Prosphere® 200 mg . Los parámetros farmacocinéticos promedio obtenidos se muestran en la Tabla 1. (10, 11) Esta vida media larga es sólo posible con la Liberación Prolongada de las Microesferas Cristalinas Bioerosionables en Suspensión Acuosa de Prosphere® 200 mg . (Ver Tabla No.1 y Figura No.4) La concentración promedio de Progesterona, después de la cuarta administración en el intervalo de dosificación (7 días) fue de 26.11 ng/mL. Esta concentración es superior a la concentración promedio de Progesterona en la Fase Lútea. (10, 11) 5.2 Distribución Aproximadamente entre 96 y 99% de la Progesterona circulante está unida a proteínas plasmáticas, principalmente a la albúmina (50 a 54%) y globulina de unión a corticosteroides (CBG o transcortina) (43 a 48%). La Progesterona no muestra unión significativa a la globulina de unión a esteroides sexuales (SHBG). (16) 10 Tabla No.1 Parámetros Farmacocinéticos en Mujeres Postmenopáusicas con la administración de Prosphere® 200 mg Unidosis y Multidosis de Progesterona Natural administrado semanalmente (cada 7 días). (10, 11) 45 200 mg 40 35 30 25 20 15 10 5 0 0 2 4 6 8 10 12 7 16 18 20 22 24 26 28 14 21 Tiempo Aplicación Semanal (cada 7 días) Figura No. 4: Perfil Plasmático en Mujeres Postmenopáusicas con la administración de Prosphere® 200 mg aplicado semanalmente (cada 7 días), durante 4 semanas. (11) 11 6. Experiencia Preclínica Estudios de Farmacocinética y Tolerabilidad Local 6.1 Farmacocinética y Biodisponibilidad 6.2 Tolerabilidad Local Los resultados de Farmacocinética comparativa evaluada en conejos, mostraron diferencias entre la absorción de la Suspensión Acuosa de Microesferas de Progesterona 100 mg cuando se comparó con la solución oleosa de Progesterona 100 mg, las concentraciones plasmáticas máximas fueron 24.6 ng/mL y 260.7 ng/mL respectivamente. El tiempo para alcanzar la concentración plasmática máxima fue de 30 minutos aproximadamente para ambos productos. Se observaron diferencias significativas en la vida media de eliminación (t1/2), la cual en caso de las Microesferas de Progesterona fue de 6 días, el doble que la obtenida con la solución oleosa. El mantenimiento de niveles superiores a los basales fue más prolongado en las Microesferas que en la Solución Oleosa. La Biodisponibilidad fue semejante entre ambos productos. En un Estudio Histopatológico Comparativo de Tolerabilidad Local realizado en conejos machos Nueva Zelanda, con una sola inyección de Prosphere® 200 mg en Suspensión Acuosa de Microesferas Cristalinas Bioerosionables de Liberación Prolongada y una inyección de solución oleosa de Progesterona en concentraciones equivalentes, se encontró que el daño tisular evaluado con indicadores histopatológicos de respuesta y reparación, fue semejante entre ambas formulaciones. Considerando que la solución oleosa se administra diariamente y que Prosphere® 200 mg se administra semanalmente (cada 7 días). El daño tisular es visiblemente menor y en consecuencia la tolerabilidad es manifiestamente mayor. (13) El Perfil Plasmático Comparativo de la Suspensión Acuosa de Microesferas Cristalinas Bioerosionables de Progesterona 100 mg y la solución oleosa de Progesterona 100 mg se muestra en la Figura No. 5. (12, 13) 140.0 Cmáx 260.7 ng/mL 200 mg 120.0 100.0 Solución oleosa de Progesterona (100 mg) 80.0 Suspensión Acuosa de Microesferas Cristalinas de Progesterona (100 mg) 60.0 40.0 20.0 0.0 0 5 10 15 20 25 30 Tiempo (Días) Figura No. 5. Perfil Plasmático Comparativo después de la Administración Intramuscular de una Suspensión Acuosa de Microesferas Cristalinas Bioerosionables de Progesterona 100 mg y una solución oleosa de Progesterona 100 mg en conejos machos Nueva Zelanda. (12) 12 7. Experiencia Clínica EFICACIA 7.1 Suplementación de la Fase Lútea La fertilización de por lo menos un óvulo ocurre en la mayoría de los ciclos con Tecnología de Reproducción Asistida, sin embargo, sólo el 2841% de los ciclos con transferencia de embrión resultan en embarazo. La implantación es un proceso crítico en los Tratamientos de Reproducción Asistida, en que la Progesterona juega un papel fundamental. Esta hormona también es crucial en el mantenimiento del embarazo durante el primer trimestre. (2, 5, 27) La suplementación intramuscular comprende una inyección diaria de Progesterona en solución oleosa, lo que obviamente es incómodo e inconveniente para las pacientes. Las reacciones secundarias locales son frecuentes y pueden ser muy intensas. (25) Se estudiaron en forma prospectiva de julio a octubre del 2006, 30 casos con Terapia Reproductiva de Baja y/o Alta Complejidad, en quienes posterior a la estimulación ovárica y procedimiento reproductivo (coito programado, inseminación intrauterina y/o fertilización in vitro) se les suplementó con una dosis semanal intramuscular de Prosphere® 200 mg en Suspensión Acuosa de Progesterona Natural (Bioidéntica) en Microesferas Bioerosionables de Liberación Prolongada. La suplementación se dió hasta la semana 12 de gestación con vitalidad fetal o hasta la prueba negativa de embarazo. (21) A menudo, los tratamientos de reproducción asistida incluyen la estimulación ovárica con agonistas de la hormona liberadora de gonadotropinas (GnRH); estos medicamentos, junto con la aspiración de las células de la granulosa que rodean al óvulo, son capaces de provocar un defecto de la fase lútea con niveles disminuidos de Progesterona, lo que disminuye la probabilidad de embarazo. (7, 19, 25) Del total de pacientes estudiadas, la proporción general de embarazos logrados fue del 26.6% con un 87.5% de vitalidad hasta la semana 12. De las pacientes que no conservaron la vitalidad fetal, no se debió a deficiencia de Progesterona sino a otras causas. En los ciclos de Reproducción Asistida, se recomienda realizar una suplementación hormonal de la Fase Lútea para aumentar las probabilidades de éxito. La Progesterona y la gonadotropina coriónica humana (hCG) han mostrado tener un impacto positivo en términos de fertilidad, sin que exista diferencia significativa entre ambos. (1, 3, 7, 9, 24, 26). Sin embargo, con la hCG existe un riesgo aumentado de Síndrome de Hiperestimulación Ovárica, lo que hace de la Progesterona la primera elección para la suplementación de la Fase Lútea. (7, 24, 25, 26). El 96.6% de pacientes manifestaron aceptación y comodidad con este esquema de suplementación de dosis semanal y continuaron su uso hasta el término del estudio. No hubo complicaciones sistémicas asociadas al medicamento y sólo un caso presentó una reacción local leve y temporal tras su aplicación. (21) Existen formulaciones de Progesterona para administración por vía oral, vaginal (gel, perlas, óvulos) e intramuscular. La administración oral se asocia con una disminución de la eficacia, que probablemente sea resultado del metabolismo de primer paso prehepático y hepático el cual es inevitable por esta vía. Tanto la vía vaginal como la intramuscular han mostrado ser eficaces; sin embargo, varios autores sugieren que la administración por vía intramuscular parece ser la Suplementación de Fase Lútea de elección. (1, 2, 3, 7, 8, 24, 26) En conclusión, la Progesterona Natural Bioidéntica Prosphere® ha demostrado una administración más cómoda (monodosis intramuscular semanal) y un soporte de fase lútea efectivo, sin los efectos gastrointestinales o vaginales secundarios que producen anteriores progesteronas en forma oleosa o perlas. (21) 13 Porcentaje de Vitalidad Fetal Porcentaje de Embarazos Logrados 27% 87.5% Porcentaje de Vitalidad Fetal lograda con Prosphere® de 87.5%(n=30) Embarazo General de 27% (n=30) Figura No. 6. Porcentaje de Embarazos logrados con la administración de Prosphere® 200 mg semanalmente (cada 7 días). (21) Porcentaje de Comodidad 96.6% Figura No. 7. Porcentaje de Vitalidad Fetal logrado con la aplicación de Prosphere® 200 mg semanalmente (cada 7 días) hasta la semana 12. (21) Prosphere® 200 mg es una Suspensión Acuosa de Microesferas Cristalinas Bioerosionables de Progesterona Natural (Bioidéntica) para administración por vía intramuscular. Las Microesferas constituyen un sistema novedoso de Liberación Prolongada por vía intramuscular, que permite mantener niveles terapéuticos de Progesterona aplicando por vía I.M. solamente una dosis a la semana (cada 7 días). Lo anterior se constituye como una ventaja radical sobre la Progesterona en solución oleosa y por otras vías, en términos de comodidad, tolerabilidad y cumplimiento del tratamiento. (21) Porcentaje de Aceptación y Comodidad 96.6% reportada por las pacientes (n=30) Figura No. 8. Porcentaje de Seguridad y Tolerabilidad con la aplicación de Prosphere® 200 mg semanalmente (cada 7 días) hasta la semana 12. (21). 14 8. Experiencia Clínica SEGURIDAD Y TOLERABILIDAD 8.1 Efectos Secundarios 8.3 Contraindicaciones La Progesterona ha sido ampliamente utilizada y su perfil de seguridad es bien conocido. Los efectos secundarios que se producen con más frecuencia durante el tratamiento con Progesterona incluyen: irregularidades menstruales, cambios en el sangrado menstrual, dismenorrea y amenorrea. La administración de Progesterona también puede causar sangrado transvaginal abundante, spotting (manchado), cambios ponderales, náusea, vómito, mastalgia y cefalea. Puede ocurrir retención de líquidos y edema durante la administración de Progesterona. (30) La Progesterona, en cualquier forma farmacéutica, está contraindicada en: enfermedad hepática, sangrado uterino anormal sin diagnóstico, cáncer de mama, cáncer en órganos genitales, embarazo ectópico, aborto incompleto; y debe ser utilizada con precaución en pacientes con: dislipidemia, diabetes, asma, insuficiencia cardiaca, enfermedad renal, trastornos psiquiátricos y en quienes tengan antecedentes de tromboflebitis o enfermedad tromboembólica. (20) 8.2 Tolerabilidad La Progesterona es susceptible de interacciones con fármacos inductores de los sistemas enzimáticos hepáticos. La administración concurrente con carbamazepina, fenitoína, fosfenitoína y posiblemente barbitúricos, puede incrementar la eliminación de la Progesterona. 8.4 Interacciones medicamentosas La administración intramuscular de Progesterona oleosa resulta a menudo en reacciones locales, que incluyen eritema, irritación, dolor e inflamación marcada en el sitio de inyección resultante en rubor, dolor y formación de abscesos. (30) El metabolismo de la Progesterona se inhibe por ketoconazol, un inhibidor conocido del citocromo P450 3A4. No se ha determinado si otros fármacos que inhiben a las enzimas CYP 3A4 tendrían un efecto similar. Otros fármacos con este efecto son cimetidina, claritromicina, danazol, diltiazem, eritromicina, fluconazol, itraconazol, voriconazol, troleandomicina, verapamilo. (30) Prosphere® 200 mg , por ser una Suspensión Acuosa de Liberación Prolongada y Administración Unidosis Semanal, disminuye ostensiblemente estos efectos por lo tanto es mejor tolerado. En los estudios clínicos realizados para evaluar la farmacocinética de Prosphere® 200 mg no se observaron eventos adversos serios o inesperados. (10, 11) En una serie de 30 casos de pacientes en ciclos de Reproducción Asistida también se reporta un perfil de elevada seguridad con una muy baja incidencia, un sólo caso, de reacción local leve. (21) 15 9. Prosphere® en la Práctica 9.1 Presentación Prosphere® 200 mg se presenta en una caja conteniendo 1 jeringa prellenada con Suspensión Acuosa Inyectable I.M. de Progesterona. 9.2 Método de Aplicación Aplicar Prosphere® 200 mg por vía intramuscular profunda en el cuadrante superior externo del glúteo. Se recomienda alternar el lado de inyección semanalmente (cada 7 días). 16 10. INFORMACIÓN PARA PRESCRIBIR REDUCIDA (IPP-R) I. DENOMINACIÓN DISTINTIVA. PROSPHERE® II. DENOMINACIÓN GENÉRICA. Progesterona III. FORMA FARMACÉUTICA Y FORMULACIÓN: Suspensión inyectable Fórmula: La jeringa prellenada con suspensión acuosa contiene: Progesterona Vehículo cbp 100 mg 1 mL 200 mg 2 mL 300 mg 2.75 mL IV. INDICACIONES TERAPÉUTICAS La Progesterona es de utilidad en las siguientes entidades nosológicas, entre otras: Amenorrea primaria y secundaria. - Hemorragia uterina disfuncional. - Endometriosis. - Síndrome premenstrual. - Hirsutismo. - Fertilización y embarazo asistido. - Amenaza de aborto o prevención de aborto Tde repetición por insuficiencia lútea. - Alteraciones de la fase lútea en el curso de un ciclo espontáneo o inducido, en caso de infertilidad o de esterilidad primaria o secundaria en especial por anovulación. - Síndrome climatérico. - Hiperplasia endometrial V. CONTRAINDICACIONES - Hipersensibilidad a los progestágenos. - Cáncer genital o mamario hormonodependiente (sospecha o confirmado). - Tromboflebitis. - Desórdenes tromboembólicos. - Antecedentes personales de aploplejia cerebral. - Insuficiencia hepática severa. - Sangrado uterino no diagnosticado. - Lactancia. - Aborto VI. PRECAUCIONES GENERALES La progesterona se debe utilizar con precaución en pacientes con antecedentes de hipertensión arterial, enfermedad cardiaca, enfermedad hepática o renal, epilepsia, antecedentes de depresión, migraña, o bien con antecedentes de retención de líquidos. VII. RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA La progesterona no es teratogénica, esto ha sido demostrado en la actualidad en una gran cantidad de nacimientos de niños, cuyo periodo embriogénico ha tenido lugar en un ambiente terapéuticamente enriquecido con esta hormona. El uso de este producto es siempre previa valoración médica evaluando el riesgo beneficio. La progesterona es excretada en la leche materna en cantidades detectables, por lo que no es aconsejable su uso en esta fase. 17 VIII. REACCIONES SECUNDARIAS Y ADVERSAS En la literatura médica se han reportado: Sistema nervioso central; Migraña, mareo, letargia, depresión mental, somnolencia, insomnio. Cardiovascular: Desórdenes tromboembólicos, embolia pulmonar. Ojos: Cambios en la visión, diplopia, papiledema, lesiones vasculares retinianas. Gastrointestinal: Enfermedad hepática, ictericia colestásica, náuseas, vómito, calambres abdominales. Genitourinario: Ginecomastia, galactorrea, candidiasis vaginal, cloasma, erosión cervical, y cambios en las secreciones, dismenorrea, amenorrea, prurito vulvar. Metabólico: Hiperglicemia, disminución de la libido, incremento transitorio del sodio, y excreción de cloro, fiebre. Piel: Acné, prurito, rash alérgico, fotosensibilidad, urticaria, alopecia. Otros: Edema, cambios en el peso, dolor en sitio de la inyección y fatiga. IX. INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO Doxorrubicina: El incremento de la doxorrubicina induce neutropenia y trombocitopenia, esto ha sido observado cuando la Progesterona intravenosa (arriba de 10 mg en 24 horas) fue administrada concurrentemente con doxorrubicina intravenosa (60 mg/m², bolo) en pacientes con malignidades avanzadas. El mecanismo de interacción no ha sido identificado. Ketoconazol: El ketoconazol es un inhibidor de las enzimas del citocromo P450 y 3A4, y ha mostrado inhibir el metabolismo de la Progesterona in vitro, dando como resultado un incremento en la biodisponibilidad de la Progesterona. La significancia clínica de esta interacción es desconocida. El efecto de la Progesterona natural micronizada puede ser disminuido por uso concomitante por tiempo prolongado de barbitúricos, carbamacepina, hidantoína o rifampicina. El uso de este medicamento puede aumentar los efectos de los betabloqueadores, de teofilina o ciclosporina. X. PRECAUCIONES Y RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS, Y SOBRE LA FERTILIDAD. Durante los estudios clínicos, la Progesterona natural no ha inducido, efectos de carcinogénesis, mutagénesis, teratogénesis, ni sobre la fertilidad. XI. DOSIS Y VÍA DE ADMINISTRACIÓN Intramuscular profunda. La dosis de la Progesterona se establece según el efecto deseado y el caso individual. Regularización del ciclo menstrual: Administrar dosis bajas constantes durante la fase secretoria del ciclo. Amenorrea primaria y secundaria, síndrome premenstrual, sangrado uterino disfuncional, endometriosis, hirsutismo: Administrar según dosis respuesta. Fertilización y embarazo asistido: Administrar dosis mayores durante el primer trimestre gestacional. La duración y frecuencia de la administración variará a criterio del médico. Amenaza prevención de aborto de repetición, por insuficiencia lútea: Administrar 100 a 300 mg IM, cada 7 días. XII. SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL No se han reportado casos de sobredosificación o ingesta accidental. 18 XIII.- PRESENTACIONES Caja con una jeringa prellenada con suspensión acuosa de progesterona 100 mg en 1.0 mL en envase de burbuja y una aguja esterilizada desechable Caja con una jeringa prellenada con suspensión acuosa de progesterona 200 mg en 2.0 mL en envase de burbuja y una aguja esterilizada desechable Caja con una jeringa prellenada con suspensión acuosa de progesterona 300 mg en 2.75 mL en envase de burbuja y una aguja esterilizada desechable XIV. LEYENDAS DE PROTECCIÓN Consérvese a temperatura ambiente a no más de 30º C. Su venta requiere receta médica. Literatura exclusiva para médicos. No se deje al alcance de los niños. XV. NOMBRE DEL LABORATORIO Y DIRECCIÓN Hecho en México por: Productos Científicos S.A de C.V Carnot® Laboratorios Nicolás San Juan 1046 Colonia del Valle, CP 03100 México D.F XVI. Número de registro del medicamento. 181M2005 SSA IV Clave IPP-R ® Marcas Registradas. 19 11. Referencias Bibliográficas 1. Abate A, Brigandi A, Abate FG, Manti F, Unfer V, Perino M. Luteal phase support with 17alpha-hydroxiprogesterone versus unsupported cycles in in vitro fertilization: a comparative randomized study. Gynecol Obstet Invest. 1999;48:78-80. 2. Abate A, Perino M, Abate FG, Brigandi A, Costabile L, Manti F. Intramuscular versus vaginal administration of progesterone for luteal phase support after in vitro fertilization and embryo transfer. A comparative randomized study. Clin Exp Obstet Gynecol. 1999;26:203-206. 3. Artini PG, Volpe A, Angioni S, Galassi MC, Battaglia C, Genazzani AR. A comparative, randomized study of three different progesterone support of the luteal phase following IVF/ET program. J Endocrinol. Invest. 1995;Jan;18(1):51-6. 4. Braendle W. Das Klimakterium. Endokrinologie, Pharmakologie der Hormone und Hormon-sustitution. Stuttgart; Wiss. Verl.-Ges. 2000;101. 5. Centres for Disease Control, USA. Assisted Reproductive Technology Success Rates. USA:CDC, 2001. [Cited 2004]. 6. Chantilis S, Zeitoun K, Patel S, Johns A, Madziar V y McIntire D. Use of Crinone® vaginal progesterone gel for luteal support in vitro fertilization cycles. Fertil Steril. Nov 1999;72(5):823-829. 7. Daya S, Gunby J. Luteal phase support in assisted reproduction cycles. Cochrane database of systematic reviews. 2007;Issue 3. Art. No. CD004830. DOI: 10.1002/14651858.CD004830. 8. Delgado J, Fernández del Castillo C. Ginecología y Reproducción Humana, temas selectos. Colegio Mexicano de Especialistas en Ginecología y Obstetricia. S. ed. 2006;Tomo II, 377. 9. Di Renzo GC, Mattei A, Gojnic M, Gerli S. Progesterone and pregnancy. Curr Opin Obstet Gynecol, 2005;17(6):598-600. 10. Estudio 0303/I/APL. Estudio de farmacocinética comparativa de microesferas cristalinas bioerosionables de progesterona en suspensión acuosa intramuscular con dos niveles de dosis, 100 y 200 mg, en mujeres postmenopáusicas. 2007. Asociación Mexicana para la Investigación Clínica. 11. Estudio 0410/I/APL. Estudio farmacocinético multidosis de tres formulaciones de microesferas cristalinas bioerosionables de progesterona en suspensión acuosa intramuscularde Progesterona a dosis de 200 y 300 mg en mujeres postmenopáusicas. 2007. Asociación Mexicana para la Investigación Clínica. 12. Estudio BIO 2002 02. Estudio preclínico de biodisponibilidad de suspensión acuosa intramuscular de microesferas cristalinas bioerosionables de progesterona 100 mg y en solución oleosa en conejos machos Nueva Zelanda. 2002. Centro AF de Estudios Tecnológicos S.A. 13. Estudio BIO 9702. Estudio de irritación de formulaciones de microesferas cristalinas bioerosionables de progesterona en suspensión acuosa intramuscular y solución oleosa de Progesterona en conejos machos Nueva Zelanda. 1997. Centro AF de Estudios Tecnológicos S.A. 20 14. Fatemi, H M, Kolibianakis E M, Camus M, Tournaye H, Donoso P, Papanikolaou, et al. Addition of estradiol to progesterone for luteal supplementation in patients stimulated with GnRH antagonist/rFSH for IVF: a randomized controlled trial. Human Reproduction. 2006;21(10) 2628-2632. 15. Germond M, Capelli P, Bruno G, Vesnaver S, Senn A, Rouge N, et al. Comparison of the efficacy and safety of two formulations of micronized progesterone (Ellios® and Utrogestan®) used as luteal phase support after in vitro fertilization. Fertil Steril. Feb 2002;77(2):313-317. 16. Goodman Gilman. Las Bases Farmacológicas de la Terapéutica. Hardman J & Limbird L. ed. 10ª edición, Vol II, Editorial Mc Graw Hill México. 2001;(58):1636-1638. 17. Kably A, Ruiz J, Walters F, Quesnel C, Karchmer S. Análisis de los resultados de la administración complementaria de estradiol y progesterona en la fase lútea contra progesterona sola en un programa de reproducción asistida. Ginecol Obstet Mex. 2005;73:173-182. 18. Licciardi F, Kwiatkowski A, Noyes N, Berkeley A, Krey L y Griffo J. Oral versus intramuscular progesterone for in vitro fertilization: a prospective randomized study. Fertil Steril. Apr 1999;71(4):614-648. 19. Macklon NS, Fauser BCJM. Impact of ovarian hyperstimulation on the luteal phase. J Reprod Fertil Suppl. 2000;55:101-108. 20. McGraw-Hill Accessmedicine. Progesterone (Monograph). Mar 2004 [Cited 2007]. 21. Menocal-Tobías G, Sánchez-UR, Dueñas RJ, et al. ProSphere a new natural progesterone (bioidentical) at in the treatment of reproductive techniques. Centro de Reproducción Médica Fértil. 2007. (in press). 22. Miles R, Paulson R, Lobo R, Presa M, Dahmous L, Sauer M. Pharmacokinetics and endometrial tissue levels of progesterone after administration by intramuscular and vaginal routes: a comparative study. Fertil Steril. Sep 1994;62(3):485-490. 23. Nardo LG, Sallam HN. Progesterone supplementation to prevent recurrent miscarriage and to reduce implantation failure in assisted reproduction cycles. Reprod Biomed. Jul 2006;13(1):47-57. 24. Pabuccu R, Akar ME. Luteal phase support in assisted reproductive technology. Curr Opin Obstet Gynecol. 2005;17(3):277-281. 25. Penzias A. Luteal phase support. Fertil Steril. Feb 2002;77(2):318-323. 26. Pritts E, Atwood A. Luteal phase support in infertility treatment: a meta-analysis of the randomized trials. Human Reproduction. 2002;17(9):2287-2299. 27. Shamma FN, Penzias AS, Thatcher S, DeCherney AH, Lavy G. Corpus luteum function in successful in vitro fertilization cycles. Fertil Steril. 1992;57:1107-1109. 21 28. Simon J, Robinson D, Andrews M, Hildebrand J, Rocci M, Blake R, Hodgen G. The absorption of oral micronized progesterone: the effect of food, dose proportionality, and comparison with intramuscular progesterone. Fertil Steril. Jul 1993;60(1):26-33. 29. Stocco C, Telleria C, Gibori G. The molecular control of corpus luteum formation, function, and regression. Endoc. Rev. Feb 2007;28(1):117-149. 30. USP for the Health Care Professional. 24th ed. Thompson Micromedex editors USA. 2004:23772384. 31. Zegers-Hochschild F, Schwarze JE, Borrero C. Delivery routes of progesterone in assisted reproduction. Exp Rev Obst & Gyn. Nov 2006;1,(2):173-182. 22