www.intramed.net Todos los derechos reservados | Copyright 1997
Anuncio

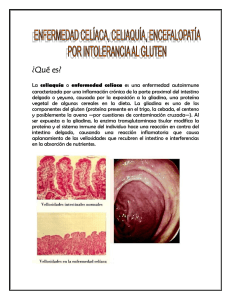
-----------------------------------------------------------------------------------------------------------ENFERMEDAD CELÍACA HOSPITAL SAN ROQUE Servicio de Gastroenterología Dra. Mitre, María Belén RESIDENTE DE TERCER AÑO DE GASTROENTEROLOGIA INTRODUCCIÓN: La enfermedad celíaca, también conocida como esprue celíaca y enteropatía sensible al gluten, se caracteriza por malabsorción resultante del daño inflamatorio de la mucosa del intestino delgado, la cual presenta linfocitos intraepiteliales, desarrollo de criptas hiperplásicas y atrofia vellositaria. Esta injuria se produce por la ingestión de alimentos con gluten o relacionados con proteínas de centeno y cebada en individuos genéticamente susceptibles. En la mayoría de los casos, la enfermedad entérica mejora su clínica e histología cuando el gluten es eliminado de la dieta. Anteriormente se pensaba en la enfermedad celíaca como un raro desorden con un rango de prevalencia menor al 0.1 %. Estudios más recientes evidenciaron que la enfermedad celíaca en una enfermedad común que afecta a 1 de 200 individuos blancos. Este cambio de prevalencia puede ser por un incremento en la vigilancia por parte del médico en la historia natural silente de la enfermedad celíaca, lo que conduce a un mejor diagnóstico.(1) RESEÑA HISTÓRICA DE LA ENFERMEDAD CELÍACA La palabra esprue, proviene del inglés sprue, que deriva de spruw, que significa enfermedad aftosa, debido a la alta prevalencia de úlceras aftosas en estos pacientes La historia de la enfermedad celíaca, data del 1er siglo (AC). En el año 1940 se estableció la relación con la ingesta de gluten.(3) Los pediatras Dicke y Dutch observaron que la condición de los niños con enfermedad celíaca mejoraba durante la falta de alimentación durante la II Guerra Mundial, donde recaían, luego de reanudar los cereales. Con posterioridad Van de Kamer, Weijers y Dicke demostraron que la fracción del gluten o proteica insoluble en agua del trigo producía malabsorción de las grasas en los pacientes con enfermedad celíaca. En 1954, Paulley, por medio del estudio de material de biopsia quirúrgica, proporcionó la primer descripción exacta de la lesión intestinal característica de los pacientes con enfermedad celíaca. A fines del año 1950 Rubin y colaboradores gracias al desarrollo de instrumentos para la toma de biopsias por aspiración peroral, demostraron en forma convincente que la enfermedad celíaca -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 1 -----------------------------------------------------------------------------------------------------------en los niños y el esprue idiopático o no tropical en los adultos eran enfermedades idénticas con las mismas características clínicas y anatomopatológicas. Más recientemente, se observó que la enfermedad celíaca se asocia con el haplotipo HLA DQ 2 los cuales presentan de preferencia péptidos derivados del gluten a las células T de la mucosa intestinal, lo que implica firmemente mecanismos genéticos e inmunes en la patogenia de la enfermedad celíaca.(4) EPIDEMIOLOGÍA La verdadera prevalencia de la enfermedad celíaca es difícil de establecer, debido a que muchos pacientes presentan síntomas atípicos o ninguno. La alta prevalencia reportada es en Europa Occidental y en lugares de emigrantes europeos, especialmente América del Norte y Australia. La enfermedad celíaca también se halla en partes del noroeste de la India y puede estar subdiagnosticada en América del Sur, Norte de África y Asia. Es rara en individuos afro caribeños, chinos o japoneses. En la mayoría de los casos hay una leve preponderancia femenina.(3) ETIOLOGÍA DE LA ENFERMEDAD CELÍACA La interacción de la fracción proteica no soluble en agua (gluten) de ciertos granos de cereales, como la harina de trigo, cebada o centeno es crucial en la patogenia de la enfermedad. Los componentes proteicos solubles en alcohol de estos granos son los que resultan tóxicos. Estas sustancias llamadas prolaminas, son las gliadinas en el trigo, las secalinas en el centeno y las hordeínas en la cebada. La gliadina puede ser separada por electroforesis en 4 fracciones,(α, β, γ y ω), las cuales todas son potenciales de producir lesión mucosa. El segmento del intestino expuesto al gluten desarrolla la lesión mucosa típica en 8 a 12 horas. Se ha debatido mucho acerca de si la instilación de harina de avena causa algún daño, ahora existen firmes evidencias clínicas de que el consumo moderado de avena en la dieta es bien tolerado.(4) Sin embargo hay que tener precaución en cuanto a la manufactura de la avena para el consumo, ya que puede estar contaminada con otros cereales, y aún avena de gran pureza puede inducir atrofia vellositaria y sintomatología en una minoría de pacientes.(5) FACTORES GENÉTICOS La prevalencia de la enfermedad celíaca en familiares de primer grado es del 10 %. (3) Los síntomas a menudo están ausentes o son tan leves que algunos familiares afectados no son concientes de alguna anormalidad. Aproximadamente el 95 % de los individuos afectados heredan los alelos DQ, DQA1, DQB1, los cuales codifican la molécula DQ2 del HLA DQ, lo cual sugiere que este heterodímero DQ confiere la susceptibilidad a la enfermedad. No se observaron anormalidades estructurales en los alelos DQ de los pacientes con enfermedad celíaca con DQ2. Aquellos individuos con enfermedad celíaca que carecen de DQ2 la mayoría exhibe el haplotipo DR4 – DQ8 asociado con los alelos DQA1 – DQB1, por lo que sugiere que estos también pueden aumentar la susceptibilidad a la enfermedad celíaca. La mayoría de los individuos con haplotipos HLA asociados con una enfermedad celíaca permanecen sanos. Por lo tanto, se desconoce la forma exacta en que las asociaciones con HLA predisponen a la enfermedad; parece que se requeriría un gen de susceptibilidad adicional, o como otra alternativa, un desencadenante ambiental más allá del gluten.(4) MECANISMOS INMUNES -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 2 -----------------------------------------------------------------------------------------------------------Las respuestas inmunes del huésped son mediadas por células productoras de inmunoglobulinas, las cuales aumentan de 2 a 6 veces en la lámina propia del intestino delgado y por linfocitos T, también presentes de manera abundante en la lámina propia. El nivel de Inmunoglobulina A sérica está aumentado mientras que el nivel sérico de Inmunoglobulina M está disminuida en muchos pacientes con enfermedad celíaca no tratados, pero no en los tratados. La Inmunoglobulina A no es crucial para el desarrollo de la enfermedad ya que la presencia simultánea de enfermedad celíaca y deficiencia de Inmunoglobulina A es aproximadamente 10 veces mayor de lo que cabría esperar. En el suero de la mayoría de los pacientes con enfermedad celíaca se hallan anticuerpos de Inmunoglobulina G contra fracciones de la gliadina. En la respuesta inmune mediada por células hay abundantes linfocitos T y la mayoría de los linfocitos intraepiteliales en abundancia son CD8+. La mayor parte de los linfocitos T activados en la lámina propia son células CD4+. Mientras que en los individuos normales, el 90% o más de los linfocitos intraepiteliales expresan el receptor de linfocitos T (α / β), la expresión del receptor de linfocitos T (γ / δ) por parte de los linfocitos intraepiteliales de pacientes con enfermedad celíaca no tratada aumenta desde 20 al 35% hasta 6 veces.(4) PATOGÉNESIS DE LA ENFERMEDAD CELÍACA La gliadina es absorbida en la lámina propia y presentada en asociación con HLA DQ2 o DQ8 de superficie por células presentadoras de antígenos, probablemente células dendríticas para sintetizar células T que expresan el receptor de linfocitos T (α / β). La transglutaminasa de tejido deamina los péptidos de la gliadina generando ácido, residuos de carga negativa de ácido glutámico de glutaminas neutrales. Debido a que la carga negativa de los residuos se encuentra preferentemente en las posiciones 4, 6 y 7 de la ligadura del antígeno con HLA DQ2, la deaminación de la gliadina induce a una fuerte respuesta de las células T. Estos linfocitos luego activan otros linfocitos, para generar citoquinas, así como interferón (γ), interleucina 4 y factor de necrosis tumoral α, las cuales dañan las vellosidades, resultando la enteritis. La inducción aberrante de los antígenos de superficie HLA clase II sobre el enterocito, puede permitir que estas células presenten antígenos adicionales para sintetizar linfocitos.(3) ANATOMÍA PATOLÓGICA La enfermedad celíaca compromete a la mucosa del intestino delgado; la submucosa, muscular y serosa por lo común no están afectadas. El examen microscópico revela una superficie mucosa plana, con ausencia de vellosidades intestinales normales. En el examen histológico, en la mayor parte de los casos el espesor total de la mucosa está sólo levemente reducido, porque las criptas intestinales están muy alongadas e hiperplásicas, lo que compensa la ausencia o el acortamiento de las vellosidades. Estos cambios en la arquitectura reducen la cantidad de superficie epitelial disponible para la digestión y la absorción en el intestino afectado. Las anormalidades estructurales de las uniones estrechas entre las células absorbentes lesionadas, explican la mayor permeabilidad de la barrera mucosa. Las enzimas que contribuyen a la digestión y a la absorción están alteradas debido al daño de estas células absorbentes. Las disacaridasas, peptidasas, la fosfatasa alcalina, la adenosina trifosfatasa y las esterasas están disminuidas y las hidrolasas ácidas están aumentadas. La celularidad de la lámina propia está aumentada, consiste principalmente en células plasmáticas y linfocitos. Las células productoras de inmunoglobulina A, M y G están aumentadas predominando las productoras de inmunoglobulina A. Los leucocitos polimorfonucleares, mastocitos, y eosinófilos pueden contribuir al aumento de la celularidad. -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 3 -----------------------------------------------------------------------------------------------------------La cantidad de linfocitos intraepiteliales por unidad de longitud del epitelio está aumentada, pero la cantidad total de linfocitos intraepiteliales no lo está, porque la superficie de absorción esta muy reducida.(4) Las anormalidades histológicas de la mucosa del intestino delgado se desarrollarían en fases consecutivas dentro del espectro de la sensibilidad al gluten. Este espectro ha sido descripto por Marsh (año 1992) y abarca 3 estadios consecutivos de daño de la mucosa.(Fotos 1-2 y3) Tipo I: infiltrativa, lesión con mayor a 30 linfocitos /100 células epiteliales Tipo II: infiltrativa hiperplásica Tipo III: atrofia vellositaria (a) parcial, (b) subtotal, (c) total.(6) Foto N1 Hi perplasiia de las criptas los linfocitos intraepiteliales Foto N2 Atrofia vellositaria Foto N3 Aumento de La longitud del intestino delgado lesionado se correlaciona con la severidad de los síntomas clínicos, cuando la lesión intestinal no compromete toda la longitud del mismo, el intestino proximal es la parte más severamente afectada y la severidad disminuye hacia el intestino delgado distal. La indemnidad del intestino proximal con sólo compromiso de la porción distal no es una característica de la enfermedad celíaca. El manejo apropiado de una dieta libre de gluten en pacientes con enfermedad celíaca lleva a una significativa mejoría de la estructura intestinal. La mucosa del intestino delgado distal mejora más rápidamente que la porción proximal severamente afectada. En algunos casos puede requerirse meses o años de supresión de gluten para que la estructura mucosa se normalice. (4) MANIFESTACIONES CLÍNICAS -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 4 -----------------------------------------------------------------------------------------------------------Enfermedad celíaca en niños: Clásicamente se presenta; entre 4 y 24 meses, con fallo en el crecimiento, diarrea y distensión abdominal. Son comunes los vómitos y edema. El comienzo de los síntomas es gradual con la introducción de los cereales en la dieta. Si bien lo típico es la presencia de diarrea algunos presentan constipación. Los pacientes con enfermedad severa y no tratada pueden presentarse con baja estatura, pubertad retrasada, deficiencia de hierro y folato con anemia y raquitismo. La enfermedad celíaca atípica, generalmente es observada en niños mayores o adolescentes, quienes frecuentemente no tienen hallazgos de malabsorción. También puede presentarse con dolor abdominal recurrente, hipertransaminasemia, estomatitis aftosa recurrente, artralgia, defectos en el esmalte dental, disturbios en su conducta y pobre rendimiento escolar.(3) Enfermedad celíaca en adultos: El diagnóstico de enfermedad celíaca aumenta comenzando a la edad adulta. Los síntomas pueden persistir durante toda la niñez, si no se instaura tratamiento, pero habitualmente disminuyen o desaparecen por completo durante la adolescencia, para reaparecer durante la edad adulta temprana ( 3º y 4º década), cerca de un 20 % de los casos ocurre en pacientes que tienen mas de 60 años. Sin embargo, muchos no tienen historia de síntomas, lo que sugiere que la enfermedad celíaca puede desarrollarse en la adultez. La enfermedad celíaca puede presentarse durante el embarazo o post parto y el diagnóstico se debería considerar en la mujer embarazada que desarrolla una anemia severa.(3) Síntomas Gastrointestinales: Los hallazgos más frecuentes en pacientes con enfermedad extensa son: diarrea, flatulencia, pérdida de peso, fatiga y dolor abdominal recurrente. La diarrea puede presentarse hasta con 10 deposiciones diarias acuosas o semi formadas, color similar a la masilla con olor desagradable y rancio, suelen ser espumosas por su alto contenido de gas y oleosas, a menudo flotan y pueden ser difíciles de eliminar del inodoro. Es posible la deshidratación por depleción de electrolitos y acidosis. No todos los pacientes se presentan con diarrea, algunos refieren constipación. En los mecanismos responsables de la diarrea intervienen varios factores: El volumen y la carga osmótica de las heces aportadas al colon están aumentadas por la malabsorción de grasas, hidratos de carbono, proteínas, agua, electrolitos y nutrientes. El exceso de grasas dietarias al colon da como resultado la producción bacteriana de hidroxiácidos grasos que son potentes catárticos irritantes. El agua y los electrolitos son secretados más que absorbidos, hacia la luz del intestino delgado proximal, lo que incrementa aún más el líquido luminal en un intestino con una capacidad de absorción ya comprometida. La liberación de colecistocinina y secretina en respuesta a una comida está alterada con la disminución del aporte de bilis y secreciones pancreáticas hacia la luz intestinal, lo que contribuye a la diarrea. Si la lesión se extiende hasta el ileon la absorción alterada de las sales biliares conjugadas produce mayor reacción catártica y empeoramiento de la diarrea. La magnitud de la pérdida de peso depende de la severidad y de la extensión de la enfermedad sobre la mucosa intestinal, y de la capacidad del paciente de compensar la malabsorción por medio del aumento de la ingesta. Algunos presentan incremento del apetito, raras veces se desarrolla anorexia. -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 5 -----------------------------------------------------------------------------------------------------------La debilidad, laxitud y fatiga se relacionan con la mala nutrición general. La debilidad muscular puede relacionarse con la pérdida de potasio en las heces. El dolor abdominal intenso no es común. La distensión abdominal con una excesiva cantidad de flatos malolientes puede llevar a un diagnóstico erróneo de síndrome de intestino irritable. La estomatitis aftosa recurrente puede ser el único síntoma de presentación.(3,4) Síntomas Extraintestinales: Aproximadamente el 50 % de los pacientes no presentan una diarrea clínicamente significativa. Las manifestaciones pueden ser: Hematopoyéticas: anemia es la presentación más común, por alteración de la absorción de hierro o folato en el intestino proximal, en caso de compromiso ileal también se altera la absorción de la vitamina B12. Puede haber púrpura, hemorragia digestiva, vaginal, nasal o renal causada por alteración en la absorción intestinal de vitamina K dando como resultado una deficiencia de protrombina, que resulta en una alteración de la coagulabilidad. El hipoesplenismo es de causa desconocida con trombocitosis, eritrocitos deformados y atrofia esplénica en 50 % de los pacientes. Esqueléticas: osteopenia debido a que la absorción de calcio está alterada por el transporte defectuoso del mismo por parte del intestino delgado afectado, también por deficiencias en la absorción de vitamina D y por fijación de calcio y magnesio intraluminales a ácidos grasos de la dieta no absorbidos. La sintomatología puede ser dolor óseo en la parte baja de la espalda, parrilla costal y pelvis. Las fracturas patológicas no son comunes. La deficiencia de magnesio y calcio puede ocasionar parestesias, calambres musculares, incluso tetania manifiesta.(3,4) Neurológicas: se estima que ocurren en un 10 % de los pacientes afectados. En un estudio de 20 pacientes con neuropatía y biopsia de intestino que confirma enfermedad celíaca el 100 % presentó disestesia y parestesias en las extremidades distales, 35 % disestesia facial, 30 % dolores corporales multifocales difusos, 25 % inestabilidad en la marcha y el 5% caída del pie. Los estudios electrofisiológicos fueron normales o levemente anormales en un 90 %.(7) Puede haber ceguera nocturna por deficiencia de vitamina A. Se ha comunicado casos de epilepsia y retardo de la memoria.(3,4,7) Endócrinas: debido a la alteración severa de la absorción del calcio puede desarrollarse hiperparatiroidismo secundario, provocando movilización del calcio de los huesos en respuesta al bajo nivel sérico de calcio, contribuyendo aún mas a la osteopenia. Puede haber amenorrea, infertilidad e impotencia en los hombres.(3,4) Enfermedades Asociadas En la mayoría de estas afecciones se ha implicado una alteración de la función inmune y algunos presentan asociación con el haplotipo HLA similar al de la enfermedad celíaca.(4) - Hepáticas: Una modesta elevación de los niveles séricos de transaminasas ocurre en un 15 a 55 % de los pacientes con enfermedad no tratada. En ausencia de otras enfermedades, la enfermedad celíaca ha sido hallada en un 9 % de los pacientes. Aparte de los disturbios hepáticos no específicos, se ha documentado asociación entre enfermedad celíaca y enfermedades hepáticas autoinmunes como cirrosis biliar primaria, hepatitis autoinmune y colangitis esclerosante primaria, por lo tanto, la posible presencia de enfermedad celíaca debería investigarse en pacientes con enfermedad hepática severa.(8,9) -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 6 -----------------------------------------------------------------------------------------------------------El mecanismo de daño hepático y enfermedad celíaca no se encuentra claro. La mala nutrición es una causa común, el aumento en la permeabilidad de la mucosa intestinal característica de la enfermedad celíaca, puede facilitar la entrada de toxinas bacterianas y otros antígenos al sistema porta. Histológicamente solo una mínima esteatosis hepática o una hepatitis reactiva no específica puede observarse en enfermos celíacos, en los cuales los niveles de enzimas hepáticas están levemente aumentadas, retornando a la normalidad con una dieta libre de gluten. Esofagitis: por reflujo: los pacientes con enfermedad celíaca presentan un retraso en el vaciamiento gástrico y valores bajos en la presión del esfínter esofágico inferior. El mecanismo por el cual, la enfermedad celíaca puede predisponer al desarrollo de esofagitis, es sólo hipotético, se ha demostrado que pacientes con enfermedad celíaca tienen un aumento de los niveles plasmáticos de enteroglucagón y neurotensina, los cuales se conoce que disminuyen la presión del esfínter esofágico inferior y retrasan el vaciamiento gástrico (10) Diabetes Tipo 1: en el 90 % de los pacientes, la diabetes se diagnostica antes que la enfermedad celíaca. El aumento de la prevalencia de enfermedad celíaca en la diabetes tipo 1 se puede explicar por la presencia común de HLA B8, DR3 y DQB1; también por la presencia de autoanticuerpos que pueden estar presentes en cualquiera de los pacientes con enfermedad celíaca y puede predecir el desarrollo futuro de enfermedad celíaca. Al momento del estudio, la mayoría de los niños no presentan disturbios gastrointestinales y en algunos casos sólo se reconoce en forma retrospectiva. Pruebas Serológicas: la inmunoglobulina A antigliadina puede presentarse como fenómeno transitorio en el comienzo de la diabetes y puede reflejar un disturbio inmunológico o un aumento de la permeabilidad intestinal en ese momento. La inmunoglobulina A antiendomisio, puede aparecer transitoriamente. El estudio de la enfermedad celíaca en pacientes diabéticos tipo 1 debería ser anualmente durante 3 años, luego a los 5 años y 5 años después, o en cualquier momento si hay indicios clínicos. Se sugiere que el estudio debería ofrecerse a familiares de 1º grado que presenten diabetes tipo 1 ya que pueden tener una enfermedad celíaca silente.(11) Dermatitis Herpetiforme: El 10 % de los pacientes con enfermedad celíaca presentan lesiones papulovesiculosas y pruriginosas que se distribuyen simétricamente sobre las superficies extensoras de extremidades, tronco, glúteos, cuero cabelludo y el cuello.(3) Se caracterizan por depósitos de inmunoglobulina A lineales en la unión de la dermis–epidermis en 5-15 % de los pacientes. Muchos no experimentan ningún síntoma intestinal. La eliminación del gluten en la dieta revierte la lesión dermatológica e intestinal. La prevalencia de HLAB8–DR3– DQ2 y anticuerpos antigliadina, antirreculina y antiendomisio circulantes es similar a la observada en la enfermedad celíaca sin enfermedad cutánea.(4) Enfermedades autoinmunes: la enfermedad celíaca es una enteropatía autoinmune desencadenada por el gluten de la dieta en individuos genéticamente susceptibles. Los trastornos autoinmunes deben cumplir ciertas condiciones: Presencia de reacción autoinmunitaria. Demostración clínica o experimental que la reacción no es secundaria a una lesión del tejido, sino que tiene significado patogénico primario. Ausencia de otra causa bien definida de enfermedad. La enfermedad celíaca parece cumplir con los criterios de enfermedad autoinmune, ya que se conoce la predisposición genética (HLA), factores exógenos desencadenantes (gluten) y autoantígenos (transglutaminasa tisular), por lo que la enfermedad celíaca puede estar asociada con mayor frecuencia a enfermedades autoimnunes (cuadros No1 y 2). La presencia de enfermedad celíaca está aumentada en familiares de pacientes con enfermedad autoinmune. -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 7 -----------------------------------------------------------------------------------------------------------Cuadro N o1 Autores Diabetes Tipo 1 Lancaster Cooper Midhagen Snook Collin 3.5 % 3.2 % ND 1.4 % 5.4 % Cuadro No 2 Enfermedades Autoinmunes Diabetes Tipo 1 Enfermedad Tiroidea Artritis crónica juvenil Alopecia Cirrosis biliar primaria. Ataxia Autoinmune Epilepsia con calcificaciones cerebrales Enfermedades Tiroideas autoinmunes 5.2 % 3.2 % 10.8 % 4.1 % 5.4 % Enfermedades del tejido conectivo 1.8 % 6.1 % 3.6 % ND 7.2 % Enf. Celíaca Silente (EmA + biopsia con atrofia) 7% 4.8 % 3.5 % 1.8 % 6% > 40 % 72 % . Por otra parte, otros anticuerpos además del anticuerpo antiendomisio pueden ser glutendependientes. Se ha demostrado que los pacientes con enfermedad celíaca sin dieta libre de gluten tienen mayor prevalencia de anticuerpos antitiroideos, antifosfolipídicos y anticuerpos asociados a diabetes (ICA, LAII e IAA), con desaparición de los mismos luego de dieta libre de gluten. Estos hallazgos han permitido plantear la hipótesis que la dieta libre en gluten podría tener un efecto protector para evitar el desarrollo de otras enfermedades autoinmunes, incorporándose el término de inmunidad gluten–dependiente (12) Otras Asociaciones: deficiencia selectiva inmunogloblina A, nefropatía por inmunoglobulina A, artritis reumatoidea y síndrome de Down. Existen otras menos comunes como: enfermedad cardiaca congénita, pericarditis recurrente, sarcoidosis, fibrosis quística, alveolitis fibrosante, hemosiderosis pulmonar, enfermedad inflamatoria intestinal, enfermedad de Addison, lupus eritematoso sistémico, vasculitis, polimiositis, miastenia gravis y esquizofrenia.(3) Hallazgos Físicos Al igual que la sintomatología varía de un paciente a otro, puede haber palidez por la anemia, emaciación, pérdida de masa muscular y pliegues cutáneos laxos.. La piel puede estar seca con turgor y elasticidad disminuidos por deshidratación, edemas principalmente en miembros inferiores por hipoproteinemia, causada por la síntesis deficiente de albúmina o la pérdida entérica de proteínas séricas. Puede haber hiperpigmentación cutánea en casos severos y dedos en palillo de tambor. Otros hallazgos son las equimosis espontáneas relacionadas con la hipoprotrombinemia por deficiencia de vitamina K, hiperqueratosis folicular por deficiencia de vitamina A y la coexistencia de dermatitis herpetiforme. El examen bucal puede revelar queilosis y glositis y defectos en el esmalte dental. -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 8 -----------------------------------------------------------------------------------------------------------A la inspección, el abdomen se muestra distendido, indoloro a la palpación pero de consistencia pastosa debido a la distensión de las asas del intestino por líquido y gas, timpanismo generalizado, la hepatomegalia es rara. Puede detectarse ocasionalmente ascitis por hipoproteinemia significativa. En los miembros inferiores y superiores se puede evidenciar pérdida de diversas modalidades sensoriales. Si la neuropatía es severa, los reflejos profundos están disminuidos o ausentes. Se puede provocar el signo de Chvostek o de Trousseau por pérdida severa de calcio o magnesio, puede haber dolor a la palpación ósea como consecuencia de osteopenia y en caso de aplastamiento de vértebras.(4) La hipotensión puede ser por depleción de líquidos y pérdida de electrolitos DIAGNOSTICO Análisis bioquímicos: Si la diarrea es severa los niveles de sodio, potasio, cloro y bicarbonato suelen estar disminuídos, en ocasiones el paciente puede presentarse con acidosis metabólica por pérdida de bicarbonato por las heces. El fósforo sérico a veces es menor a lo esperado, la fosfatasa alcalina está aumentada en pacientes con osteopenia.(3) La albúmina sérica y en menor medida las globulinas pueden estar bajas debido a una filtración excesiva de las mismas hacia la luz intestinal. En pacientes con esteatorrea los niveles séricos de colesterol suelen estar disminuidas.(4) La hipertransaminasemia persistente es frecuente.(3) Análisis Hematológico: La anemia presente en la enfermedad celíaca puede ser secundaria a la deficiencia de hierro y folato, o consecutiva a enteropatía del intestino delgado proximal o menos frecuentemente a deficiencia de vitamina B12 por afección del ileón, por lo que los eritrocitos pueden variar de microcíticos o macrocíticos. La leucopenia y trombocitopenia son raras, pero pueden deberse a una deficiencia severa de folato o vitamina B12.(4) Hallazgos de hipoesplenismo como los cuerpos de Howell – Jolly y trombocitosis, son frecuentemente observados en personas añosas con enfermedad celíaca.(13) El tiempo de protrombina puede estar prolongado por la malabsorción de la vitamina K por lo que su administración lo corregirá, siempre y cuando no haya enfermedad hepática.(13) Examen de materia fecal: Para comprobar la esteatorrea se puede realizar un análisis cuantitativo de grasa en una muestra de material fecal de 72 hs. siempre y cuando el paciente ingiera una dieta rica en grasas (por lo menos 100 grs. por día). Con esta dieta los pacientes normales eliminan menos de 7 grs. de grasa por día (coeficiente de absorción menor a 93 %).(13) La evaluación microscópica del contenido graso de materia fecal teñida con Sudán III o IV muestra glóbulos de grasa neutra de color naranja (triglicéridos). Si la hidrólisis detecta ácidos grasos libres sugiere enfermedad del intestino delgado.(4) Hay un 25 % de falsos negativos cuando la esteotorrea es leve, o sea menor a 10 grs. / 24 hs., la tasa de falsos positivos es del 15 %.(13) Pruebas de tolerancia oral: Las más útiles son las de tolerancia a la xylosa (absorbida preferentemente en intestino delgado proximal) y a la lactosa.(13) La excreción urinaria de xylosa diferencia entre malabsorción por una enfermedad del intestino delgado y la debida a una insuficiencia exócrina pancreática. Luego de la administración oral de 25 grs. de D-xylosa, la excreción urinaria de 5 grs. o más en 5 hs. es normal. La absorción y -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 9 -----------------------------------------------------------------------------------------------------------excreción de xylosa están disminuídas (menor a 5 grs.) en pacientes con daño en intestino delgado proximal y en el crecimiento bacteriano excesivo en intestino delgado (las bacterias catabolizan la xylosa). En caso de una insuficiencia pancreática, la excreción de xylosa es normal. Las alteración del vaciamiento gástrico, función renal (aunque quizás no tenga una lesión renal obvia, pero si una depuración de creatinina baja), ascitis y metabolismo de la sustancia de prueba pueden alterar los resultados.(13) La concentración sanguínea pico de xylosa, después de la primera hora de ingerirla, está disminuída ya que una concentración mayor o igual a 30 mg. /100 ml indican una absorción normal.(13) En pacientes celìacos la lesión de las células absorbentes también da como resultado una deficiencia secundaria de lactosa, por eso los nivel de glucosa en sangre pueden no aumentar normalmente después de la ingesta de lactosa. La prueba del aliento de lactosa-H2, también llamada del aire espirado, sustituyó a la de la intolerancia a la lactosa por su mayor sensibilidad y especificidad. Se administra lactosa por vía oral (1 gr./Kg.) y un aumento de H2. en el aliento mayor de 20 ppm sobre H2 basal, indica malabsorción de lactosa (liberación de H2 de la lactosa no absorbida por metabolismo bacteriano).(13) Existen otras pruebas menos utilizadas, como: determinación de la excreción urinaria luego de la ingestión oral de dosis de prueba de ácido etilenodiaminotetracético marcado con Cr51, polietilenglicol 400 o la relación entre la excreción de un monosacárido como la L- ramnosa y la excreción de un disacárido como la lactosa.(4) Pruebas Serológicas: La alta sensibilidad y especificidad de los marcadores serológicos facilita el diagnóstico de enfermedad celíaca. Las pruebas serológicas son utilizadas cuando se sospecha la enfermedad, monitoreo de la adherencia, respuesta a una dieta libre de gluten y en pacientes con manifestaciones extra intestinales atípicas.(3) El anticuerpo inmunoglobulina A antiendomisio es usualmente detectado por inmunofluorescencia indirecta con el uso de partes de cordón umbilical humano o partes de músculo liso esofágico de mono. Se ha publicado una sensibilidad del 85 % – 98 % y una especificidad del 97 % – 100 %.(3) La transglutaminasa de tejido es un autoantígeno reconocido por el anticuerpo antiendomisio. La enzima de inmunoglobulina A se realiza por ensayo de inmunoabsorbencia usando transglutaminasa de tejido de conejillo de Indias, el cual es más barato, fácil de realizar y más sensible, pero menos específica que el anticuerpo antiendomisio.(3) Los falsos negativos de los anticuerpos antiendomisio y de transglutaminas de tejido pueden ocurrir en una enteropatía leve, en niños menores de 2 años de edad y especialmente en deficiencia de Inmunoglobulina A. (3) La sensibilidad de la inmunoglobulina A antigliadina es del 75 % - 90 % con una especificidad del 82 % al 95 %. Muchas personas normales, así como pacientes con inflamación gastrointestinal por otras causas presentan una prueba positiva para anticuerpo antigliadina, por lo que el valor predictivo positivo del anticuerpo antigliadina en la población general es pobre. (3) Las pruebas de inmunoglobulina A antigliadina son usadas para el monitoreo del cumplimiento dietético junto a la Inmunoglobulina A antiendomisio. El anticuerpo Inmunoglobulina A antiendomisio generalmente comienza a ser indetectable entre los 3 y 6 meses, luego de comenzar la dieta libre en gluten.(3) Cuando la concentración de alaninaminotransferasa retorna a lo normal, ninguno de los anticuerpos deberían detectarse, mientras que ambos, anticuerpos y transaminasas están persistentemente elevados en pacientes con un pobre cumplimiento.(9) Los resultados positivos de estas pruebas pueden inducir al médico a realizar una biopsia de mucosa intestinal en pacientes en que el grado de sospecha de una esprue celíaca no es elevado.(4) -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 10 -----------------------------------------------------------------------------------------------------------Sin embargo, la determinación de anticuerpos séricos no debe reemplazar a la biopsia de la mucosa intestinal como procedimiento diagnóstico clave antes de someter a los pacientes en quienes se sospecha enfermedad celíaca a una vida sin gluten.(4) Se ha demostrado la posibilidad de detectar anticuerpo antitransglutaminasa tisular en saliva por medio de una fase fluida de radioinmunoensayo (RIA) para el estudio de enfermedad celíaca. La sensibilidad y especificidad de este método son más altas en comparación con el anticuerpo antiendomisio sérico. No hay aspectos técnicos que limiten la aplicabilidad de este nuevo método. Esta técnica tiene dos consideraciones: - La saliva humana es una muestra que tiene un gran potencial para el screening y el monitoreo de la enfermedad. - Puede ser obtenido fácilmente y repetidamente por técnicas no invasivas..(14) La inmunoglobulina A antigliadina detectada en saliva tiene generalmente baja sensibilidad. La inmunoglobulina A antiendomisio salival que no se produce localmente y tiene una baja sensibilidad, por lo que la saliva no se debe considerar como herramienta para tal finalidad.(14) Estudios Radiográficos: La radiografía con bario evidencia dilatación del intestino delgado y reemplazo del patrón mucoso normal por un marcado engrosamiento de los pliegues mucosos.(3) Si la enfermedad es leve o moderada el patrón mucoso está distorsionado en el intestino delgado proximal; si la enfermedad es severa, la distorsión se encuentra en el intestino delgado proximal hasta el ileon. La excesiva secreción de líquidos junto con la absorción defectuosa en el intestino delgado proximal, causa dilución del bario ingerido y da como resultado una disminución del contraste del bario en el intestino (patrón en “nevado”). (4) (Fotos N0 4-5-6) -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 11 ------------------------------------------------------------------------------------------------------------ Foto N 4 Sonda para enteroclisis Foto N 5: Ausencia de pliegues en yeyuno Foto N 6: Yeyunalización del ileon Las radiografías óseas son útiles para revelar desmineralización ósea difusa. En forma ocasional se ven efectos secundarios de una osteopenia que incluyen las fracturas por compresión de las vértebras y pseudofracturas (líneas de Milkman).(4) Las imágenes de TAC abdominal o resonancia magnética (IRM) pueden sugerir el diagnóstico de enfermedad celíaca por la detección de hipoesplenismo, ascitis o linfadenopatía, incluyendo cavitaciones mesentéricas de nódulos linfoides, mientras que el adelgazamiento del intestino delgado puede sugerir la presencia de linfomas.(3) Endoscopia digestiva alta En el pasado las muestras de biopsias del intestino fueron tradicionalmente obtenidas usando cápsulas de succión. Sin embargo, en las últimas décadas la biopsia del duodeno distal es útil en el diagnóstico de enfermedades difusas del intestino delgado, por lo tanto, la endoscopia digestiva alta ha comenzado a ser un procedimiento común en pacientes con enfermedad celíaca. -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 12 -----------------------------------------------------------------------------------------------------------Se han descripto varios marcadores endoscópicos para la enfermedad celíaca. Los hallazgos incluyen reducción o ausencia de los pliegues de Kerkring que fue descripto por Brocchi y col. vasos visibles, la apariencia en mosaico de la mucosa y el signo del peine, reportada por Jabbari y col. La visualización endoscópica de por lo menos un marcador, tiene una sensibilidad del 87,50% al 100% y una especificidad del 92-100%, con un valor predictivo positivo del 84-100 % y un valor predictivo negativo del 96 - 99 %.(15) La reducción o la disminución en el número de pliegues de Kerkring fue el signo endoscópico más sensible y específico indicativo de enfermedad celíaca en un estudio realizado por Mauriño y col. Otros estudios, parecen atribuirle una óptima sensibilidad para predecir atrofia vellositaria a los hallazgos de la mucosa en mosaico y al signo del peine.(15) (Fig N0 7-8-9) Fig 7: Mucosa en mosaico los pliegues Fig 8: Signo del peine Fig 9: Disminución de El valor de los marcadores endoscópicos en el diagnóstico de la enfermedad celíaca ha sido cuestionado recientemente. En una gran muestra de pacientes (n=1200) con dispepsia sintomática, la sensibilidad de los marcadores endoscópicos para la búsqueda de enfermedad celíaca fue del 50% y el valor predictivo positivo del 60%.(16) La discrepancia de los resultados obtenidos a través de diferentes estudios, puede explicarse por diferencias en la proporción de casos con enfermedad severa y leves. Estudios de presentaciones individuales con sintomatología típica de enfermedad celíaca pueden evidenciar el alto grado de detección en comparación con grupos no selectos sin hallazgos clínicos sugestivos de enfermedad celíaca. Otros investigadores, sin embargo argumentan que lo anterior no puede ser razón de baja especificidad. El diagnóstico de falsos negativos, también puede ocurrir en pacientes celíacos tratados con atrofia vellositaria leve. La agudeza de las evaluaciones endoscópicas depende de la experiencia del endoscopista.(16) La tinción con azul de metileno al 1 % es útil para una mejor definición del patrón en mosaico y para el signo del peine, pero no provee una información diagnóstica adicional para valorar la reducción en el número de pliegues duodenales.(15) -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 13 -----------------------------------------------------------------------------------------------------------La magnificación endoscópica junto a la tinción, tienen una alta sensibilidad (94%) y especificidad (88%) en la identificación de pacientes con atrofia vellositaria, esta técnica es más exacta (91%) para identificar pacientes con atrofia vellositaria parcial en comparación con la endoscopía estandar (9%).(1) Recientemente se ha incorporado un nuevo método de estudio, la cápsula endoscópica que puede facilitar el diagnóstico de la enfermedad celíaca con una alta magnificación, brinda detalles en la visión de la mucosa y tiene la habilidad de scannear la totalidad del intestino delgado. Es indolora, segura y bien tolerada por el paciente.(1) El examen histológico de la muestra de biopsia del intestino delgado es el “patrón de oro”, para el diagnóstico de la enfermedad celíaca.(3) Las piezas deben obtenerse del duodeno distal (segunda o tercera porción), para evitar la distorsión producida por las glándulas de Brunner o por duodenitis péptica, lo que puede confundir la interpretación de la arquitectura de la mucosa. La ausencia , o aplanamiento vellositario, si están presentes, deben orientar al posible diagnóstico de enfermedad celíaca, aunque no son específicas de la misma.(3,4) La lesión clásica en pacientes con enfermedad celíaca no tratada, se caracteriza histológicamente por cambios de la arquitectura de la mucosa, con ausencia vellositaria, criptas hiperplásicas y un número elevado de linfocitos intraepiteliales en la lámina propia. La severidad y la extensión de las anormalidades histológicas en la enfermedad celíaca varían extensivamente.(3) DIAGNOSTICO DIFERENCIAL Alteraciones de la digestión: Insuficiencia pancreática exócrina: produce una esteatorrea mayor a 50 gr. grasa / día. Estados posgastrectomía: tipo Billroth I y II, vagotomía en antrectomía, vagotomía y piloroplastia. La patogenia es multifactorial, pérdida de la función de reservorio con vaciamiento rápido, asincronía poscibal, como sucede en procedimientos tipo Billroth II donde el alimento puede llegar al yeyuno antes que las sales biliares y las enzimas pancreáticas y por la presencia de estasis que origina crecimiento bacteriano excesivo en el intestino delgado. La esteatorrea suele ser leve, menos de 10 gr. grasa / día.(13) Gastrinoma: como en el síndrome de Zolinger Ellison. La hipersecreción extrema de ácido, inactiva de manera irreversible la lipasa y origina insuficiencia pancreática secundaria. Este ambiente ácido precipita las sales biliares y puede causar alteraciones en el intestino delgado.(13) Concentración reducida de sales biliares Hepatopatías: La esteatorrea suele ser leve en enfermedades hepáticas agudas o crónicas (cirrosis biliar primaria), tal vez por deterioro de la síntesis y excreción de sales biliares conjugadas.(13) Crecimiento bacteriano excesivo: en el intestino delgado acompañado de malabsorción de nutrientes se denomina síndrome de estasis o de asa ciega. La flora del intestino delgado se asemeja a la del colon y el crecimiento excesivo compite con el huésped por los nutrientes ingeridos.(13) Enfermedad o resección ileal: hay una interrupción de la circulación enterohepática de ácidos biliares conjugados, dando por resultado una disminución del fondo común de ácidos biliares y esteatorrea. El grado de ésta es proporcional a la cantidad de intestino enfermo o resecado. Si se dañan o resecan menos de 100 cm. de intestino proximal a la válvula ileocecal provocando -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 14 -----------------------------------------------------------------------------------------------------------diarrea colerética, la esteatorrea es leve; si es mayor a 100 cm. la esteatorrea suele ser mayor.(13) Anormalidades de la Mucosa Intestinal: Deficiencia de disacaridasas o malabsorción de monosacáridos: La deficiencia de disacaridasa más común es la de la lactasa. La malabsorción de monosacáridos es más rara y es de glucosagalactosa.(13) Enfermedad de Crohn: la malabsorción suele deberse a disminución de la superficie de absorción por enfermedad activa o resección quirúrgica, agotamiento de sales biliares por enfermedad ileal y crecimiento bacteriano excesivo secundario a dilatación del intestino y resección de la válvula ileocecal.(13) Enteritis eosinofílica: se caracteriza por eosinofilia en sangre periférica e infiltración del tubo digestivo. Se observan tres patrones: invasión de las capas musculares del estómago e intestino delgado que origina obstrucción, inclusión de la mucosa del intestino delgado que causa obstrucción y afección de la subserosa que produce ascitis. La mayoría de los pacientes no tienen alergia o sensibilidad alimentaría. Enteritis por radiación: Produce malabsorción por daño extenso de la mucosa, linfagiectacia por obstrucción y crecimiento bacteriano excesivo. Es posible que la malabsorción se manifieste poco después de la exposición o años más tarde. Superficie de absorción inadecuada. Síndrome de Intestino Corto: Por resección extensa del intestino delgado. Es notable la capacidad del intestino restante para adaptarse a un aumento de la absorción de nutrientes por hipertrofia de las vellosidades residuales. Los pacientes evolucionan muy bien, a pesar de la resección, siempre y cuando queden de 90 a 100 cm. de duodeno, yeyuno e ileon terminal (válvula ileocecal intacta). Derivación yeyunoileal: Algunos pacientes con obesidad mórbida fueron sometidos a procedimientos quirúrgicos como anastomosis de 35 cm. de yeyuno proximal a 10 cm. de ileon terminal, originando malabsorción, motivo por el cual no se utiliza esta técnica. Infección: Esprue tropical: ocurre en regiones tropicales ( Lejano Oriente, India y Caribe), se caracteriza por un crecimiento excesivo de coliformes en yeyuno, los cuales elaboran una enterotoxina que origina secreción de líquidos. Esta enfermedad, no es un crecimiento bacteriano excesivo verdadero. La biopsia no muestra atrofia vellositaria total sino acortamiento o engrosamiento de las mismas con infiltración celular de la lámina propia. Enfermedad de Whipple: por lo general son varones con esteatorrea, pérdida de peso, dolor abdominal, fiebre, artritis no deformante. Puede haber una enteropatía perdedora de proteínas por obstrucción linfática. La biopsia es diagnóstica con infiltración intensa de la mucosa y ganglios linfáticos del intestino delgado, por macrófagos positivos para la tinción de Schiff (PAS). Obstrucción linfática: Linfoma intestinal: hay malabsorción por invasión de la mucosa, obstrucción linfática y crecimiento bacteriano excesivo secundario a dilatación del intestino con ectasia. Los principales síntomas son fiebre, dolor abdominal y esteatorrea. La biopsia del intestino delgado puede parecerse a una enfermedad celíaca, pero la afección no responde a una dieta libre de gluten. -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 15 -----------------------------------------------------------------------------------------------------------Linfangiectasia: la linfangiectasia primaria o congénita se caracteriza por esteatorrea leve, enteropatía perdedora de proteínas, edema y conductos linfáticos dilatados anormales en la biopsia de intestino delgado. Trastorno Cardiovasculares: Insuficiencia cardiaca congestiva, pericarditis constrictiva, insuficiencia vascular mesentérica, pueden producir disminución del riego sanguíneo, originando esteatorrea. Malabsorción inexplicable: Diabetes, hipertiroidismo, hipotiroidismo, síndrome carcinoide, SIDA, infecciones entéricas (Giardia lamblia, Cryptosporidium, Mycobacterium ovium, Isospara belli), afección del intestino delgado por sarcoma de Kaposi.(3,4,13) TRATAMIENTO DIETA: La eliminación del gluten tóxico de la dieta es esencial para el tratamiento de los pacientes con enfermedad celíaca. Aunque la eliminación completa de la dieta de todos los granos de cereales que contienen gluten tóxico (trigo, cebada y centeno) parece bastante simple, para los pacientes es muy difícil de lograr y mantener principalmente en niños y adolescentes, por lo tanto no se la debe indicar sino se tiene un diagnóstico de enfermedad celíaca firmemente establecido. Los lineamientos iniciales para comenzar el tratamiento dietario son: Al principio evitar el gluten de la avena. Utilizar sólo harinas, comidas o almidones de arroz, maíz, trigo sarraceno, semillas de soja o tapioca. Una vez establecido el diagnóstico, puede probarse el almidón de trigo, del cual se habrá eliminado el gluten. Leer todas las etiquetas y estudiar los ingredientes de los alimentos procesados. Estar alerta al gluten de los aditivos, emulsionadores o estabilizadores de los alimentos. Inicialmente limitar la leche y los productos lácteos. Las fuentes obvias de gluten tóxico, como los alimentos horneados, los cereales secos que contienen trigo o los tallarines, son fáciles de evitar. El trigo se utiliza con frecuencia para diluir alimentos procesados, y en muchas marcas de helado comercialmente disponibles, en aderezos de ensaladas alimentos enlatados, entre ellos vegetales y sopas. De hecho algunas marcas de café instantáneo, ketchup, mostaza y la mayoría de las golosinas. Por lo tanto la institución de una dieta de este tipo requiere una instrucción extensa y repetida del paciente por parte del médico y el dietista. Además de no contener gluten, la dieta debe equilibrarse con cantidades normales de grasa, hidratos de carbono y proteínas.(4) El consumo de moderadas cantidades de avena (50 –70 grs./día) durante 6 a 12 meses no es tóxico. Los pacientes que la consumieron no mostraron diferencias en cuanto a los síntomas, estado nutricional o la histología de la mucosa duodenal de aquellos pacientes que mantuvieron una dieta libre de gluten, rígidamente limitada de avena. Sin embargo, los productos de avena pueden estar contaminados por pequeñas cantidades de trigo, por lo tanto, en los pacientes recientemente diagnosticados de enfermedad celíaca se recomienda que la eviten hasta que se -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 16 -----------------------------------------------------------------------------------------------------------logre la remisión. Luego los pacientes pueden comenzar con una ingesta de hasta 55 grs. de avena por día. Además de la dieta libre en gluten, todos los pacientes con diagnóstico reciente de enfermedad celíaca y con evidencias clínicas de malabsorción deberán recibir inicialmente preparados multivitamínicos, suplementos para la deficiencia de hierro y folato. Los pacientes con esteatorrea, hipocalcemia o enfermedad ósea osteopénica deberán recibir calcio vía oral y suplementos de vitamina D. Aquéllos con hipoesplenismo deberían recibir profilaxis antibiótica antes de someterse a procedimientos invasivos y también se beneficiarán con la vacunación para pneumococo. Ocasionalmente, la terapia corticoidea endovenosa, se requiere para pacientes críticamente enfermos con crisis celíaca aguda, manifestada por severa diarrea, deshidratación, pérdida de peso, acidosis, hipocalcemia e hipoproteinemia, afección conocida como shock por gliadina.(3,4,5) RESPUESTA A LA DIETA Aproximadamente el 70 % de los pacientes tiene mejoría de los síntomas dentro de las 2 semanas luego de haber comenzando la dieta libre en gluten. Si un paciente no mejora en las semanas posteriores de comenzado la dieta, la causa más común es la remoción incompleta del gluten en la dieta.(3) La velocidad y el grado de mejoramiento histológico son impredecibles. A pesar del retorno normal de los hallazgos histológicos común en niños, la mitad de los adultos tienen sólo una resolución parcial en la biopsia. Los síntomas persistentes pueden ser por enfermedades coexistentes como: síndrome de intestino irritable, intolerancia a la lactosa, colitis microscópica o insuficiencia pancreática.(3,17) Un estudio demostró que a pesar de la adherencia a una dieta libre de gluten se hallan anormalidades endoscópicas e histológicas en el duodeno de la mayoría de los pacientes con enfermedad celíaca.No está claro por qué la histología no retorna a lo normal en algunos pacientes. A pesar de la presencia de atrofia vellositaria, la mayoría de los pacientes tienen serología negativa para anticuerpos antiendomisio e inmunoglobulina A antigliadina. El anticuerpo antiendomisio usualmente desaparece en respuesta a una dieta libre de gluten dentro de los 6 y 12 meses. Sin embargo, le puede tomar hasta 31 meses dependiendo de cuán alta haya sido la titulación. La positividad persistente se considera como una continuidad en la ingestión de gluten. Sin embargo la serología negativa no excluye la ingestión de gluten. En conclusión, la desaparición del anticuerpo antiendomisio no es indicativa de recuperación histológica en pacientes con enfermedad celíaca y el diagnóstico de ésta requiere de una biopsia anormal del intestino delgado junto con un mejoramiento clínico en respuesta a una dieta libre de gluten.(4,17) REPETICIÓN DE LA BIOPSIA La utilidad de las pruebas serológicas ha reducido la necesidad de una segunda biopsia. Esta segunda biopsia se puede reservar para determinados pacientes, quienes tienen una respuesta clínica insatisfactoria o no esperada frente a una dieta estricta. En la práctica diaria el desafío de una dieta libre de gluten es reservada para unos pocos pacientes en quienes el diagnóstico permanece en duda luego de un periodo de restricción al gluten, por ejemplo pacientes que comienzan con una dieta empírica libre de gluten sin documentación de la lesión intestinal característica o presencia de anticuerpo antiendomisio o de tranglutaminasa tisular. El desafío del gluten, debería ser considerado si el diagnóstico de enfermedad celíaca fue hecho durante la niñez en base a la biopsia del intestino delgado sin que el anticuerpo antiendomisio fuera -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 17 -----------------------------------------------------------------------------------------------------------positivo ya que un número de enteropatías en los niños puede imitar una enfermedad celíaca histológicamente.(3) COMPLICACIONES Existe un riesgo alto de enfermedades malignas en pacientes con enfermedad celíaca, en comparación con la población general.(4) Adenocarcinoma de Intestino delgado: Se ha sugerido que el adenocarcinoma del intestino delgado surge a través de la secuencia adenoma-carcinoma, ya que se han publicado adenoma de intestino delgado en la enfermedad celíaca. El riesgo parece ser mayor en pacientes con enfermedad celíaca de larga data. Se han descrito pacientes en que el diagnóstico de enfermedad celíaca se realizó en el momento de la resección del adenocarcinoma, el examen histológico de la pieza, evidenció atrofia vellositaria en la mucosa adyacente a la neoplasia. La mayoría de las neoplasias ocurren más distalmente en el intestino.(18) Enteropatía asociada a linfoma de células T: En algunos pacientes con un linfoma manifiesto la histología de la mucosa adyacente al linfoma y lejos de él, es indiferenciable de la enfermedad celíaca no tratada, pero no responde a la eliminación del gluten de la dieta. Es discutible si estos pacientes tienen una enfermedad celíaca latente que se torna evidente luego del desarrollo del linfoma, o si el linfoma intestinal primario induce una enteropatía refractaria indiferenciable por medio de criterios histológicos de la enfermedad celíaca. Enfermedad celíaca refractaria: También llamada esprue no clasificada. Estos pacientes responden a la eliminación de gluten de la dieta en una fase temprana de la enfermedad, pero después de un período de remisión experimentan una recaída a pesar de continuar cumpliendo con la dieta. En algunos casos, esta enfermedad puede responder a la terapia inmunosupresora. La enfermedad celíaca refractaria es un diagnóstico de exclusión, una vez que se haya eliminado otras causas de una enteropatía semejante a la enfermedad celíaca. Presentación y diagnóstico: la enfermedad celíaca refractaria se presenta de una o dos maneras. En la mayoría de los casos, hay una resistencia primaria a la dieta libre de gluten, llamada enfermedad celíaca refractaria primaria. Un pequeño grupo con enfermedad celíaca que responde inicialmente a la dieta libre de gluten, pero recae reiteradamente, se la designa enfermedad celiaca refractaria secundaria. Se ha sugerido que el periodo de un año libre de gluten es un periodo arbitrario razonable para esperar la resolución histológica antes de hacer el diagnóstico de enfermedad celíaca refractaria. Los no respondedores a una dieta libre de gluten se pueden clasificar en: los clínicamente no respondedores y los histológicamente no respondedores. El primer grupo se manifiesta por persistencia de los síntomas. El segundo, por persistencia de hallazgos histológicos. No se conoce la prevalencia de inmunoglobulina A antigliadina y del anticuerpo antiendomisio en pacientes con enfermedad celíaca refractaria debida a la falta de grandes series de pacientes. En una revisión de casos publicados, el 55% tuvo inmunoglobulina A antigliadina positivo, y el 57% anticuerpo antiendomisio positivo. Tratamiento: -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 18 -----------------------------------------------------------------------------------------------------------Dieta y nutrición: el primer paso es excluir la posibilidad de ingestión inadvertida de gluten debido a que muchos de estos pacientes tienen una malabsorción severa. La estimación del estado nutricional es imperativo, se debe realizar la medición del índice de masa corporal, proteínas totales, albúmina, concentración de hemoglobina, vitamina B 12, ferritina, calcio, magnesio y oligoelementos como cobre y zinc. Los pacientes con pérdida de peso severa, pérdida de masa muscular, deficiencia nutricional múltiple y edema secundario a hipoproteinemia, pueden requerir una nutrición parenteral. Inmunosupresión: los corticoides son drogas de primera línea en el tratamiento de la enfermedad celíaca refractaria con grados variables de mejoría histológica. Se ha sugerido su uso en tres situaciones: incapacidad o rehuso a la tolerancia de una dieta libre en gluten, a pesar del deterioro de la salud; yeyunitis ulcerativa complicada; y deterioro de la salud a pesar del la adherencia a la dieta libre de gluten y de lactosa. La azatriopina, ha sido reportada como exitosa en algunos pacientes con enfermedad celíaca refractaria, pero no en otros. La respuesta a la terapia inmunosupresora, sugiere que es un daño intestinal mediado inmunológicamente y que no se diferencia entre enfermedad celíaca y enteropatía autoinmune. La ciclosporina también ha sido utilizada exitosamente en casos severos. Se debería utilizar en pacientes que no responden a los corticoides. La terapia inmunosupresora puede teóricamente aumentar el riesgo de desarrollo franco de linfoma, facilitando aún más el curso agresivo de la enteropatía asociada a linfoma T o enmascarar sus signos y síntomas. Yeyunoileítis Ulcerosa: Representa una complicación infrecuente pero a menudo fatal. Junto con el desarrollo de linfoma o adenocarcinoma, este tipo de ulceración intestinal es la causa principal de muerte. Estos pacientes generalmente tienen de 60 – 70 años en el momento del diagnóstico, sus características patológicas son inespecíficas. La mucosa a menudo muestra atrofia parcial de las vellosidades, pero puede ser normal. Si bien éstas lesiones pueden ser histológicamente “benignas” en el transcurso de uno o dos años, se ha detectado la presencia de linfoma en éstos pacientes. Esprue colagenosa: Estos pacientes pueden presentarse inicialmente con síntomas y hallazgos biópsicos compatibles con una enfermedad celíaca. Sin embargo, no responden a la eliminación del gluten de la dieta y con el tiempo desarrollan extensos depósitos de colágeno en la lámina propia debajo del epitelio de absorción. El pronóstico es malo. Otras complicaciones son el carcinoma orofaringeo y esofágico.(4) PRONOSTICO Si no se reconoce la enfermedad y se la trata de forma apropiada, los pacientes pueden desarrollar desnutrición, debilidad marcada y morir por complicaciones tales como una hemorragia o infección intercurrente. El pronóstico de los pacientes con enfermedad celíaca correctamente diagnosticada y tratada es excelente y la mayoría de los pacientes fallecen por otras causas que parecen no estar relacionadas con la enfermedad. CALIDAD DE VIDA -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 19 -----------------------------------------------------------------------------------------------------------El concepto de calidad de vida es amplio. Ha sido definida por la Organización Mundial de la Salud como “la percepción del individuo sobre su posición en la vida en el contexto de la cultura y sistema de valores en el cual ellos viven, y en relación a sus objetivos, expectativas, estándares e intereses”. Es desde este marco conceptual que se evalúan los aspectos clínicos, respuesta al tratamiento y aspectos psicológicos involucrados en la enfermedad celíaca. Para la evaluación de la calidad de vida se utilizan cuestionarios validados previamente como el SF-36, la escala de valoración de síntomas gastrointestinales y cuestionarios de valoración de estado psicológico. El cuestionario SF-36 incluye ocho variables desarrolladas en múltiples puntos: 10 items de la funcionalidad física, 2 items de la función social, 4 items de las limitaciones por trastornos físicos, 3 items de las limitaciones por trastornos emocionales, 5 items de salud mental, 4 items de energía y vitalidad, 2 items de percepción del dolor y 5 items de percepción general del estado de salud. La escala de valoración de síntomas gastrointestinales, se constituye de un cuestionario de 15 preguntas sobre molestias percibidas por los pacientes debido a síntomas gastrointestinales como dolor abdominal, ardor, reflujo, náuseas, distensión, eructos, meteorismo, constipación, diarrea, urgencia defecatoria y sensación de evacuación incompleta. Para cada síntoma el paciente deberá calificar sus molestias según 7 categorías establecidas y elegir la que mejor represente su grado de molestia. Finalmente el inventario de depresión de Beck, proveerá la información necesaria para evaluar este frecuente trastorno. Se debe tener en cuenta para la comprensión total acerca de la calidad de vida, otras preguntas que no entran en la escala de valores del test. Las mismas deben versar sobre los niveles socio – económicos (mediante una historia clínica social que incluye datos personales, laborales, de la vivienda y de los convivientes), así como traumas psico-sociales, lo que nos permite ver las diferencias entre la calidad de vida en los distintos estratos sociales y además la posibilidad de la adhesión a la dieta, en relación con la capacidad económica de los distintos grupos y enfermedades crónicas. La respuesta adecuada de cuánto se afecta la calidad de vida en el celíaco en sus diferentes formas de presentación o de que manera se modifica iniciada la dieta libre de gluten necesita de un mejor análisis global y del tiempo que nos permita conocer la historia natural de las formas oligosintomáticas y asintomáticas.(19) BIBLIOGRAFÍA Petroniene R, Dubcenco E, Baker J.P, Warren R.E, Streuther C.J, Gardiner G.W, Jeejeebhoy K.N. Clínica Endoscópica Gastrointestinal en Norte América. Ryan B.M, Kelleher D. Enfermedad celíaca refractaria. Gastroenterology 2000; 119:243-251. Farrell R.J, Kelly C.P. NEJM vol 346 nº3. Enero 17,2002,180-187. Sleisenger M.H, Feldmans M, Scharschmidt B.F. Enfermedades Gastrointestinales y Hepáticas. Ed 6º. Montevideo, Uruguay. Editorial Panamericana. Año 2002, vol 2, 1671-1689. Lundin K.E.A, Nilsen E.M, Scott H.G, Löberg E.M, Gjöen A, Bratlie J, Skar V, Mendez E, Lövik A, Kett K. La avena induce a la atrofia vellositaria en la enfermedad celíaca. Gut vol 52. Nov 2003, 1649-1652. Tursi A, Brandimarte G. La respuesta sintomática e histológica de la dieta libre de gluten en pacientes con enteropatía borderline. J. Clin. Gastroenterology 2003:36(1):13-17. Chin R.L, Sander H.W, Brannagan T.H, Green P.H.R, Hays A.P, Alaedini A, Latov N. Neuropatía celíaca. Neurology 2003;60:1581-1585. Kaukinen K, Halme L, Collin P, Färkkila M, Mäki M, Vehmanen P, Partanen J, Höckerstedt K. Enfermedad celíaca en pacientes con enfermedad hepática severa: la dieta libre de gluten puede reveer la falla hepática. Gastroenterology 2002; 122:881-888. Votta V, De Franceschi L, Lari F, Molinaro N, Zoli M, Bianchi F.B. Enfermedad celíaca e hipertransaminasemia criptogénica. Lancet vol 352. Julio 4, 1998:26-29. -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 20 -----------------------------------------------------------------------------------------------------------Cuomo A, Romano A, Budillon G, Del Vecchio Blanco C, Nardone G. Esogagitis por reflujo en la enfermedad celíaca del adulto: efecto beneficioso de la dieta libre de gluten. Gut 2003; 52:514517. Holmes G.K, La búsqueda de enfermedad celíaca en diabéticos tipo I. Archives of Disease in Chilhood 2001; 18:169-177. Gomez J.C. Enfermedades autoinmunes. Efecto de la dieta libre de gluten. Sesión Plenaria del Congreso Argentino de Gastroenterología y Endoscopía Digestiva 2004. Wyngaarden J.B, Smith L.H, Bennett J.C. Cecil Tratado de Medicina Interna. 19ºed. México. Editorial Panamericana. 1994. Vol1 Bonamico M, Ferri M, Nenna R, Virrienti A, Di Mario V, Tiberti C. La detección en saliva humana del anticuerpo transglutaminasa tisular: un poderoso método para la búsqueda de enfermedad celíaca. J. Pediatr 2004; 144:632-636. Niveloni S, Fiorini A, Dezi R, Pedreira S, Smewol E, Vazquez H, Cabanett Boerr L.A, Valero J, Kogan Z, Mauriño E, Bai J.C. La utilidad de la videoduodenoscopía y la tinción como indicadores de atrofia de la mucosa en la enfermedad celíaca: estimación interobservador. Gastrointest Endosc 1998; 47:223-229. Bardella M.T, Minoli G, Radaelli F, Quatrini M, Bianchi P.A, Conte D. Revaluación de los marcadores endoscópicos duodenales en el diagnóstico de la enfermedad celíaca. Gastrointest Endosc 2000; 51,nº6. Lee S.K, Lo W, Memeo L, Rotterdam H, Green P.H.R. La histología duodenal en pacientes con enfermedad celíaca luego del tratamiento con dieta libre de gluten. Gastrointest Endosc 2003; 57:187-191. Rampertab S.D, Forde K.A, Green P.H.R. Neoplasias del intestino delgado en la enfermedad celíaca. Gut 2003; 52:1211-1214. Mauriño E. Calidad de vida en la enfermedad celíaca. Sesión Plenaria del Congreso Argentino de Gastroenterología y Endoscopía Digestiva 2004. -----------------------------------------------------------------------------------------------------------www.intramed.net Todos los derechos reservados | Copyright 1997-2004 Página 21