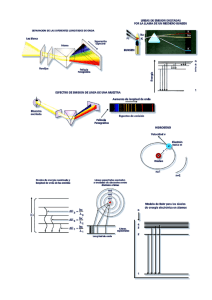
OM Enlazante Otra manera de describir el enlace covalente en términos de la Mecánica Cuántica consiste en la teoría de los orbitales moleculares (OM). Según esta teoría, cuando los átomos interaccionan sus orbitales atómicos pierden su individualidad y se transforman en orbitales moleculares que son orbitales que dejan de pertenecer a un solo núcleo para pasar a depender de dos o más núcleos. El tratamiento matemático que utiliza la Mecánica Cuántica para el cálculo de los orbitales moleculares es el método de la combinación lineal de orbitales atómicos, o método CLOA, que considera que el orbital molecular, y, es el resultado de la combinación lineal, es decir, una suma o una resta, de los dos orbitales atómicos implicados, F1 y F2. Cuando los orbitales atómicos se combinan para formar orbitales moleculares, el número de orbitales moleculares que resulta, siempre es igual al número de orbitales atómicos que se combinan. El caso más sencillo es el de la interacción de dos átomos, cada uno con un solo orbital atómico ocupado por un único electrón, es decir, el caso ya considerado desde el punto de vista de la teoría del enlace de valencia, de la formación de la molécula de hidrógeno. Se verá que la descripción del enlace H-H es la misma, o al menos muy similar a la descripción de los enlaces en moléculas más complejas. Cuando los dos orbitales 1s de dos átomos de hidrógeno interaccionan se transforman en dos orbitales moleculares, uno enlazante, que queda ocupado por los dos electrones, que dejan de pertenecer a un solo núcleo para pasar a pertenecer a los dos núcleos atómicos, y otro antienlazante, que quedará vacío. El orbital molecular enlazante es de menor energía que los orbitales atómicos originales y el antienlazante de mayor energía que éstos. Por ello al formarse el enlace y pasar los electrones al orbital molecular enlazante se desprende una determinada energía que es la que se ha definido en la teoría del enlace de valencia como energía de disociación de enlace. El orbital enlazante, yE, es el resultado de la suma, F1 + F2, de los dos orbitales atómicos: La formación del orbital antienlazante, yA, es el resultado de la otra combinación posible, la resta F1- F2, de los dos orbitales atómicos 1s de los átomos de hidrógeno: El diagrama de energías relativas de los orbitales moleculares de la molécula de hidrógeno muestra la situación inicial y final, así como la disminución de energía alcanzada por el sistema: Enlace sigma En química, el enlace sigma (enlace σ) es el tipo más fuerte de enlace químico covalente, incluso más fuerte que el enlace pi, el cual forma el doble enlace. La orbital sigma se define de forma más clara para moléculas diatómicas usando el lenguaje y las herramientas de la simetría de grupos. En esta aproximación formal, un enlace σ es simétrico con respecto a la rotación alrededor del eje del enlace. Por esta definición, las formas comunes de enlace σ son sus, pz+pz, s+pz, y dz2+dz2 (donde z está definido como el eje del enlace). La teoría cuántica también indica que los orbitales moleculares de simetría idéntica realmente se mezclan. Una consecuencia práctica de esta mezcla de moléculas diatómicas (equivalente a la hibridación de la Teoría del enlace de valencia), es que las funciones de onda de los orbitales moleculares s+s y pz+pz están mezclados. El alcance de esta mezcla de orbitales depende de las energías relativas de los orbitales moleculares de similar simetría. Para moléculas homodiatómicas, los orbitales σ enlazantes no tienen planos nodales entre los átomos enlazantes. El orbital anti u orbital σ* correspondiente está definido por la presencia de un plano nodal entre estos dos átomos enlazados. Dado que los enlaces sigma son el tipo más fuerte de enlace covalente, los electrones en estos enlaces son denominados algunas veces como electrones sigma. El símbolo σ es la letra griega para s. Esto se debe a la similitud en forma de un enlace σ enlazante con el orbital atómico s Enlace triple Los enlaces se forman cuando los átomos se unen y forman compuestos, esto lo pueden hacer ganando, perdiendo o compartiendo electrones. En los enlaces covalentes (Polares o no polares) cada uno de los átomos participantes, aporta un electrón para formar el enlace. Entonces en un enlace covalente triple, cada uno de los átomos participantes aportará 3 electrones, desapareados, que se aparearán, (Es decir formaran pares) y así se forma este tipo de enlace. Uno de los átomos que puede hacer esto, es el átomo de carbono, y se presenta en las Alquinos. Los alquinos son hidrocarburos alifáticos con al menos un triple enlace -C≡Centre dos átomos de carbono. Se trata de compuestos metaestables debido a la alta energía del triple enlace carbono-carbono. Su fórmula general es CnH2n2.. Estereoisómero Es un isómero de una molécula que tiene las mismas conexiones átomo a átomo que dicha molécula, pero difiere en la orientación espacial de los mismos. Los estereoisomeros se pueden clasificar en: - Isómeros conformacionales, o rotameros, interconvertibles entre sí por la rotación en torno a enlaces. - Isómeros configuracionales, interconvertibles entre sí mediante ruptura de enlaces. Existen varios tipos de isómeros configuracionales, como son los enantiómeros y los diasteroisómeros. Los enantiómeros son imágenes especulares entre sí. Los isómeros configuracionales son aislables ya que es necesaria una gran cantidad de energía para interconvertilos (energía necesaria para la ruptura de enlaces), mientras que los conformacionales generalmente no lo son debido a la facilidad de interconversión aun a relativamente bajas temperaturas. La rama de la estereoquímica que estudia los isomeros conformacionales que son aislables (la mayoría derivados del bifenilo) se llama atropisómeria. En la ciencia de la química se dice que dos estereoisómeros son enantiómeros si la imagen especular de uno no puede ser superpuesta con la del otro. Dicho de otra forma: un enantiómero es una imagen especular no superponible de sí mismo. Tienen las mismas propiedades físicas y químicas, excepto por la interacción con el plano de la luz polarizada o con otras moléculas quirales. Son moléculas quirales. La mezcla de enantiómeros en una solución se denomina mezcla racémica. Diastereoisómeros o diastereómeros, clase de estereoisómeros que no tienen una imagen especular entre ellos, es decir, no son enantiómeros. Entre ellas pueden tener diversas características físicas y diferente reactividad. Fuerzas dipolo-dipolo Consiste en la atracción electrostática entre el extremo positivo de una molécula polar y el negativo de otra. El enlace de hidrógeno es un tipo especial de interacción dipolo-dipolo. Interacción entre los dipolos eléctricos de las moléculas de cloruro de hidrógeno. Las fuerzas electrostáticas entre dos iones disminuyen de acuerdo con un factor 1/d2 a medida que aumenta su separación d. En cambio, las fuerzas dipolo varían según 1/d3 (d elevado a la tercera potencia) y sólo son eficaces a distancias muy cortas; además son fuerzas más débiles que en el caso ion-ion porque q+ y q- representan cargas parciales. Las energías promedio de las interacciones dipolo son aproximadamente 4 kJ por mol, en contraste con los valores promedio para energías características de tipo iónico y de enlace covalente (~400 kJ por mol). Estas son ligeramente direccionales, es decir, al elevarse la temperatura, el movimiento transicional, rotacional y vibracional de las moléculas aumenta y produce orientación más aleatoria entre ellas. En consecuencia, la fuerza de las interacciones dipolo-dipolo disminuye al aumentar la temperatura. Miscibilidad Es un término usado en química que se refiere a la propiedad de algunos líquidos para mezclarse en cualquier proporción, formando una solución. En principio, el término es también aplicado a otras fases (sólidos, gases), pero se emplea más a menudo para referirse a la solubilidad de un líquido en otro. El agua y el etanol (alcohol etílico), por ejemplo, son miscibles en cualquier proporción. La miscibilidad es parcialmente una función de la entropía, y por lo tanto se observa más comúnmente en los estados de la materia que poseen más entropía. Los gases se mezclan con bastante facilidad, pero los sólidos raramente son miscibles. Dos excepciones notables a esta regla son las soluciones sólidas de cobre con níquel (el cuproníquel resultante es usado para la fabricación de monedas y tuberías) , y las de silicio con germanio usadas en electrónica. Las sustancias con entropía configuracional extremadamente baja, los polímeros especialmente, tienen poca probabilidad de ser miscibles entre sí incluso en el estado líquido. Dos sustancias son miscibles si la mezcla tiene como resultado una menor energía libre que cada uno de los componentes por separado. Grupo funcional Es un átomo o conjunto de átomos unidos a una cadena carbonada, representada en la fórmula general por R para los compuestos alifáticos y como Ar (radicales alifáticos) para los compuestos aromáticos. Los grupos funcionales son responsables de la reactividad y propiedades químicas de los compuestos orgánicos. La combinación de los nombres de los grupos funcionales con los nombres de los alcanos de los que derivan brinda una nomenclatura sistemática poderosa para denominar a los compuestos orgánicos. Los grupos funcionales se asocian siempre con enlaces covalentes, al resto de la molécula. Cuando el grupo de átomos se asocia con el resto de la molécula primero mediante fuerzas iónicas, se denomina más apropiadamente al grupo como un ion poliatómico o ion complejo. Ejemplo: Una serie homóloga es un conjunto de compuestos que comparten el mismo grupo funcional y, por ello, poseen propiedades y reacciones similares. Por ejemplo: la serie homóloga de los alcoholes primarios poseen un grupo OH (hidroxilo) en un carbono terminal o primario. Las series homólogas y grupos funcionales listados a continuación son los más comunes.1 En las tablas, los símbolos R, R', o similares, pueden referirse a una cadena hidrocarbonada, a un átomo de hidrógeno, o incluso a cualquier conjunto de átomos. OM antienlazante En el contexto de la teoría de orbitales moleculares, un orbital de antienlace es aquel orbital molecular caracterizado porque hay una densidad electrónica pequeña entre los núcleos atómicos, existiendo uno o más nodos perpendiculares al eje internuclear. Según el método de combinación lineal de orbitales atómicos, un orbital antienlazante se forma mediante la interferencia destructiva de dos orbitales atómicos de simetría apropiada. De esta forma, se obtiene un orbital con mayor energía que cualquiera de los dos orbitales atómicos originales, lo que desfavorece la formación del enlace químico entre los dos átomos. Puesto que los orbitales de antienlace o antienlazantes tienen mayor energía que los orbitales atómicos que les dieron origen, en una estructura electrónica molecular suelen ser llenados en último término. Enlace π En química, los enlaces pi (enlaces π) son enlaces químicos covalentes donde dos lóbulos de un orbitalinvolucrado en el enlace solapan con dos lóbulos del otro orbital involucrado. Estos orbitales comparten un plano nodal que pasa a través de los núcleos involucrados. La letra griega π en su nombre se refiere a los orbitales p, dado que la simetría de los orbitales de los enlaces pi es la misma de la de los orbitales p. Generalmente, los orbitales p están involucrados en este tipo de enlace. Se asume que los orbitales d también participan en el enlace pi, pero esto no es necesariamente el caso en la realidad, aunque el concepto de enlace por medio de orbitales d explica bien la hipervalencia. Los enlaces pi son generalmente más débiles que los enlaces sigma, porque su densidad electrónica negativamente cargada está más lejos de la carga positiva del núcleo atómico, lo que requiere más energía. Desde la perspectiva de la mecánica cuántica, la debilidad del enlace se explica por el traslape significativamente menor entre los componentes de los orbitales p, debido a la orientación paralela. SOMERÍA CONSTITUCIONAL Isomería constitucional. Aquellas moléculas iguales según los criterios 1 a 3 pueden poseer distinta conectividad de sus átomos. Es en este punto cuando se habla de isomería. Los isómeros constitucionales son sustancias que poseen la misma fórmula molecular pero difieren en la secuencia en la que están enlazados sus átomos. Se subdividen en distintos tipos, aunque aquí no los veremos todos, se enumeran a continuación algunos ejemplos: a) Isómeros de cadena: poseen distinta distribución de los átomos de carbono, como es el caso entre el butano y el isobutano. Momento dipolar de enlace El momento dipolar de enlace o momento de enlace usa la idea del momento dipolar eléctrico para medir la polaridad de un enlace químico dentro de una molécula. El dipolo de enlace, μ, está dado por: \mu = \delta \, d. El dipolo de enlace está modelado como +δ — δ-, con una distancia d entre las cargas parciales +δ y -δ. Es un vector, paralelo al eje de enlace, apuntando desde la menos hasta el más, como está convenido1 para los vectores momento dipolar eléctrico. (Algunos químicos dibujan el vector en la otra forma, apuntando del positivo al negativo, pero sólo en situaciones donde la dirección no importa.)1 Este vector puede ser interpretado físicamente como el movimiento efectuado por los electrones cuando los dos átomos se colocan a la distancia d uno del otro, y se les permite interactuar; los electrones se moverán de sus posiciones de libre estado para estar localizados más cerca al átomo más electronegativo. La unidad SI para el momento eléctrico dipolar es el culombio·metro, pero es demasiado grande para ser práctico en la escala molecular. Los enlaces dipolares de enlace suelen ser medidos en debye, representados por el símbolo D, que es lo que se obtiene si se mide la carga \delta en unidades de 10-10 estatoculombios, y se mide la distancia d en Angstroms. Obsérvese que 10-10 estatoculombios es 0,48 unidades de carga elemental. El factor de conversión más útil es 1 C·m = 2.9979×1029 D. Los momentos dipolares de enlace típicos para moléculas diatómicas simples están en el rango de 0 a 11D. En un extremo, las moléculas simétricas como el dicloro, Cl2, tiene un momento dipolar de enlace de cero, mientras que cerca al extremo opuesto, el bromuro de potasio en fase gaseosa, KBr, que es altamente iónico, tiene un momento dipolar de enlace de 10,5D.2 Las fuerzas de dispersión de London Son un tipo de fuerza intermolecular, denominadas así por el físico alemán Fritz London, quien las investigó en 1930. Surgen entre moléculas no polares, en las que pueden aparecer dipolos instantáneos. Son más intensas cuanto mayor es la molécula, ya que los dipolos se pueden producir con más facilidad. Dipolo-dipolo: consiste en la atracción electrostática entre el extremo positivo de una molécula polar y el negativo de otra. El enlace de hidrógeno es un tipo especial de interacción dipolo-dipolo. Sólo son eficaces a distancias muy cortas; además son fuerzas más débiles que en el caso ion-ion porque q+ y qrepresentan cargas parciales. Así como las moléculas polares presentan algún tipo de fuerzas intermoleculares como las ya mencionadas, también las sustancia conformadas por moléculas no polares y los átomos que constituyen los gases nobles experimentan atracciones muy débiles llamadas fuerzas de london. La intensidad de la fuerza de dispersión depende de cierto número de factores. Sin embargo, dar un enfoque cualitativo y predictivo debe considerar que las fuerzas de dispersión se relacionan con el número de electrones que se encuentren en el átomo o en la molécula. Así, bajo dicha base, es el número de electrones el que determinará la facilidad con la que se puede polarizar la densidad del electrón y a mayor polarización, son más intensas las fuerzas de dispersión. A su vez, la intensidad de estas fuerzas intermoleculares determina el punto de fusión y el punto de ebullición de la sustancia: cuando más intensas son las fuerzas intermoleculares, más altos son los puntos de fusión y de ebullición. Hidrocarburos Son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno. La estructura molecular consiste en un armazón de átomos de carbono a los que se unen los átomos de hidrógeno. Los hidrocarburos son los compuestos básicos de la Química Orgánica. Las cadenas de átomos de carbono pueden ser lineales o ramificadas y abiertas o cerradas. Los que tienen en su molécula otros elementos químicos (heteroátomos) se denominan hidrocarburos sustituidos. Los hidrocarburos se pueden clasificar en dos tipos, que son alifáticos y aromáticos. Los alifáticos, a su vez se pueden clasificar en alcanos, alquenos y alquinos según los tipos de enlace que unen entre sí los átomos de carbono. Las fórmulas generales de los alcanos, alquenos y alquinos son CnH2n+2, CnH2n y CnH2n-2, respectivamente. Orbital híbrido Cada uno de los orbitales equivalentes que pueden obtenerse mediante combinación lineal de orbitales atómicos distintos. La hibridación de orbitales da como resultados orbitales de enlace que son combinación lineal de sus componentes. Los orbitales híbridos más generalizados son los siguientes: sí, sp2, sp3 y spd. Los orbitales moleculares, que representan la distribución espacial de los electrones de enlace en una molécula, son, fundamentalmente, orbitales híbridos. Las formas de las moléculas enlazadas por hibridaciones de sus orbitales son forzadas por los ángulos entre sus átomos: Sin hibridación: forma lineal Hibridación sp: forma lineal con ángulos de 180° Hibridación sp²: forma trigonal plana con ángulos de 120°. Por ejemplo B Cl 3. Hibridación sp³: forma tetraédrica con ángulos de 109.5°. Por ejemplo C Cl 4?. Hibridación sp³d: forma trigonal bipiramidal con ángulos de 90° y 120°. Por ejemplo P Cl 5. Hibridación sp³d²: forma octaédrica con ángulos de 90°. Por ejemplo SF6. Enlace Doble En un enlace covalente doble, los núcleos de los átomos comparten más que dos electrones. Ej. Molécula de Oxígeno Z=8 Distribución electrónica < —- > 2-6 Como el átomo de oxígeno tiene seis electrones de valencia, va a compartir dos electrones con el otro átomo. Cada átomo de oxígeno pasa a quedarse con ocho electrones de valencia, adquiriendo la configuración electrónica de un gas noble (muy estable).