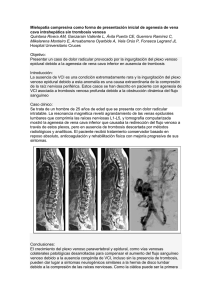
MANIFESTACIÓN TARDÍA ANÓMALA DE LA AGENESIA DE VENA CAVA INFERIOR
Anuncio

MANIFESTACIÓN TARDÍA ANÓMALA DE LA AGENESIA DE VENA CAVA INFERIOR Abril Arjona, Yolanda Berga Fauria, Carme Sempere Dura, Tomás (*) García Vidal, Raúl Mellado Joan, Meritxell Fariña Alija, Mª Palma Argilés Mattes, Nuria Martín Parededo, Vicente Servicio de Angiología, Cirugia Vascular y Endovascular. (*) Servicio de Radiodagnóstico. Hospital Universitari Joan XXIII. Tarragona. 1 MANIFESTACIÓN TARDÍA ANÓMALA DE LA AGENESIA DE VENA CAVA INFERIOR RESUMEN: La agenesia de la Vena Cava Inferior (VCI) constituye una malformación congénita poco frecuente, habiéndose reconocido la existencia de asociación con trombosis venosas profundas (TVP) idiopáticas, particularmente en pacientes jóvenes. Dicha anomalía puede no dar manifestaciones hasta fases tardías de la vida , pero suelen aparecer signos de alerta en la juventud que nos pueden hacer sospechar en su existencia. Presentamos el caso de una paciente de 48 años con cuadro de una semana de evolución de lesión cutánea en flanco derecho de aspecto “serpenteante” eritro-violáceo, indurado y doloroso, acompañándose de cordón flebítico en territorio de vena safena interna (VSI) de la extremidad inferior derecha (EID). Como antecedentes destacaba TVP de la EID hacía 20 años durante el puerperio e historia prolongada de varices y úlcera flebostática recidivante. Durante el ingreso, se diagnosticó una tromboflebitis de VSI y se realizó estudio con TAC para descartar patología oncológica asociada, objetivándose una agenesia de vena cava inferior con retorno venoso mediante colateralidad hacia tejido celular subcutáneo, que aparecía parcialmente trombosado. Además se realizó estudio completo de trombofilia que resultó patológico, con la mutación la Protrombina o Factor V Leiden. La agenesia de VCI está probablemente infradiagnosticada, ya que existen casos de TVP que se les ha atribuido factores de riesgo concomitantes que han podido ocultarla. Es por ello, que consideramos razonable la indicación de pruebas diagnósticas de imagen como técnica de cribado en TVP idiopáticas en pacientes jóvenes. 2 PERSONA Y MÉTODO: CASO CLÍNICO Presentamos paciente mujer de 48 años, con único antecedente de interés de trombosis venosa profunda femoral de extremidad inferior derecha (EID) a los 27 años, coincidiendo con el puerperio que fue diagnosticada mediante Ecografia doppler, suponiéndose la causa etiológica más probable su estado puerperal, sin considerar necesarios otros estudios ni métodos diagnósticos complementarios. La paciente fue tratada con HBPM a dosis anticoagulantes durante 6 meses. La paciente en los años posteriores siguió controles semestrales por Cirugía Vascular por síndrome postrombótico de dicha extremidad y por aparición de úlcera supramaleolar interna exudativa de difícil curación, que debido al antecedente trombótico sufrido se consideró como una seqüela postrombótica. Se intervino de varices de pierna derecha hacía aproximadamente tres años, realizándose una técnica CHIVA 1 con desconexión de perforante de Cockett, tras la cual refirió mejoría en la evolución de la úlcera flebostática, consiguiéndose su curación completa, pero desde hacía unos seis meses había reaparecido de nuevo y seguía curas ambulatorias con antibioterapia por sobreinfección de ésta. La paciente fue remitida de forma urgente a nuestras consultas por aparición de cordón indurado, doloroso, con signos inflamatorios en territorio de vena safena interna de la extremidad inferior derecha de unos días de evolución, además destacaba a la exploración física una lesión cutánea de aspecto serpenteante eritro-violáceo en flanco derecho dolorosa a la palpación, que presentaba desde hacía aproximadamente unas dos semanas. (ver figura 1) 3 Figura 1: La fotografia muestra la presencia de circulación colateral en pared abdominal y la flebitis venosa superficial en flanco derecho. Como primera prueba diagnóstica se realizó una ecografia doppler que confirmó el diagnóstico de tromboflebitis de vena safena interna que se extendía hasta unos 2 -3 cm del cayado y se decidió con diagnóstico preliminar de probable “Tromboflebitis Migrans”, la realización de angio-tomografïa computerizada abdominal (TC) para excluir patología maligna asociada. La TC toraco-abdominal, se observaron los siguientes hallazgos: arteria subclavia derecha aberrante como variante de la normalidad. Cayado de vena ácigos prominente con atresia de vena cava inferior intrahepática y ausencia de VCI con drenaje de vena renal izquierda al sistema hemiácigos homolateral. Descenso de vena renal derecha, formando un plexo venoso y retornando mediante colateralidad hacia tejido subcutáneo. En el espesor de la pared abdominal, se aprecia un defecto de replección de su luz con trombosis de venas parietales, junto a trombosis de la vena safena derecha. En fase venosa tardía se aprecia retraso funcional en la eliminación renal derecha. ( Fig: 2, 3, 4, 5 ) 4 (2) Figura 2 i 3: Reconstrucción por TC a nivel torácio que muestra un desarrollo prominente de cayado de vena ácigos. (3) 5 (4) Figura 4 y 5: La TC abominal muestra la agenesia de vena cava inferior. Se objetiva el descenso de vena renal derecha, formando un plexo venoso (flecha pequeña) y retornando mediante colateralidad a nivel de tejido subcutáneo, observando trombosis de venas superficiales (flecha gruesa). (5) Tras descartar patología neoplásica asociada y con el diagnóstico de tromboflebitis de VSI supragenicular de EID y flebitis superficial de venas parietales abdominales en paciente con agenesia de VCI, se decidió iniciar tratamiento antiinflamatorio con AINES y anticoagulante con heparina de bajo peso molecular y posterior paso a acenocumarol en rangos de INR entre 2-3. 6 (6) Figura 6 ,7: Imagen de reconstrucción por TAC, donde se observa los signos de colateralidad en la pared parietal que corresponden a flebitis superficial en flanco derecho. (7) RESULTADOS: La paciente tras instauración del tratamiento mejoró en pocos días, los signos inflamatorios y la clínica dolorosa tanto de la tromboflebitis de safena interna como de la flebitis en flanco 7 derecho disminuyeron. Además, se decidió mantener reposo en cama durante la transición a anticoagulación oral, manteniendo la extremidad en posición de Trendelenburg. Se mantuvo tratamiento con acenocumarol oral durante cuatro mesos, con controles seriados por Unidad de Hematología. Se suspendió el tratamiento anticoagulante para proceder al estudio completo de trombofilia que confirmó la presencia de la mutación congénita de la Protrombina 20210, más conocida como resistencia a la Proteina C Activada (PCA) o Fenotipo Factor V Leiden (heterozigoto GA). Tras la confirmación de la alteración del estudio de trombofilia se decidió mantener el tratamiento anticoagulante oral de por vida, debido al alto riesgo trombogénico asociado tanto por la agenesia VCI existente como por la alteración congénita del factor de coagulación. Se realizó un seguimiento clínico de la paciente a los 2, 4 y 6 meses, objetivando una desaparición de la flebitis de la pared abdominal pero se mantenía abierta, exudativa y con eritema perilesional la úlcera supramaleolar de EID (fig. 5), por lo que se recomendó el seguimiento exhaustivo ambulatorio con curas locales, manteniendo un tratamiento con soporte elástico, medidas posturales y ejercicio físico, además de los controles habituales de anticoagulación por Hematología. CONSIDERACIONES FINALES: El desarrollo del sistema venoso en el feto humano se produce entre la sexta y la octava semana de gestación, por fusión y regresión de tres pares de venas del sistema cardinal: supracardinal, cardinal posterior y subcardinal [1]. Este complejo origen embrionario da lugar a múltiples posibilidades de malformaciones. De los casos con malformación congénita de VCI, el 90% afecta a la porción suprarrenal, mientras que sólo el 6% lo hace el segmento renal o infrarrenal [2]. 8 La ausencia de la VCI suprarrenal ocurre como resultado del fallo en la formación de la vena subcardinal derecha: el segmento hepático drena directamente en la aurícula derecha y la sangre de VCI infrarrenal drena a través de las venas ácigos y hemiácigos, tendiendo a asociarse con otras anomalías congénitas. Entre las que se distinguen las de tipo cardiovascular (dextrocardia, comunicación interauricular, canal atrioventricular estenosis de la arteria pulmonar), transposición de visceras abdominales, disginesia pulmonar, polisplenia o asplenia [3]. La ausencia de la VCI infrarrenal, con preservación del segmento suprarrenal, implica un fallo en el desarrollo de la vena supracardinal derecha. La ausencia completa de la VCI implica un fallo en el desarrollo de los tres pares venosos [4, 5]. (Figura: 8) Figura 8: Proceso embriológico del desarrollo de la VCI desde la 7º semana de gestación (A) al adulto (B). 9 Actualmente existe controversia en si la agenesia de VCI se debe realmente a una anomalía en el desarrollo o es el resultado de una trombosis de la VCI en el periodo perinatal que provocaría una regresión y desaparición del sistema [6]. La agenesia del sistema del la VCI constituye una malformación congénita poco frecuente, se presenta entorno al 0,3% - 0,5% de los individuos sanos y en el 0,6-2% de los pacientes con otras anomalías cardiovasculares [1,5]. Su incidencia se cifra entorno al 0.0005 – 1% en la población general y en algunos estudios recientes estiman una prevalencia entorno al 5% en pacientes jóvenes (< 30 años) que han sufrido TVP sin factores de riesgo identificados [1,7]. Por lo que parecería confirmarse como un importante factor de predisposición para el desarrollo de una TVP. Así, la presencia de una agenesia o hipoplasia de la VCI debe considerarse siempre en pacientes jóvenes con TVP idiopática, recurrente y/ o bilateral. Clínicamente, dicha anomalía provoca un inadecuado retorno venoso a través de la colateralidad existente, provocando un incremento de la presión venosa de las piernas, facilitando la trombosis venosa, la aparición de varices y úlceras crónicas. [6,8] Algunos datos clínicos se presentan en mayor frecuencia en casos de agenesia de VCI y TVP por lo que los debemos tener en cuenta ya que nos pueden hacer sospechar su presencia: los pacientes suelen ser jóvenes, la mayoría de ellos no presentan factores precipitantes ni existencia de alteraciones de la coagulación, las venas ilíacas están afectadas en mayor frecuencia, mayor probabilidad de trombosis bilateral y de recurrencia de TVP, puede asociarse conjuntamente con un embolismo pulmonar [9, 12]. El principal test diagnóstico para la TVP es la Ecografia Doppler, con una sensibilidad de hasta el 97%, es la primera prueba diagnóstica a realizar, pero las anomalías a nivel de VCI 10 pueden pasar desapercibidas. En caso de sospecha de posibles anomalías de VCI asociadas, es preciso la realización de una Angiotomografía Computerizada o una Angiorresonancia Magnética, en las cuales se observa una extensa circulación colateral, prominencia del sistema ácigos y hemiácigos, desarrollo importante de colateralidad a nivel de venas lumbares, plexo venoso paravertebral y venas de la pared anterior abdominal; como nuestra paciente, la cual presentaba un drenaje venoso a través del sistema subcutáneo de la pared abdominal, encontrándose parcialmente trombosado [10,11]. ( Ver Fig:4,5 ) La tomografía computerizada (TC) y la resonancia magnética (RMN) son los métodos más utilizados para su diagnóstico. La RMN presenta ventajas respecto la TC, ya que no existe inyección de contraste y además permite la visualización de otras anomalías congénitas, por lo que actualmente es probablemente el mejor método diagnóstico [5]. La flebografía se reserva para casos no concluyentes con las demás pruebas de imagen, es un método invasivo, pero se considera el método “gold standard”. No existen en la literatura datos suficientes para establecer cuál es el manejo adecuado de la TVP asociada con anomalías de la VCI. En el momento agudo es necesaria la anticoagulación (Heparina sódica, HBPM), aunque la duración no está establecida. La mayoría de autores opta por la anticoagulación de por vida, basándose en el riesgo de recurrencia de la TVP, aunque éste no esté completamente demostrado [5,8]. Existen casos descritos en que sólo se asoció anticoagulación durante 6 meses sin sufrir complicaciones. En nuestro caso, se decidió suspender el tratamiento anticoagulante a los cuatro meses para la realización del estudio de trombofilia, pero al confirmarse la mutación existente (Factor V de Leiden) se decidió instaurar tratamiento anticoagulante de por vida. 11 Se debe asociar al tratamiento el uso de soporte elástico, medidas posturales, ejercicio físico y evitar todos los factores de riesgo adicionales, como la inmovilización prolongada y el uso de anticonceptivos [12]. Se desconoce el pronóstico a largo plazo de estos pacientes, aunque se cree que probablemente tengan una supervivencia normal [1] . En conclusión, la agenesia de la VCI debe considerarse siempre en pacientes jóvenes con TVP sin factores de riesgo asociados y debe ser investigada, realizando métodos diagnósticos (TAC o RMN). El tratamiento, aunque aún no exista una evidencia establecida, se recomienda mantener la anticoagulación generalmente de por vida por su elevado riesgo de recurrencia trombótica. REFERENCIAS: [1] Jiménez Gil R, Miñano Pérez A, Bercial Arias J, Bernabeu Pascual F, Sansegundo Romero E. Agenesis of the inferior vena cava associated with lower extremities and pelvic venous trombosis. J Vasc Surg 2006; 44: 1114-6. [2] Martínez Aguilar E, Medina- Maldonado FJ, Flórez González A, Varela Casariego C, Gómez Penas M, Acín F. Hipoplasia de la vena cava inferior asociada a una trombosis de vena profunda de los miembros inferiores. Angiología 2008; 60 (1): 55-59. [3] Dougherty MJ, Calligaro KD, Delaurentis DA. Congenitally absent inferior vena cava presenting in adulthood with venous stasis and ulceration: a surgically treated case. J Vasc Surg 1996; 23: 141-6. [4] Bass JE, Redwine MD, Kraner LA, Huynh PT, Harris JH. Spectrum of congenital anomalies of the inferior vena cava: crossectional Imaging findings. Radiographics 2000; 20: 639 – 52. [5] Yun SS, Kim KH, Sung GY, Leedo S, Kim JS, Moon LS, et al. Deep venous trombosis caused by congenital absence of inferior vena cava, combined with hyper-homocysteinemia. Ann Vasc Surg 2004; 18: 124-9. [6] Ramanathan T, Hughes MD, Richardson AJ. Perinatal inferior vena cava trombosis and absence of the infrarrenal inferior vena cava. J Vasc Surg 2001; 33. 1097-9. [7] Ruggeri M, Tosetto A, Castman G, Rodeghiero F. Congenital absence of inferior vena cava: a rare risk factor for idiopathic deep vein trombosis. Lancet 2001; 357: 441. [8] Obernosterer A, Aschauer M, Schnedl W, Lipp RW. Anomalies of the inferior vena cava in patients with iliac venous trombosis. Ann Intern Med 2002; 136: 37-41. [9] Schneider JG, Eynatten MV, Dugi KA, Duex M, Nawroth PP. Recurrent deep venous trombosis caused by congenital interruption of the inferior vena cava and heterozygous factor V Leiden mutation. J Intern Med 2002; 252: 276-80. [10] Sneed D, Hamdallah J, Sardi A. Absence of the retrohepatic inferior vena cava: what the surgeon should know. Am Surg 2005; 71: 502-4. [11] Vermeulen EG, Van Urk H. Agenesis of the inferior vena cava. Eur J Vasc Endovasc Surg 1996; 12: 493-6. [12] Cho BC, Choi HJ, Kang SM, Chang J, Lee SM, et al. Congenital absence of inferior vena cava as a rare cause of pulmonary troembolism. Yonsei Med J 2004; 45: 947-51. 12