T-1 BIOQUIMICA.key
Anuncio

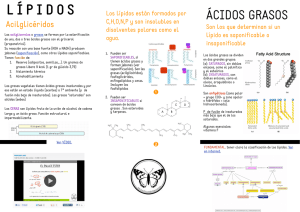
Tema 1: Los seres vivos: composición y función https://www.youtube.com/watch?v=-S28CyDWaUo El nivel atómico El nivel atómico Bioelementos: elementos que constituyen la materia viva Fundamentales: C, H, O, N. Secundarios: P, S, Ca, Na, K, Mg, Cl Oligoelementos: Fe, Zn, Cu, Co, Mn, I, Li. El nivel molecular Biomoléculas: compuestos que constituyen los seres vivos y pueden extraerse de ellos por procedimientos físicos sencillos. Inorgánicos: Orgánicos: Agua Glúcidos Sales minerales Lípidos Proteínas Ac. nucleicos El nivel molecular 1. Agua Estructura de la molécula: “dipolo” Inorgánicas 1. Agua Propiedades: Funciones: capacidad calórica termorregulador cohesión capilaridad viscosidad lubricante reactividad (disolvente) transporte, medio de reacción, reactivo 2. Sales minerales Sólidas: esqueletos caparazones Disolución: (aniones Cl-, SO4=, HCO3-, HPO4= ; cationes Na+, K+, Ca++, Mg++) regulación pH regulación presión osmótica transmisión impulsos ner viosos contracción muscular Orgánicas 3. Glúcidos compuestos por: C, H, O (Hidratos de carbono) función: energética (estructural) química: derivados de monosacáridos. http://ies.rayuela.mostoles.educa.madrid.org/deptos/dbiogeo/recursos/Apuntes/ ApuntesBioBach2/1-Bioquimica/Glucidos.htm monosacáridos polialcoholes de entre tres y siete átomos de carbono, con un grupo aldehído o cetona. azúcares (dulces, solubles, cristalizables) según nºC: triosas, tetrosas, pentosas, hexosas. según carbonilo: cetosas, aldosas en disolución: formas cíclicas. ejemplos monosacáridos triosas tetrosas ejemplos monosacáridos pentosas hexosas ciclación ejemplos moléculas cicladas disacáridos unión de dos monosacáridos con pérdida de una molécula de agua. función energética. Ejemplos: lactosa, maltosa, sacarosa polisacáridos polímeros formados por numerosas moléculas de glucosa con diferentes enlaces entre ellas. Función energética Función estructural polisacáridos 4. Lípidos compuestos por: C, H, O (P, N). químicamente muy heterogéneos: familias. común: insolubles en agua. funciones: energética, estructural, actividad vital (hormonas, vitaminas) Clasificación lípidos Ácidos grasos ácidos orgánicos de cadena larga y nº par de átomos de carbono. saturados (no enlaces dobles) insaturados (enlaces dobles) Ácidos grasos Acil-glicéridos Esteres de la glicerina y ácidos grasos glicerina: CH2OH-CHOH-CH2OH (polialcohol) mono, di, triacilglicéridos (coloquialmente triglicéridos) Aceites: si tienen ác. grasos insaturados (líquidos) Sebos: con todos sus ác. grasos saturados (sólidos) Mantecas: semisólidos Fosfolípidos esteres de la glicerina con dos ácidos grasos y un ácido fosfórico (H3PO4). Bipolares: cabeza hidrófila (H3PO4) y cola hidrófoba (ác. grasos). función estructural: lípidos de membrana. Isoprenoides Esteroides derivados del isopreno derivados del esterano ejemplos: ejemplos: pigmentos: carotenos hormonas (sexuales) vitaminas (A, E, K) colesterol esencias: mentol, limoneno Vit. D 5. Proteínas Compuestas por: C, H, O, N (S, P, Fe...) Química: derivados de aminoácidos Funciones: estructural, dinámica (enzimas), defensa, transporte, reserva, hormonal, coagulación). aminoácidos sustancias químicas sencillas con un grupo ácido y otro amino unidos al mismo átomo de carbono. el resto puede ser muy variado: hay hasta veinte diferentes en las proteínas. se unen mediante enlaces peptídicos. los aminoácidos esenciales enlace peptídico dipéptidos, tripéptidos, ..., polipéptidos Proteínas: Cientos o miles de aa unidos mediante enlaces peptídicos. (macromoléculas) Especificidad (infinitas combinaciones; derivan del código genético). 4 niveles estructurales. Desnaturalización. (Tª, pH, sales, etc.) Clasificación: globulares, fibrilares. Holo y heteroproteínas Estructura de las proteínas Primaria: secuencia de aa. (nº, cuales, secuencia) Secundaria: alfa hélice, hoja plegada beta. Terciaria: conformación tridimensional (globulares, fibrilares) Cuaternaria: unión de varias subunidades estructura primaria estructura secundaria: disposición espacial estructura terciaria: conformación 3D estructura cuaternaria: unión varias cadenas (protómeros) Desnaturalización y Renaturalización de una proteína Proteínas: ejemplos. actina, miosina hemoglobina fibrinógeno mucina trombina caseina albúmina inmunoglogulinas colágeno queratina 6. Ácidos nucleicos Compuestos por C,H,O,N,P. Derivados de nucleótidos: ✓ pentosa: ribosa, desoxirribosa ✓ base nitrogenada: púricas (Adenina, Guanina), pirimidínicas (Citosina, Timina, Uracilo) ✓ ác. fosfórico. constitución ác. nucleicos Nucleósidos y nucleótidos ADN vs ARN Desoxirribosa Ribosa A, G, T, C A, G, U, C A--T; G--C A--U; G--C Doble hélice Cadena simple (bucles) Núcleo Núcleo y citoplasma Portador información Ejecutor órdenes. ADN: la doble hélice Actividad vital Ác. nucleicos ADN: Duplicación (copia de los genes para pasar la información genética a la descendencia). ARNm: Transcripción (copia los genes y los transporta al citoplasma para fabricar las proteínas) ARNr: constituye los ribosomas. ARNt: “pinzas” de precisión para incorporar los aa ala protrina en formación. Traducción.