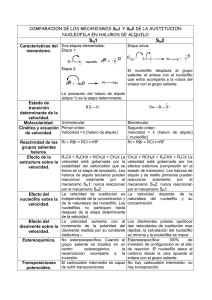
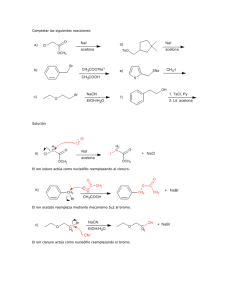
+ X
Anuncio

QUÍMICA ORGÁNICA AVANZADA TEMA 5 OBJETIVOS DIDÁCTICOS PERSEGUIDOS EN EL TEMA Revisión de los mecanismos de reacción ya estudiados dispersos en los capítulos dedicados a la descripción de grupos funcionales. Profundizar en ciertos aspectos de estos mecanismos de reacción. Estudio de mecanismos de reacción nuevos. Descripción y análisis de reacciones nuevas como casos prácticos de los mecanismos de reacción en estudio. 2 ASPECTOS FUNDAMENTALES DEL ESTUDIO DE UN MECANISMO DE REACCIÓN • COMPRENSIÓN RAZONADA DE LA DENOMINACIÓN DEL PROCESO • DESCRIPCIÓN DE LOS REACTIVOS INTERVINIENTES Y DE LOS MÓVILES DEL ATAQUE • ESPECIFICACIÓN DETALLADA DEL MECANISMO EN CUANTO A : INTERMEDIOS DE REACCIÓN ESTADOS DE TRANSICIÓN FLUJO ELECTRÓNICO • CINÉTICA DE LA REACCIÓN • BALANCE ENERGÉTICO (TERMODINÁMICA) • DESARROLLO ESTEREOQUÍMICO Y SUS IMPLICACIONES • ESTUDIO DE LA REACTIVIDAD (JUSTIFICACIÓN Y PREDICCIÓN) • PECULIARIDADES ESPECÍFICAS DEL PROCESO. 3 Esto es una demostración de la sistemática de preparación y estudio teórico de un mecanismo de reacción descrito: • SUSTITUCIÓN NUCLEÓFILA ALIFÁTICA 4 SUSTITUCIÓN NUCLEÓFILA ALIFÁTICA SN 5 SUSTITUCIÓN NUCLEÓFILA ALIFÁTICA Reemplazo de un grupo por otro en la cadena carbonada Características electrónicas del reactivo empleado Naturaleza del carbono donde se da la reacción Utilidad sintética : R-X + ZC saturado + nucleófilo R-Z + Xproducto + grupo saliente CONDICION : Z reactivo y X buen saliente Productos : ALCOHOLES, TIOLES, ÉTERES, TIOÉTERES, ALQUINOS, NITRILOS, ÉSTERES, AMINAS ... 6 6 CINÉTICAS DE LA SUSTITUCIÓN NUCLEOFÍLICA ORDEN 2 (BIMOLECULAR) vR * * * * * vR = k2 (R-X) (Z-) * vR * * (R-X) (Z-) ORDEN 1 (UNIMOLECULAR) * vR * * * (R-X) 7 * * vR = k1 (R-X) vR * * * (Z-) * * Proposición de mecanismo cinéticamente compatible : H Nu – H H H (-) X ‡ Nu X H H (-) H Nu H MECANISMO SN2 : proceso concertado 8 H + X – Interpretación de orbitales frontera : H HOMO Nu : LUMO X HH ‡ H (-) (-) Nu X H H H Nu 9 HH Diagrama de OM resultantes en el E.T. (‡) de la SN2 : Nu C X energía C Nu 10 Nu C X Nu C X X Orientación del ataque nucleófilo : * Por el lado opuesto al halógeno unido : favorable estéricamente favorable electrónicamente máxima interacción con la mayor densidad del σ* Nu 11 C X Otras orientaciones dan interacciones menos eficaces : X C Nu •Menor densidad del orbital σ* •Interacción enlazante y otra antienlazante por ser una superficie nodal entre ambos átomos (C, X). 12 Valoración termodinámica del proceso SN2 ( 1 paso) : energía ENERGÍA DE ACTIVACIÓN - ESTABILIDAD ESTADO DE TRANSICIÓN - VELOCIDAD DE REACCIÓN reacción 13 ESTEREOQUÍMICA EN SN2 - Inversión de la configuración como consecuencia del mecanismo - Repercusión cuando es centro quirógeno - ¿ Cambio en la designación de la configuración absoluta R-S ? H3C C Br H C2H5 (R)-2-bromobutano 14 HO- CH3 HO C H C2H5 (S)-2-butanol REACTIVIDAD FACTORES RELATIVOS AL ESTADO DE TRANSICIÓN : ESTÉRICOS : impedimento del estado de transición pentacoordinado CH3 > 1º > 2º > 3º ELECTRÓNICOS : C eléctricamente neutro en el estado de transición posible conjugación del orbital tipo p del estado de transición con sistemas π vecinos como alilo o bencilo 15 X Nu 16 X Nu UN CASO DE ALTA REACTIVIDAD : en α-halocarbonilos y otros sistemas π deficientes, causas : - C sp2 contiguo menor impedimento que el C sp3 - interacción del orbital π* (C=O) con el σ* (C-X) Br Br O O Br O Br combinación π* + σ* O Ataque nucleófilo 17 Otra interpretación : el orbital π* (LUMO, C=O) interactúa con el tipo p desarrollado en el estado de transición estabilizándolo : π∗ energía X O Nu π O.M. Estado transición 18 C=O contiguo EFECTO DEL GRUPO SALIENTE EN LA SN2 : - orden de reactividad : I- > Br- > Cl- >> F- fuerza de enlace EFECTO DISOLVENTE EN LA SN2 : - disolventes polares próticos - disolventes polares apróticos - polaridad del disolvente 19 MECANISMO SN1 : C C+ 20 + Nu X rápido lento C+ C Nu + X- + Nu C energía Valoración termodinámica del proceso SN1 ( 2 pasos) : evolución reacción 21 ESTEREOQUÍMICA EN SN1 GS 22 :GS ESTEREOQUÍMICA EN SN1 RACEMIZACIÓN 23 REACTIVIDAD EN SN1 FACTORES RELATIVOS AL INTERMEDIO DE REACCIÓN : ( ESTABILIDAD DE IONES CARBENIO ) - geometría plana permitida - factores electrónicos efecto inductivo efecto conjugativo - factores estéricos no críticos : C tricoordinado - orden de reactividad : 3º > 2º > bencílicos alílicos 24 1º > CH3X EFECTO DEL GRUPO SALIENTE EN LA SN1 : - orden de reactividad : I- > Br- > Cl- >> F- fuerza de enlace - comportamiento similar a SN2 EFECTO DISOLVENTE EN LA SN1 : - favorecida por disolventes polares - no es crítica la desactivación del nucleófilo por efecto solvatación ¡ transposiciones ! 25 DESCRIPCIÓN DE NUCLEÓFILOS FACTORES QUE CONTROLAN EL ATAQUE NUCLEÓFILO SUFICIENTE ATRACCIÓN ELECTROSTÁTICA PRODUCTIVA INTERACCIÓN HOMO - LUMO ( NUCLEÓFILO – ELECTRÓFILO ) condición suficiente y necesaria 26 CLASIFICACIÓN DE NUCLEÓFILOS CONCEPTO EFECTO DOMINANTE TAMAÑO BASE CONJUGADA DENSIDAD DE CARGA BLANDOS DUROS INTERACCIÓN HOMO-LUMO ATRACCIÓN ELECTROSTÁTICA VOLUMINOSOS PEQUEÑOS DE ÁCIDO FUERTE DE ÁCIDO DÉBIL BAJA (POLARIZABILIDAD) ALTA ENERGÍA HOMO ALTA BAJA ELECTRONEGATIVIDAD BAJA ALTA REACCIÓN PREFERENTE CARBONOS SATURADOS ABSTRACCIÓN DE PROTÓN RSH, RS-, I-, R3P, CN-, CO, RCH=CHR RO-, NH2, MeLi, OH-,RCOO-, F-, RNH2, ROH EJEMPLOS 27 ESTUDIO COMPARATIVO DE AMBOS MECANISMOS 28 CONCEPTO SN1 S N2 CINETICA ORDEN 1 ORDEN 2 MECANISMO 2 PASOS 1 PASO ESTEREOQUÍMICA RACEMIZACIÓN INVERSIÓN ESPECIE CLAVE IÓN CARBENIO ESTADO DE TRANSICIÓN MAYOR REACTIVIDAD 3º, CONJUGADOS FACTORES DOMINANTES TRANSPOSICIONES ELECTRÓNICOS 1º, αCARBONILICOS ESTÉRICOS Y CONJUGATIVOS NO POSIBLES ¿ mecanismo único ? FACTORES DETERMINANTES DEL MECANISMO ELEGIDO : - tipo de halogenuro de alquilo - naturaleza y concentración del nucleófilo - grupos vecinos - disolvente ( constante dieléctrica y solvatación ) AMBOS MECANISMOS CON VARIABLE PARTICIPACIÓN Reacción * o * * o MeBr EtBr i-ProBr más rápida 29 S N1 * S N2 o o t-ButBr