Document
Anuncio

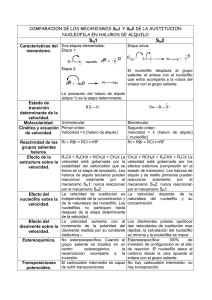
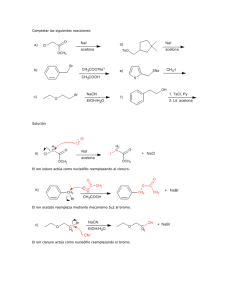
SUSTITUCIONES NUCLEOFÍLICAS EN EL C R-OH + H-X R-X + H-OH NUCLEOFILO GRUPO SALIENTE 2 posibles mecanismos: Primero se va el grupo saliente Luego ataca el nucleófilo El nucleófilo ataca al mismo tiempo que se va el grupo saliente rápido t-butanol CH3 OH Bromuro de t-butilo < RCH2OH < R2CHOH < R3COH carbocationes más estables Hibridización Sp2 Catión metilo muy inestable Estructura planar , menor repulsión entre los pares de e- enlazantes Orbital p vacío Estabilización extra por superposición del orbital p vacio con uniones σ Alcohol terciario Alcohol alílico Alcohol bencílico Carbocationes estables S N1 formación del carbocatión captura del carbocatión por el nucleófilo v Ejemplos: Formación del cation ciclohexenilo 2 reacciones idénticas con el Bromuro Cation butenilo deslocalizado Formación del catión bencilo deslocalización Especialmente estable : tritilo Alcohol primario Cloruro de tritilo éter formación de tritil éteres SN1 lento rápido rápido Velocidades de solvólisis de cloruros de alquilo en 50% agua-etanol . Compuesto veloc. relativa primario: todo SN2 secundario: puede dar SN1 pero no muy bien Terciario: muy bueno SN1 Primario pero alílico: SN1 catión alílico secundario en un extremo alílico y terciario en un extremo Primario pero alílico y bencílico Estereoquímica de la SN1 Secundario catión butilo racémico Mecanismo SN2 Velocidad Nucleófilos con oxígeno: Nucleófilo pKa ác. conjugado velocidad SN2 rápido razonable lento lento Diagrama de energía de una reacción SN2 energía Estado de transición Nu + MeX Me-Nu + X- Progreso de la reacción La velocidad de SN2 depende de: nucleófilo esqueleto carbonado grupo saliente Grupos salientes en una reacción SN2 Haluro en MeX pKa del HX velocidad de reacción con NaOH muy lento moderado rápido muy rápido Grupos salientes en SN1 y SN2 Haluro Fluoruro Cloruro Bromuro ioduro fuerza unión C-X pKa de HX Un mismo compuesto según las condiciones puede reaccionar por los dos mecanismos SN 2 paso determinante de la velocidad paso determinante de la velocidad rápido SN 1 Velocidad de reacción de nucleófilos con PhCH2S+PH2 Nucleófilo velocidad Los tres primeros SN1 Los otros dos SN2 Velocidad relativa de reacción ( agua=1)de nucleófilos con MeBr Nucleófilo velocidad Todos SN2 estructura Tipo metil primario secundario terciario SN1? no no si bueno SN2? bueno bueno si no + rápida Velocidades relativas de reacción con CH3Br en Etanol Nucleofilo X pKa HX veloc. relativa Velocidades relativas de reacción con CH3Br en Etanol Nucleofilo X pKa HX veloc. relativa I- menos básico pero más grande y más polarizable; F- más solvatado Efecto del solvente solvatación de sales por solventes polares próticos Hay más de una molécula de solvente para cada ión sal Catión solvatado por donación de e- del O Anión solvatado por aceptar e- por puente H solvatación de sales por solventes apróticos sal Catión solvatado por donación de e- del O Anión no solvatado desnudo reordenamientos Migración de metilo reordenamie nto