Citrato y calculos renales - Calculos Renales Ecuador. No Mas
Anuncio

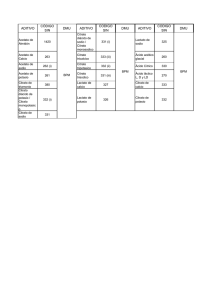
( OXALATO de CALCIO ) ( ÁCIDO ÚRICO ) =0 No más cálculos Mineral Electrolyte Metab. 13: 257-266 (1987) CITRATO Y CÁLCULOS RENALES Charles Y. C. Pak Sección de metabolismo mineral, Southwestern Medical School, University of Texas Health Science Center at Dallas. Tex. USA. Palabras clave: Citrato, Citrato de Potasio, Cálculos renales, Acidosis tubular renal, Hipocitraturia, Nefrolitiasis, Oxalato de calcio, Litiasis por ácido úrico. Abstracto: El citrato de potasio es una nueva y prometedora opción terapéutica que ha ampliado nuestra capacidad para el control clínico de la enfermedad litiásica renal. La discusión sumariza los datos que avalan la utilidad del citrato de potasio en el manejo de la acidosis tubular renal con cálculos de calcio, la nefrolitiasis hipocitratúrica por oxalato de calcio (idiopática o secundaria a síndrome diarreico crónico o terapéutica con tiazidas) y la litiasis por ácido úrico con o sin cálculos de calcio. Razonamiento para la terapéutica con citrato de potasio Muchas condiciones, tales como la acidosis tubular renal por cálculos de calcio, nefrolitiasis hipocitratúrica por oxalato de calcio y la litiasis por ácido úrico con o sin cálculos de calcio, se caracterizan por hipocitraturia y un pH inusualmente bajo. Estos descalabros fisiológicos predisponen al entorno urinario a favorecer la cristalización de las sales de calcio y ácido úrico, y por tanto contribuyen en la formación de cálculos. El razonamiento para el uso de citrato de potasio está basado en la capacidad de este tratamiento de sobreponerse a los disturbios fisiológicos y al marco fisicoquímico anormal antes descritos. Con la intención de aclarar este concepto, se proporcionará una breve descripción de la fisicoquímica de la formación de cálculos y los efectos del citrato y pH sobre el proceso de cristalización. Físico química de la formación de cálculos. La formación de cálculos comienza con la formación de un nido de cristal seguido del crecimiento del nido hacia un cálculo macroscópico por crecimiento de los cristales, agregación de cristales y crecimiento epitaxial. La nucleación es el mecanismo por el cual se forma un nido de cristal. Puede ser homogéneo cuando el cristal se forma de novo, o heterogéneo cuando se produce material cristalino heterólogo. El crecimiento del cristal representa su crecimiento sobre el nido de igual composición química, donde el término epitaxial hace referencia al “sobrecrecimiento” de material cristalino heterólogo. La agregación de cristales describe el proceso mediante el cual los cristales preformados se agregan a grupos grandes [1]. Actualmente disponemos de técnicas para cuantificar los diferentes pasos en la formación de los cálculos. El rango de saturación relativa (RSR) [2] provee una medida estimada de la saturación urinaria. El rango calculado del producto de actividades iónicas en la orina (ej. iones de oxalato y calcio), el producto de la solubilidad termodinámica (representa el producto de actividad en equilibrio en un medio sintético que contiene una fase sólida) sugiere el rango de saturación relativa. El rango de actividad de productos (RAP) [3], otra medida de saturación urinaria, es obtenida incubando una muestra de orina hasta el “equilibrio” con una fase sintética sólida contra la cual se mide el estado de saturación. El rango de actividad de productos, antes y después de la incubación, representa el estado de saturación. Mayor a 1 denota súper saturación y menor a 1 sub saturación. 1 El rango de formación de productos (RFP) [3] es el menor estado de súper saturación en el que se inicia la nucleación, y por tanto define el límite metaestable. Usado principalmente en estudios bien controlados, el RFP es el número de veces que la muestra de orina debe ser sobresaturada para permitir la precipitación espontánea. Un score discriminante (SD) RFP-RAP [4] provee una medida cuantitativa de la propensión a la nucleación espontánea. El SD refleja tanto la saturación (RAP) como la actividad inhibitoria (RFP), y por tanto es una medida para determinar la posibilidad de nucleación espontánea, donde los valores positivos representan una propensión incrementada y los valores negativos una propensión disminuida. El incremento permisible (IP) de oxalato [5] provee una versión más simple que el SD en la estimación de la nucleación espontánea de oxalato de calcio. Este representa la cantidad mínima de oxalato adicional (como oxalato de sodio soluble) que puede ser agregado a la orina (desarrollo de cristales), antes de que se inicie la precipitación espontánea de oxalato de calcio a las 3 horas. La concentración de acido úrico no disociado [6] da una medida de la saturación de ácido úrico. Es mayor a pH bajo, particularmente por debajo de la constante de disociación con pH 5.5. Usando las definiciones descritas arriba, la formación de cálculos, así como su prevención, podrían ser cuantificadas (Tabla I). Tabla I Cuantificacion de la formación de cálculos y prevención Parámetro Medición RAP RSR RFP RFP-RAP SD saturación saturación límite metaestable posibilidad de nucleación espontánea posibilidad de nucleación espontánea PI Cálculo Formación incremento incremento disminución incremento Prevención disminución disminución incremento disminución disminución incremento La formación de cálculos podría ser facilitada cuando la saturación urinaria es alta o sobresaturada (incremento de RAP y RSR), el límite metaestable es bajo (RFP bajo) o si hay un incremento de posibilidades de nucleación espontánea (SP alta o IP baja). Alternativamente, la formación de cálculos puede ser prevenida mediante el uso de medidas para reducir la saturación urinaria, incrementar el límite metaestable o reducir la propensión de nucleación espontánea. Efectos fisicoquímicos del citrato y el pH. El citrato es un inhibidor bien conocido de la cristalización de las sales de calcio. Primero, el citrato disminuye la concentración de calcio iónico mediante la unión en complejos y por tanto reduce la saturación de oxalato de calcio y fosfato de calcio (en este caso sí el pH no está alterado). Segundo, el citrato inhibe directamente la nucleación espontánea de oxalato de calcio y brucita (CaHPO4-2H2O). En una solución artificial, la adición de citrato incrementó significativamente la formación de productos, e incrementó permisivamente ambas sales de calcio. 2 Los pH extremos incrementan el riesgo de formación de cálculos. Un ambiente urinario inusualmente ácido (pH < 5.5) puede ser asociado a litiasis por ácido úrico debido a la predominancia de ácido úrico no disociado; la disociación constante del ácido úrico comienza a una pH 5.47 [8]. Por otra parte, una pH inusualmente alto (>7) favorece la formación de cálculos de fosfato de calcio (apatita) debido al incremento de la disociación del fosfato, especialmente si hay presencia de hipercalciuria y el pH urinario alto no se acompaña de un incremento de la actividad inhibitoria. En general, el mantenimiento de un pH urinario entre 6 y 7 es deseable para el control de la litiasis por ácido úrico y la nefrolitiasis por oxalato de calcio. En tal rango de pH, la concentración de ácido úrico no disociado se espera sea baja debido a que la mayoría del ácido úrico estaría disociada [8]. A dicho pH, habría un reforzamiento de la actividad inhibitoria de citrato y pirofosfato debido a que la mayoría de ellos estaría en su forma de iones activos. Aun, las concentraciones de calcio ionizado disminuyen a medida que el pH incrementa, debido al refuerzo de la disociación de fosfato y citrato, y la formación de complejos de calcio por estos aniones, reduciendo así la saturación de oxalato de calcio. Ocurrencia frecuente de hipocitraturia en nefrolitiasis. Hay numerosos reportes que demuestran que el citrato urinario está disminuido en pacientes con nefrolitiasis[9-11], variando entre 19 a 63%. En el estudio de Dallas[17], la hipocitraturia se presentó sola en 5% de los pacientes y coexistió con otras anormalidades en 50% de los pacientes. La hipocitraturia fue un resultante de la acidosis tubular renal, acidosis metabólica adquirida por estados diarreicos crónicos, la hipokalemia inducida por tiazidas o de causas desconocidas (idiopática). En el caso de la hipocitraturia, la formación de los cálculos de calcio (tanto de oxalato de calcio como de fosfato de calcio) está incrementada, debido a la reducción en la acción protectiva del citrato previamente citado. La saturación urinaria de oxalato de calcio y fosfato de calcio se incrementa debido a la reducción en la formación de complejos de citrato de calcio. El proceso de cristalización de ambas sales de calcio se vería facilitado debido a la pérdida de la actividad inhibidora directa del citrato. De la discusión precedente, queda claro que un ambiente inusualmente ácido y la hipocitraturia son contribuyentes en la formación de cálculos de ácido úrico y de sales de calcio, respectivamente. Por otro lado, aparentemente las maniobras que mantienen el pH entre 6 y 7, y que incrementan el citrato urinario a niveles normales, serían deseables para la prevención de la formación de cálculos tanto de ácido úrico como de oxalato de calcio, sin exagerar la formación de cálculos de fosfato de calcio. Hay amplia evidencia que indica que el tratamiento con citrato de potasio cubre este propósito de manera óptima. Efectos fisiológicos y fisicoquímicos del citrato de potasio. Acción fisiológica del citrato de potasio. Efecto sobre el pH urinario y el citrato. En todos los 8 estudios a corto plazo [12-16], la terapéutica con citrato de potasio (30-80 mEq/d) incrementó de manera significativa el pH urinario y el citrato (Tabla II). El pH urinario se mantuvo entre 6 y 7 durante el tratamiento, excepto en la acidosis tubular renal. El citrato urinario estuvo dentro del rango normal y se aproximó a una media de 640 mg/d, luego del tratamiento. En 89 pacientes sometidos a tratamientos a largo plazo, el citrato de potasio (30-100 mEq/d) causó un incremento significativo sostenido en el pH urinario y el citrato [17]. Durante el tratamiento, el pH urinario se mantuvo en una media de 6.5 y el citrato urinario promedio se mantuvo entre 400-700 mg/d, dentro de límites normales. 3 La hipokalemia resultantes de la terapia con diuréticos tiazídicos podría causar hipocitraturia, probablemente debido a que podría causar acidosis intracelular [12], y por tanto podría atenuar el efecto benéfico hipocitratúrico de este tratamiento en la formación de cálculos renales [16-18]. Tabla II. Efecto de la terapeutica con citrato de potasio en el pH urinario y citrato Estudio Pak et al. [13] Pak et al. [13] Sakhaee et al. [14] Nicar et al. [12] Preminger et al. [15] Pak et al. [16] Nicar et al. [35] Griffith [36] Pacientes Ambiente 5 12 5 13 9 13 28 49 metabólico ambulatorio metabólico ambulatorio metabólico ambulatorio ambulatorio ambulatorio Tratamiento dosis mEq/d 60 60-80 60 30-60 60-80 30-60 60 30-60 Duración del tratamiento antes 1 semana 1-15 meses 4 semanas > 1 semana 3-8 meses 4 meses 1 semana 4 meses 5.57 ± 0.36 5.35 ± 0.18 5.84 ± 0.49 6.47 ± 0.28 6.21 ± 0.39 5.94 ± 0.51 - pH urinario después de citrato de potasio 6.56 ± 0.44*** 6.68 ± 0.14*** 6.66 ± 0.27*** 7.05 ± 0.16*** 6.61 ± 0.34*** 6.77 ± 0.39*** - Citrato urinario mg/d antes después de citrato de potasio 579 ± 227 203 ± 119 398 ± 119 243 ± 147 221 ± 163 284 ± 105 387 ± 151 325 ± 255 1.012 ± 194** 739 ± 228*** 856 ± 103*** 636 ± 218*** 494 ± 304*** 547 ± 213*** 749 ± 272*** 658 ± 331*** Los valores de pH y citrato urinario fueron dados como promedios ± DS. Las diferencias significativas antes y después de la fase de tratamiento con citrato de potasio, obtenidas por pruebas T pareadas se muestran con ** para p< 0.01 y *** para p< 0.001 Se ha sugerido que el citrato de potasio podría ser menos efectivo que el cloruro de potasio en la corrección de la hipokalemia inducida por los diuréticos tiazídicos, debido a la pobre reabsorción de citrato a nivel de los túbulos renales [19]. Sin embargo, en 13 pacientes con nefrolitiasis por oxalato de calcio que tomaban tiazidas y fueron randomizados a citrato de potasio y cloruro de potasio a dosis equivalentes [12], el citrato de potasio fue igual de efectivo que el cloruro de potasio en la corrección de hipokalemia inducida por tiazidas. Además, la adición de citrato de potasio a la terapéutica tiazídica incrementa el pH urinario y los niveles de citrato [12,16]. Otros efectos bioquímicos del citrato de potasio. Durante terapia a corto plazo (menos de un mes), la terapéutica con citrato de potasio redujo el calcio urinario en pacientes con litiasis por ácido úrico o nefrolitiasis idiopática por oxalato de calcio [14]. Sin embargo, con terapia continua, este efecto hipocalciúrico se desvanecía. En pacientes con acidosis tubular renal la terapia con citrato potásico causó una reducción sostenida del calcio urinario [15]. El potasio urinario se incrementó en un monto (40-70 mEq/d) que se aproximaba a la cantidad de potasio contenida en la medicación durante tratamientos a corto plazo [14] y largo plazo [17]. El amonio urinario disminuyó significativamente durante el tratamiento con citrato de potasio de 30.1 +/- 7.8 a 9.7 +/- 3.6 mEq/d (p< 0.001), reflejando la entrega de una carga alcalina [14]. En estudios metabólicos [14] en los que la ingesta de líquidos se mantuvo constante, la terapia con citrato de potasio no modificó los volúmenes urinarios ni los niveles de oxalato, fósforo, sodio, magnesio, sulfato o ácido úrico. En un estudio a largo plazo de 89 pacientes conducido en un ambiente ambulatorio [17], el volumen urinario promedio aumentó durante la terapéutica con citrato de potasio; sin embargo, este cambio no fue significativo durante la mayoría de periodos de tratamiento. No se observó cambios significativos o consistentes en el ácido úrico urinario, oxalato, sodio o fósforo. 4 Acciones fisicoquímicas del citrato de potasio. Efecto sobre la cristalización del oxalato de calcio. En estudios a corto plazo, el citrato potásico redujo significativamente la saturación urinaria del oxalato de calcio (Tabla III). Tabla III. Efecto de la terapeutica con citrato de potasio en la saturación urinaria de oxalato de calcio Estudio Sakhaee et al. [14] Preminger et al. [15] Nicar et al. [12] Nicar et al. [35] Pacientes 5 9 13 28 Diagnóstico Tratamiento dosis mEq/d AU ATR TZ I 60 60-80 30-60 60 Duración del tratamiento antes Saturación despues de citrato de potasio 4 semanas 3-8 meses < 1 semana 1 semana (RAP) 3.21 ± 0.96 (RSR) 5.73 ± 2.08 (RSR) 5.66 ± 2.58 (RSR) 7.78 ± 4.97 1.69 ± 0.76** 3.14 ± 1.23*** 4.04 ± 2.05* 4.68 ± 2.64** Valores para saturación, derivados de RAP o RSR están dados como medias ± DS. La diferencia significativa producida por el citrato de potasio determinado por pruebas t pareadas, se muestra con * para p< 0.05, ** para p< 0.01 y *** para p< 0.001. En el estudio de Nicar et al [12], la fase pretratamiento esta representada por tiazidas solas, y la fase de tratamiento por citrato de potasio y tiazidas. AU: litiasis por ácido úrico; ATR: acidosis tubular renal, TZ: hipocitraturia inducida por tiazidas, I: nefrolitiasis idiopática por oxalato de calcio. Previo al tratamiento, el grupo de 89 pacientes sometidos a estudios a largo plazo [17] tuvo un RSR de oxalato de calcio significativamente superior a lo encontrado en el grupo control de 4.01 +/- 2.41 (p< 0.001, prueba T de Student). Como vemos, el entorno urinario en los pacientes que participaron en el estudio fue sobresaturado en oxalato de calcio con relación a los individuos control. Posterior al tratamiento con citrato de potasio (30-100 mEq/d), usualmente 20 mEq tres veces al día, el RSR urinario de oxalato de calcio disminuyó significativamente y se mantuvo dentro del rango encontrado en los individuos control durante el tratamiento. Por lo tanto, la terapia con citrato de potasio redujo la extensión de la sobresaturación urinaria en relación a los niveles de oxalato de calcio encontrados en sujetos normales sin litiasis renal. En un estudio agudo, el RFP de oxalato de calcio aumentó significativamente de 16.1 +/- 5.6 a 22.2 +/- 6.6 (p< 0.05) cuando se administró citrato de potasio por 4 semanas en una dosis de 60 mEq/d, indicativo de un nivel mayor de meta estabilidad [3]. La propensión de nucleación espontánea de oxalato de calcio fue reducida significativamente por el tratamiento, dado que las DS de RFP y RAP [4] disminuyeron de + 0.378 +/- 0.102 a 0.250 +/- 0.122 (indistinguible del control normal) luego del tratamiento (p< 0.001). El IP en oxalato [5] fue medido en muestras de orina de 89 pacientes en un estudio a largo plazo en Dallas [17]. Antes del tratamiento con citrato de potasio, el IP de oxalato de 35.4 +/- 30.1 mg/l fue significativamente inferior a los encontrados en individuos normales sin cálculos. Entonces, sería necesario añadir más oxalato soluble a la orina para desencadenar una precipitación espontánea de oxalato de calcio luego del tratamiento con citrato de potasio. Efectos del citrato de potasio en la cristalización de ácido úrico. La litiasis por ácido úrico está típicamente asociada con un ambiente urinario inusualmente ácido (pH < 5.5) [20]. Algunos pacientes podrían tener diátesis gotosa con hiperuricemia y gota clínica. 5 El tratamiento con citrato de potasio incrementó significativamente el pH urinario desde un valor promedio bajo de 5.3 a un superior de 5.8, pero menor a 7. Debido a esta disociación reforzada de ácido úrico resultante, la cantidad de ácido úrico no disociado disminuyó significativamente a niveles promedio encontrados en individuos normales sin cálculos (< 150 mg/d). La terapia con citrato de potasio incrementó significativamente la solubilidad del ácido úrico [6]. Resumen de las acciones fisiológicas y fisicoquímicas. El citrato de potasio es capaz de mantener el pH urinario entre 6 y 7, y el citrato urinario en niveles normales en pacientes con acidosis tubular renal, nefrolitiasis hipocitratúrica por oxalato de calcio, y litiasis por ácido úrico con o sin cálculos de calcio. En la acidosis tubular renal, este tratamiento podría disminuir el calcio urinario así como mejorar el balance de calcio. En la hipocitraturia inducida por tiazidas , la terapéutica con citrato de potasio refuerza la excreción de citrato manteniendo los electrolitos séricos normales. Los cambios bioquímicos de la terapéutica con citrato de potasio descritos arriba, resultan en la creación de un ambiente fisicoquímico normal y pobremente útil para la formación de cálculos. La cristalización de oxalato de calcio es inhibida ya que la saturación urinaria disminuye y la actividad inhibitoria aumenta. La cristalización del ácido úrico es prevenida por la disociación incrementada de ácido úrico y la disminución resultante de el ácido úrico no disociado. Estas acciones del citrato de potasio son únicas para esta sal. (Tabla IV) Tabla IV. Especificidad de la acción del citrato de potasio ph urinario Citrato Urinario Calcio urinario (agudo) Saturación urinaria Fosfato de Calcio Oxalato de Calcio Urato de Sodio Límite urinario de metaestabilidad Oxalato de Calcio Duración de la acción Efectividad de la hipocitraturia inducida por tiazidas K citrato K HCO3 larga si corta si KCI corta parcial NaCI Na3 Citrato corta no larga no Na HCO3 corta no Otras sales de potasio solubles, con componentes aniónicos que son metabolizados in vivo a alkalis, podrían tener cualitativamente acciones similares a las del citrato de potasio. El "=" significa sin cambios En términos fisiológicos y fisicoquímicos, la terapia con citrato de potasio podría ser útil en la prevención de la formación de cálculos en la acidosis tubular renal, la nefrolitiasis hipocitratúrica por oxalato de calcio y en la litiasis por ácido úrico con o sin cálculos de calcio (Tabla V). Los parámetros fisicoquímicos actuales obtenidos durante el tratamiento, se aproximan a aquellos predictivos de formación de cálculos en la Tabla I. Estudios clínicos con citrato de potasio. Respuesta clínica en indicaciones específicas. Acidosis tubular renal distal incompleta. Nueve pacientes con acidosis tubular renal distal incompleta, recibieron citrato de potasio (60-80 mEq/d) [15]. Seis pacientes no formaron posteriormente cálculos. Tres pacientes continuaron pasando cálculos. Para este análisis, los cálculos que pasaron fueron considerados como de reciente formación, aunque más parecería representar el pasaje de cálculos preexistentes [15]. 6 Tabla V Efectos fisiológicos y fisicoquímicos de la terapia con citrato de potasio Acidosis tubular renal Litiasis por ácido úrico con o sin calculos de Ca Orina pH Citrato Calcio Nefrolitiasis hipocitratúrica por oxalato de calcio incremento incremento disminución incremento incremento transitorio incremento incremento transitorio Oxalato de calcio RAP/RSR RFP RFP-RAP SD PI disminución desconocido desconocido incremento disminución desconocido desconocido incremento disminución incremento disminución incremento Acido úrico No disociado disminución disminución disminución Fosfato de calcio RAP/RSR disminución incremento incremento Usando esta asumpción, la tasa de remisión fue del 66.7%: la tasa de formación disminuyó individualmente en los nueve pacientes, y la tasa promedio de formación de cálculos del grupo disminuyó en 91.2% luego de instituida la terapéutica por citrato de potasio (Tabla VI). Tabla VI. Respuesta clínica a la terapia con citrato de potasio en indicaciones específicas Acidosis Nefrolitiasis hipocitratúrica por oxalato de calcio tubular renal Idiopático SDC Citrato de K Citrato de K combinado + Tiazidas Pacientes n. Pretratamiento duración años/paciente tasa de formación de cálculos, n/año Tratamiento duración años/paciente tasa de formación de cálculos, n/año Remision % Tasa de reduccion individual de formación de cálculos % Reduccion en la tasa de formación de cálculos pre vs post tratamiento 9 23 12 35 Litiasis por ácido úrico TZ 9 13 17 3 13.1 ± 26.6 3 1.36 ± 2.45 3 3.80 ± 9.43 3 2.20 ± 5.84 3 4.96 ± 10.7 2.09 5.12 ± 10.87 3 1.25 ± 1.71 2.20 1.15 ± 2.23* 66.7 1.74 0.14 ± 0.55** 87.0 1.67 0.81 ± 2.82** 91.7 1.71 0,42 ± 1,72* 88.6 3.07 0,57 ± 1.34** 66.7 1.76 0,77 ± 1.65** 76.9 2,27 0.01 ± 0,04*** 94.4 100 100 100 100 100 100 100 91.2 89.7 78.7 80.9 88.5 85.0 99.2 En la nefrolitiasis por oxalato de calcio hipocitraturica inducida por tiazidas, los valores pretratamiento representan la terapéutica con tiazidas solas, y la fase de tratamiento indica la terapéutica combinada con tiazidas y citrato de potasio. La diferencia significativa en la tasa individual de formación de cálculos producida por le tratamiento, determinada por la prueba t de Wilcoxon se muestra con * para p< 0.05, ** p< 0.01, y *** para p< 0.001. SDC= Sindrome diarréico crónico, TZ= Tiazidas, TZ/A= Tiazidas o alopurinol. 7 Nefrolitiasis hipocitratúrica idiopática por oxalato de calcio. Esta entidad incluye la hipocitraturia ocurriendo sólo con cálculos de calcio [9], la hipocitraturia ocurriendo en conjunto con hipercalciurias renales y absortivas [21], y nefrolitiasis hiperuricosúrica por oxalato de calcio [21]. Los cálculos formados fueron predominantemente compuestas de oxalato de calcio. Durante el tratamiento con citrato, 88.6% de los pacientes estuvieron en remisión, todos los pacientes experimentaron una reducción en la tasa de formación de cálculos, y la tasa promedio de formación de cálculos del grupo disminuyó en un 80.9% (Tabla VI). Síndrome diarreico crónico. En nueve pacientes con síndrome de diarrea crónica con hipocitraturia, como en los grupos previos, fue establecida una respuesta similar favorable al tratamiento con citrato de potasio. (Tabla VI). Hipocitraturia inducida por tiazidas. Trece pacientes con nefrolitiasis hipercalciurica por oxalato de calcio (11 con hipercalciuria absortiva y 2 con hipercalciuria renal [21]) continuaron formando cálculos de calcio (principalmente de oxalato de calcio) cuando recibieron tratamiento con tiazidas (5.12 +/- 10.87 cálculos/paciente/año) [16]. Debido a que ellos tuvieron hipocitraturia (250 +/- 86 mg/d vs. 643 +/- 236 mg/d en sujetos normales), el citrato de potasio (10-20 mEq tres veces al día) fue adicionado al tratamiento en curso con tiazidas. Durante el tratamiento combinado con citrato de potasio y tiazidas, 10 pacientes dejaron de formar nuevos cálculos y los 13 tuvieron una tasa de formación reducida (Tabla VI). Litiasis por ácido úrico con o sin cálculos de calcio. En esta condición, el pH urinario es típicamente menor de 5.5., algunos pacientes con litiasis por ácido úrico pueden formar cálculos mixtos con oxalato de calcio y pueden, ocasionalmente formar cálculos con predominio de oxalato de calcio. Durante la terapéutica con citrato de potasio, la tasa de formación de nuevos cálculos disminuyó de 1.25 +/- 1.71 a 0.01 +/- 0.04 cálculos/año (p< 0.001, test x2). La remisión se experimentó en 94.4% de los pacientes, y la tasa de formación en el grupo disminuyó en 99.2% (Tabla VI). Evidencia para los efectos específicos favorables de la terapéutica con citrato de potasio. A pesar de la carencia de randomización en los estudios abiertos descritos hasta ahora [17], las siguientes líneas de evidencia sugieren que el citrato de potasio ejerce un efecto favorable específico en el curso de la enfermedad litiásica, exclusivo del efecto clínico del cálculo (alta ingesta de líquidos y modificaciones en la dieta) [22]. Prevención en la formación de cálculos en pacientes con recurrencias en otros tratamientos. Quince pacientes continuaron formando cálculos (4.9 +/- 10.1 cálculos/año) mientras se mantenían en una terapéutica convencional (tiazidas, alopurinol o conservador) [17]. La adición de citrato de potasio redujo significativamente la tasa de formación de cálculos de 0.69 +/- 1.98 cálculos/año, causó remisión en 66.7% y redujo la tasa de formación de cálculos individualmente en el 100% de los pacientes. Este efecto clínico sobre los cálculos [22] no puede todavía ser implicado, dado que el mismo tratamiento conservador basado en recomendaciones dietéticas y de hidratación fue proporcionado en la misma clínica durante la recesión de la enfermedad con tratamiento convencional, así como luego de la adición de citrato de potasio. 8 Recurrencia luego de suspendida la terapéutica. Diez pacientes (8 con nefrolitiasis hipocitratúrica por oxalato de calcio, 1 con litiasis por ácido úrico solo y 1 con cálculos de ácido úrico y calcio) requirieron la cesación de la terapéutica con citrato de potasio (2 semanas a 16 meses). En 4, el tratamiento fue reiniciado. Cinco de 10 pacientes formaron cálculos cuando el tratamiento fue suspendido. Para el grupo, la tasa de formación de cálculos disminuyó de 3.15 +/- 4.57 cálculos/paciente/año antes del tratamiento (3 años) a una cesación total de la formación de cálculos durante un promedio de 7.5 meses de tratamiento de citrato de potasio (p < 0.05). Esto se incrementó a 10.9 +/- 17.4 cálculos/paciente/año luego de la cesación de la terapéutica (promedio 4.2 meses; no diferencias significativas con el valor pretratamiento). Al reasumir la terapéutica, la formación de cálculos fue de 0.38 cálculos/paciente/año (sobre una media de 20.3 meses). Se impuso el mismo cuidado conservador en cuanto a fluidos y modificación dietética a lo largo del seguimiento (antes, durante, a la interrupción, a la reasumpsión del tratamiento). Entonces la recurrencia de formación de cálculos luego de cesada la terapéutica, sugiere un efecto específico de la droga. Superioridad del citrato de potasio sobre el tratamiento conservador. Para poder establecer el efecto del tratamiento médico específico en el efecto clínico sobre los cálculos [22], los resultados de la terapia con citrato de potasio de nuestros estudios clínicos a largo plazo [17], fueron comparados con 11 estudios publicados con terapéuticas conservadoras o placebo [22-31]. Dado que los pacientes participantes en estos estudios conservadores o con placebo tiene enfermedades litiásicas con severidad de leve a moderada, 54 pacientes con una formación de cálculos de 1 o menos/año, fueron seleccionados para ser comparados con los 89 pacientes [32]. La tasa inicial de formación de cálculos varió de 0.31 a 0.78/paciente/año en los estudios conservadores o de placebo, comparable con 0.48 a 0.75/paciente/año en los grupos de citrato de potasio. Durante el manejo conservador o con placebo, la formación de cálculos persistió entre 0.11 y 0.33/paciente/año. Sin embargo, la formación de nuevos cálculos virtualmente cesó en el grupo del citrato de potasio (0-0.06/paciente/año). La tasa de remisión fue menor durante la terapia con citrato de potasio (89-100% vs. 43-83%). El promedio de formación de cálculos del grupo disminuyó en 13-84% del valor pretratamiento cuando se aplicó un tratamiento conservador o placebo, pero disminuyó mucho más (89-100%) luego del tratamiento con citrato de potasio. Los determinantes previos fueron normalizados para todos los pacientes que participaron en el grupo de tratamiento conservador o placebo y para todos los pacientes en los cuatro grupos del citrato de potasio. La tasa de formación de cálculos antes de iniciar el tratamiento fue comparable entre los grupos combinados de tratamiento conservador y placebo (0.54 cálculos/paciente/año) y los grupos combinados de pacientes que recibieron tratamiento con citrato de potasio (0.52 cálculos/paciente/año). Durante el tratamiento con citrato de potasio, sólo dos nuevos episodios de nuevos cálculos se dieron entre los 54 pacientes, dando una tasa de formación de nuevos cálculos de 0.02 cálculos/paciente/año. Esta tasa fue sustancialmente menor que el valor de 0.25 cálculos/paciente/año del grupo de tratamiento conservador o placebo. La tasa de remisión para todos los grupos en el estudio del citrato de potasio fue de 96% mientras que solamente 61% de los pacientes con tratamiento conservador o placebo permanecieron sin cálculos. En adición, la tasa de disminución en la formación de cálculos no fue tan dramática en el grupo de tratamiento conservador o placebo (0.54 a 0.25 cálculos/paciente/año, 54% de disminución) como lo fue en el estudio de citrato de potasio, donde la tasa de formación de cálculos cayó en 96%, de 0.52 a 0.02 cálculos/paciente/año (p < 0.001). Entonces, en este grupo de pacientes con enfermedad litiásica con severidad de leve a moderada, el tratamiento con citrato de potasio virtualmente eliminó la formación de nuevos cálculos. La respuesta ampliamente superior al citrato de potasio sugiere que este tratamiento médico específico ejerce un efecto favorable adicional sobre el tratamiento clínico en la enfermedad litiásica. 9 Eliminación total de la formación de nuevos cálculos con tiazidas y citrato de potasio. En 10 pacientes con nefrolitiasis hipercalciurica por oxalato de calcio (hipercalciuria absortiva) tomando tiazidas y citrato de potasio concurrentemente [17], ninguno formó nuevos cálculos durante el tratamiento. Esta remisión del 100% es claramente superior a los estudios publicados con tiazidas que mostraban persistencia en la formación de cálculos en algunos pacientes [18, 24, 25, 28]. En la clínica de Dallas, en donde el estudio de terapia combinada de tiazidas y citrato de calcio dió un 100% de remisión [17], las tiazidas solas en un grupo similar de pacientes con nefrolitiasis hipercalciurica por oxalato de calcio, dieron una tasa de remisión de 38%. Dado que se había proporcionado las mismas medidas generales de cuidado a los pacientes en los dos grupos, la superioridad de la terapia combinada sugiere que el citrato de potasio ejerció un efecto favorable adicional. Requerimientos disminuidos de cirugía por litiasis. En 89 pacientes que participaron en un estudio a largo plazo [17], algunos pacientes requirieron cirugía para la remoción de los cálculos, antes y después del tratamiento con citrato de potasio. Todas las cirugías fueron por “emergencias”, dadas por obstrucción, sangrado intratable, dolor o fiebre. Ninguna fue efectiva. Durante los tres años previos al tratamiento, los 89 pacientes participantes en el estudio requirieron 61 cirugías para remoción de cálculos (45 abiertas, 16 canastas). Durante un promedio de 2 años de tratamiento con citrato de potasio, solo se requirió 10 cirugías (8 abiertas, 2 canastas), todas por cálculos, las cuales ya estaban presentes cuando se inició el tratamiento [17]. Los resultados obtenidos apoyaron la evidencia de que el tratamiento con citrato de potasio inhibe la formación de nuevos cálculos. Disolución de los cálculos de calcio existentes. En aproximadamente 40 pacientes con nefrolitiasis de calcio presente, la terapia con citrato de potasio (> 9meses) causó una reducción de la masa del cálculo, lo cual no siempre era cuantificable por el paso de los cálculos [33]. Seguridad Examen endoscópico de la mucosa gastrointestinal alta. Aunque no hay literatura sobre los efectos adversos de una preparación sólida de citrato de potasio, McMahon et al. [34] encontró una ocurrencia más frecuente de lesiones mucosas del tracto gastrointestinal alto luego de la ingesta de cloruro de potasio de liberación lenta. El estudio en Dallas [17], realizado en 30 voluntarios normales, fue randomizado, doble ciego. Los sujetos eran adultos saludables de cualquier sexo, sin antecedentes de enfermedad gastrointestinal o uso de medicaciones ulcerogénicas. Luego de una endoscopía de evaluación, los sujetos sin o con una enfermedad de la mucosa incipiente fueron randomizados para recibir SlowK (96 mEq/d), Urocit (95 mEq/d) o placebo. Las drogas de estudio fueron administradas tres veces al día, una antes de cada comida, por una semana, con glicopirrolato (2 mg tres veces al día). Los sujetos fueron tratados como ambulatorios. La calificación en este estudio fue realizada por dos endoscopistas quienes mantuvieron scores separados y no se consultaron el uno al otro. La calificación era la siguiente: 0 = no lesión, 1 = eritema, 2 = eritema y friabilidad, 3 = erosiones, exudado o sangrado, 4 = úlcera o úlceras. Cada paciente era examinado en 10 sitios anatómicos diferentes. El score de cada área era sumado, y luego se añadieron los scores de ambos endoscopistas. 10 Cuarenta y dos voluntarios fueron analizados para proveer los 30 sujetos de estudio, 10 en cada grupo. Para resumir, de los 10 pacientes de Urocit, 8 mostraron lesiones en la endoscopía postestudio. Cuatro sujetos mostraron erosiones y ninguno úlceras. El score total fue de 63. En el grupo de SlowK, 7 pacientes tuvieron lesiones, 5 erosiones y ninguno úlceras. El score total fue de 75. En el grupo placebo hubo 1 paciente con una lesión menor, ninguno tuvo erosiones ni úlceras. El score total fue de 5. En este estudio el Urocit parecía ser tan imitativo como el SlowK. Ambas drogas fueron considerablemente más imitativas que el placebo. El estudio fue repetido con un protocolo ligeramente diferente. Los sujetos reclutados fueron 7 pacientes en el grupo de SlowK y 8 pacientes en el grupo de Urocit, quienes mostraron lesiones en la mucosa en el primer estudio. El único sujeto con alteraciones gástricas del grupo de placebo no fue incluido. Los sujetos recibieron la misma droga que recibieron inicialmente, pero no se uso glicopirrolato. En la endoscopia de evaluación inicial, 2 individuos del grupo de Urocit tuvieron lesiones mucosas antes de recibir la droga. Ambos refirieron exposición a drogas ulcerogénicas (1 fue expuesto a agente antiinflamatorio no esteroidal y 1 a una dosis inusual de alcohol), ellos fueron descartados, entonces fueron seis pacientes en el grupo de Urocit y siete en el de SlowK quienes completaron el estudio. Esta vez los 6 pacientes del grupo de Urocit tuvieron lesiones, pero solo 1 tuvo erosiones; no hubo úlceras, el score total fue de 36. En el grupo de SlowK, los 7 sujetos tuvieron lesiones. Dos tuvieron erosiones, y no hubo úlceras, el score total fue de 37. Los scores en cada grupo fueron reducidos significativamente con relación a los previos con glicopirrolato. Entonces, el potencial irritativo de Urocit parece ser similar al de SlowK. Reacciones adversas Veintidós de 81 pacientes (27.2%) tomando citrato de potasio líquido (en agua), y 7 de 75 pacientes (9.3%) tomando citrato de potasio sólido (Urocit) mostraron efectos adversos gastrointestinales (diarrea, indigestión, nausea, pirosis). Ningún paciente refirió melena. Estudios de sangre oculta en heces (Hemoccult test) fueron negativos en los 59 pacientes que tomaron Urocit en quienes el test fue realizado. Entre los 89 pacientes participantes en el estudio a largo plazo en Dallas, no se observó ningún cambio significativo en la cuenta reticulocitaria en sangre venosa, calcio sérico o aclaramiento de creatinina. Hubo un leve incremento en el hematocrito de sangre venosa, potasio sérico y dióxido de carbono durante algunos periodos de tratamiento; sin embargo, estos valores permanecieron dentro de límites normales. No se observó cambios significativos en otros índices celulares en sangre, hierro sérico, fósforo, sodio, cloro, albúmina, proteínas totales, bilirrubina, deshidrogenasa láctica, glutamato-oxaloacetato, transaminasas o fosfatasa alcalina. Referencias 1. Pak, C. Y. C.: Calcium urolithiasis: pathogenesis, diagnosis and management. pp. 5-36 (Plenum Press. New Cork 1978). 2. Pak, C. Y. C.; Havashi, Y.; Finlyson, B.; Chu, S.: Estimation of the state of saturation of brushite and calcium oxalate in urine: A comparison of three methods. J. Lab. Clin. Med. 89: 891-901 (1977). 3. Pak, C. Y. C.; Holt, K.: Nucleation and growth of brushite and calcium oxalate in urine of stone formers. Metabolism 25; 665-673 (1976). 4. Pak, C. Y. C.; Galosy, R. A.: Urinary FPR-APR discriminant store for the quantitative assessment of the propensity for spontaneous nucleation of calcium oxalate. Am. J. Med. 69: 681-689 (1980). 5. Nicar, M. J.; Hill, K,; Pak, C. Y. C.: A simple technique for assessing the propensity for crystallization of calcium oxalate and brushite in urine from the increment in oxalate of calcium necessary to elicit precipitation. Metabolism 32; 906-910 (1983). 6. Pak, C. Y. C.; Sakhaee, K.; Fuller, C.: Successful management of Eric acid of nephrolithiasis with potassium citrate. Kidney int. (in press). 7. Pak, C. Y. C.; Nicar, M.; Northcutt, C.: The definition of the mechanism of hypercalciuria is necessary for the treatment of recurrent stone formers. Contr. Nephrol., vol 33, pp. 136-151 (Karger, Basel 1982). 8. Finlayson, B.; Smith, A. : Stability of first dissociable proton of uric acid. J. chem. Engng. Data 19: 94-97 (1974). 9. Nicar, M. J.; Skurla, C.; Sakhaee, K.; Pak, C. Y. C.: Low urinary citrate excretion in nephrolithiasis. Urology 21: 8-14 (1983). 10. Menon, M.; Khalifa, M. S.; Mahle, C.J.: Urinary citrate excretion is decreased in patients with renal calculi (Abstract). Am. Urol. Ass. Abstr. 365, 169 (1982). 11. Schwille, P. O.; Schotz, D.; Schwille, K.; Leutsebalt, R.; Goldberg, E.; Sigel, A.: Citrate in urine and serum and associated variables in subgroups of urolithiasis. Nephron, 31: 194-202 (1982). 11 12. Nicar, M. J.; Peterson, R.; Pak, C. Y. C.: Use of potassium citrate as potassium suplement during thiazide therapy of calcium nephrolithiasis. J. Urol. 131: 430-433 (1984). 13. Pak, C. Y. C.; Skurla, C.; Brinkley, L.; Sakhaee, K.: Augmentation of renal citrate excretion by oral potassium citrate administration: time course, dose frequency Schedule, and dose-response relationship. J. clin. Pharm. 24: 19-26 (1984). 14. Sakhaee, H.; Nicar, M.; Hill, K.; Pak, C. Y. C.: Contrasting effects of potassium citrate and sodium citrate therapies on urinary chemistries and crystallization of stone-forming salts. Kidney int. 24; 348-352 (1983). 15. Preminger, G.,; Sakhaee, H.; Skurla, C.; Pak, C. Y. C.: Prevention of recurrent calcium stone formation with potassium citrate therapy in patients with distal renal tubular acidosis. J. Urol. 134: 20-23 (1985). 16. Pak, C. Y. C.; Peterson, R.; Sakhaee, K.; Fuller, C.; Preminger, G.; Reisch, J.: Correction of hypocitraturia and prevention of stone formation by combined thiazide and potassium citrate therapy in thiazide unresponsive hypercalciuric nephrolithiasis. Am. J. Med. 134: 11-19 (1985). 17. Pak, C. Y. C.; Fuller, C.; Sakhaee, K.; Preminger, G.; Britton, F.: Long-term treatment of calcium nephrolithiasis with potassium citrate. J. Urol. 134: 11-19 (1985) 18. Yendt, F.R.; Cohanim, M.: Prevention of calcium stones with thiazides. Kidney int. 13: 397-409 (1978). 19. Kassirer, J. P.; Berkman, P. M.; Lawrenz, D.R.; Schwartz, W. B.: The critical role of chloride in the correction of hypokalemic alkalosis in man. Am. J. Med. 38: 172-189 (1965). 20. Pak, C. Y. C.: Renal calculi in Wyngarden, Smith, Plum, Cecil textbook of medicine. 89th ed. pp. 628-633 (Saunders, Philadelphia 1985). 21. Pak, C. Y. C.; Britton, F.; Peterson, R.; Ward, D.; Northcutt, C.; Brestau, N. A.; McGuire, J.; Sakhaee, K.; Bush, S.; Nicar, M.; Norman, D. A.; Peters, P.: Ambulatory evaluation of nephrolithiasis. Classification, clinical presentation and diagnostic criteria. Am. J. Med. 69: 19-30 (1980). 22. Hosking, D. H.; Ericsson, S. B.; Van der Berg, C. J.; Wilson, D. M.; Smith, L. H.: The stone clinic effect in patients with idiopathic calcium urolithiasis. J. Urol. 130: 1115-1118 (1983). 23. Etlinger, B.: Recurrent nephrolithiasis: natural history and effect of phosphate therapy. A double-blind controlled study. Am. J. Med. 61: 200-206 (1976). 24. Coe, E. L.: Treated and untreated recurrent calcium nephrolithiasis in patients with idiopathic hypercalciuria, hyperuricosuria, or no metabolic disorder. Ann. intern. Med. 87: 404-410 (1977). 25. Brocas, P.; Dahl, C.; Wolf, I. L.: Do thiazides prevent recurrent idiopathic renal calcium stones? Lancet ii: 124-125 (1981). 26. Johansson, G.; Backman, U.; Danielson, B. G.;Fellstrom, B.; Ljungball, S.; Wikstrom, B.: Biochemical and clinical effects of the prophylactic treatment of renal calcium stones with magnesium hydroxide. J. Urol. 124: 770-774 (1980). 27. Ljungball, S.; Backman, U.; Danielson, B. G.; Fellstrom, B.; Johanson, G. Wikstrom, B.; Walinder, O.: Experiences with long-term use of sodium cellulose phosphate for prevention of renal calcium stones: in Smith, Robertson, Finlayson, Urolithiasis: clinical and base research. pp 275-282 (Plenum Press. New York 1981). 28. Scholz, D.; Schwille, P. O.; Sigel, A.: Double-blind study with thiazide in recurrent calcium lithiasis. J. Urol. 128: 903-907 (1982). 29. Etlinger, B.; Citton, J. T.; Tang, A.; Dolman, L.; Livermore, B.: controlled studies in stone prophylaxis: comparison of placebo versus allopurinol/chlortalidone/magnesium hydroxide: in Cohn, Potts, Fujita, Endocrine control of bone and calcium metabolism. pp. 128-129 (Elsevier, Ámsterdam 1984). 30. Ulmann, A.; Clavel, J.; Sayeg, F.: A prospective study of the efficacy on stone recurrence of water diuresis alone or associated with thiazide or phosphate therapy: in Cohn, Potts, Fujita, Endocrine control of bone and calcium metabolism. pp. 134-135 (Elsevier, Ámsterdam 1984). 31. Wikstrom, B.; Backman, U.; Danielson, B. G.; Fellstrom, B.; Johansson, G.; Ljunghall, S.; Wide, U.: Long-term phosphate treatment in calcium urolithiasis: in Cohn, Potts, Fujita, Endocrine control of bone and calcium metabolism. pp. 136-137 (Elsevier, Ámsterdam 1984). 32. Preminger, G. M.; Harvey, J. A.; Pak, C. Y. C.: Comparative efficacy of “specific” potassium citrate therapy vs. conservative management in nephrolithiasis of mild-moderate severity J. Urol. 134: 658-661 (1985). 33. Pak, C. Y. C.; Sakhace, K.; Fuller, C. J.: Physiological and physicochemical prevention of calcium stone formation by potassium citrate therapy. Trans. Ass. Am. Physns. 96: 294-305 (1983). 34. McMahon, E. G.; Ryan, J. R.; Akdamar, K.; Ertam, A.: Effect of potassium chloride supplements on upper gastrointestinal mucosa. Clin. Pharmacol. Ther. 35: 852-855 (1984). 35. Nicar, M. J.; Hsu. M. C.; Fetner, C.: Urinary response to oral potassium citrate therapy for nephrolithiasis in a private practice setting. Clin. Therapeutics. 8: 219-225 (1986). 36. Griffith, D.: Personal communication. Charles Y. C. Pak, MD. Section on Mineral Metabolism. Southwestern Medical School. University of Texas. Health Sciences Center at Dallas. Dallas, TX 75235 (USA). 12 DOSIS: 1 tableta 2 veces al día