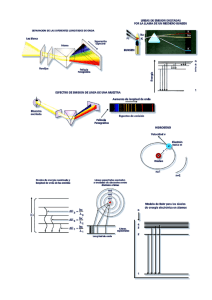
EL CARBONO: ALOTROPÍA Y OTRAS CARACTERISTICAS OBJETIVO: El estudiante analizara las características del átomo de carbono para comprender la gran cantidad de compuestos orgánicos que forma CARACTERISTICAS DEL ATOMO DE CARBONO SIMBOLO GRUPO C IV A ELECTRONES DE VALENCIA NUMERO ATOMICO (Z) TIPO DE ELEMENTO NO METAL C 4 CONFIGURACION ELECTRONICA BASAL 1s2 2s2 2px1 2py1 2pz0 -C- 12 6 ESTRUCTURA DE LEWIS MASA ATOMICA (A) FORMAS ALOTRÓPICAS DIAMANTE, GRAFITO, FULLERENO, NANOTUBOS CONFIGURACION ELECTRONICA EXCITADO 1s2 2s1 2px1 2py1 2pz1 ENLACES QUE FORMA C= =C= -C EL CARBONO EN LA NATURALEZA LAS HIBRIDACIONES DEL ATOMO DE CARBONO OBJETIVO: El estudiante comprenderá la geometría que presentan los estados híbridos del átomo de carbono y sus tipos de enlace. HIBRIDACION SP3 Se dice que se produce una hibridación sp3 en el átomo de carbono, cuando sus orbitales 2s, 2px, 2py y 2pz se mezclan o hibridizan formando cuatro orbitales híbridos sp3. Estos orbitales híbridos tendrán la misma forma y la misma energía, por ello se dice, que son equivalentes. La hibridacion sp3 es característica de los alcanos (enlace sencillo). Presentan un arreglo geométrico tetraédrico y sus ángulos de enlace son de 109.5o. HIBRIDACION SP2 En este tipo de hibridación se mezclan el orbital 2s y los orbitales 2px y 2py, quedando el orbital 2pz sin hibridizar. 2s 2pz 2px 2py La hibridación sp2 es característica de los alquenos (enlace doble), ella nos permite explicar sus características químicas, su geometría trigonal y los ángulos de enlace de 120°. Los tres orbitales híbridos sp2 son usados por el átomo de carbono para formar tres enlaces sigma (σ) y el orbital pz puro para formar el enlace pi (π). (π) (σ) ENLACE SIGMA (σ): Se forma por la unión frontal de dos orbitales híbridos. ENLACE PI (π): Se forma por la unión lateral de dos orbitales “p” puros HIBRIDACION SP En este tipo de hibridación, se mezclan el orbital 2s con el orbital 2px, quedando los orbitales 2py y 2pz puros sin hibridizar. La hibridación sp es característica de los alquinos (enlace triple), ella nos permite explicar sus características químicas, su geometría lineal y los ángulos de enlace de 180°. Estructura de Lewis Las estructuras de Lewis se utilizan para representar mediante puntos o cruces, los electrones de valencia de un átomo o los electrones compartidos entre los átomos al formar un enlace covalente. El átomo de carbono se representa así: En el tema de hibridación planteamos que el átomo de carbono utiliza sus 4 electrones externos para formar enlaces covalentes simples, dobles y triples. Concatenación La concatenación es una de las razones principales para que existan demasiados compuestos del carbono. A la característica que presenta el átomo de carbono de unirse consigo mismo, se le denomina concatenación. El átomo de carbono se puede unir formando cadenas abiertas o cerradas, con enlaces simples, dobles o triples. LOS COMPUESTOS ORGANICOS