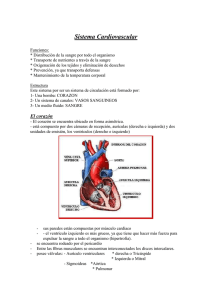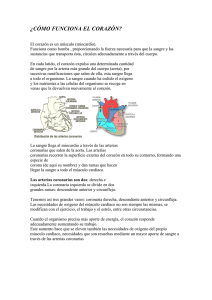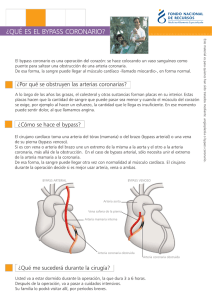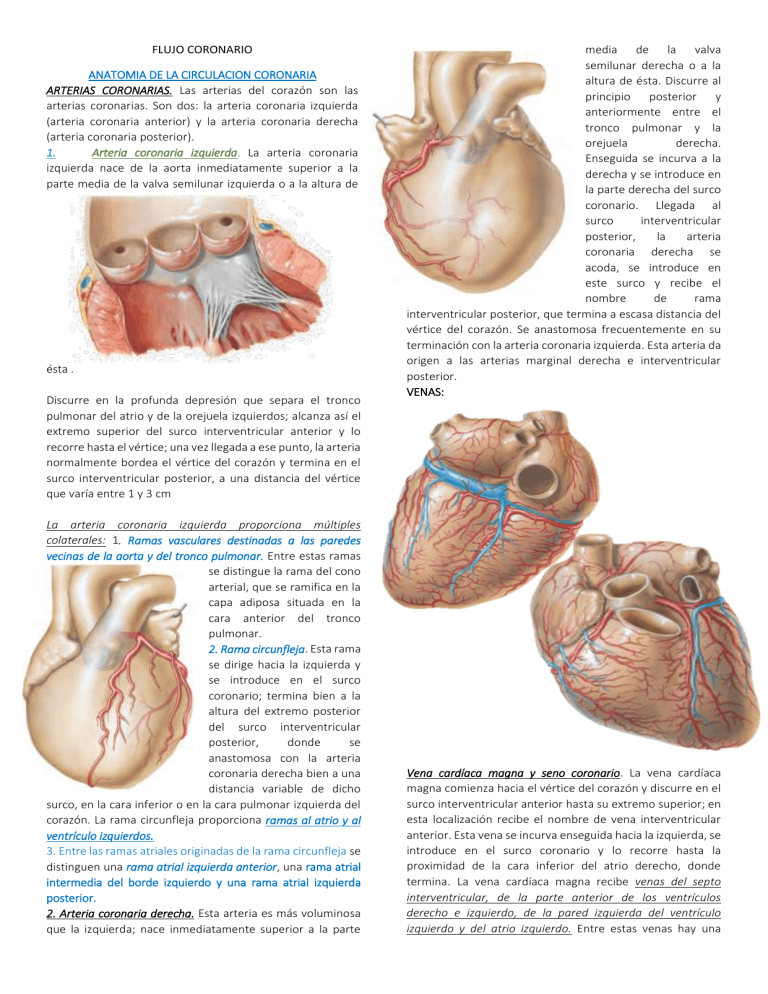
FLUJO CORONARIO ANATOMIA DE LA CIRCULACION CORONARIA ARTERIAS CORONARIAS. Las arterias del corazón son las arterias coronarias. Son dos: la arteria coronaria izquierda (arteria coronaria anterior) y la arteria coronaria derecha (arteria coronaria posterior). 1. Arteria coronaria izquierda. La arteria coronaria izquierda nace de la aorta inmediatamente superior a la parte media de la valva semilunar izquierda o a la altura de ésta . Discurre en la profunda depresión que separa el tronco pulmonar del atrio y de la orejuela izquierdos; alcanza así el extremo superior del surco interventricular anterior y lo recorre hasta el vértice; una vez llegada a ese punto, la arteria normalmente bordea el vértice del corazón y termina en el surco interventricular posterior, a una distancia del vértice que varía entre 1 y 3 cm La arteria coronaria izquierda proporciona múltiples colaterales: 1. Ramas vasculares destinadas a las paredes vecinas de la aorta y del tronco pulmonar. Entre estas ramas se distingue la rama del cono arterial, que se ramifica en la capa adiposa situada en la cara anterior del tronco pulmonar. 2. Rama circunfleja. Esta rama se dirige hacia la izquierda y se introduce en el surco coronario; termina bien a la altura del extremo posterior del surco interventricular posterior, donde se anastomosa con la arteria coronaria derecha bien a una distancia variable de dicho surco, en la cara inferior o en la cara pulmonar izquierda del corazón. La rama circunfleja proporciona ramas al atrio y al ventrículo izquierdos. 3. Entre las ramas atriales originadas de la rama circunfleja se distinguen una rama atrial izquierda anterior, una rama atrial intermedia del borde izquierdo y una rama atrial izquierda posterior. 2. Arteria coronaria derecha. Esta arteria es más voluminosa que la izquierda; nace inmediatamente superior a la parte media de la valva semilunar derecha o a la altura de ésta. Discurre al principio posterior y anteriormente entre el tronco pulmonar y la orejuela derecha. Enseguida se incurva a la derecha y se introduce en la parte derecha del surco coronario. Llegada al surco interventricular posterior, la arteria coronaria derecha se acoda, se introduce en este surco y recibe el nombre de rama interventricular posterior, que termina a escasa distancia del vértice del corazón. Se anastomosa frecuentemente en su terminación con la arteria coronaria izquierda. Esta arteria da origen a las arterias marginal derecha e interventricular posterior. VENAS: Vena cardíaca magna y seno coronario. La vena cardíaca magna comienza hacia el vértice del corazón y discurre en el surco interventricular anterior hasta su extremo superior; en esta localización recibe el nombre de vena interventricular anterior. Esta vena se incurva enseguida hacia la izquierda, se introduce en el surco coronario y lo recorre hasta la proximidad de la cara inferior del atrio derecho, donde termina. La vena cardíaca magna recibe venas del septo interventricular, de la parte anterior de los ventrículos derecho e izquierdo, de la pared izquierda del ventrículo izquierdo y del atrio izquierdo. Entre estas venas hay una ventricular, generalmente más voluminosa que las demás, denominada vena posterior del ventrículo izquierdo. Venas cardíacas anteriores o venas anteriores del ventrículo derecho. Las venas cardíacas anteriores o venas anteriores del ventrículo derecho (pequeñas venas cardíacas o venas cardíacas accesorias) proceden de la parte anterior y derecha del ventrículo derecho. Desembocan directamente en el atrio derecho, inmediatamente superiores al surco coronario, por medio de pequeños orificios denominados orificios de las venas cardíacas anteriores. La más importante de estas venas es la vena marginal derecha, que asciende sobre el borde lateral del ventrículo derecho y se abre en el atrio derecho a la altura de su base. Venas cardíacas mínimas. Se denomina así a pequeñas vénulas que proceden de las paredes del corazón y que se abren en las cavidades vecinas, atrios o ventrículos, a través de pequeños orificios denominados orificios de las venas cardíacas mínimas. Las venas cardíacas mínimas se encuentran sobre todo en las paredes de los atrios y en los músculos papilares de los ventrículos. FISIOLOGIA: La arteria coronaria izquierda nutre principalmente las porciones anterior e izquierda de las porciones laterales del ventrículo izquierdo, mientras que la arteria coronaria derecha nutre principalmente la mayor parte del ventrículo derecho y también la parte posterior del ventrículo izquierdo en el 80 al 90% de las personas. La mayoría del flujo sanguíneo venoso coronario del músculo ventricular izquierdo vuelve hacia la aurícula derecha del corazón a través del seno coronario, que supone aproximadamente el 75% del flujo sanguíneo coronario total. Y la mayoría de la sangre venosa coronaria del músculo ventricular derecho vuelve a través de pequeñas venas cardíacas anteriores que fluyen directamente en la aurícula derecha, y no a través del seno coronario. Una cantidad muy pequeña de la sangre venosa coronaria también vuelve hacia el corazón a través de las mínimas venas de Tebesio, que vacían directamente en todas las cámaras del corazón El flujo sanguíneo coronario en reposo del ser humano alcanza un promedio en reposo de 70 ml/min/100 g de peso del corazón, o 225 ml/min, que es un 4-5% del gasto cardíaco total. En este diagrama, el flujo sanguíneo de los capilares coronarios del músculo ventricular izquierdo desciende hasta un valor bajo durante la sístole, que es lo contrario de lo que sucede con el flujo en los lechos vasculares de cualquier otra zona del organismo. La razón es la importante compresión del músculo ventricular izquierdo que rodea los vasos intramusculares durante la contracción sistólica. Durante la diástole el músculo cardíaco se relaja y ya no obstruye el flujo sanguíneo a través de los capilares musculares del ventrículo izquierdo, de forma que la sangre fluye rápidamente durante toda la diástole. El flujo sanguíneo que atraviesa los capilares coronarios del ventrículo derecho también sufre cambios fásicos durante el ciclo cardíaco, pero como la fuerza de contracción del músculo ventricular derecho es mucho menor que la del músculo ventricular izquierdo, los cambios fásicos inversos sólo son parciales, al contrario de lo que sucede en el músculo ventricular izquierdo. Las arterias epicárdicas coronarias de la superficie externa que nutren la mayor parte del músculo. Las arterias intramusculares, más pequeñas, derivan de las arterias epicárdicas y penetran en el músculo, aportando los nutrientes necesarios. Inmediatamente por debajo del endocardio se encuentra un plexo de arterias subendocárdicas. Durante la sístole, el flujo sanguíneo a través del plexo subendocárdico del ventrículo izquierdo, en el que los vasos coronarios intramusculares se comprimen mucho con la contracción del músculo ventricular, tiende a disminuir pero los vasos extra del plexo subendocárdico normalmente compensan este descenso. El flujo sanguíneo que atraviesa el sistema coronario está regulado principalmente por la vasodilatación arteriolar local en respuesta a las necesidades nutricionales del músculo cardíaco. Es decir, siempre que aumente la fuerza de la contracción cardíaca, la velocidad del flujo sanguíneo coronario también lo hace. Por el contrario, el descenso de la actividad cardíaca se acompaña de un descenso del flujo coronario. El flujo sanguíneo en las arterias coronarias está regulado casi exactamente en proporción a las necesidades de oxígeno de la musculatura cardíaca. Se desconoce por qué el aumento del consumo de oxígeno provoca la dilatación coronaria. Muchos investigadores han propuesto que el descenso de la concentración de oxígeno en el corazón provoca la liberación de sustancias vasodilatadoras desde los miocitos, que dilatan las arteriolas. La adenosina es una sustancia con una gran actividad vasodilatadora. En presencia de concentraciones muy bajas de oxígeno en los miocitos, una gran proporción del ATP celular se degrada a monofosfato de adenosina, pequeñas porciones del cual se degradan después y liberan la adenosina hacia los líquidos tisulares del músculo cardíaco, con el aumento consiguiente del flujo sanguíneo coronario local. Después de que la adenosina provoque la vasodilatación, una gran parte de ella se reabsorbe hacia las células cardíacas para ser reutilizada. La distribución de las fibras nerviosas parasimpáticas (vagales) hacia el sistema coronario ventricular no es muy grande, pero la acetilcolina liberada por la estimulación parasimpática tiene un efecto directo dilatando las arterias coronarias. La inervación simpática de los vasos coronarios es mucho más extensa. Los receptores constrictores se denominan receptores α y los dilatadores son los receptores β. En los vasos coronarios hay receptores tanto α como β. En general, los vasos coronarios epicárdicos preponderan sobre los receptores α, mientras que las arterias intramusculares preponderan sobre los receptores β. Por tanto, la estimulación simpática puede provocar, al menos en teoría, una pequeña constricción o dilatación coronaria, habitualmente una constricción. El músculo cardíaco consume normalmente ácidos grasos para aportar la mayoría de la energía, y no hidratos de carbono (aproximadamente el 70% de su energía procede de los ácidos grasos). Sin embargo, también es así en otros tejidos, y el metabolismo cardíaco puede activar mecanismos de glucólisis anaeróbica para obtener energía en condiciones anaerobias o de isquemia. Por desgracia, la glucólisis consume cantidades enormes de glucosa sanguínea, a la vez que forma grandes cantidades de ácido láctico en el tejido cardíaco, que es quizás una de las causas de dolor cardíaco en las afecciones cardíacas isquémicas. Los nervios simpáticos discurren por todo el corazón siguiendo a los vasos arteriales. La estimulación de estos nervios condiciona que el corazón lata con más frecuencia y con más fuerza. Los receptores adrenérgicos β1 en los miocitos cardíacos actúan como mediadores de estas respuestas cronotrópicas e inotrópicas. El incremento del trabajo metabólico del miocardio da lugar a vasodilatación coronaria a través de vías metabólicas. Sin embargo, durante la inhibición farmacológica de los receptores β1, que impide el incremento del metabolismo, la estimulación simpática da lugar a vasoconstricción coronaria. Esta respuesta es el efecto directo de la actividad nerviosa simpática sobre los receptores adrenérgicos α en las CMLV de los vasos de resistencia coronarios. Así, el bloqueo de los receptores β1 «desenmascara» la vasoconstricción adrenérgica. Sin embargo, en condiciones normales (es decir, sin bloqueo β), la tendencia de las vías metabólicas a vasodilatar supera con mucho la tendencia de las vías simpáticas a vasoconstreñir. NOTA: Cuando un músculo se contrae en un medio anaerobio, el glucógeno desaparece y aparece lactato; cuando se admite oxígeno, tiene lugar la recuperación aerobia, y ya no se produce lactato. No obstante, si ocurre contracción en condiciones aerobias, no hay acumulación de lactato, y el piruvato es el principal producto terminal de la glucólisis. El piruvato se oxida más hacia CO2 y agua. Cuando hay carencia de oxígeno, la reoxidación mitocondrial de NADH formado durante la glucólisis está alterada, y el NADH se reoxida al reducir piruvato a lactato, de modo que se permite que continúe la glucólisis. Si bien la glucólisis puede ocurrir en condiciones anaerobias, esto tiene un precio, puesto que limita la cantidad a 2 mol de ATP formado por cada mol de glucosa oxidada, de modo que debe metabolizarse mucha más glucosa en condiciones anaerobias que en condiciones aerobias. ISQUEMIA: En medicina, se denomina isquemia (del griego ἴσχειν, ísjein, ‘detener’ y αἷμα, aíma, ‘sangre’) al estrés celular causado por cualquier disminución transitoria o permanente del flujo sanguíneo en el capilar y consecuente disminución del aporte de oxígeno (hipoxia) y de la eliminación de productos del metabolismo del tejido. Este sufrimiento celular puede ser suficientemente intenso como para causar la muerte celular del tejido al que pertenece (necrosis). Si la isquemia es muy grave puede llegar a la anoxia, lo que implica que los tejidos de esa región no podrán contar con la energía necesaria para sobrevivir y el tejido morirá. Durante la isquemia el músculo cardíaco no dispone de un aporte suficiente de nutrientes desde la vascularización coronaria para mantener la polarización normal de las membranas. La presencia de un flujo sanguíneo insuficiente al músculo cardíaco reduce el metabolismo del músculo por tres motivos: 1) ausencia de oxígeno; 2) acumulación excesiva de anhídrido carbónico, y (3) ausencia de suficientes nutrientes alimenticios. En consecuencia, no se puede producir la repolarización de la membrana muscular en las zonas de isquemia miocárdica grave. En la isquemia coronaria intensa el ATP se degrada primero a difosfato de adenosina, después a monofosfato de adenosina y, por último, a adenosina. Como la membrana celular del músculo cardíaco es ligeramente permeable a la adenosina, gran parte de ella puede difundir desde los miocitos hacia la sangre circulante. Normalmente, una persona no puede «sentir» su corazón, pero el músculo cardíaco isquémico provoca una sensación de dolor, a veces intenso. Se desconoce qué es lo que causa este dolor, pero se cree que la isquemia hace que el músculo libere sustancias ácidas, como el ácido láctico u otros productos que estimulan el dolor, como la histamina, las cininas o las enzimas proteolíticas celulares, que no se eliminan con la rapidez suficiente debido a que el flujo sanguíneo coronario se desplaza lentamente. Las concentraciones altas de estos productos anormales estimulan después las terminaciones nerviosas del dolor en el músculo cardíaco, enviando los impulsos de dolor a través de las fibras nerviosas sensibles aferentes hacia el sistema nervioso central. PATOFISIOLOGÍA La isquemia miocárdica ocurre cuando hay un desequilibrio entre el suministro y la demanda de oxígeno miocárdico. La demanda de oxígeno del miocardio depende de varios factores, como la frecuencia cardíaca, la contractibilidad del miocardio, la poscarga (por razones prácticas, la presión arterial sistólica a menudo se toma como un sustituto) y la tensión de la pared ventricular (precarga). Sin embargo, para fines clínicos, la frecuencia cardíaca, la presión arterial sistólica y el producto doble calculado (FC x PA sistólica) se consideran los determinantes más importantes de la demanda miocárdica de oxígeno. El espasmo de la arteria coronaria es una causa conocida de reducción primaria en el suministro de sangre que puede conducir a isquemia miocárdica. Los mecanismos precisos por los cuales, en un individuo dado, algunos episodios isquémicos están asociados con dolor torácico y otros no presentan síntomas, no se conocen bien. Los mecanismos que se han propuesto para explicar el desarrollo de la isquemia miocárdica silenciosa incluyen: ● Incapacidad para alcanzar el umbral de dolor durante un episodio de isquemia. ● Menor gravedad y menor duración de los episodios isquémicos. ● Presencia de un umbral más alto para el dolor. ● Percepción generalizada defectuosa de estímulos dolorosos. ● Mayores niveles de beta-endorfina ● Mayor producción de citocinas antiinflamatorias, que pueden bloquear las vías de transmisión del dolor y aumentar el umbral para la activación nerviosa. Enfermedad cardíaca isquémica: una condición en la cual el desequilibrio entre el suministro y la demanda de oxígeno del miocardio, causado con mayor frecuencia por la aterosclerosis de las arterias coronarias, produce hipoxia miocárdica y acumulación de metabolitos de desecho.(1)